文档内容
专题讲座(二) 整合有效信息书写陌生化学方程
式
目录
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查非氧化还原反应陌生化学(离子)方程式的书写
高频考点2 考查氧化还原反应陌生化学(离子)方程式的书写
高频考点3 陌生电极反应式的书写
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 非氧化还原反应陌生化学(离子)方程式的书写
新情境下非氧化还原类化学(离子)方程式的书写,因没有涉及元素化合物的变化,故组成物质的各
元素在发生反应时复分解重组,生成常见物质,一般用观察法即可配平。
1、书写非氧化还原反应化学(离子)方程式的步骤:
①根据实验事实写出反应物和生成物的化学式。
②配平化学方程式。
③注明化学方程式发生的条件并注明“↑ ”、“↓”。
2、书写技巧
(1)运用“证据→推理→符号”思路书写新情况化学(离子)方程式的基本过程如下:“读”取题目中
的有效信息(证据),写出反应物和生成物的符号(推理+表征),再依据质量守恒、电荷守恒(基本规律),即
可轻松写出规范的方程式。
(2)根据“中和”原理或“强酸制弱酸”原理书写化学(离子)方程式,如酸(酸式盐)与碱可发生中和反
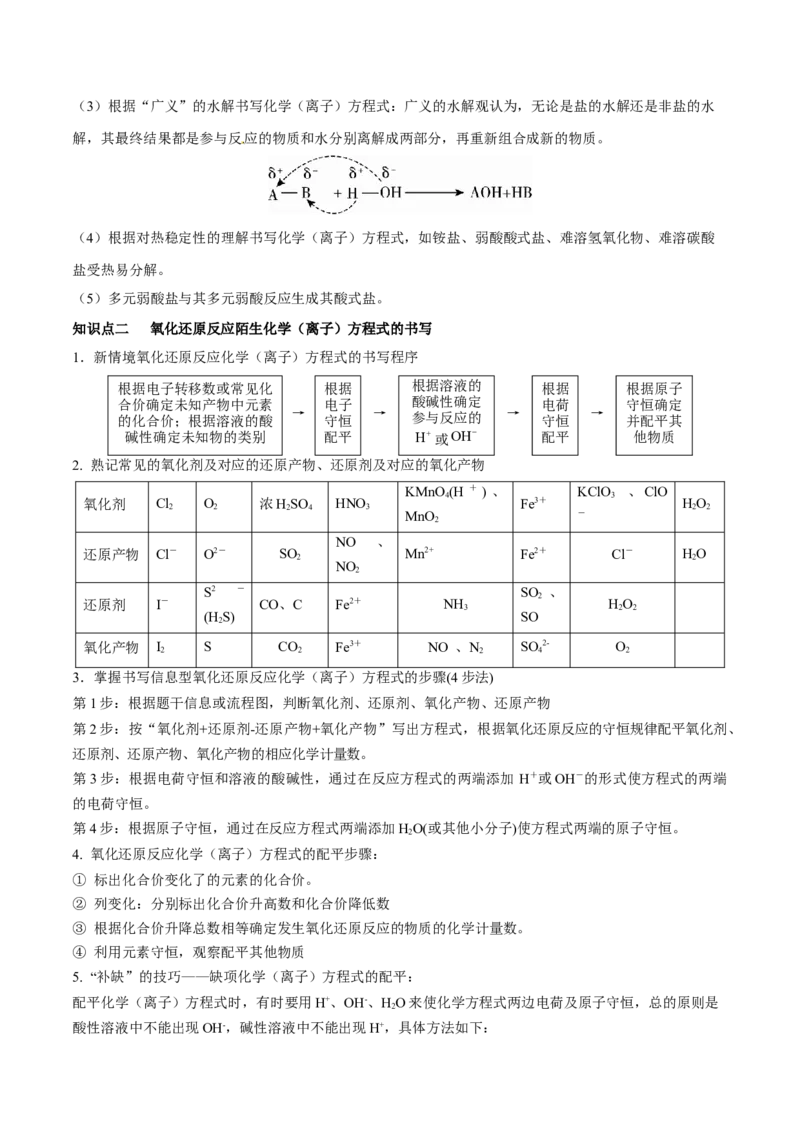
应、强酸与弱酸盐可以反应。(3)根据“广义”的水解书写化学(离子)方程式:广义的水解观认为,无论是盐的水解还是非盐的水
解,其最终结果都是参与反应的物质和水分别离解成两部分,再重新组合成新的物质。
(4)根据对热稳定性的理解书写化学(离子)方程式,如铵盐、弱酸酸式盐、难溶氢氧化物、难溶碳酸
盐受热易分解。
(5)多元弱酸盐与其多元弱酸反应生成其酸式盐。
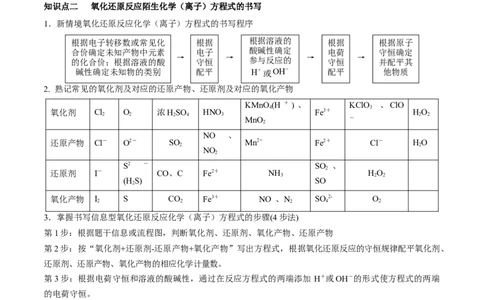
知识点二 氧化还原反应陌生化学(离子)方程式的书写
1.新情境氧化还原反应化学(离子)方程式的书写程序
根据电子转移数或常见化 根据 根据溶液的 根据 根据原子
合价确定未知产物中元素 电子 酸碱性确定 电荷 守恒确定
→ → → →
的化合价;根据溶液的酸 守恒 参与反应的 守恒 并配平其
碱性确定未知物的类别 配平 H或OH 配平 他物质
2. 熟记常见的氧化剂及对应的还原产物、还原剂及对应的氧化产物
KMnO (H + ) 、 KClO 、ClO
4 3
氧化剂 Cl O 浓HSO HNO Fe3+ HO
2 2 2 4 3 2 2
MnO -
2
NO 、
还原产物 Cl- O2- SO Mn2+ Fe2+ Cl- HO
2 2
NO
2
S2 - SO 、
2
还原剂 I- CO、C Fe2+ NH HO
3 2 2
(H S) SO
2
氧化产物 I S CO Fe3+ NO 、N SO 2- O
2 2 2 4 2
3.掌握书写信息型氧化还原反应化学(离子)方程式的步骤(4步法)
第1步:根据题干信息或流程图,判断氧化剂、还原剂、氧化产物、还原产物
第2步:按“氧化剂+还原剂-还原产物+氧化产物”写出方程式,根据氧化还原反应的守恒规律配平氧化剂、
还原剂、还原产物、氧化产物的相应化学计量数。
第3步:根据电荷守恒和溶液的酸碱性,通过在反应方程式的两端添加 H+或OH-的形式使方程式的两端
的电荷守恒。
第4步:根据原子守恒,通过在反应方程式两端添加HO(或其他小分子)使方程式两端的原子守恒。
2
4. 氧化还原反应化学(离子)方程式的配平步骤:
① 标出化合价变化了的元素的化合价。
② 列变化:分别标出化合价升高数和化合价降低数
③ 根据化合价升降总数相等确定发生氧化还原反应的物质的化学计量数。
④ 利用元素守恒,观察配平其他物质
5. “补缺”的技巧——缺项化学(离子)方程式的配平:
配平化学(离子)方程式时,有时要用H+、OH-、HO来使化学方程式两边电荷及原子守恒,总的原则是
2
酸性溶液中不能出现OH-,碱性溶液中不能出现H+,具体方法如下:酸性环境 碱性环境
反应物中少氧 左边加HO,右边加H+ 左边加OH-,右边加HO
2 2
反应物中多氧 左边加H+,右边加HO 左边加HO,右边加OH-
2 2
【易错提醒】绝不可能出现的情况:H+→OH- 或者OH-→H+。
知识点三 陌生电极反应式的书写
近年来氧化还原反应和电化学原理结合的题型比较多,我们只要抓住氧化还原反的本质以及原电池或
电解池中两极的放电情况,就会迎刃而解。书写电极反应方程式的一般方法:
第一步:确定原电池的正负极,列出正负极上的反应物质,并标出相同数目电子的得失。
第二步:原电池负极或电解池阳极的电极反应式,按“还原剂-ne-=氧化产物”书写;原电池正极或电解
池阴极的电极反应式,按“氧化剂+ne-=还原产物”书写。
【特别注意】负极反应生成的阳离子与电解质溶液中的阴离子是否共存。若不共存,则该电解质溶液中的
阴离子应写入负极反应式,如Al-Cu-NaHCO 溶液构成的原电池中,因Al失去电子生成的Al3+能与
3
HCO -反应:Al3++3HCO-=Al(OH) ↓+3CO ↑,故铝件(负极)上发生的反应为:Al-3e-+3HCO-
3 3 3 2 3
=Al(OH) ↓+3CO ↑,而不是仅仅写为:Al-3e-=Al3+。
3 2
第三步:根据电荷守恒和反应混合物的酸碱性,补充H+、OH-或HO等,并配平电极反应。
2
【特别注意】若正极上的反应物质是O,且电解质溶液为中性或碱性,电极反应式中不能出现H+,且水
2
必须写入正极反应式中,与O 结合生成OH-,若电解质溶液为酸性,电极反应式中不能出现OH-,且
2
H+必须写入正极反应式中,与O 结合生成水。
2
第四步:正负极反应式相加(电子守恒)得到电池反应的总反应式。若已知电池反应的总反应式,可先写
出较易书写的电极反应式,然后在电子守恒的基础上,总反应式减去较易写出的电极反应式,即得到较难
写出的电极反应式。
【特别提醒】(1)根据“电池充电时,原电池的负极与外接电源的负极相连作电解池的阴极,原电池的
正极与外接电源的正极相连作电解池的阳极”知,可充电电池(二次电池)充电时阴极的电极反应是其放电
时负极反应的逆过程,充电时阳极的电极反应是其放电时正极反应的逆过程。
(2)电解池中的阳极有最强的氧化能力,阴极有最强的还原能力,所以可以发生平常不能发
生的一些氧化还原反应。电解液中氧化性的离子可以在阴极得电子,还原性离子则可以在阳极失电子。同
时考虑得失电子产物与电解液可能发生的反应。
(3)书写电极反应式经验总结与分享:巧妙结合新情境题目信息,先确定部分反应物和产物,
然后遵循“电荷守恒,查氧补水,差几个氧原子补几分子水”。
总之,信息型化学(离子、电极)方程式书写题的基本解题思路是:第三部分:典型例题剖析
高频考点1 考查非氧化还原反应陌生化学(离子)方程式的书写
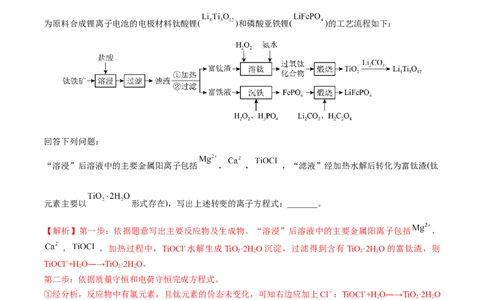
例1.(2022·湖南·郴州一中高三期中)以钛铁矿(主要成分为 ,还含有MgO、CaO、 等杂质)
为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂( )的工艺流程如下:
回答下列问题:
“溶浸”后溶液中的主要金属阳离子包括 , , ,“滤液”经加热水解后转化为富钛渣(钛
元素主要以 形式存在),写出上述转变的离子方程式:_______。
【解析】第一步:依据题意写出主要反应物及生成物。“溶浸”后溶液中的主要金属阳离子包括 ,
, ,加热过程中,TiOCl+水解生成TiO·2H O沉淀,过滤得到含有TiO·2H O的富钛渣,则
2 2 2 2
TiOCl++H O―→TiO·2H O。
2 2 2
第二步:依据质量守恒和电荷守恒完成方程式。
①经分析,反应物中有氯元素,且钛元素的价态未变化,可知右边应加上Cl-:TiOCl++H O―→TiO·2H O
2 2 2
+Cl-。
②右边比左边多两个氧原子,且左边电荷数为+1,右边电荷数为-1,溶液呈酸性,根据电荷守恒,可知右
边还应补充H+:TiOCl++H O―→TiO·2H O+Cl-+H+。依据右边有4个氧原子,可知左边HO前的系数
2 2 2 2
为3,氯原子与钛原子个数相等,左边电荷数为+1,可知右边H+的系数为2,即TiOCl++3H O TiO·2H O
2 2 2
+Cl-+2H+。
【答案】TiOCl++3H O TiO·2H O+Cl-+2H+
2 2 2
【题后归纳】运用“证据→推理→符号”思路书写新情况方程式的基本过程如下:“读”取题目中的有效
信息(证据),写出反应物和生成物的符号(推理+表征),再依据质量守恒、电荷守恒(基本规律),即可轻松写出规范的方程式。
【变式训练1】(根据“中和”原理或“强酸制弱酸”原理书写陌生化学(离子)方程式)(2022·江苏·
盐城中学三模)硫化氢(H S)是一种有毒气体,高于200℃分解,脱除HS的方法很多,如用NaCO 吸收,
2 2 2 3
含HS的气体与饱和NaCO 溶液在吸收塔内逆流接触,生成两种酸式盐。该反应的离子方程式为_____。
2 2 3
【解析】HS的气体与饱和NaCO 溶液生成两种酸式盐可知为NaHS和NaHCO ,反应的离子方程式为:
2 2 3 3
HS+CO2—=HS—+HCO—,故答案为:HS+CO2—=HS—+HCO—;
2 3 3 2 3 3
【答案】HS+CO2—=HS—+HCO—
2 3 3
【变式训练2】(根据“广义”的水解原理书写陌生化学(离子)方程式)(2021·全国·高三)按要求完成下
列反应的化学方程式:
(1)一氯胺(NH Cl)是一种重要的水消毒剂,写出产生消毒物质的化学方程式:
2
____________________________________________________________。
(2)写出亚硫酰氯(SOCl )在潮湿的空气中产生白雾的化学方程式:
2
____________________________________________________________。
(3)乙酸乙酯与偏铝酸钠溶液共热产生白色胶状沉淀的化学方程式:
____________________________________________________________________。
(4)常用尿素[CO(NH)]除去工业废水中Cr3+,流程如下: ,
2 2
完成该转化的离子方程式:_____________________________________________________。
【解析】(1)一氯胺(NH Cl)在中性或酸性环境中会发生强烈水解,生成具有强烈杀菌作用的 HClO,反应用
2
=号,氯胺与水反应方程式为NH Cl+H O=HClO+NH ↑;
2 2 3
(2)SO Cl 发生水解反应得到硫酸和盐酸,化学方程式为:SO Cl+2H O=HSO +2HCl;
2 2 2 2 2 2 4
(3)乙酸乙酯与偏铝酸钠溶液共热产生白色胶状沉淀,可以理解为乙酸乙酯先水解生成乙酸和乙醇,乙酸再与
偏铝酸钠溶液反应生成 Al(OH) 白色胶状沉淀,故反应方程式为 CHCOOCH CH+NaAlO+2HO
3 3 2 3 2 2
Al(OH) ↓+CH COONa+CHCHOH;
3 3 3 2
(4)从流程上看,可以看着尿素先水解生成CO 和NH ·HO,NH ·HO再与Cr3+反应生成Cr(OH) ,故反应
2 3 2 3 2 3
方程式为3CO(NH)+2Cr3++9HO=2Cr(OH) ↓+3CO↑+6NH +。
2 2 2 3 2 4
【答案】(1)NH Cl+H O=HClO+NH ↑(2)SO Cl+2H O=HSO +2HCl
2 2 3 2 2 2 2 4
(3)CH COOCH CH+NaAlO+2HO Al(OH) ↓+CH COONa+CHCHOH
3 2 3 2 2 3 3 3 2
(4)3CO(NH)+2Cr3++9HO=2Cr(OH) ↓+3CO↑+6NH +
2 2 2 3 2 4
【变式训练3】(根据物质的热稳定性书写陌生化学(离子)方程式)(2021·全国·高三(节选))磷尾矿
渣的主要成分是白云石(CaCO·MgCO )和磷灰石[Ca (PO )F],某研究性学习小组设计用磷尾矿制备有用的
3 3 5 4 3
CaCO 、Mg(OH) 的流程如下:
3 2已知Ca (PO )F在950℃不分解,完成下列变化的化学方程式:
5 4 3
(1)950℃煅烧磷尾矿的主要化学方程式是
__________________________________________________________。
(2)由磷矿Ⅰ生成浸取液Ⅰ的离子方程式:
_____________________________________________________________________。
(3)在浸取液Ⅱ中通入NH ,发生反应的化学方程式:
3
________________________________________________________。
【解析】(1)根据题给化学工艺流程和信息知磷尾矿[主要含Ca (PO )F和CaCO •MgCO]在950℃下煅烧,
5 4 3 3 3
其中Ca (PO )F不分解,碳酸钙和碳酸镁分解,生成气体的成分为二氧化碳(CO)和相应的氧化物,则反应
5 4 3 2
方程式为:CaCO ·MgCO 2CO+CaO+MgO;
3 3 2
(2)NH NO 溶液中铵离子水解呈酸性,H+能从磷矿I中浸取出Ca2+,发生的离子方程式为CaO+2NH +=Ca2+
4 3 4
+2NH +H O;
3 2
(3)根据化学工艺流程判断浸取液II的主要成分为硫酸镁溶液,通入NH ,发生反应的化学方程式是
3
MgSO +2NH+2H O=Mg(OH)↓+(NH)SO 。
4 3 2 2 4 2 4
【 答 案 】 ( 1 ) CaCO ·MgCO 2CO++MgO(2)CaO+2NH +=Ca2+
3 3 2 4
+2NH +H O(3)MgSO +2NH+2H O=Mg(OH)↓+(NH)SO
3 2 4 3 2 2 4 2 4
高频考点2 考查氧化还原反应陌生化学(离子)方程式的书写
例2.(2022·全国·高三专题练习)KCr O 能与硫酸酸化的NaC O 溶液反应,生成Cr3+和CO,该反应的离
2 2 7 2 2 4 2
子方程式为_______。
【解析】第一步:依题意,锰元素的化合价降低,故KCr O 是氧化剂,Cr3+是还原产物;碳元素的化合价
2 2 7
升高,故NaC O(碳元素化合价为+3价)是还原剂,CO 是氧化产物。
2 2 4 2
第二步:按“氧化剂+还原剂―→还原产物+氧化产物”把离子方程式初步写成:Cr O2-+
2 7
C O―→2Cr3++CO↑。
2 2
由Cr O2-→Cr3+,铬元素总的降了6价;由C O→CO ,碳元素总的升了2价,1 mol C O共失去2 mol e-,
2 7 2 2 2
最小公倍数为6,故在C O前配3,在Cr O2-前配1,在还原产物Cr3+前配6,氧化产物CO 前配2,即
2 2 7 2
Cr O2-+3C O―→2Cr3++6CO↑。
2 7 2 2
第三步:反应在硫酸中进行,故在左边补充H+,右边补充H O,Cr O2-+3C O+H+―→2Cr3++6CO↑+
2 2 7 2 2HO。
2
第四步:依据电荷守恒及H、O原子守恒配平如下:
Cr O2-+3C O+14H+=2Cr3++6CO↑+7HO。
2 7 2 2 2
【答案】Cr O2-+3C O+14H+=2Cr3++6CO↑+7HO
2 7 2 2 2
【题后归纳】书写信息型氧化还原反应的步骤(4步法)
第1步:根据题干信息或流程图,判断氧化剂、还原剂、氧化产物、还原产物
第2步:按“氧化剂+还原剂-还原产物+氧化产物”写出方程式,根据氧化还原反应的守恒规律配平氧化剂、
还原剂、还原产物、氧化产物的相应化学计量数。
第3步:根据电荷守恒和溶液的酸碱性,通过在反应方程式的两端添加 H+或OH-的形式使方程式的两端
的电荷守恒。
第4步:根据原子守恒,通过在反应方程式两端添加HO(或其他小分子)使方程式两端的原子守恒。
2
【变式训练1】(根据已知反应物书写陌生化学(离子)方程式)(2022·河南安阳·模拟预测(节选))三氧
化二铬(CrO)可用作着色剂、分析试剂、催化剂等。一种利用铬铁矿(主要成分为FeO·Cr O,还含有
2 3 2 3
Al O、SiO 等杂质)清洁生产Cr O 的工艺流程如下:
2 3 2 2 3
已知铬酸酐(CrO )常用作氧化剂,写出“氧化酸浸”时FeO·Cr O 反应的化学方程式是___________。
3 2 3
【解析】已知铬酸酐(CrO )常用作氧化剂,其作用是将Fe2+氧化为Fe3+,“氧化酸浸”时FeO·Cr O 与稀硫
3 2 3
酸反应生成硫酸亚铁和硫酸铬,铬酸酐(CrO )将硫酸亚铁氧化为硫酸铁,则反应的化学方程式是
3
6FeO·Cr O+30H SO + 2CrO =3Fe (SO )+7Cr (SO )+30H O;
2 3 2 4 3 2 4 3 2 4 3 2
【答案】6FeO·Cr O+30H SO + 2CrO =3Fe (SO )+7Cr (SO )+30H O
2 3 2 4 3 2 4 3 2 4 3 2
【变式训练2】(根据实验流程书写陌生化学(离子)方程式)(2022·全国·高三(节选))NaClO 是一种重
2
要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
写出“反应”步骤中生成ClO 的化学方程式: 。
2【解析】由流程图可知,NaClO 与HSO 、SO 反应生成NaHSO 和ClO ,根据电子守恒、元素守恒可写
3 2 4 2 4 2
出并配平反应方程式为2NaClO+H SO +SO===2ClO +2NaHSO 。
3 2 4 2 2 4
【答案】2NaClO+H SO +SO===2ClO +2NaHSO
3 2 4 2 2 4
【变式训练3】(根据电子得失数目定量分析判断产物书写陌生化学(离子)方程式)以废旧铅酸电池中
的含铅废料(Pb、PbO、PbO 、PbSO 及炭黑等)和HSO 为原料,制备高纯PbO,实现铅的再生利用。其
2 4 2 4
工作流程如下:
过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++ PbO +4H++SO2−=2Fe3++PbSO+2H O
2 4 4 2
ii: ……
① 写出ii的离子方程式:________________。
【解析】催化剂通过参加反应,改变反应历程,降低反应的活化能,加快化学反应速率,而本身的质
量和化学性质反应前后保持不变。根据题给信息知反应i中Fe2+被PbO 氧化为Fe3+,则反应ii中Fe3+被Pb
2
还原为Fe2+,离子方程式为2Fe3++Pb+SO 2—==PbSO +2Fe2+。
4 4
【答案】2Fe3++Pb+SO 2—==PbSO +2Fe2+
4 4
【变式训练4】(根据题中图像书写陌生化学(离子)方程式)(2022·广东潮州·二模(节选))二氧化碳
的回收利用是环保领域研究热点。
在太阳能的作用下,以CO 为原料制取炭黑的流程如图所示。总反应的化学方程式为 。
2
【解析】首先明确反应的目的是以CO 为原料制取炭黑,并且要求写总反应的化学方程式,根据地图示,
2
化学方程式为:CO C+O 。
2 2
【答案】CO C+O
2 2
高频考点3 陌生电极反应式的书写例3.(2021·全国·高三)铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni O+3HO=Fe(OH) +
2 3 2 2
2Ni(OH) ,电池放电时正极的电极反应式为__________________________________。
2
【解析】第一步,反应前后Ni元素化合价由+3价(NiO)降低到+2价[Ni(OH) ],故Ni O 是氧化剂,
2 3 2 2 3
Ni(OH) 是还原产物。
2
第二步,原电池的正极反应按“氧化剂+ne-=还原产物”先初步写为:
Ni O+2e-=2Ni(OH) 。
2 3 2
第三步,根据氢元素守恒及电池放电时总反应中HO是反应物,在电极反应式的左边反应物中补充HO,
2 2
再由电荷守恒在电极反应式右边生成物中补充带负电荷的OH-,
Ni O+2e-+HO=2Ni(OH) +OH-,
2 3 2 2
配平后正极的电极反应为:Ni O+2e-+3HO=2Ni(OH) +2OH-。
2 3 2 2
【答案】Ni O+2e-+3HO=2Ni(OH) +2OH-
2 3 2 2
【题后归纳】“三步法”书写陌生电极反应式
第一步:根据元素化合价的升降判断氧化剂、还原剂、氧化产物、还原产物。
第二步:原电池负极或电解池阳极的电极反应式,按“还原剂-ne-=氧化产物”书写;原电池正极或电解
池阴极的电极反应式,按“氧化剂+ne-=还原产物”书写。
第三步:根据电荷守恒和反应混合物的酸碱性,补充H+、OH-或HO等,并配平电极反应。
2
【变式训练1】(原电池中陌生电极反应式的书写)(2021·全国·高三)以固体氧化物为电解质(能传导O2-)
的新型NH 燃料电池,属于环境友好电池(产物对环境无污染),其结构如图所示:
2 4
电极甲上发生的电极反应为____________。
【解析】结合该电池产物对环境无污染可知,产物为 N 和HO,电极甲上肼失去电子,发生氧化反应,电
2 2
极反应式为NH-4e-+2O2-===N ↑+2HO。
2 4 2 2
【答案】NH+2O2--4e-===N ↑+2HO
2 4 2 2
【变式训练2】(电解池中陌生电极反应式的书写)(2021·全国·高三)直接电解吸收也是脱硝的一种方法,
用6%的稀硝酸吸收NO 生成HNO(一元弱酸),再将吸收液导入电解槽电解,使之转化为硝酸。电解装置
x 2如下图所示。
①图中b应连接电源的________(填“正极”或“负极”)。
②阳极的电极反应式为_______________________________。
【解析】由实验目的知,a极上HNO 转化为HNO ,N元素化合价升高,发生氧化反应,则a极为阳极,
2 3
电极反应式为HNO -2e-+HO===3H++NO。b极为阴极,电极反应式为2H++2e-===H ↑,应接外加电
2 2 2
源的负极。
【答案】①负 ②HNO-2e-+HO===3H++NO
2 2
【变式训练3】(原电池、电解池综合陌生电极反应式的书写)(2021·全国·高三)SO 是主要的大气污染气
2
体,利用化学反应原理是治理污染的重要方法。工业上用NaSO 吸收尾气中SO 使之转化为NaHSO ,再
2 3 2 3
以SO 为原料设计原电池,然后电解(惰性电极)NaHSO 制取HSO ,装置如下:
2 3 2 4
(1)甲图中A电极上的反应式为__________________。
(2)甲图中B与乙图________(填“C”或“D”)极相连,进行电解时乙图Z中Na+向________(填“Y”或“W”)
中移动。
(3)该电解池阴极的电极反应式为____________________;阳极的电极反应式为____________
_______________。
【解析】(1)从题目信息可知,SO 反应生成HSO ,所以SO 作负极,失去电子和水结合生成硫酸。(2)甲
2 2 4 2
中A为负极,B为正极,因为乙中C极附近加入NaHSO 得到NaSO ,说明H元素化合价降低生成H,在
3 2 3 2
阴极反应,所以连接电源的负极,即B连接D;进行电解时乙图中Na+向阴极移动,即向Y中移动。(3)阴
极是HSO反应生成SO和H,右侧为阳极室,据此写出对应的电极反应式。
2【答案】(1)SO +2HO-2e-===4H++SO
2 2
(2)D Y
(3)2HSO+2e-===2SO+H↑ HSO+HO-2e-===SO+3H+
2 2