文档内容
第二章 化学物质及其变化
专题讲座(二) 整合有效信息书写陌生化学(离子)方程式 (精练)
完卷时间:50分钟
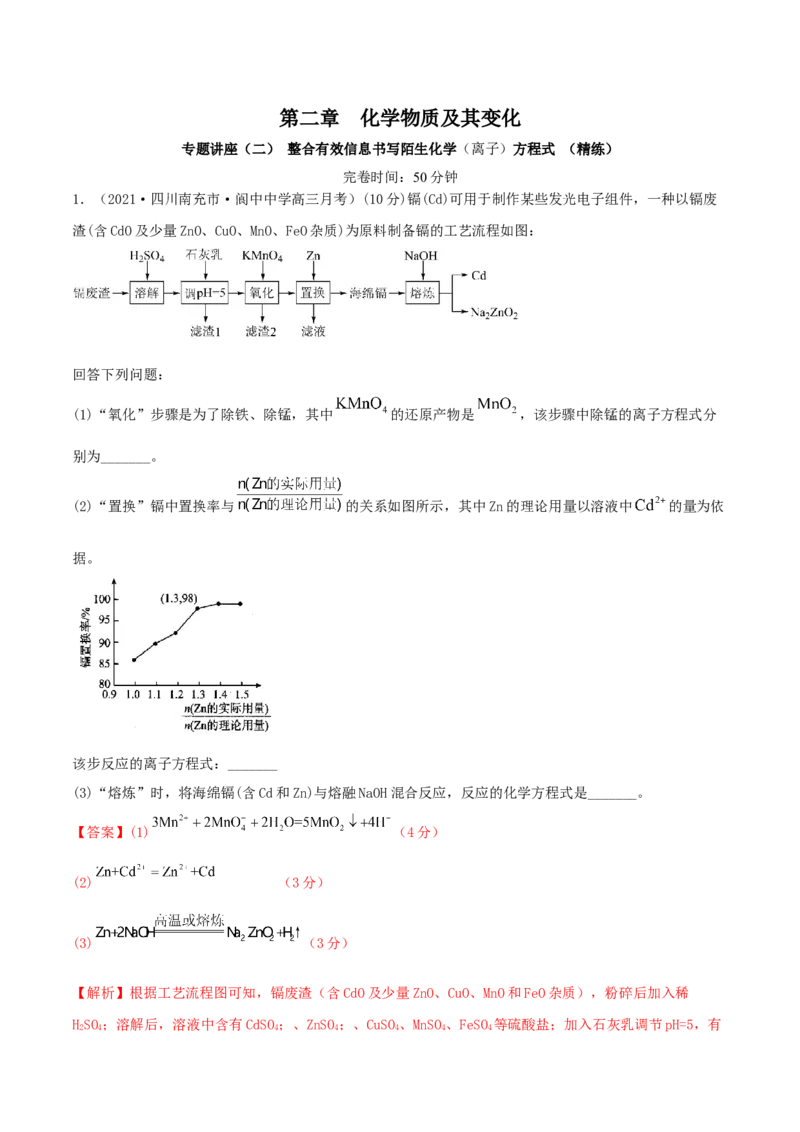
1.(2021·四川南充市·阆中中学高三月考)(10分)镉(Cd)可用于制作某些发光电子组件,一种以镉废
渣(含CdO及少量ZnO、CuO、MnO、FeO杂质)为原料制备镉的工艺流程如图:
回答下列问题:
(1)“氧化”步骤是为了除铁、除锰,其中 的还原产物是 ,该步骤中除锰的离子方程式分
别为_______。
(2)“置换”镉中置换率与 的关系如图所示,其中Zn的理论用量以溶液中 的量为依
据。
该步反应的离子方程式:_______
(3)“熔炼”时,将海绵镉(含Cd和Zn)与熔融NaOH混合反应,反应的化学方程式是_______。
【答案】(1) (4分)
(2) (3分)
(3) (3分)
【解析】根据工艺流程图可知,镉废渣(含CdO及少量ZnO、CuO、MnO和FeO杂质),粉碎后加入稀
HSO;溶解后,溶液中含有CdSO;、ZnSO;、CuSO、MnSO、FeSO 等硫酸盐;加入石灰乳调节pH=5,有
2 4 4 4 4 4 4CaSO 生成,同时沉淀除去Cu(OH);在滤液中加入KMnO 溶液,将Fe2+氧化为Fe3+,形成Fe(OH) 沉淀,同
4 2 4 3
时将Mn2+氧化生成MnO 沉淀;在滤液中再加入锌置换出Cd,得到海绵镉;海绵镉用NaOH溶解其中过量的
2
Zn,得到Cd和NaZnO;
2 2
(1) “氧化”时,KMnO 氧化Mn2+,得到MnO 沉淀,还原产物是MnO,故离子方程式为
4 2 2
(2)该反应为置换反应,离子方程式为 ;、
(3) “熔炼”时,将海绵镉(Cd和过量的Zn)与NaOH混合反应,过量的Zn被NaOH溶解,反应的化学方程
式是 ;
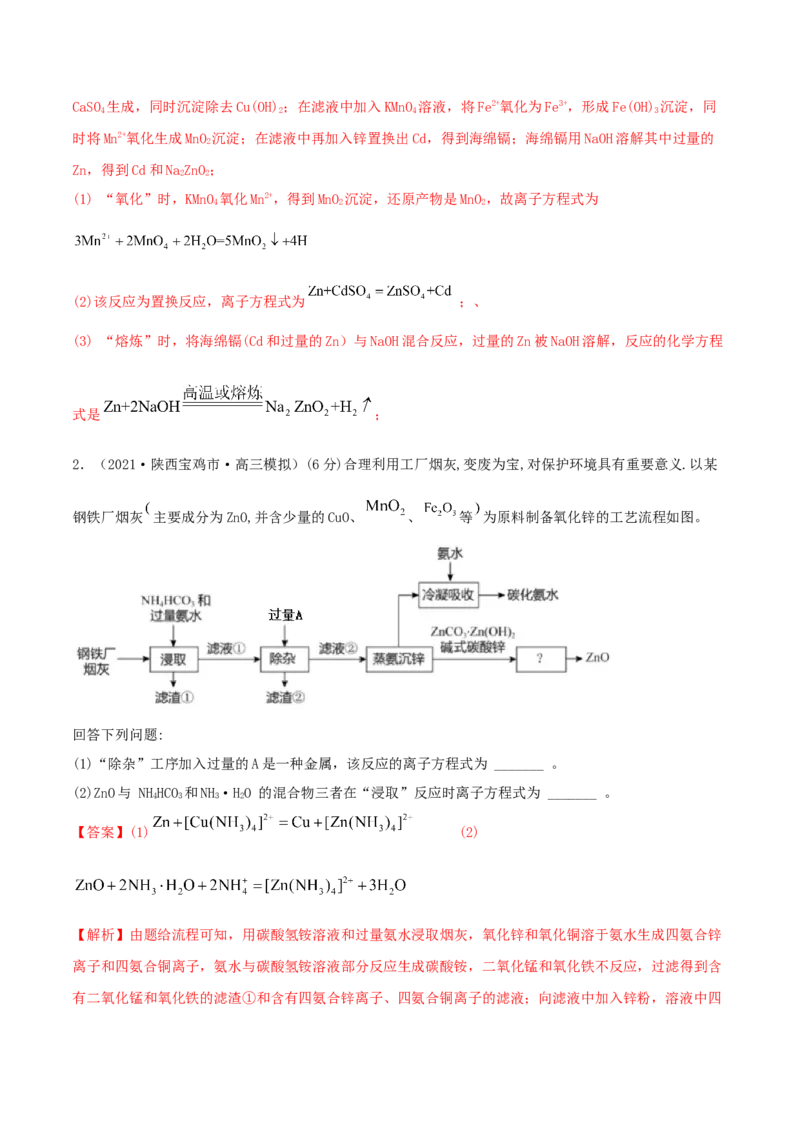
2.(2021·陕西宝鸡市·高三模拟)(6分)合理利用工厂烟灰,变废为宝,对保护环境具有重要意义.以某
钢铁厂烟灰 主要成分为ZnO,并含少量的CuO、 、 等 为原料制备氧化锌的工艺流程如图。
回答下列问题:
(1)“除杂”工序加入过量的A是一种金属,该反应的离子方程式为 _______ 。
(2)ZnO与 NHHCO 和NH·HO 的混合物三者在“浸取”反应时离子方程式为 _______ 。
4 3 3 2
【答案】(1) (2)
【解析】由题给流程可知,用碳酸氢铵溶液和过量氨水浸取烟灰,氧化锌和氧化铜溶于氨水生成四氨合锌
离子和四氨合铜离子,氨水与碳酸氢铵溶液部分反应生成碳酸铵,二氧化锰和氧化铁不反应,过滤得到含
有二氧化锰和氧化铁的滤渣①和含有四氨合锌离子、四氨合铜离子的滤液;向滤液中加入锌粉,溶液中四氨合铜离子和锌发生置换反应生成四氨合锌离子和铜,过滤得到含有锌、铜的滤渣②和含有四氨合锌离子
的滤液,则A为锌粉;加热滤液,滤液中Zn(NH)(HCO) 和Zn(NH)CO 反应变为NH 和碱式碳酸锌沉淀,
3 4 3 2 3 4 3 3
碱式碳酸锌高温煅烧得到氧化锌;氨及其盐从固液混合物中蒸出,蒸出物经冷凝吸收后加入氨水得到的碳
化氨水,碳化氨水可返回到浸取工序中循环使用。
(1)由分析可知,在除杂工序中加入过量的锌粉,溶液中四氨合铜离子和锌发生置换反应生成四氨合锌离
子和铜,反应的离子方程式为Zn+[Cu(NH)]2+=Cu+[Zn(NH)]2+;
3 4 3 4
(2) 由分析可知,在“浸取”反应时氧化锌发生的反应为氧化锌与碳酸氢铵和氨水的混合溶液反应成配离
子[Zn(NH)]2+和水,反应的离子方程式为Zn+[Cu(NH)]2+=Cu+[Zn(NH)]2+;
3 4 3 4 3 4
3.(2021·全国高三专题练习)(9分)碳酸锰(MnCO)是制造电信器材的软磁铁氧体,也用作脱硫的催化
3
剂,瓷釉、涂料和清漆的颜料。工业上利用软锰矿(主要成分是MnO,还含有FeO、CaCO、CuO等杂质)制
2 2 3 3
取碳酸锰的流程如下图所示:
已知:还原焙烧的主反应为2MnO+C 2MnO+CO↑。
2 2
可能用到的数据如下:
Fe(OH)
氢氧化物 Fe(OH) Cu(OH) Mn(OH)
2 2 2
3
开始沉淀pH 1.5 6.5 4.2 8.3
沉淀完全pH 3.7 9.7 7.4 9.8
根据要求回答下列问题:
(1)步骤D中氧化剂与还原剂的物质的量之比为___________。
(2)步骤G发生的离子方程式为___________。
(3)实验室可以用NaSO 溶液来检验Mn2+是否完全发生反应,原理为___________Mn2++___________SO +
2 2 8 2
___________HO→___________H++___________SO +___________MnO 。试配平该离子方程式。
2___________
【答案】(1)1∶2 (2)Mn2++2 =MnCO↓+CO↑+HO
3 2 2
(3)2Mn2++5 +8HO=16H++10 +2
2
【解析】软锰矿主要成分为MnO,还含有CaCO、FeO、AlO 等杂质,还原焙烧主反应为:
2 3 2 3 2 3
2MnO+C═2MnO+CO↑,加入硫酸酸浸过滤后的溶液中加入二氧化锰氧化亚铁离子,加入10%的氢氧化钠溶
2 2
液调节溶液pH=4.5使铁离子全部沉淀,过滤后的滤液中加入NaS沉淀重金属离子可以除去Pb2+、Al3+等离
2
子,滤液中加入碳铵发生复分解反应生成碳酸锰,分离烘干得到成品。
(1)步骤D中加入MnO 氧化溶液中的Fe2+,其中Mn从+4价降为+2价,Fe从+2价升高为+3价,Fe2+是还
2
原剂,根据电子守恒,氧化剂与还原剂的物质的量之比为1∶2;
(2)在含有Mn2+的溶液中加入NHHCO 生成MnCO 沉淀,发生反应的离子方程式为Mn2++2 =MnCO↓+
4 3 3 3
CO↑+HO;
2 2
(3)Mn从+2价升高为+7价,S从+7价降为+6价,根据电子守恒,Mn2+前系数为2, 前系数为5,再结
合电荷守恒和原子守恒得此反应的离子方程式2Mn2++5 +8HO=16H++10 +2 。
2
4.(2019·沈阳市第二十八中学高三月考)(6分)以碳酸锰铜矿(主要成分为 MnCO、CuCO,还含有 FeO
3 3 3 4
杂质)为原料制备硫酸锰并回收铜的一种工艺流程如图:
已知:Ksp[Fe(OH)]=4.0×10-38,Ksp[Cu(OH)]=2.2×10-20,Ksp[Fe(OH)]=8.0×10-16,
3 2 2
Ksp[Mn(OH)]=2.1×10-13
2
(1)写出“酸浸”时,杂质 FeO 与稀硫酸反应的化学方程式:_______
3 4
(2)“沉锰”时,发生反应的离子方程式为_______
【答案】(1)FeO+4HSO=Fe(SO)+ FeSO+4HO
3 4 2 4 2 4 3 4 2
(2)Mn2++2HCO = MnCO↓+CO↑+HO
3 2 2【解析】碳酸锰铜矿主要成分为 MnCO、CuCO,还含有 FeO 杂质,用硫酸酸浸,得到硫酸锰、硫酸铜、
3 3 3 4
硫酸铁、硫酸亚铁的混合溶液,加入二氧化锰,Fe2+被氧化为Fe3+;加入MnCO 调节pH生成氢氧化铁沉淀;
3
过滤后向溶液中通入氨气生成氢氧化铜沉淀,过滤,向滤液中加入NHHCO,生成MnCO 沉淀,MnCO 沉淀中
4 3 3 3
加硫酸,得到硫酸锰溶液。
(1) “酸浸”时,FeO 与稀硫酸反应生成硫酸铁、硫酸亚铁和水,反应的化学方程式是
3 4
FeO+4HSO=Fe(SO)+ FeSO+4HO;
3 4 2 4 2 4 3 4 2
(2)“沉锰”时,锰离子和碳酸氢根离子反应生成碳酸锰沉淀、二氧化碳、水,发生反应的离子方程式为
Mn2++2HCO = MnCO↓+CO↑+HO。
3 2 2
5.(9分)现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如
图所示(图中有些反应的生成物和反应的条件没有标出)。
请根据以上信息完成下列各题:
(1)写出实验室制备黄绿色气体乙的化学方程式:_______,
(2)反应③中的离子方程式是_______
(3)反应⑤的离子方程式是_______
【答案】(1)4HCl(浓)+MnO Cl↑+MnCl+2HO
2 2 2 2
(2) 2Al+2OH-+2HO=2AlO +3H↑
2 2
(3)2Fe2++Cl=2Fe3++2Cl-
2
【解析】金属单质A焰色反应呈黄色,则A是Na,Na与HO反应产生气体甲是H,D溶液为NaOH,金属B
2 2
和氢氧化钠溶液反应,说明B为Al,黄绿色气体乙为Cl,气体甲和氯气反应生成丙为HCl,物质E为盐酸
2
溶液,物质D是氢氧化钠,D和物质G反应生成红褐色沉淀H为Fe(OH),盐酸与金属C反应产生金属氯化
3
物,该氯化物与NaOH溶液反应产生Fe(OH),则C是Fe,F为FeCl、G为FeCl。
3 2 3
(1)气体乙为氯气,实验室利用二氧化锰和浓盐酸共热制取氯气,化学方程式为4HCl(浓)+MnO
2Cl↑+MnCl+2HO;
2 2 2
(2)反应③为铝和NaOH溶液的反应,生成偏铝酸钠、氢气,离子方程式为2Al+2OH-+2HO= +3H↑;
2 2
(3)结合分析可知,反应⑤为FeCl 与Cl 反应生成FeCl,其离子方程式是2Fe2++Cl=2Fe3++2Cl-;
2 2 3 2
6.(2021·福建三明市·高三二模)(9分)从分金渣(主要成分为:AgCl、AgS、PbSO、BaSO)中获取高
2 4 4
纯银的流程如图所示:
已知:K(AgCl)=1.8×10-10,K(AgS)=6.3×10-50。
sp sp 2
(1)“预处理”时主要反应的化学方程式为_______。
(2)“分银”时AgCl与NaSO 反应生成Ag(SO) 的离子方程式为_______。
2 3 3
(3)“还原”时HCHO转化为HCOOH,其化学方程式为_______。
【答案】(1)2FeCl+AgS=2FeCl+S+2AgCl
3 2 2
(2) AgCl+2SO = Ag(SO) +Cl-
3
(3)2AgCl+HCHO+HO=2Ag+HCOOH+2HCl
2
【解析】分金渣加入氯化铁进行预处理,氯化铁与硫酸银反应生成氯化亚铁、单质硫;分银时,加入亚硫
酸钠,AgCl与NaSO 反应生成Ag(SO) ,而PbSO、BaSO 及生成的单质S不溶于水,则分银渣为PbSO、
2 3 3 4 4 4
BaSO 及生成的单质S;过滤加入盐酸,使Ag(SO) 生成氯化银沉淀,过滤氯化银与甲醛反应生成甲酸、
4 3
单质银和氯化氢。
(1)根据分金渣的成分,加入氯化铁时,氯化铁具有强氧化性,则只能与硫化银发生氧化还原反应,方程
式为2FeCl+AgS=2FeCl+S+2AgCl;
3 2 2
(2) “分银”时AgCl与NaSO 反应生成Ag(SO) 和氯离子,离子方程式为AgCl+2SO = Ag(SO) +Cl-;
2 3 3 3
(3)“还原”时HCHO与氯化银、水反应生成HCOOH、单质银,化学方程式为
2AgCl+HCHO+HO=2Ag+HCOOH+2HCl;
27.(2021·福建福州市·高三二模)(6分)某冶炼厂利用镉熔炼碱渣(约含 及 、 、
)和铜镉渣(含 、 、 、 等单质)联合工艺制备黄钠铁钒[ ],并回收
、 等金属。
(1)滤渣Ⅰ主要含 和 ,请写出热水溶浸时发生反应的化学方程式:_______。
(2)制得黄钠铁矾[ ]的离子方程式为_______。
【答案】(1)
(2)
【解析】镉熔炼碱渣(约含 及 、 、 )用热水溶浸,在碱性环境下反应、过滤,滤
渣Ⅰ主要含 和 ,则热水溶浸反应为氧化锌和氢氧化钠溶液反应,得到滤液I为偏锌酸钠、过量氢
氧化钠混合溶液;铜镉渣(含 、 、 、 等单质)用稀硫酸酸浸, 不溶解、 、 、 与
硫酸反应而溶解,滤液中加入过氧化氢溶液,亚铁离子被氧化为铁离子,预中和、加入碳酸氢铵调pH约为
1.5,得到黄钠铁钒[ ],过滤后,所得滤液含锌离子、镉离子、铵离子、氢离子,再
予以回收利用。
(1)滤渣Ⅰ主要含 和 ,则热水溶浸反应为氧化锌和氢氧化钠溶液反应,得到偏锌酸钠和水、反应
的化学方程式: 。(2) 在 约为1.5时,钠离子、铁离子、硫酸根离子和水反应制得黄钠铁矾[ ],离
子方程式为 。
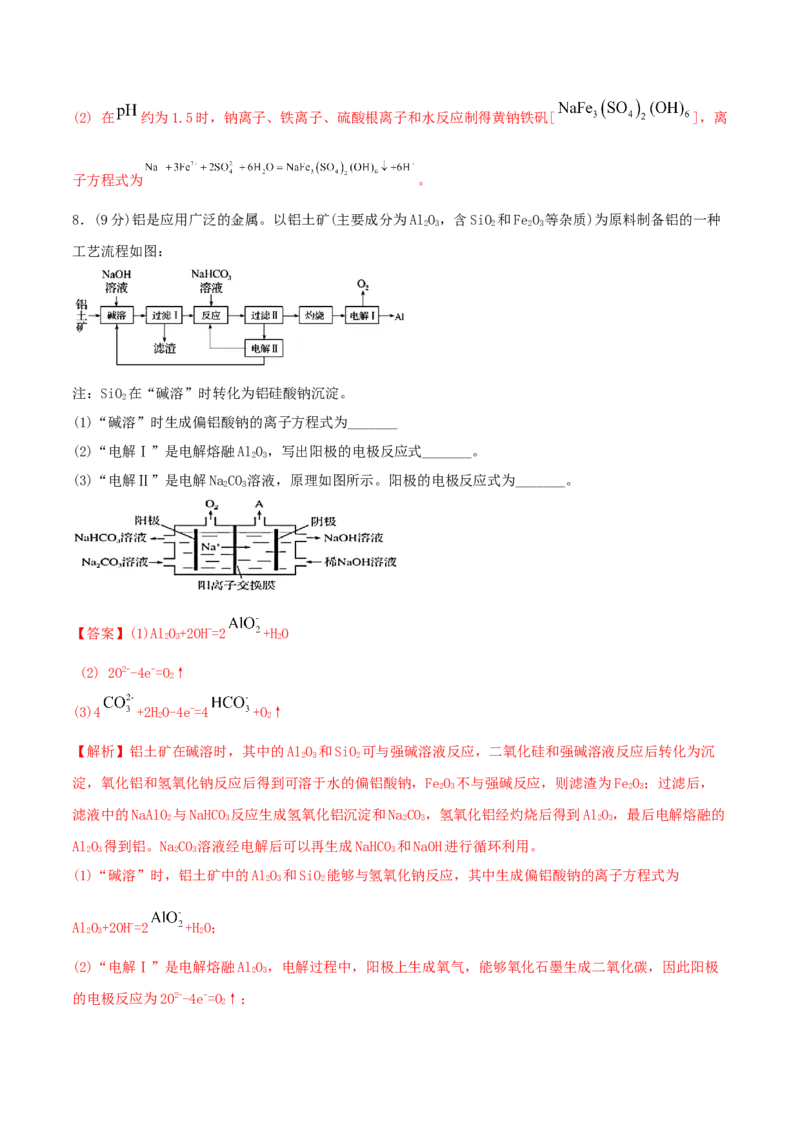
8.(9分)铝是应用广泛的金属。以铝土矿(主要成分为AlO,含SiO 和FeO 等杂质)为原料制备铝的一种
2 3 2 2 3
工艺流程如图:
注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
2
(1)“碱溶”时生成偏铝酸钠的离子方程式为_______
(2)“电解Ⅰ”是电解熔融AlO,写出阳极的电极反应式_______。
2 3
(3)“电解Ⅱ”是电解NaCO 溶液,原理如图所示。阳极的电极反应式为_______。
2 3
【答案】(1)AlO+2OH-=2 +HO
2 3 2
(2) 2O2--4e-=O↑
2
(3)4 +2HO-4e-=4 +O↑
2 2
【解析】铝土矿在碱溶时,其中的AlO 和SiO 可与强碱溶液反应,二氧化硅和强碱溶液反应后转化为沉
2 3 2
淀,氧化铝和氢氧化钠反应后得到可溶于水的偏铝酸钠,FeO 不与强碱反应,则滤渣为FeO;过滤后,
2 3 2 3
滤液中的NaAlO 与NaHCO 反应生成氢氧化铝沉淀和NaCO,氢氧化铝经灼烧后得到AlO,最后电解熔融的
2 3 2 3 2 3
AlO 得到铝。NaCO 溶液经电解后可以再生成NaHCO 和NaOH进行循环利用。
2 3 2 3 3
(1)“碱溶”时,铝土矿中的AlO 和SiO 能够与氢氧化钠反应,其中生成偏铝酸钠的离子方程式为
2 3 2
AlO+2OH-=2 +HO;
2 3 2
(2)“电解Ⅰ”是电解熔融AlO,电解过程中,阳极上生成氧气,能够氧化石墨生成二氧化碳,因此阳极
2 3
的电极反应为2O2--4e-=O↑;
2(3)“电解Ⅱ”是电解NaCO 溶液,阳极上是溶液中的水失电子生成氧气,产生的氢离子与碳酸根离子反应
2 3
生成碳酸氢根离子,电极反应为4 +2HO-4e-=4 +O↑;
2 2
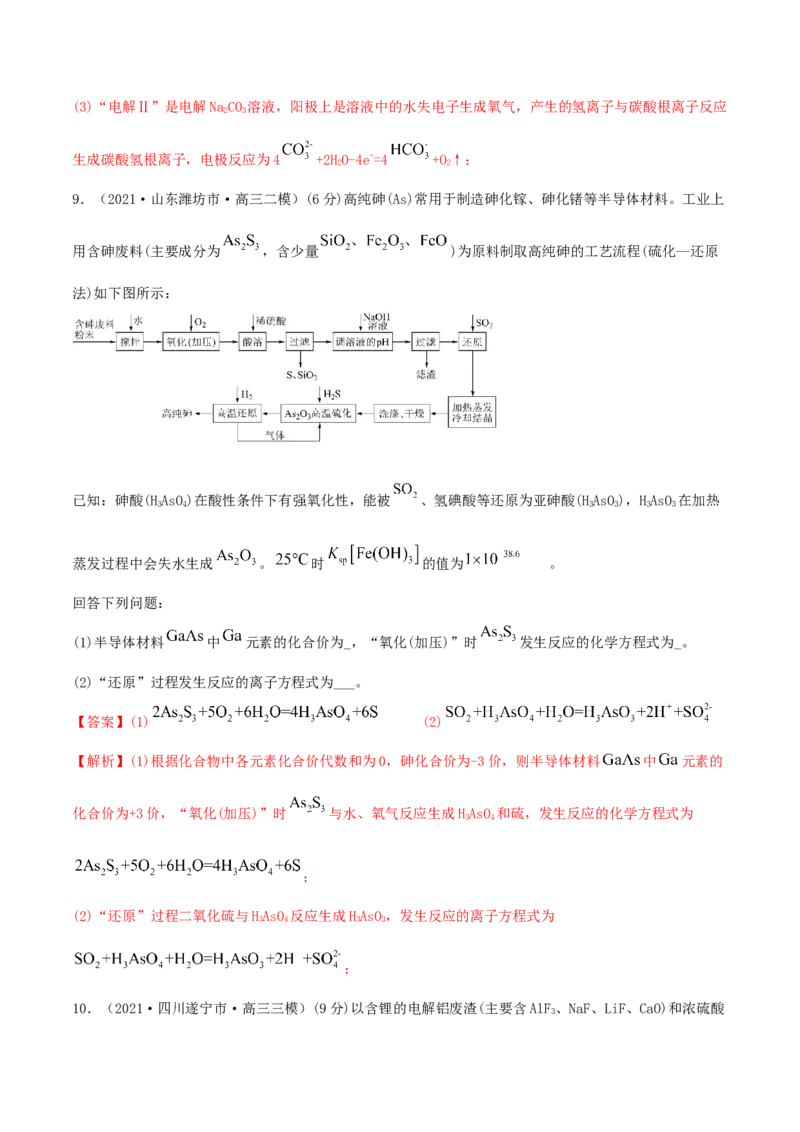
9.(2021·山东潍坊市·高三二模)(6分)高纯砷(As)常用于制造砷化镓、砷化锗等半导体材料。工业上
用含砷废料(主要成分为 ,含少量 )为原料制取高纯砷的工艺流程(硫化—还原
法)如下图所示:
已知:砷酸(HAsO)在酸性条件下有强氧化性,能被 、氢碘酸等还原为亚砷酸(HAsO),HAsO 在加热
3 4 3 3 3 3
蒸发过程中会失水生成 。 时 的值为 。
回答下列问题:
(1)半导体材料 中 元素的化合价为_,“氧化(加压)”时 发生反应的化学方程式为_。
(2)“还原”过程发生反应的离子方程式为___。
【答案】(1) (2)
【解析】(1)根据化合物中各元素化合价代数和为0,砷化合价为-3价,则半导体材料 中 元素的
化合价为+3价,“氧化(加压)”时 与水、氧气反应生成HAsO 和硫,发生反应的化学方程式为
3 4
;
(2)“还原”过程二氧化硫与HAsO 反应生成HAsO,发生反应的离子方程式为
3 4 3 3
;
10.(2021·四川遂宁市·高三三模)(9分)以含锂的电解铝废渣(主要含AlF、NaF、LiF、CaO)和浓硫酸
3为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如下:
已知:LiOH易溶于水,LiCO 微溶于水。回答下列问题:
2 3
(1)碱解反应中,同时得到气体和沉淀,反应的离子方程式为___________。
(2)上述流程得到的副产品冰晶石的化学方程式___________
(3)电池级LiCO 可由高纯度LiOH转化而来。将电池级LiCO 和C、FePO 高温下反应,生成LiFePO 和一种
2 3 2 3 4 4
可燃性气体,该反应的化学方程式为___________。
【答案】(1)2Al3++3CO +3HO=2Al(OH)↓+3CO↑
2 3 2
(2)6HF+NaSO+NaAlO=NaAlF+HSO+2HO
2 4 2 6 2 4 2
(3)LiCO+2C+2Fe PO 2LiFePO+3CO↑
2 3 4 4
【解析】AlF、NaF、LiF、CaO和浓硫酸反应生成硫酸铝、硫酸钠、硫酸锂、硫酸钙和HF气体,硫酸钙微
3
溶于水,水浸得到硫酸铝、硫酸钠、硫酸锂溶液,滤渣1是硫酸钙;向溶液中加入碳酸钠溶液,生成氢氧
化铝沉淀、LiCO 沉淀、二氧化碳气体,过滤,得硫酸钠溶液和固体氧化铝、LiCO,氧化铝、LiCO 固体
2 3 2 3 2 3
加水调浆,加入氧化钙将碳酸锂转化为氢氧化锂溶液,过滤,滤渣2是氢氧化铝,氢氧化锂溶液中通入二
氧化碳生成LiCO 产品;氢氧化铝加入氢氧化钠生成偏铝酸钠,偏铝酸钠、HF、硫酸钠反应生成NaAlF 和
2 3 3 6
HSO。
2 4
(1)碱解反应中,硫酸铝与碳酸钠反应生成氢氧化铝沉淀、二氧化碳气体,反应的离子方程式为2Al3++3CO
+3HO=2Al(OH)↓+3CO↑;
2 3 2
(2) 偏铝酸钠、HF、硫酸钠反应生成NaAlF 和HSO,反应的化学方程式为
3 6 2 4
6HF+NaSO+NaAlO=NaAlF+HSO+2HO;
2 4 2 6 2 4 2
(3)将电池级LiCO 和C、FePO 高温下反应,生成LiFePO 和一种可燃性气体,根据化合价升降规律,可知
2 3 4 4
生成的可燃性气体是CO,该反应的化学方程式为LiCO+2C+2Fe PO 2LiFePO+3CO↑。
2 3 4 411.(2021·宁夏中卫市·高三模拟)(6分)某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Fe及其他不
溶于酸、碱的杂质。现用含镍废催化剂制备NiSO·7HO,其流程图如下:
4 2
部分金属化合物的K 近似值如表所示:
sp
化学式 Fe(OH) Fe(OH) Al(OH) Ni(OH) NiCO
2 3 3 2 3
K 近似值 1.0×10-17 1.0×10-38 1.0×10-34 1.0×10-15 1.0×10-5
sp
回答下列问题:
(1)“碱浸”时发生反应的离子方程式为___________。
(2)析出NiSO·7HO后失去结晶水后得到NiSO 在强碱溶液中用NaC1O氧化,可制得碱性镍镉电池电极材
4 2 4
料NiOOH。该反应的离子方程式为___________。
【答案】(1)2Al+2OH-+2HO=2AlO +3H↑
2 2
(2)2Ni2++ClO—+4OH—=2NiOOH↓+Cl—+HO
2
【解析】由题给流程可知,含镍废催化剂碱浸时,铝与碱溶液反应生成偏铝酸盐,镍、铁和不溶于酸、碱
的杂质不与酸反应,过滤得到含有偏铝酸盐的滤液和含有镍、铁的滤渣;为防止产品中混有杂质,向滤渣
中加入稀硫酸酸浸,镍、铁与稀硫酸反应溶解得到硫酸盐,过滤除去不溶于酸、碱的杂质得到含有硫酸镍
和硫酸亚铁的滤液;向滤液中加入过氧化氢溶液将亚铁离子氧化为铁离子,再调节溶液pH使溶液中铁离子
好完全转化为氢氧化铁沉淀,过滤得到硫酸镍溶液,将硫酸镍溶液加热浓缩、冷却结晶、过滤、洗涤、干
燥得到七水硫酸镍晶体。
(1) “碱浸”时发生的反应为铝与强碱溶液反应生成偏铝酸根离子和氢气,反应的离子方程式为2Al+
2OH-+2HO=2AlO +3H↑,故答案为:2Al+2OH-+2HO=2AlO +3H↑;
2 2 2 2
(2)由题意可知,碱性条件下,溶液中镍离子与次氯酸根离子发生氧化还原反应生成碱式氧化镍、氯离子
和水,反应的离子方程式为2Ni2++ClO—+4OH—=2NiOOH↓+Cl—+HO;
2
12.(2021·山东高三模拟)(6分)三氧化二钴(CoO)主要用作颜料、釉料、磁性材料、催化剂和氧化剂
2 3
等。以含钴废料(主要成分为CoO,含有少量MnO、NiO、FeO)为原料制备CoO 的流程如图所示。
2 3 2 3 4 2 3已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+等。
Ⅱ.部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
沉淀物 Fe(OH) Co(OH) Ni(OH)
3 2 2
完全沉淀时的pH 3.7 9.0 9.2
①“酸浸”时发生的主要反应是___(写离子方程式)。
②写出高温煅烧时发生的化学反应方程式___。
【答案】①CoO+HO+4H+=2Co2++3HO+O↑ ②2Co(OH)CO+O 2CoO+2HO+2CO
2 3 2 2 2 2 2 2 3 22 2 3 2 2
【解析】由题给流程可知,向研磨后的含钴废料中加入硫酸和双氧水,酸性条件下,氧化钴与双氧水发生
氧化还原反应生成亚钴离子,四氧化三铁与双氧水发生氧化还原反应生成铁离子,氧化亚镍溶于硫酸生成
亚镍离子,二氧化锰不溶解,过滤得到含有氢离子、亚钴离子、铁离子、亚镍离子的酸浸液和二氧化锰;
调节酸浸液的pH为3.7,铁离子转化为氢氧化铁沉淀,过滤得到含有亚钴离子、亚镍离子的滤液和滤渣1
氢氧化铁;向滤液中加入萃取剂,萃取分液得到含有亚钴离子的水相和含有亚镍离子的有机相;向水相中
加入氨水和碳酸氢铵溶液,亚钴离子离子转化为Co(OH)CO 沉淀,过滤得到含有硫酸铵的滤液和
2 2 3
Co(OH)CO 沉淀;高温煅烧,Co(OH)CO 与空气中的氧气发生氧化还原反应生成氧化钴、二氧化碳和水。
2 2 3 2 2 3
①含钴废料中含有CoO、NiO、FeO,“酸浸”后的溶液中含有Co2+,“酸浸”时发生的主要反应为CoO
2 3 3 4 2 3
氧化HO,生成O 和Co2+,反应的离子方程式为CoO+HO+4H+=2Co2++3HO+O↑;
2 2 2 2 3 2 2 2 2
②高温煅烧时,Co(OH)CO 被氧化为CoO,所以反应的化学方程式为2Co(OH)CO+O
2 2 3 2 3 2 2 3 22
2CoO+2HO+2CO;
2 3 2 2
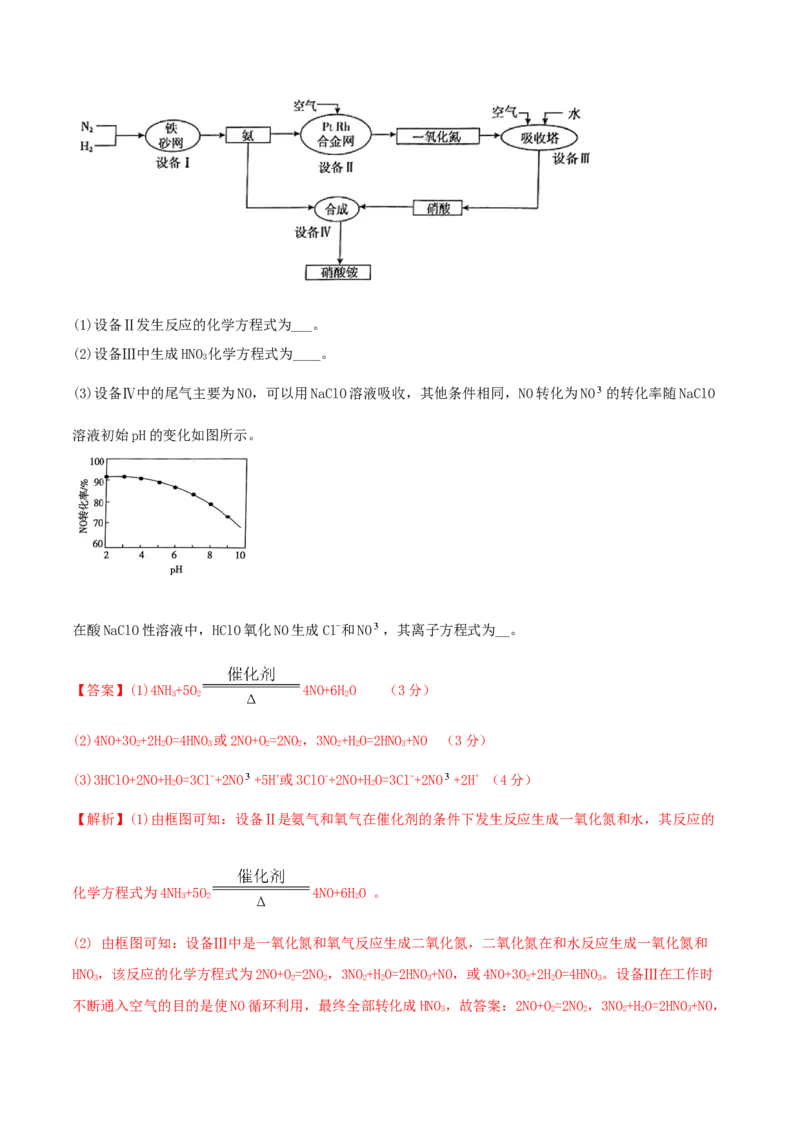
13.(2021·福建高三模拟)(10分)工业上制取硝酸铵的流程图如图,回答下列问题:(1)设备Ⅱ发生反应的化学方程式为___。
(2)设备Ⅲ中生成HNO 化学方程式为____。
3
(3)设备Ⅳ中的尾气主要为NO,可以用NaClO溶液吸收,其他条件相同,NO转化为NO 的转化率随NaClO
溶液初始pH的变化如图所示。
在酸NaClO性溶液中,HClO氧化NO生成Cl-和NO ,其离子方程式为__。
【答案】(1)4NH+5O 4NO+6HO (3分)
3 2 2
(2)4NO+3O+2HO=4HNO 或2NO+O=2NO,3NO+HO=2HNO+NO (3分)
2 2 3 2 2 2 2 3
(3)3HClO+2NO+HO=3Cl-+2NO +5H+或3ClO-+2NO+HO=3Cl-+2NO +2H+ (4分)
2 2
【解析】(1)由框图可知:设备Ⅱ是氨气和氧气在催化剂的条件下发生反应生成一氧化氮和水,其反应的
化学方程式为4NH+5O 4NO+6HO 。
3 2 2
(2) 由框图可知:设备Ⅲ中是一氧化氮和氧气反应生成二氧化氮,二氧化氮在和水反应生成一氧化氮和
HNO,该反应的化学方程式为2NO+O=2NO,3NO+HO=2HNO+NO,或4NO+3O+2HO=4HNO。设备Ⅲ在工作时
3 2 2 2 2 3 2 2 3
不断通入空气的目的是使NO循环利用,最终全部转化成HNO,故答案:2NO+O=2NO,3NO+HO=2HNO+NO,
3 2 2 2 2 3或4NO+3O+2HO=4HNO;可使NO循环利用,全部转化成HNO。
2 2 3 3
(3)在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO ,其离子方程式为3HClO+2NO+HO=3Cl-+2NO +5H+或
2
3ClO-+2NO+HO=3Cl-+2NO +2H+。
2