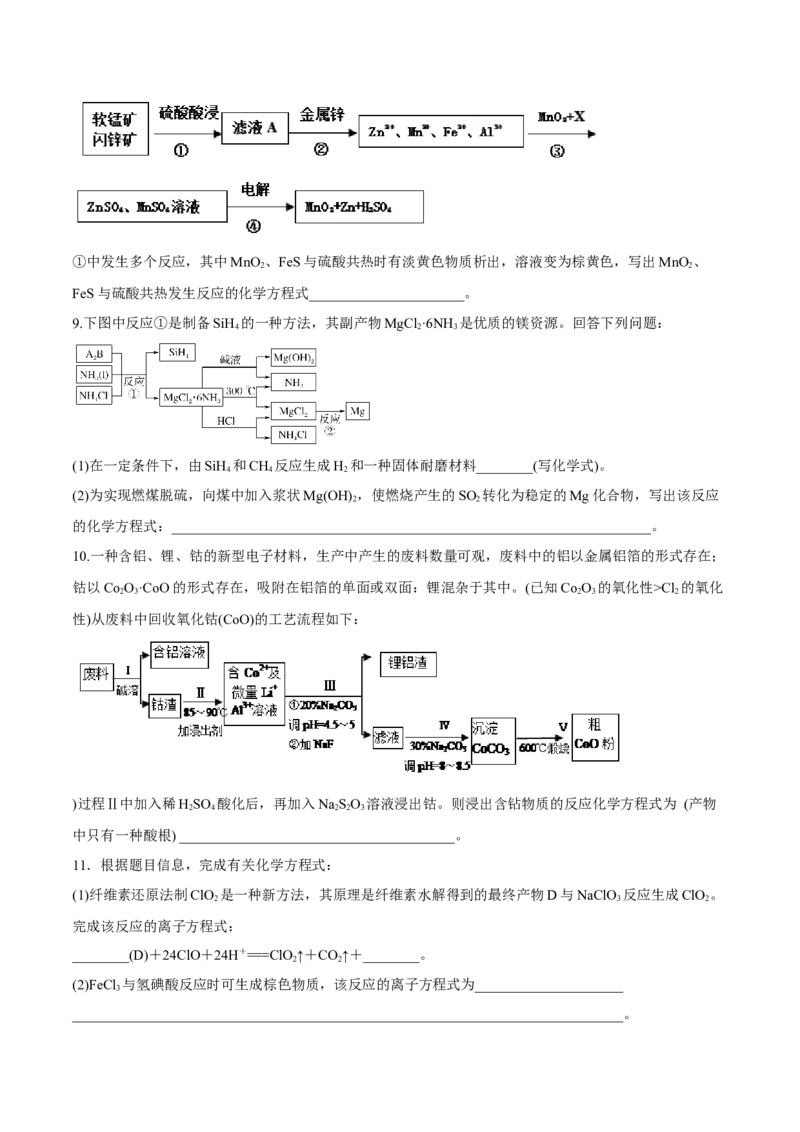文档内容
专题讲座(二)陌生化学方程式书写
【练基础】
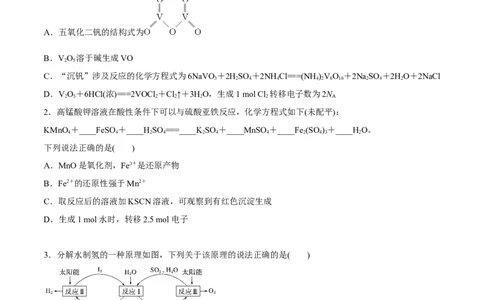
1.五氧化二钒(V O)是一种两性氧化物,具有强氧化性,其制备方法如下图所示。下列关于五氧化二钒的
2 5
说法中错误的是( )
A.五氧化二钒的结构式为
B.VO 溶于碱生成VO
2 5
C.“沉钒”涉及反应的化学方程式为6NaVO +2HSO +2NH Cl===(NH)VO +2NaSO +2HO+2NaCl
3 2 4 4 4 2 6 16 2 4 2
D.VO+6HCl(浓)===2VOCl +Cl↑+3HO,生成1 mol Cl 转移电子数为2N
2 5 2 2 2 2 A
2.高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,化学方程式如下(未配平):
KMnO +____FeSO +____HSO ===____K SO +____MnSO +____Fe (SO )+____HO。
4 4 2 4 2 4 4 2 4 3 2
下列说法正确的是( )
A.MnO是氧化剂,Fe3+是还原产物
B.Fe2+的还原性强于Mn2+
C.取反应后的溶液加KSCN溶液,可观察到有红色沉淀生成
D.生成1 mol水时,转移2.5 mol电子
3.分解水制氢的一种原理如图,下列关于该原理的说法正确的是( )
A.反应过程中化合价改变的元素共有H、O、S
B.涉及的反应类型只有分解反应和化合反应
C.理论上,每生成16 g O,就能得到标准状况下22.4 L H
2 2
D.理论上,每分解18 g HO,就需向体系内再补充32 g SO
2 2
4.KClO 可以和草酸(H C O)、硫酸反应生成高效的消毒杀菌剂ClO ,还生成CO 和KHSO 等物质。写出
3 2 2 4 2 2 4该反应的化学方程式___________________________________。
5.(1)工业上,通过如下转化可制得KClO 晶体:
3
NaCl溶液――→NaClO 溶液――→KClO 晶体
3 3
完成Ⅰ中反应的总化学方程式:NaCl+HO NaClO+________。
2 3
(2)硫化氢具有还原性,可以和许多氧化剂反应。在酸性条件下,HS和KMnO 反应生成S、MnSO 、
2 4 4
KSO 和HO,写出该反应的化学方程式______________________________。
2 4 2
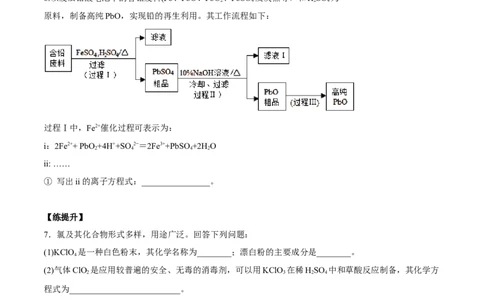
6.以废旧铅酸电池中的含铅废料(Pb、PbO、PbO 、PbSO 及炭黑等)和HSO 为
2 4 2 4
原料,制备高纯PbO,实现铅的再生利用。其工作流程如下:
过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++ PbO +4H++SO2−=2Fe3++PbSO+2H O
2 4 4 2
ii: ……
① 写出ii的离子方程式:________________。
【练提升】
7.氯及其化合物形式多样,用途广泛。回答下列问题:
(1)KClO 是一种白色粉末,其化学名称为________;漂白粉的主要成分是________。
4
(2)气体ClO 是应用较普遍的安全、无毒的消毒剂,可以用KClO 在稀HSO 中和草酸反应制备,其化学方
2 3 2 4
程式为__________________________。
(3)氨气可以检验输送氯气的管道是否泄漏,试写出化学反应方程式:
________________________________。
(4)向200 mL NaOH溶液中通入一定量Cl 恰好完全反应,得到0.1 mol NaClO 和0.1 mol NaClO 则原
2 3 ,
NaOH溶液的物质的量浓度为________。
8.软锰矿的主要成分为MnO ,含少量Al O 和SiO。闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂
2 2 3 2
质。现以软锰矿和闪锌矿为原料制备MnO 和Zn,其简化流程如下(中间产物的固体部分已经略去)。
2①中发生多个反应,其中MnO 、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO 、
2 2
FeS与硫酸共热发生反应的化学方程式______________________。
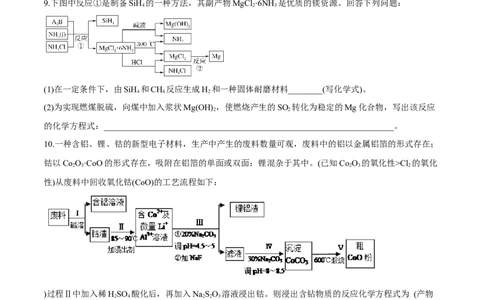
9.下图中反应①是制备SiH 的一种方法,其副产物MgCl ·6NH 是优质的镁资源。回答下列问题:
4 2 3
(1)在一定条件下,由SiH 和CH 反应生成H 和一种固体耐磨材料________(写化学式)。
4 4 2
(2)为实现燃煤脱硫,向煤中加入浆状Mg(OH) ,使燃烧产生的SO 转化为稳定的Mg化合物,写出该反应
2 2
的化学方程式:____________________________________________________________________。
10.一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;
钴以Co O·CoO的形式存在,吸附在铝箔的单面或双面:锂混杂于其中。(已知Co O 的氧化性>Cl 的氧化
2 3 2 3 2
性)从废料中回收氧化钴(CoO)的工艺流程如下:
)过程Ⅱ中加入稀HSO 酸化后,再加入NaSO 溶液浸出钴。则浸出含钻物质的反应化学方程式为 (产物
2 4 2 2 3
中只有一种酸根) _______________________________________。
11.根据题目信息,完成有关化学方程式:
(1)纤维素还原法制ClO 是一种新方法,其原理是纤维素水解得到的最终产物D与NaClO 反应生成ClO 。
2 3 2
完成该反应的离子方程式:
________(D)+24ClO+24H+===ClO ↑+CO↑+________。
2 2
(2)FeCl 与氢碘酸反应时可生成棕色物质,该反应的离子方程式为_____________________
3
______________________________________________________________________________。高铁酸钾(K FeO)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl 与KClO在强碱性条件下反
2 4 3
应可制取KFeO,其反应的离子方程式为__________________________
2 4
_____________________________________________________________________________。
(3)Na S溶液长期放置有硫析出,原因为__________________________________________
2
____________________________________________________________(用离子方程式表示)。
(4)PbO 与浓盐酸共热生成黄绿色气体,反应的离子方程式为_______________________
2
____________________________________________________________________________。
12.磷化铝(AlP)和磷化氢(PH )都是粮食储备常用的高效熏蒸杀虫剂。
3
(1)磷元素位于元素周期表第________周期________族。AlP遇水蒸气会发生反应放出PH 气体,该反应的
3
另一种产物的化学式为________。
(2)PH 具有强还原性,能与CuSO 溶液反应,配平该反应的化学方程式:
3 4
CuSO +PH +HO===Cu P↓+HPO +HSO
4 3 2 3 3 4 2 4
(3)工业制备PH 的流程如图所示。
3
①白磷和烧碱溶液反应的化学方程式为____________________________________________
_____________________________,次磷酸属于________(填“一”“二”或“三”)元酸。
②若起始时有1 mol P 参加反应,则整个工业流程中共生成________mol PH 。(不考虑产物的损失)
4 3
13.(1)据报道,有一种叫Thibacillus Ferroxidans的细菌在有氧气存在的酸性溶液中,可将黄铜矿CuFeS
2
氧化成硫酸盐:4CuFeS+2HSO +17O===4CuSO+2Fe (SO )+2HO。利用反应后的溶液,按如下流程
2 2 4 2 4 2 4 3 2
可制备胆矾(CuSO ·5H O),在实验室中,设计两个原理不同的方案,从溶液B中提炼金属铜(要求:一种方
4 2
案只用一个反应来完成)。写出两种方案中涉及的化学方程式: 。
(2)Cu S是火法炼铜的重要原料之一,下面是由Cu S冶炼铜及制取CuSO ·5H O的流程图。火法炼铜的
2 2 4 2
反应原理是___________ (用化学方程式表示)。向Cu O、CuO中加入足量稀硫酸得到的体系
2
A中溶液呈蓝色,且有红色物质生成,写出生成红色物质的离子方程式:___________。
Cu S――→Cu――→Cu O、CuO――→A――→B――→胆矾
2 2
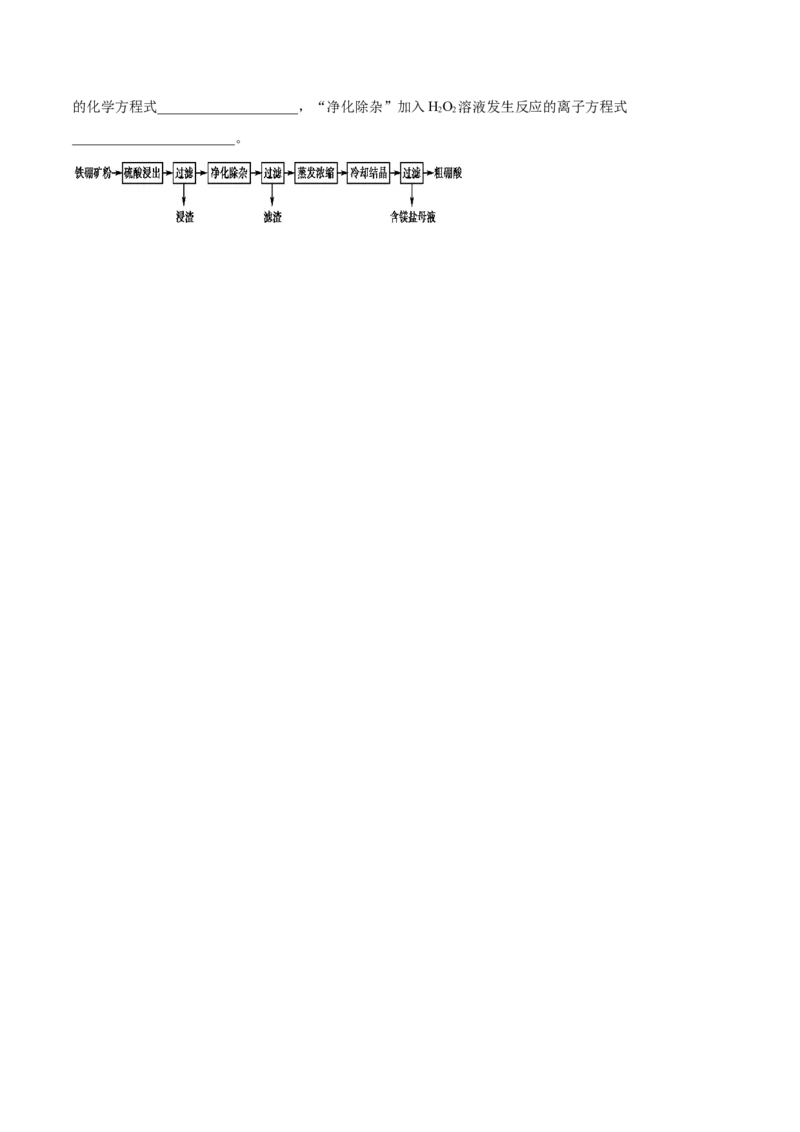
14.硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为MgB O·H O和Fe O,还有少量Fe O、
2 2 5 2 3 4 2 3
FeO、CaO、Al O 和SiO 等)为原料制备硼酸(H BO)的工艺流程如图所示,写出MgB O·H O与硫酸反应
2 3 2 3 3 2 2 5 2的化学方程式____________________,“净化除杂”加入HO 溶液发生反应的离子方程式
2 2
_______________________。