文档内容
专题讲座(四) 常见气体的实验室制备、净化和收集(精讲)
【考情分析】
在近几年的高考气体制备及性质验证实验命题中,尤其是全国I卷、北京卷、江苏卷、浙江卷、海南卷
等都出现过三颈瓶、双耳球、恒压滴液漏斗等陌生仪器的使用,这些仪器属于不常用仪器,同时在试题中
还常出现一些仪器的创新使用。这类题通过装置重新组合扩充的方式,考查考生全面的系统的知识,培养
了考生的实验创新精神。如将传统实验中涉及的实验仪器和用品进行有效替换,以提高化学实验的效果,
但考生往往因为装置新颖,药品在平时的学习中没有见过,在解题时形成了心理压力,导致不能静心分析,
去伪存真,从而失分较多。预计今后高考命题仍将会以仪器装置和制备方法等的创新为命题热点。
【核心素养分析】
宏观辨识与微观探析:能根据气体的性质,辨识发生装置、净化装置、收集装置、尾气处理的选择,能解
释这样选择和连接规律。
科学探究与创新意识:将化学实验仪器及装置运用组合法、扩充法或替代法等,进行重新组合或者拆分,
来进行实验研究,解决实际问题。
科学态度与社会责任:具有安全意识,严谨求实的科学态度,具有探索未知、崇尚真理的意识和保护环境
的可持续发展的意识。
【知识梳理】
智能点一 常见气体的制备
1.气体制备实验的基本思路
(1)根据反应物的状态及反应条件选择气体发生装置;
(2)根据制备气体及气体杂质的性质选择气体净化装置;
(3)根据制备气体的性质选择干燥剂及干燥装置;
(4)根据制备气体的水溶性及气体的密度选择收集方法及收集装置;
(5)根据制备气体的毒性选择尾气吸收剂及吸收装置。
2.气体制备实验的操作顺序
(1)仪器安装
①由下到上
(如制氯气的发生装置安装顺序是:放铁架台→摆酒精灯→固定铁圈→放置石棉网→固定圆底烧瓶)。
②从左到右
(如制氯气:发生装置→除杂装置→干燥装置→性质探究或收集装置→尾气处理装置(注意防倒吸)。
③先塞后定
(把带导管的胶塞在烧瓶固定前塞好,以免烧瓶固定后因不宜用力而塞不紧或因用力过猛而损坏仪器)。
(2)加试剂顺序
固体先放入,液体后滴加(即先固后液)。
(3)其他操作顺序及连接顺序⑩
①先检验气密性,后装入药品(便于在装置漏气时进行调整或更换仪器),最后点燃酒精灯(所有准备工作完毕后);
②洗气瓶:在连接导管时,应长进短出;
③量气装置的导管应短进长出;
④干燥管应大口进小口出;
⑤U形管:无前后;
⑥加热玻璃管:无前后。
⑦有些实验为防倒吸,往往最后停止加热或最后停止通气;有些实验为防氧化往往最后停止通气。
⑧仪器拆卸的一般过程:从右到左,自上而下,先拆主体,后拆部件。
⑨净化气体时,一般先除去有毒、有刺激性气味的气体,后除去无毒、无气味的气体,最后除去水蒸气。
⑩制备易潮解的物质时,装置最后要连干燥装置。
3.常见气体的发生装置
根据反应物状态和反应条件我们主要掌握以下三类气体发生装置:
(1)固体+固体――→气体:可选择 等装置,能制备O、NH 、CH 等;
2 3 4
操作注意事项①试管要干燥;②试管口略低于试管底;③加热时先预热再固定加热;④用KMnO 制取O 时,
4 2
需在管口处塞一小团棉花。
(2)固(或液)体+液体――→气体:可选择 等装置,能制备Cl、C H、NH 等;
2 2 4 3
(3)固体+液体―→气体:可选择 、 、 等装置,能制备H 、NH 、CO 、
2 3 2
O 等。
2
4.气体的干燥、净化装置
(1)除杂试剂选择的依据:主体气体和杂质气体性质上的差异,如溶解性、酸碱性、氧化性、还原性。
(2)除杂原则:①不损失主体气体;②不引入新的杂质气体;③在密闭装置内进行;④先除易除的杂质气体。
(3)气体净化与干燥的先后顺序
1)若采用溶液除杂:应该是除杂在前,干燥在后。其原因是:气体除杂过程中会从溶液中带入水蒸气,干
燥剂可除去水蒸气。
如实验室中利用大理石与稀盐酸反应制备 CO ,欲制得干燥、纯净的CO ,可先将产生的气体通过饱和
2 2
NaHCO 溶液,除去混入其中的HCl气体,再通过浓硫酸除去水蒸气。
3
2)若采用加热除杂:则一般是干燥在前。如N 中混有O 、CO 、HO(g),可先将混合气体通过碱石灰,除去
2 2 2 2
CO 和HO(g),再将从干燥管中导出的气体通过装有灼热铜网的硬质玻璃管,除去O,即可得到干燥、纯净
2 2 2
的N。若将混合气体先通过灼热的铜网,因气体中混有水蒸气,易使硬质玻璃管炸裂。
2
(4)根据制备气体及气体杂质的性质选择如下气体净化装置及干燥装置:
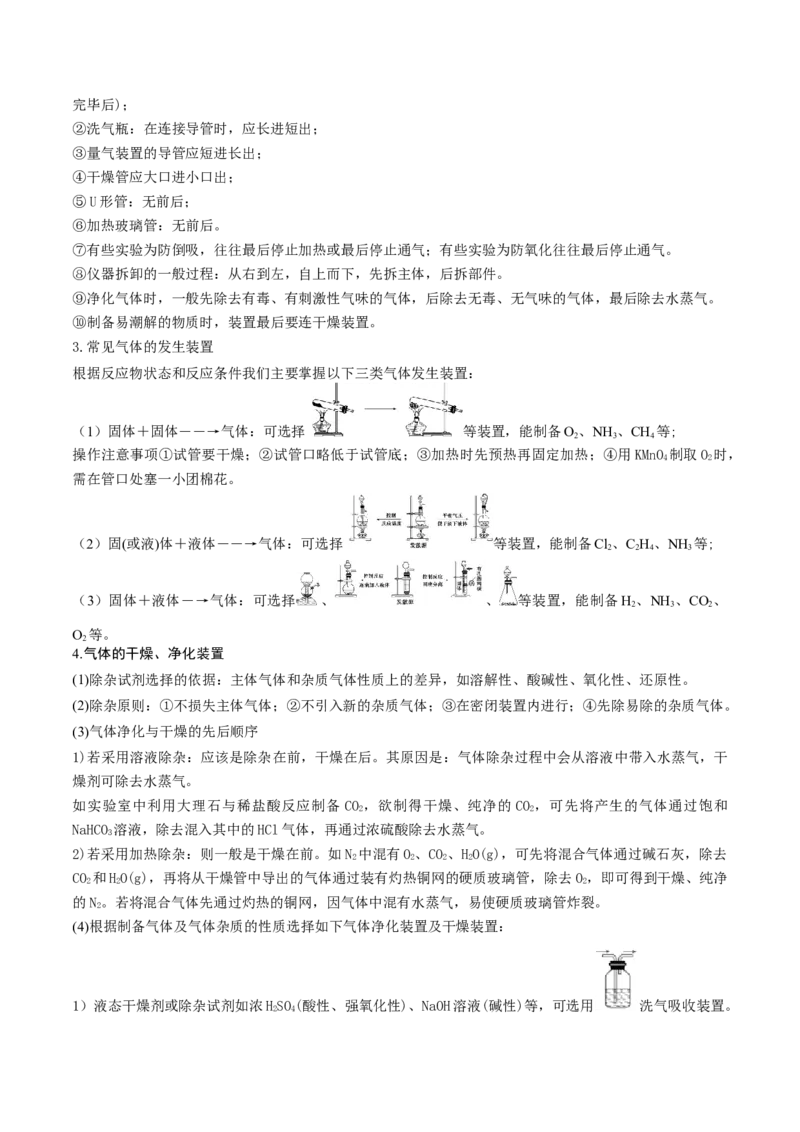
1)液态干燥剂或除杂试剂如浓HSO(酸性、强氧化性)、NaOH溶液(碱性)等,可选用 洗气吸收装置。
2 42)固态干燥剂如无水氯化钙(中性)、碱石灰(碱性)等,可选用 干燥管或 U形管吸收装置。
3)固态除杂试剂如Cu、CuO、Mg等,需加热,可选用 加热的硬质玻璃管吸收装置。
【注意】净化气体遵循的原则:不损失要净化的气体,不引入新的杂质气体。
5.气体的收集方法及收集装置
根据制备气体的水溶性及气体的密度选择收集方法及收集装置:
(1)排液法:难溶于水(或某溶液)或微溶于水(或某溶液),又不与其反应的气体可用排液法收集,选用
、 等收集装置收集。用该装置可收集 O 、H 、Cl(饱和 NaCl 溶液)、NO、CO(饱和
2 2 2 2
NaHCO 溶液)、CO、C H、C H 等气体。
3 2 2 2 4
(2)向上排空气法:密度大于空气且不与空气中的成分反应的气体可用向上排空气法收集,选用
等收集装置收集。用该装置可收集Cl、SO 、NO 、CO 等气体。
2 2 2 2
(2)向下排空气法:密度小于空气且不与空气中的成分反应的气体可用向下排空气法收集,选用
等收集装置收集。用该装置可收集H、NH 、CH 等气体。
2 3 4
6.气体的量取装置
对难溶于水且不与水反应的气体,往往利用量筒或滴定管组装如图所示的装置量取其体积。
7.尾气的处理
(1)原因:有些气体有毒或有可燃性,任其逸散到空气中,会污染空气或者引发火灾、爆炸等灾害。
(2)处理方法:一般根据气体的相关性质,使其转化为非气态物质或无毒物质,如酸性有毒气体用碱溶液吸
收,可燃性气体用点燃等措施。实验室中常见有毒气体的处理方法如下表:
Cl SO NO HS HCl NH CO NO
2 2 2 2 3
CuSO 溶液或NaOH 与O 混合后通
4 2
NaOH溶液 水 水或浓硫酸 点燃
溶液 入NaOH溶液
(3)直接排空处理:主要是针对无毒、无害气体的处理,如N、O、CO 等。
2 2 2
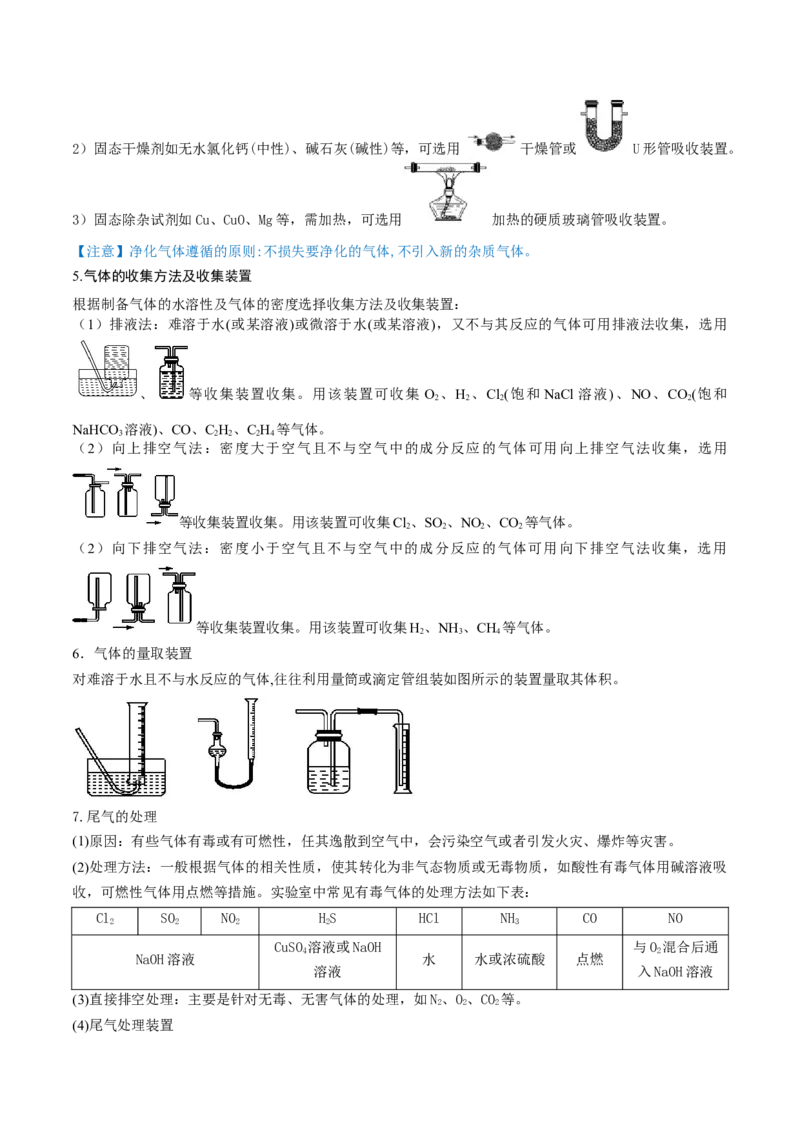
(4)尾气处理装置①在水中溶解度较小的有毒气体,多数可通入盛有某种试剂的烧杯中被吸收除去(如图甲),如Cl 、NO 均
2 2
可通入NaOH溶液中除去。
②某些可燃性气体可用点燃(如图丙)或转化的方法除去,如CO、H 可点燃或通过灼热的CuO除去。
2
③某些可燃性气体可以采用收集的方法除去(如图丁),如CH、CH、H、CO等。
4 2 4 2
④对于溶解度很大、吸收速率很快的气体,吸收时应防止倒吸,典型装置如图乙。常见的防倒吸装置还有
如下改进装置(以NH 的吸收为例,未注明的液体为水)。
3
智能点二 装置的改进或创新
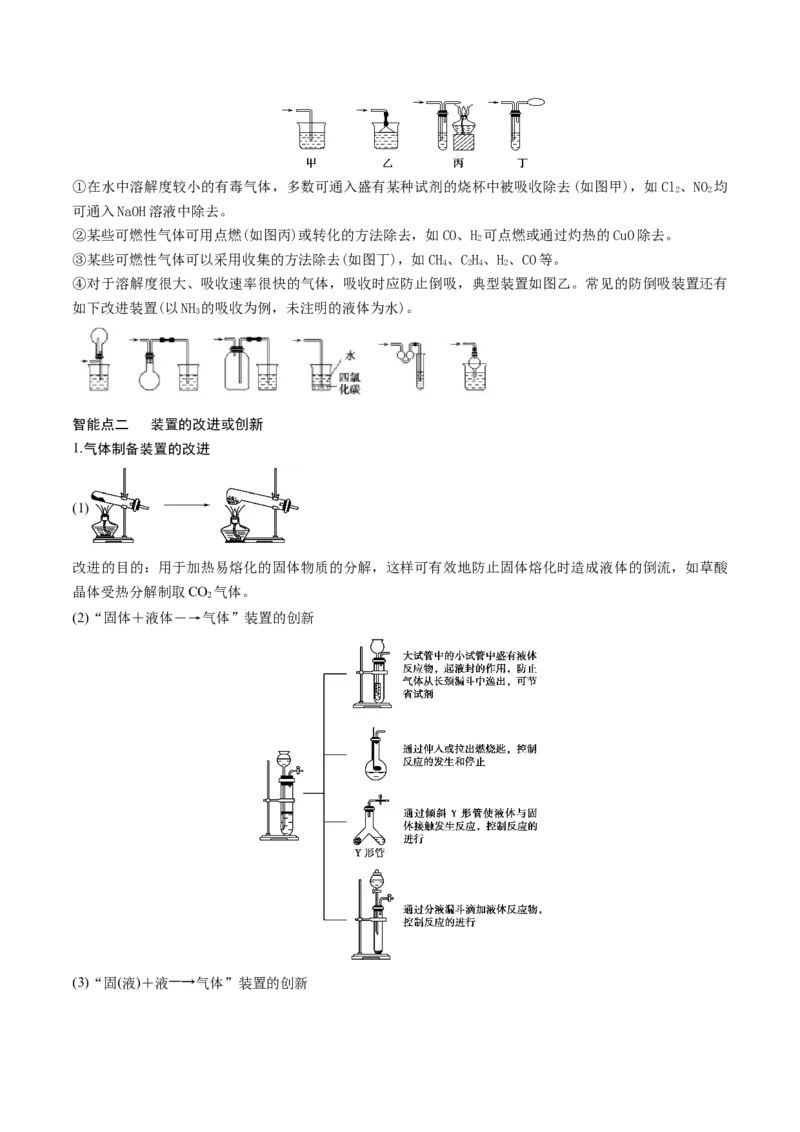
1.气体制备装置的改进
(1)
改进的目的:用于加热易熔化的固体物质的分解,这样可有效地防止固体熔化时造成液体的倒流,如草酸
晶体受热分解制取CO 气体。
2
(2)“固体+液体―→气体”装置的创新
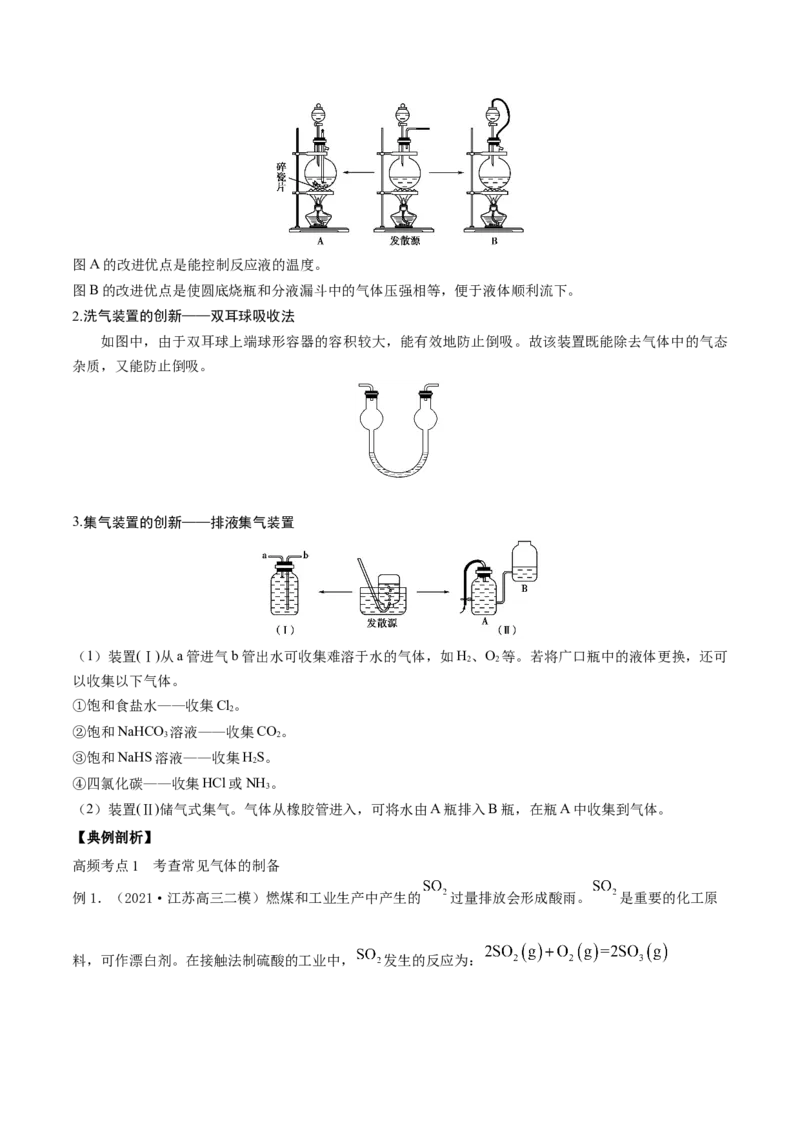
(3)“固(液)+液――→气体”装置的创新图A的改进优点是能控制反应液的温度。
图B的改进优点是使圆底烧瓶和分液漏斗中的气体压强相等,便于液体顺利流下。
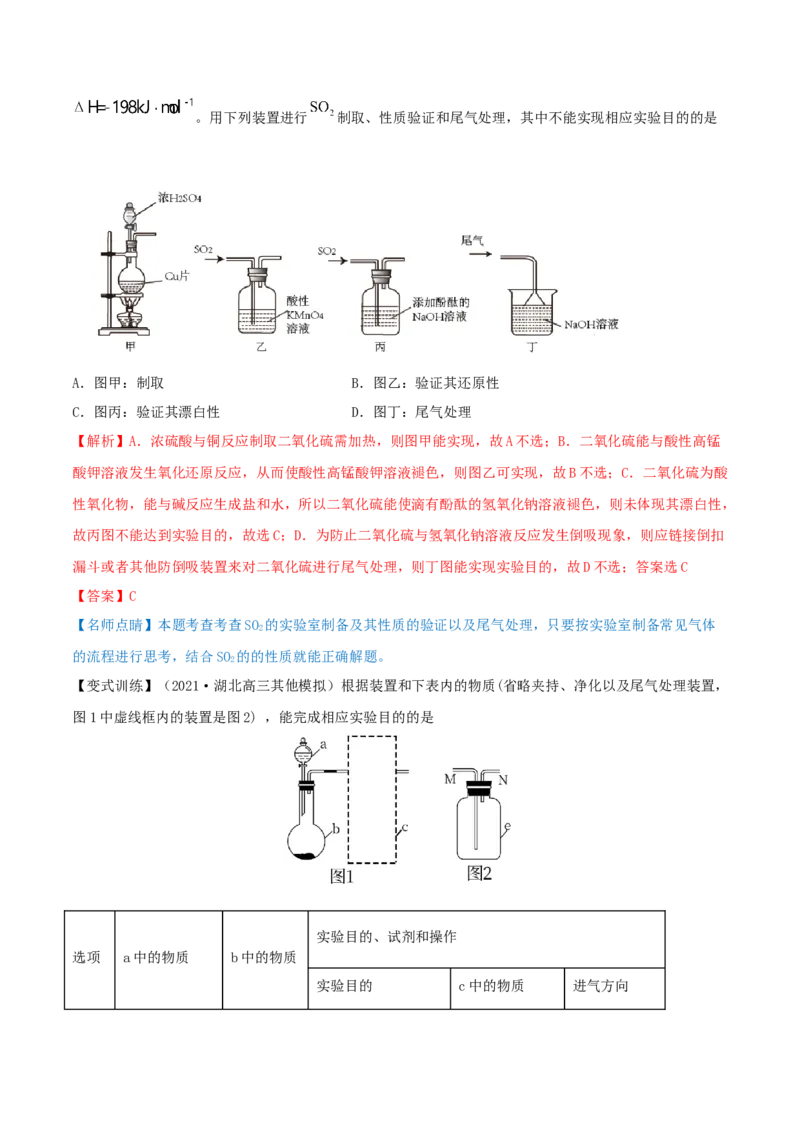
2.洗气装置的创新——双耳球吸收法
如图中,由于双耳球上端球形容器的容积较大,能有效地防止倒吸。故该装置既能除去气体中的气态
杂质,又能防止倒吸。
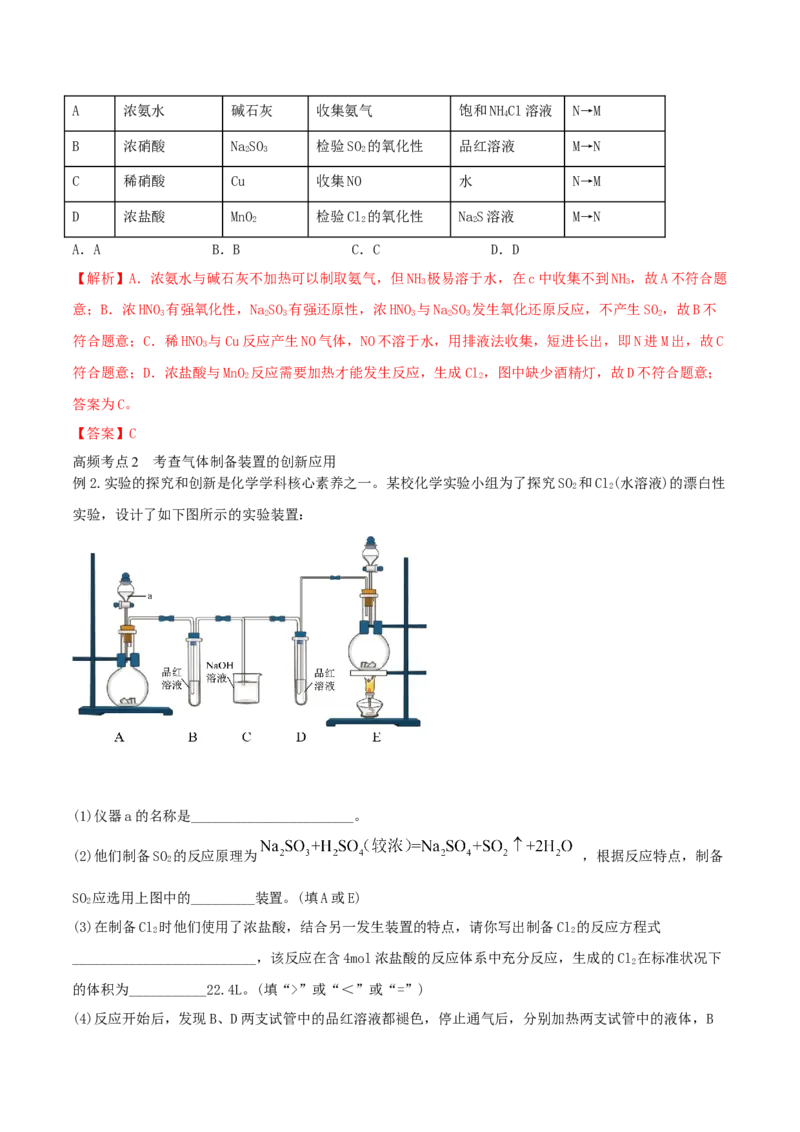
3.集气装置的创新——排液集气装置
(1)装置(Ⅰ)从a管进气b管出水可收集难溶于水的气体,如H 、O 等。若将广口瓶中的液体更换,还可
2 2
以收集以下气体。
①饱和食盐水——收集Cl。
2
②饱和NaHCO 溶液——收集CO。
3 2
③饱和NaHS溶液——收集HS。
2
④四氯化碳——收集HCl或NH 。
3
(2)装置(Ⅱ)储气式集气。气体从橡胶管进入,可将水由A瓶排入B瓶,在瓶A中收集到气体。
【典例剖析】
高频考点1 考查常见气体的制备
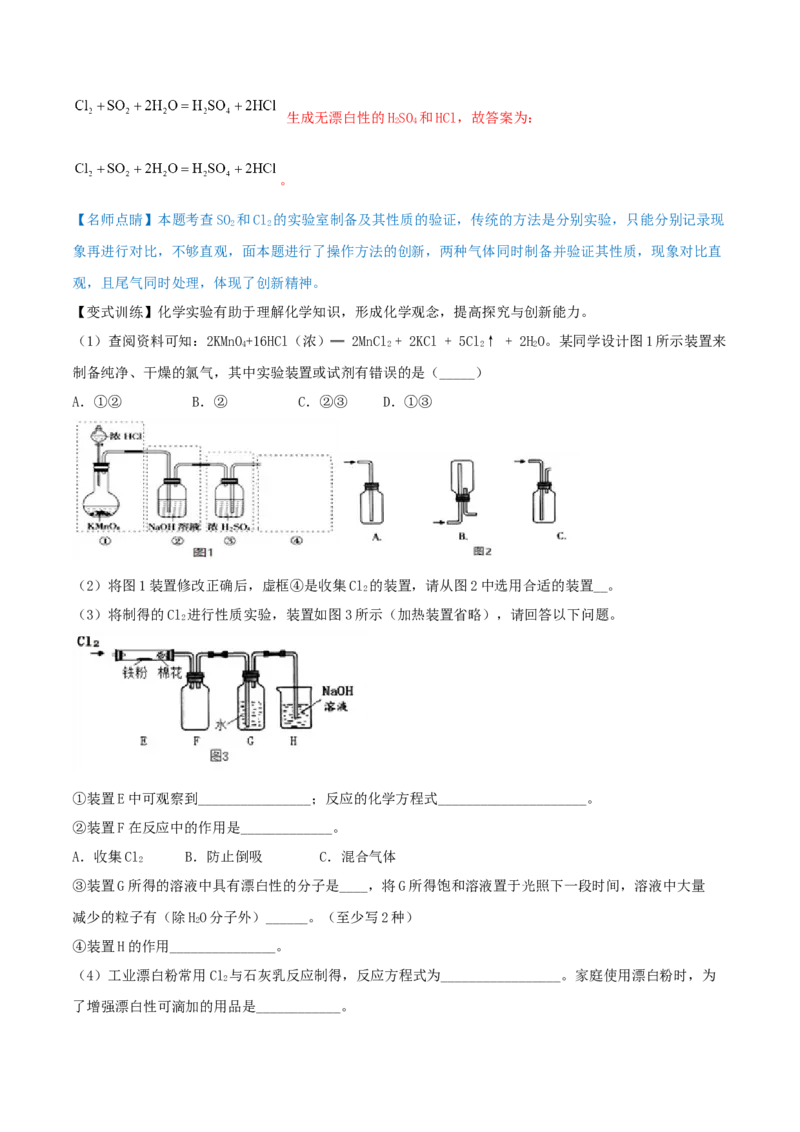
例1.(2021·江苏高三二模)燃煤和工业生产中产生的 过量排放会形成酸雨。 是重要的化工原
料,可作漂白剂。在接触法制硫酸的工业中, 发生的反应为:。用下列装置进行 制取、性质验证和尾气处理,其中不能实现相应实验目的的是
A.图甲:制取 B.图乙:验证其还原性
C.图丙:验证其漂白性 D.图丁:尾气处理
【解析】A.浓硫酸与铜反应制取二氧化硫需加热,则图甲能实现,故A不选;B.二氧化硫能与酸性高锰
酸钾溶液发生氧化还原反应,从而使酸性高锰酸钾溶液褪色,则图乙可实现,故B不选;C.二氧化硫为酸
性氧化物,能与碱反应生成盐和水,所以二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,则未体现其漂白性,
故丙图不能达到实验目的,故选C;D.为防止二氧化硫与氢氧化钠溶液反应发生倒吸现象,则应链接倒扣
漏斗或者其他防倒吸装置来对二氧化硫进行尾气处理,则丁图能实现实验目的,故D不选;答案选C
【答案】C
【名师点睛】本题考查考查SO 的实验室制备及其性质的验证以及尾气处理,只要按实验室制备常见气体
2
的流程进行思考,结合SO 的的性质就能正确解题。
2
【变式训练】(2021·湖北高三其他模拟)根据装置和下表内的物质(省略夹持、净化以及尾气处理装置,
图1中虚线框内的装置是图2) ,能完成相应实验目的的是
实验目的、试剂和操作
选项 a中的物质 b中的物质
实验目的 c中的物质 进气方向A 浓氨水 碱石灰 收集氨气 饱和NHCl溶液 N→M
4
B 浓硝酸 NaSO 检验SO 的氧化性 品红溶液 M→N
2 3 2
C 稀硝酸 Cu 收集NO 水 N→M
D 浓盐酸 MnO 检验Cl 的氧化性 NaS溶液 M→N
2 2 2
A.A B.B C.C D.D
【解析】A.浓氨水与碱石灰不加热可以制取氨气,但NH 极易溶于水,在c中收集不到NH,故A不符合题
3 3
意;B.浓HNO 有强氧化性,NaSO 有强还原性,浓HNO 与NaSO 发生氧化还原反应,不产生SO,故B不
3 2 3 3 2 3 2
符合题意;C.稀HNO 与Cu反应产生NO气体,NO不溶于水,用排液法收集,短进长出,即N进M出,故C
3
符合题意;D.浓盐酸与MnO 反应需要加热才能发生反应,生成Cl,图中缺少酒精灯,故D不符合题意;
2 2
答案为C。
【答案】C
高频考点2 考查气体制备装置的创新应用
例2.实验的探究和创新是化学学科核心素养之一。某校化学实验小组为了探究SO 和Cl(水溶液)的漂白性
2 2
实验,设计了如下图所示的实验装置:
(1)仪器a的名称是_______________________。
(2)他们制备SO 的反应原理为 ,根据反应特点,制备
2
SO 应选用上图中的_________装置。(填A或E)
2
(3)在制备Cl 时他们使用了浓盐酸,结合另一发生装置的特点,请你写出制备Cl 的反应方程式
2 2
__________________________,该反应在含4mol浓盐酸的反应体系中充分反应,生成的Cl 在标准状况下
2
的体积为___________22.4L。(填“>”或“<”或“=”)
(4)反应开始后,发现B、D两支试管中的品红溶液都褪色,停止通气后,分别加热两支试管中的液体,B试管中的现象是_______________。
(5)C烧杯中NaOH溶液的作用是_________________。
(6)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两
种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,写出反应的化学方程式
__________________。
【答案】(1)分液漏斗
(2)A
(3) <
(4)溶液由无色变为红色
(5)尾气处理,或吸收多余的SO 和C1
2 2
(6)
【解析】(1)由仪器a的构造可知a为分液漏斗,故答案为:分液漏斗;
(2)由制备原理可知制备二氧化硫常温下即可实现,选用装置A,故答案为:A;
(3)实验室制取氯气所用药品是固体和液体,反应条件是加热,所以应选用E装置,实验室制取氯气的反应
方程式为: ;随反应的进行盐酸的浓度降低,而稀盐酸不能与二氧
化锰反应制氯气,因此含4mol浓盐酸的反应体系中实际反应的HCl的量小于4mol,则产生氯气的物质的
量小于1mol,标况下的体积小于22.4L;故答案为: ;<;
(4)氯气与水反应生成次氯酸,二氧化硫以及次氯酸都具有漂白性,可使品红褪色,次氯酸的漂白性是利
用次氯酸的强氧化性,二氧化硫的漂白性是利用二氧化硫和有色物质生成无色物质,次氯酸的漂白性是永
久性的,二氧化硫的漂白性是暂时的;加热时,次氯酸漂白过的溶液无变化,二氧化硫和有色物质生成的
无色物质不稳定,加热时能重新变成红色,故答案为:溶液由无色变为红色;
(5)氯气和二氧化硫有毒,不能排放到空气中,但氯气和二氧化硫都和碱反应,所以装置C的作用是吸收多
余的氯气和二氧化硫,故答案为:尾气处理,或吸收多余的SO 和Cl;
2 2
(6)氯气有强氧化性,二氧化硫有还原性,二者能按1:1发生氧化还原反应:生成无漂白性的HSO 和HCl,故答案为:
2 4
。
【名师点睛】本题考查SO 和Cl 的实验室制备及其性质的验证,传统的方法是分别实验,只能分别记录现
2 2
象再进行对比,不够直观,面本题进行了操作方法的创新,两种气体同时制备并验证其性质,现象对比直
观,且尾气同时处理,体现了创新精神。
【变式训练】化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力。
(1)查阅资料可知:2KMnO+16HCl(浓)═ 2MnCl + 2KCl + 5Cl↑ + 2HO。某同学设计图1所示装置来
4 2 2 2
制备纯净、干燥的氯气,其中实验装置或试剂有错误的是(_____)
A.①② B.② C.②③ D.①③
(2)将图1装置修改正确后,虚框④是收集Cl 的装置,请从图2中选用合适的装置__。
2
(3)将制得的Cl 进行性质实验,装置如图3所示(加热装置省略),请回答以下问题。
2
①装置E中可观察到________________;反应的化学方程式_____________________。
②装置F在反应中的作用是_____________。
A.收集Cl B.防止倒吸 C.混合气体
2
③装置G所得的溶液中具有漂白性的分子是____,将G所得饱和溶液置于光照下一段时间,溶液中大量
减少的粒子有(除HO分子外)______。(至少写2种)
2
④装置H的作用_______________。
(4)工业漂白粉常用Cl 与石灰乳反应制得,反应方程式为_________________。家庭使用漂白粉时,为
2
了增强漂白性可滴加的用品是____________。【答案】 (1) C (2)C (3)①剧烈反应,生成棕红(褐)色的烟 2Fe+3Cl 2FeCl ②B ③HClO
2 3
Cl、HClO、ClO- ④尾气处理 (4)2Cl+2Ca(OH)=CaCl+Ca(ClO)+2HO 食醋
2 2 2 2 2 2
【解析】(1)KMnO 和浓盐酸在常温下就可以反应生成氯气,①正确(这里不需要酒精灯加热);反应产生
4
的氯气可能混有HCl,需要进行净化,但不能使用NaOH,因为氯气也能和NaOH反应,应该使用饱和食盐水,
②错误;净化后的氯气可以用浓硫酸干燥,但气体应用长导管直接通入浓硫酸中,即:导管应长进短出,
③错误;答案选C;
(2)氯气的密度大于空气且有毒,可以选择向上排空气法收集但应该有尾气处理,不能直接排放到空气
中,故应该选用装置c;
(3)①装置E中氯气与铁在高温条件下剧烈反应,生成棕红(褐)色的烟;反应的化学方程式为:2Fe+3Cl
2
2FeCl;②装置F两导管都为短的,在反应中的作用是防止倒吸,答案选B;③装置G所得的溶液为新制
3
氯水,其中具有漂白性的分子是HClO,将G所得饱和溶液置于光照下一段时间,次氯酸分解生成盐酸和氧
气,氯气进一步的溶解并反应与水生成盐酸和次氯酸,溶液中大量减少的粒子有Cl、HClO、ClO-;④氯气
2
有毒,过量的氯气直接排放会造成空气污染,装置H装有氢氧化钠溶液能与氯气反应,起到尾气处理的作
用;
(4)工业漂白粉常用 Cl 与石灰乳反应制得,反应生成氯化钙、次氯酸钙和水,其反应方程式为:
2
2Cl+2Ca(OH)=CaCl+Ca(ClO)+2HO;家庭使用漂白粉时,为了增强漂白性可滴加的用品是食醋,滴加后漂
2 2 2 2 2
白粉中的有效成分次氯酸钙与醋酸反应生成次氯酸,迅速起到漂白效果。