文档内容
主题五 物质的结构与性质测试(二)
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 K-39 Cr-52 Mn-55
第Ⅰ卷(选择题 共45分)
一、选择题(本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
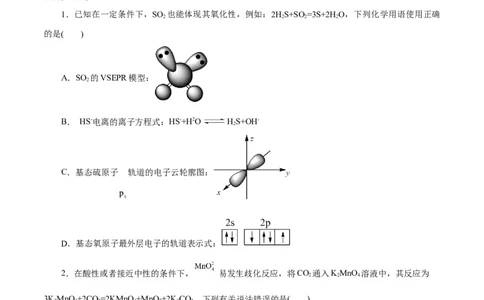
1.已知在一定条件下,SO 也能体现其氧化性,例如:2HS+SO=3S+2H O,下列化学用语使用正确
2 2 2 2
的是( )
A.SO 的VSEPR模型:
2
B. HS-电离的离子方程式:HS-+H2O HS+OH-
2
C.基态硫原子 轨道的电子云轮廓图:
D.基态氧原子最外层电子的轨道表示式:
2.在酸性或者接近中性的条件下, 易发生歧化反应,将CO 通入KMnO 溶液中,其反应为
2 2 4
3KMnO +2CO =2KMnO +MnO+2K CO。下列有关说法错误的是( )
2 4 2 4 2 2 3
A.CO2-的空间结构为三角锥形
3
B.CO 中心原子的杂化方式是sp
2
C.基态钾原子的价电子排布式:4s1
D.基态Mn2+的价电子轨道表示式:
3.下列关于物质结构和性质的说法正确的是( )A.键角:HS>PH>SiH B.熔点:CsCl>KCl>NaCl
2 3 4
C.NO -、NO -的VSEPR模型相同 D.酸性:CHCOOH>CCl COOH>CF COOH
3 2 3 3 3
4.实验室中利用CoCl 制取配合物[Co(NH )]Cl 的反应为2CoCl + 10NH + 2NH Cl+H O
2 3 6 3 2 3 4 2 2
=2[Co(NH)]Cl +2H O。下列叙述正确的是( )
3 6 3 2
A.Co2+的价电子排布图为 B.1 mol [Co(NH)]3+中含σ键为18 mol
3 6
C.HO 中氧原子采用sp3杂化 D.氨分子间存在氢键,因而NH 易溶于水
2 2 3
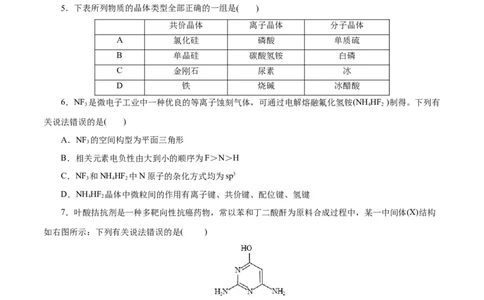
5.下表所列物质的晶体类型全部正确的一组是( )
共价晶体 离子晶体 分子晶体
A 氯化硅 磷酸 单质硫
B 单晶硅 碳酸氢铵 白磷
C 金刚石 尿素 冰
D 铁 烧碱 冰醋酸
6.NF 是微电子工业中一种优良的等离子蚀刻气体,可通过电解熔融氟化氢铵(NH HF )制得。下列有
3 4 2
关说法错误的是( )
A.NF 的空间构型为平面三角形
3
B.相关元素电负性由大到小的顺序为F>N>H
C.NF 和NH HF 中N原子的杂化方式均为sp3
3 4 2
D.NH HF 晶体中微粒间的作用有离子键、共价键、配位键、氢键
4 2
7.叶酸拮抗剂是一种多靶向性抗癌药物,常以苯和丁二酸酐为原料合成过程中,某一中间体(X)结构
如右图所示:下列有关说法错误的是( )
A.基态N原子的核外电子空间运动状态有5种
B.沸点: 高于
C.X结构中,C、N原子杂化方式种数相同D.X结构中含有 大 键
8.镍二硫烯配合物基元的COFs材料因具有良好的化学稳定性、热稳定性和导电性而应用于电池领域。
一种基于镍二硫烯配合物的单体结构简式如下图所示,下列关于该单体的说法不正确的是( )
A.Ni属于d区元素 B.S与Ni形成配位键时,S提供孤电子对
C.组成元素中电负性最大的是O D.醛基中C原子的价层电子对数为4
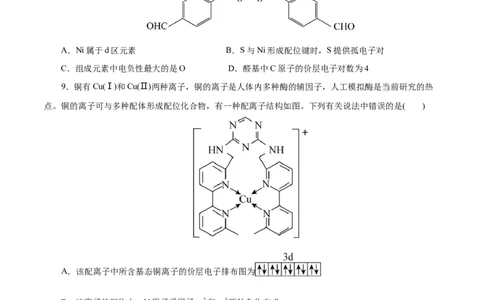
9.铜有Cu(Ⅰ)和Cu(Ⅱ)两种离子,铜的离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热
点。铜的离子可与多种配体形成配位化合物,有一种配离子结构如图。下列有关说法中错误的是( )
A.该配离子中所含基态铜离子的价层电子排布图为
B.该离子的配体中,N原子采用了sp2和sp3两种杂化方式
C.该配离子中铜的配位数和所含配位键的数目均为4
D.从核外电子排布角度分析,稳定性:Cu(Ⅰ)<Cu(Ⅱ)
10.W、X、Y、Z为原子序数递增的短周期主族元素,四种元素可组成一种新型化合物WXYZ ,其
2 6
中W的原子半径在短周期主族元素中最大,X的质子数是Z核外最外层电子数的2倍。下列叙述正确的是
( )
A.四种元素对应的最高价氧化物的水化物中,只有一种是强酸B.W与另外三种元素形成的二元化合物均含离子键,水溶液呈碱性
C.简单离子半径:Z>Y>W
D.简单气态氢化物的稳定性:X>Z
11.X、Y、Z、M、Q五种短周期元素,原子序数依次增大。X只有1个s能级的电子。YQ 是一种平
3
面正三角形分子。Z的p能级电子半充满。M元素焰色试验焰色呈黄色。下列说法不正确的是
A.电负性:Z>Y>X,第一电离能:Z>Y>X
B.YQ 与ZX 能通过配位键化合
3 3
C.YZX 分子是苯的等电子体,结构相似
3 3 6
D.MYX 是一种离子化合物,溶于水能放出氢气
4
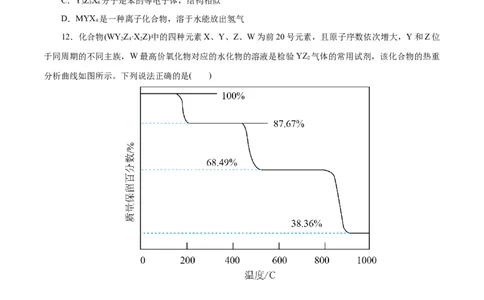
12.化合物(WYZ·X Z)中的四种元素X、Y、Z、W为前20号元素,且原子序数依次增大,Y和Z位
2 4 2
于同周期的不同主族,W最高价氧化物对应的水化物的溶液是检验YZ 气体的常用试剂,该化合物的热重
2
分析曲线如图所示。下列说法正确的是( )
A.X、Y、Z、W四种元素只能形成一种离子化合物W(XYZ )
3 2
B.200~400℃阶段热分解将失去1个XZ
2
C.400~600℃热分解后生成的固体化合物是XYZ ,且该反应为非氧化还原反应
3
D.该反应过程最终分解得到的固体产物属于碱性氧化物
13.W、X、Y、Z为原子序数依次增大的短周期元素,原子序数之和为 32;M是由这四种元素组成
的化合物,其化学式为YZX W(其中每种元素只有一种化合价);将8.0gM投入水中有刺激性气味的气体
2 2
放出,该气体能使湿润的红色石蕊试纸变蓝,向所得溶液中通入足量的 CO ,经过滤等一系列操作后得到
27.8g的白色固体。下列叙述错误的是( )
A.四种元素中有两种金属元素
B.原子半径:Y>Z>X
C.M与盐酸反应能生成三种离子化合物
D.Y元素最高价氧化物的水化物能溶解Z元素最高价氧化物
14.前四周期元素M、Q、W、X、Y、Z原子序数依次增大。M的单质常用作保护气,W是元素周期
表中电负性最大的元素,X与Y形成化合物的化学式为YX且其焰色试验为紫色(透过蓝色钴玻璃),Z的原
子序数为28,Q和Y形成的一种化合物甲的晶胞在xy平面、xz平面、yz平面上的投影图甲所示。W、
Y、Z三种元素组成的化合物乙的晶体结构如图乙所示。
下列关于化合物乙的说法不正确的是( )
A.该晶体中Z的化合价为+2
B.与Z等距最近的W有6个
C.图中A、B原子间的距离为
D.图中B的原子分数坐标可表示为
15.自然界中原生铜的硫化物经氧化、淋滤后变成CuSO 溶液,遇到闪锌矿(ZnS)可慢慢转变为铜蓝
4
(CuS)。已知: K (ZnS)=2 ×10-22, K (CuS)=6 ×10-36。下列说法正确的是( )
sp sp
A.Cu2+基态核外电子排布式为[Ar]3d84s1B.反应ZnS(s)+Cu2+(ag) CuS(s)+Zn2+(aq)正向进行,需满足
C.ZnS 晶胞(见如图)中S2-的配位数为4
D.生成铜蓝后的溶液中一定存在: c(S2-)= 且c(S2- )>
第II卷(非选择题 共55分)
二、填空题(本题共4小题,共55分)
16.(12分)氮元素及其化合物在生产、生活中用途广泛。回答下列问题:
(1)基态氮原子的价电子排布式为___________。
(2)与N同周期的元素中第一电离能比N大的元素有____________种。
(3)三硝基胺N(NO)(其结构为 )是一种新型的火箭燃料,因硝基吸电子能力强,中心N原
2 3
子上无孤电子对,则中心N原子的杂化方式为___________,并且与三个硝基中的N构成___________形。
(4)(CN) 、(SCN) 的性质与卤素单质的相似,称为拟卤素。其分子内各原子均达到8电子稳定结构,则
2 2
1mol(CN) 分子中含___________molπ键,SCN-的空间构型为___________形。
2
(5)白磷在氯气中燃烧可以得到PCl 和PCl ,研究发现固态PCl 和PBr 均为离子晶体,但其结构分别
3 5 4 5
为[PCl ]+[PCl ]-和[PBr ]+Br-,分析PCl 和PBr 结构存在差异的原因:___________。
4 6 4 5 5
(6)过渡金属氮化物因其优异的催化性能(加氢处理、光和电化学催化等)受到了广泛关注。贵金属钼
(Mo)的氮化物可作将N 还原为氨的反应的催化剂。贵金属钼的氮化物的立方晶胞如图所示。已知晶胞参数
2
为anm,则该晶体的化学式为___________,晶体的密度为___________(列出计算式)g·cm-3。
17.(14分)镍是一种硬而有延展性并具有铁磁性的金属,它能够高度磨光和抗腐蚀,用镍制造不锈钢
和各种合金钢被广泛地用于飞机、舰艇、雷达、导弹、陶瓷颜料、永磁材料、电子遥控等领域。回答下列
问题:(1)基态Ni原子的价电子轨道表示式(电子排布图)为___。
(2)具有不对称结构的Schiff碱及其与过渡金属形成的配合物结构类似于生命体系的真实情况。有一种
广泛用于生命体系中金属蛋白的模拟研究,其结构如图所示。
该配合物中C原子的杂化方式为___;该配合物中除H之外的组成元素的第一电离能由小到大的顺序
是___。
(3)二氧化硒主要用于电解锰行业,其中一种制备方法为2NiSeO 2NiSeO+O ↑、NiSeO
4 3 2 3
NiO+SeO。下列分子或离子的VSEPR模型为平面三角形的是___(填字母)。
2
A.SeO2- B.SeO2- C.NiO D.SeO
4 3 2
(4)草酸镍可用于制镍粉和镍的催化剂等,加热分解的化学方程式为NiC O NiO+CO+CO ,属于非极
2 4 2
性分子的产物是___,等物质的量的CO(C≡O)与CO 分子中的π键比为___,与CO 互为等电子体(等电子体
2 2
是指价电子数和原子数相同的分子、离子或原子团)的阴离子为___(任写一种)。
(5)氢能是一种重要的二次能源,其独有的优势和丰富的资源引起人类广泛的兴趣,然而氢的储存是目
前氢能利用的一大难题,现有La、Ni合金是较为理想的储氢材料,其晶胞结构如图所示:
①该储氢材料的化学式为___。
②已知晶胞参数边长为anm,高为bnm,设阿伏加德罗常数的值为N 一个晶胞内可以储存18个氢原
A
子,储氢后的晶胞密度为___g·cm-3。
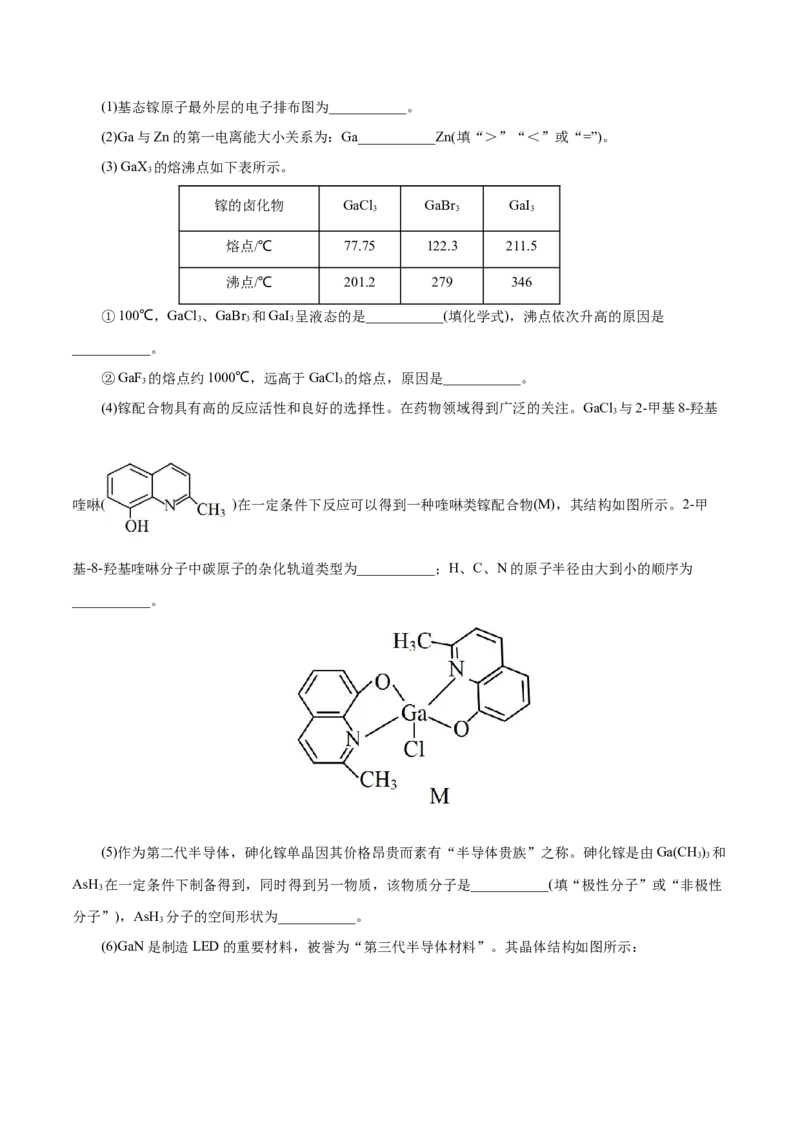
18.(15分)含镓(Ga)化合物在半导体材料、医药行业等领域发挥重要作用。回答下列问题:(1)基态镓原子最外层的电子排布图为___________。
(2)Ga与Zn的第一电离能大小关系为:Ga___________Zn(填“>”“<”或“=”)。
(3) GaX 的熔沸点如下表所示。
3
镓的卤化物 GaCl GaBr GaI
3 3 3
熔点/℃ 77.75 122.3 211.5
沸点/℃ 201.2 279 346
①100℃,GaCl 、GaBr 和GaI 呈液态的是___________(填化学式),沸点依次升高的原因是
3 3 3
___________。
②GaF 的熔点约1000℃,远高于GaCl 的熔点,原因是___________。
3 3
(4)镓配合物具有高的反应活性和良好的选择性。在药物领域得到广泛的关注。GaCl 与2-甲基8-羟基
3
喹啉( )在一定条件下反应可以得到一种喹啉类镓配合物(M),其结构如图所示。2-甲
基-8-羟基喹啉分子中碳原子的杂化轨道类型为___________;H、C、N的原子半径由大到小的顺序为
___________。
(5)作为第二代半导体,砷化镓单晶因其价格昂贵而素有“半导体贵族”之称。砷化镓是由Ga(CH ) 和
3 3
AsH 在一定条件下制备得到,同时得到另一物质,该物质分子是___________(填“极性分子”或“非极性
3
分子”),AsH 分子的空间形状为___________。
3
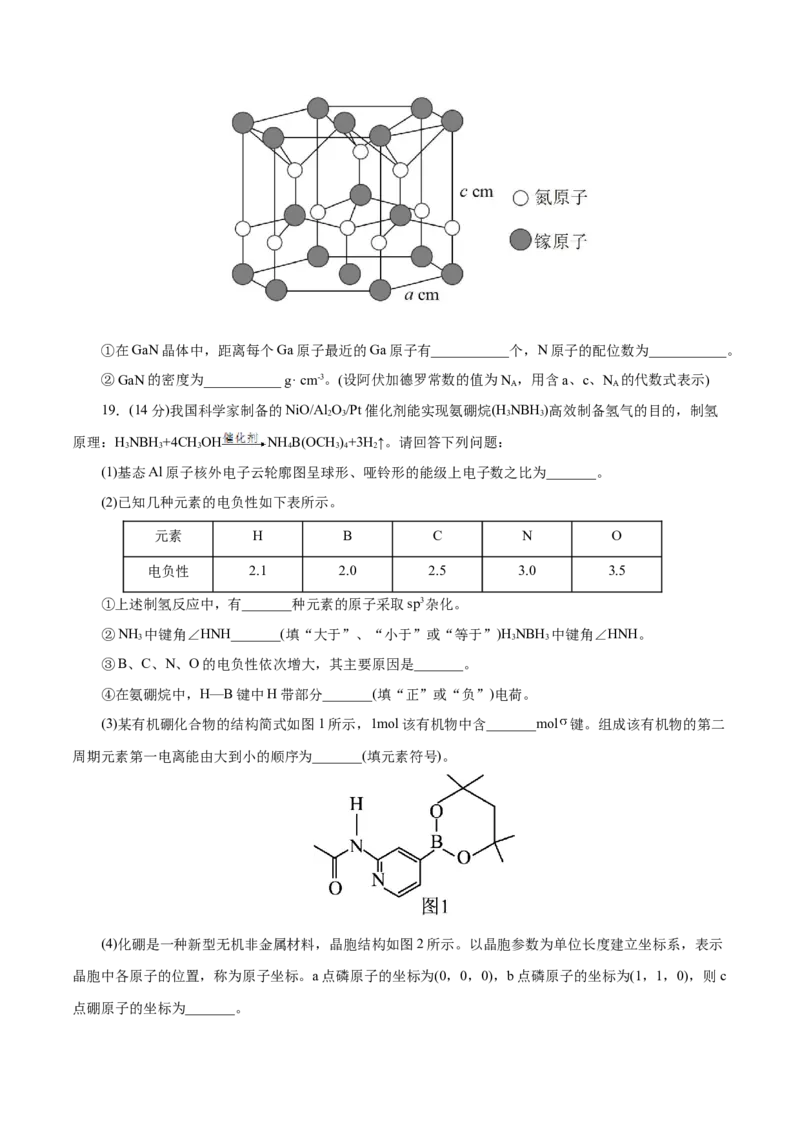
(6)GaN是制造LED的重要材料,被誉为“第三代半导体材料”。其晶体结构如图所示:①在GaN晶体中,距离每个Ga原子最近的Ga原子有___________个,N原子的配位数为___________。
②GaN的密度为___________ g· cm-3。(设阿伏加德罗常数的值为N ,用含a、c、N 的代数式表示)
A A
19.(14分)我国科学家制备的NiO/Al O/Pt催化剂能实现氨硼烷(H NBH )高效制备氢气的目的,制氢
2 3 3 3
原理:HNBH +4CH OH NH B(OCH )+3H ↑。请回答下列问题:
3 3 3 4 3 4 2
(1)基态Al原子核外电子云轮廓图呈球形、哑铃形的能级上电子数之比为_______。
(2)已知几种元素的电负性如下表所示。
元素 H B C N O
电负性 2.1 2.0 2.5 3.0 3.5
①上述制氢反应中,有_______种元素的原子采取sp3杂化。
②NH 中键角∠HNH_______(填“大于”、“小于”或“等于”)H NBH 中键角∠HNH。
3 3 3
③B、C、N、O的电负性依次增大,其主要原因是_______。
④在氨硼烷中,H—B键中H带部分_______(填“正”或“负”)电荷。
(3)某有机硼化合物的结构简式如图1所示,1mol该有机物中含_______mol 键。组成该有机物的第二
周期元素第一电离能由大到小的顺序为_______(填元素符号)。
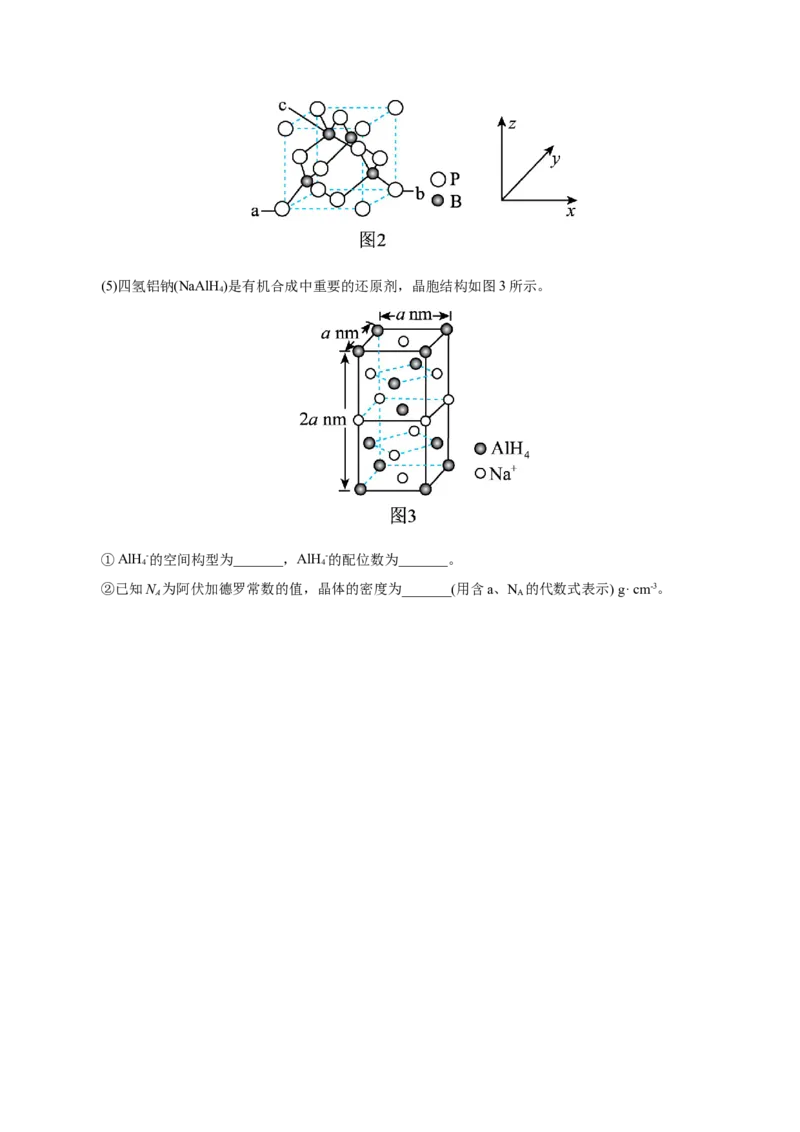
(4)化硼是一种新型无机非金属材料,晶胞结构如图2所示。以晶胞参数为单位长度建立坐标系,表示
晶胞中各原子的位置,称为原子坐标。a点磷原子的坐标为(0,0,0),b点磷原子的坐标为(1,1,0),则c
点硼原子的坐标为_______。(5)四氢铝钠(NaAlH )是有机合成中重要的还原剂,晶胞结构如图3所示。
4
①AlH-的空间构型为_______,AlH-的配位数为_______。
4 4
②已知N 为阿伏加德罗常数的值,晶体的密度为_______(用含a、N 的代数式表示) g· cm-3。
A A