文档内容
绝密★启用前
2025 年高考考前信息必刷卷 03(浙江专用)
化 学
考情速递
高考·新动向:部分考生认为化学简单到离谱,甚至觉得不需要动脑子就能做对题目,这些考生平日里
知识积累扎实,在这次考试中做题得心应手。然而,对于那些化学基础稍薄弱或者对新题型预估不足
的考生,情况则不太乐观。新的大题题型打乱了他们的解题节奏,在考场上花费大量时间理解题意和
摸索解题思路,导致时间紧张。
高考·新考法:非选择题由原来的5道精简为4道。在分值分配上,第一大题16分,第二大题12分,
第三大题12分,第四大题12分。这种变化对考生的知识综合运用能力和思维转换能力提出了更高要求。
例如物质结构和无机流程融合成了16分的第一道大题,考生不仅要熟知物质结构的微观奥秘,还要能
将其与宏观的无机流程顺畅对接,增加了答题的难度和对知识综合运用的要求。题型布局打乱,一直
以来考生习惯的大题数量和出题套路被彻底打破,出题人改变了原有的题型布局。这种变化让考生失
去了熟悉题型带来的优势,需要在考场上重新适应新的题型结构,增加了考试的挑战性。
命题·大预测:在2025浙江化学第二次考试中,难度比首考略有增加。物质分类可能会给出一些特殊的
新材料或者新型化合物,要求依据物质分类的基础定义和特殊情况进行判断。在反应分类中,可能会
出现一些新的化学反应类型组合或者特殊反应条件下的反应分类。随着新能源的发展,2025年的化学
情景可能更多涉及新能源相关化学知识。例如在氢能的利用方面。在环境方面,可能会涉及到新型的
环境治理化学方法或者污染物检测的化学原理。
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Na-23 Mg-24 Al-27 S-32 Cl-35.5
K-39 Ca-40 Mn-55 Fe-56 Cu-64 Zn-65 Br-80 I-127 Ag-108 Ba-137 Hg-201 Bi-209
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一项是符合题
目要求的,不选、多选、错选均不得分)
1.下列分子属于极性分子的是( )
A.CH B.CO C.SO D.NH
4 2 3 3
【答案】D【解析】A项,CH 空间构型为正四面体,结构对称,属于非极性分子,故不选A;B项,CO 空间构
4 2
型为直线形分子,结构对称,属于非极性分子,故不选B;C项,SO 空间构型为平面三角形分子,结构
3
对称,属于非极性分子,故不选C;D项,NH 空间构型为三角锥,结构不对称,正负电荷的重心不重合,
3
属于极性分子,故选D;选D。
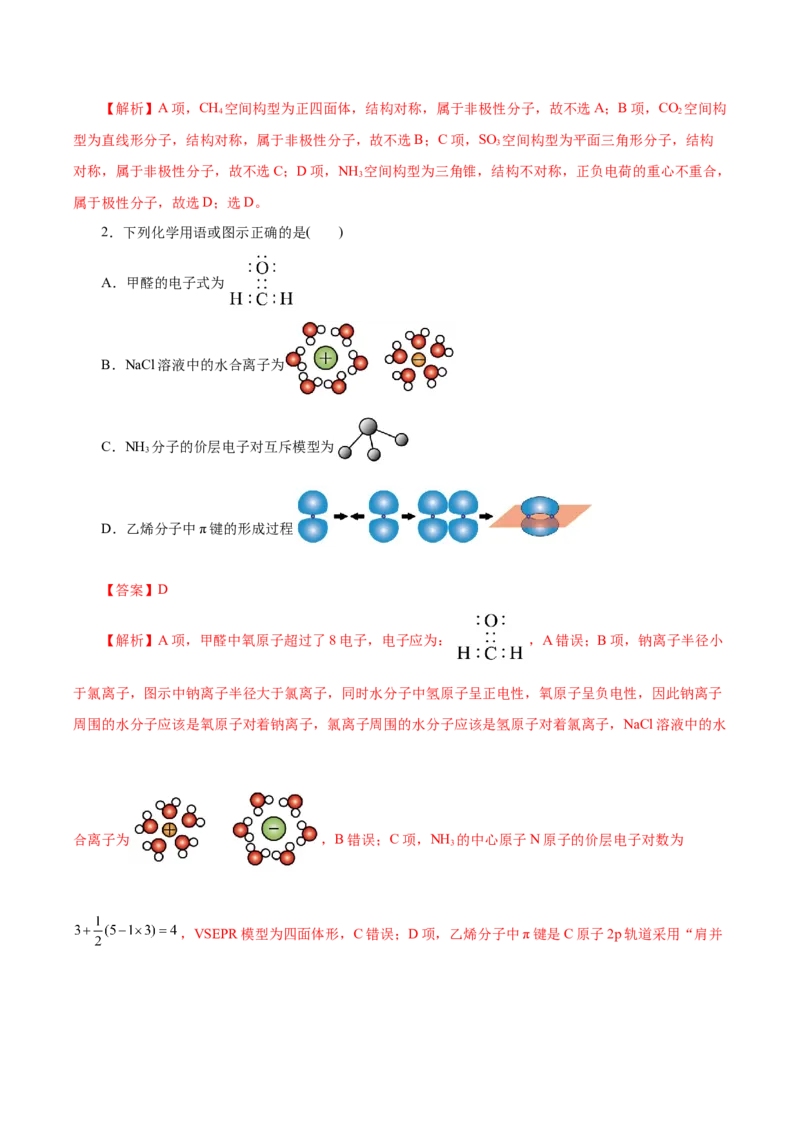
2.下列化学用语或图示正确的是( )
A.甲醛的电子式为
B.NaCl溶液中的水合离子为
C.NH 分子的价层电子对互斥模型为
3
D.乙烯分子中π键的形成过程
【答案】D
【解析】A项,甲醛中氧原子超过了8电子,电子应为: ,A错误;B项,钠离子半径小
于氯离子,图示中钠离子半径大于氯离子,同时水分子中氢原子呈正电性,氧原子呈负电性,因此钠离子
周围的水分子应该是氧原子对着钠离子,氯离子周围的水分子应该是氢原子对着氯离子,NaCl溶液中的水
合离子为 ,B错误;C项,NH 的中心原子N原子的价层电子对数为
3
,VSEPR模型为四面体形,C错误;D项,乙烯分子中π键是C原子2p轨道采用“肩并肩”的方式重叠形成,过程为 ,D正确;故选D。
3.下列关于元素及其化合物的性质说法不正确的是( )
A.NaOH与铝粉反应会释放出大量气体,可作管道疏通剂
B.SO 具有氧化性,可作暂时性漂白剂
2
C.HCO 酸性比柠檬酸弱,能除去水垢(主要成分为CaCO 、MgCO )
2 3 3 3
D.HNO 具有腐蚀性和挥发性,使用时应注意防护和通风
3
【答案】B
【解析】A项,NaOH与铝粉反应会释放出大量氢气气体,故可作管道疏通剂,A正确;B项,SO 具
2
有漂白性,可用来漂白纸浆,B错误;C项,HCO 酸性比柠檬酸弱,则柠檬酸能和碳酸钙、碳酸镁生成
2 3
二氧化碳气体,用于除去水垢(主要成分为CaCO 、MgCO ),C正确;D项,硝酸为强酸,具有腐蚀性和
3 3
挥发性,使用时须注意防护和通风,D正确;故选B。
4.下列有关物质结构与性质的比较正确的是( )
A.单电子数:Fe>V>Ge B.沸点:AsH >PH >NH
3 3 3
C.电负性: B<Be<C D.键角:SeO<SeO2-<SeO2-
3 4 3
【答案】A
【解析】A项,Fe、V、Ge的单电子数分别为4、3、2,A项正确;B项,NH 能形成分子间氢键,
3
AsH 比PH 相对分子质量大,沸点:NH >AsH >PH ,B项错误;C项,电负性Be<B<C,C项错误;
3 3 3 3 3
D项,SeO 为sp2杂化,键角120°,SeO2-、SeO2-都为sp3杂化,但SeO2-有一对孤电子对,键角小于
3 4 3 3
SeO2-,键角为:SeO>SeO2->SeO2-,D项错误;故选A。
4 3 4 3
5.关于实验室安全,下列表述错误的是( )
A.具有 标识的化学品为爆炸类物质,实验时不准敲击、摩擦和挤压
B.在做钠在空气中燃烧的实验过程中,移动坩埚时应使用坩埚钳夹取
C.不慎将苯酚沾到皮肤上,应立即用NaOH溶液冲洗,再用水冲洗
D.氯气有毒,有关氯气性质的实验要在通风橱中进行
【答案】C
【解析】A项,爆炸类物质实验时,不准敲击、摩擦和挤压,A正确;B项,在做钠在空气中燃烧的
实验过程中,移动坩埚时应使用坩埚钳夹取,以防烫伤,B正确;C项,苯酚有毒,对皮肤有腐蚀性,
NaOH溶液对皮肤也有腐蚀性,不慎将苯酚沾到皮肤上,应立即用乙醇冲洗,再用水冲洗,C错误;D项,氯气有毒,有关氯气性质的实验要在通风橱中进行,防止发生中毒,D正确;故选C。
6.水体中氨氮含量过高会导致水体富营养化,用次氯酸钠除去氨氮(以NH 表示)的反应为:
3
3NaClO+2NH =3NaCl+N↑+3H O。下列说法不正确的是(N 为阿伏加德罗常数的值) ( )
3 2 2 A
A.NaClO是氧化剂,NH 是还原剂
3
B.氧化产物与还原产物物质的量之比为1∶3
C.反应温度越高,氨氮的去除率也越高
D.生成1molN ,反应转移电子数为6N
2 A
【答案】C
【解析】A项,NaClO中氯元素的化合价由+1价降低为-1价,NaCIO是氧化剂,NH 中氮元素的化合
3
价由-3价升高为0价,NH 是还原剂,故A正确;B项,N 是氧化产物,NaCl是还原产物,氧化产物与还
3 2
原产物物质的量之比为1:3,故B正确;C项,反应温度过高,NaClO会分解,氨氮的去除率降低,故C
错误;D项,生成1molN ,反应转移电子数为6N ,故D正确;故选C。
2 A
7.从结构探析物质性质和用途是学习化学的有效方法。下列实例与解释不相符的是( )
选项 实例 解释
将95%乙醇加入[Cu(NH )]SO 溶液中 乙醇极性较小,降低了[Cu(NH )]SO 的溶
A 3 4 4 3 4 4
析出深蓝色晶体 解
铁丝在酒精喷灯上灼烧,焰色无明显变
B 铁原子核外电子在灼烧时没有发生跃迁
化
DNA中碱基A与T、G与C的互补配
C 分子间氢键作用实现了超分子的分子识别
对
D 熔点:C HNH NO <NH NO 引入乙基减弱了离子间的相互作用
2 5 3 3 4 3
【答案】B
【解析】A项,将95%乙醇加入[Cu(NH )]SO 溶液中析出深蓝色晶体,原因是乙醇分子的极性小,加
3 4 4
入乙醇后溶剂的极性减小,降低了[Cu(NH )]SO 的溶解,故A不符合题意;B项,焰色试验是金属单质或
3 4 4
离子的电子在吸收能量后,从基态跃迁到激发态,激发态不稳定,跃迁到低能量级时,会释放光子,光子
的频率若在可见光频率范围内,则金属表现为有焰色。铁丝在酒精喷灯上灼烧,焰色无明显变化,并不是
铁原子核外电子在灼烧时没有发生跃迁,而是放出的光子频率不在可见光频率范围内,故B符合题意;C
项,O元素、N元素的电负性较大,能与氢形成分子间氢键,DNA中的碱基A与T、G与C的互补配对是
通过氢键来实现的,分子间氢键作用实现了超分子的分子识别,故C不符合题意;D项,硝酸铵中铵根离
子和硝酸根离子间存在离子键,铵根离子其中一个H被乙基替代,引入乙基减弱了离子间的相互作用,所
以熔点:C HNH NO <NH NO ,故D不符合题意;故选B。
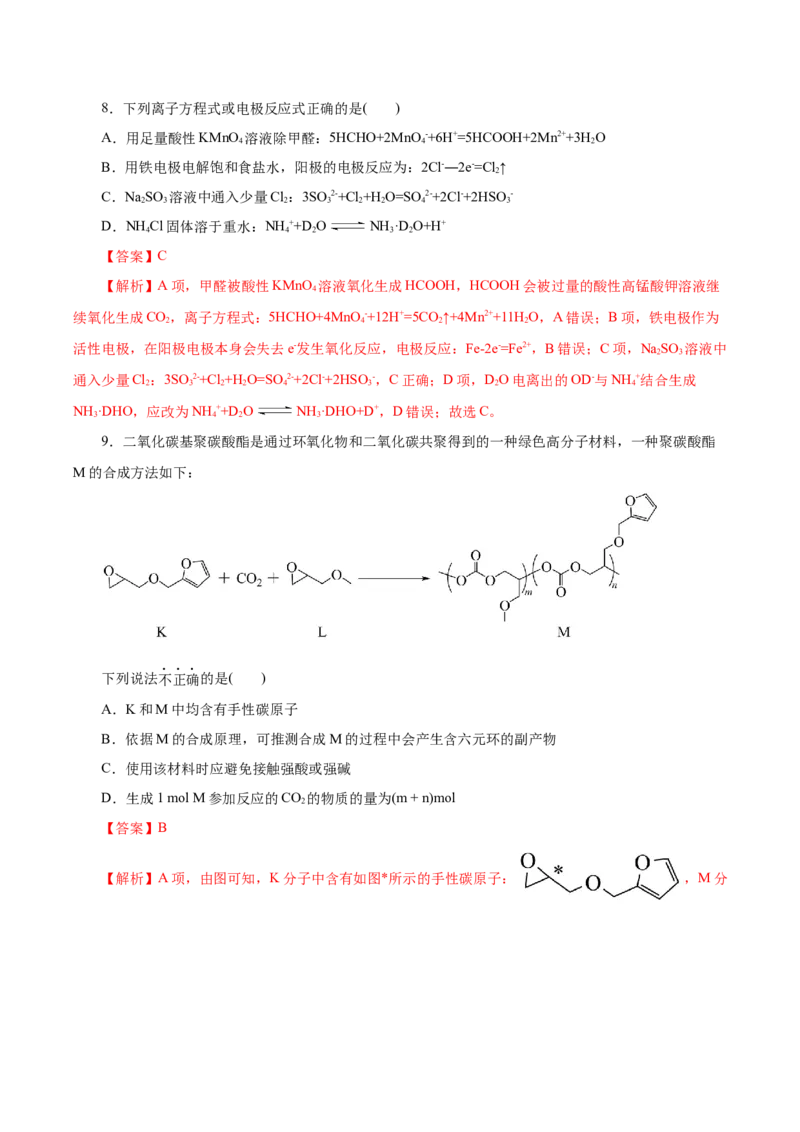
2 5 3 3 4 38.下列离子方程式或电极反应式正确的是( )
A.用足量酸性KMnO 溶液除甲醛:5HCHO+2MnO -+6H+=5HCOOH+2Mn2++3H O
4 4 2
B.用铁电极电解饱和食盐水,阳极的电极反应为:2Cl-―2e-=Cl↑
2
C.NaSO 溶液中通入少量Cl:3SO 2-+Cl+H O=SO 2-+2Cl-+2HSO -
2 3 2 3 2 2 4 3
D.NH Cl固体溶于重水:NH ++D O NH ·D O+H+
4 4 2 3 2
【答案】C
【解析】A项,甲醛被酸性KMnO 溶液氧化生成HCOOH,HCOOH会被过量的酸性高锰酸钾溶液继
4
续氧化生成CO,离子方程式:5HCHO+4MnO -+12H+=5CO ↑+4Mn2++11H O,A错误;B项,铁电极作为
2 4 2 2
活性电极,在阳极电极本身会失去e-发生氧化反应,电极反应:Fe-2e-=Fe2+,B错误;C项,NaSO 溶液中
2 3
通入少量Cl:3SO 2-+Cl+H O=SO 2-+2Cl-+2HSO -,C正确;D项,DO电离出的OD-与NH +结合生成
2 3 2 2 4 3 2 4
NH ·DHO,应改为NH ++D O NH ·DHO+D+,D错误;故选C。
3 4 2 3
9.二氧化碳基聚碳酸酯是通过环氧化物和二氧化碳共聚得到的一种绿色高分子材料,一种聚碳酸酯
M的合成方法如下:
下列说法不正确的是( )
A.K和M中均含有手性碳原子
B.依据M的合成原理,可推测合成M的过程中会产生含六元环的副产物
C.使用该材料时应避免接触强酸或强碱
D.生成1 mol M参加反应的CO 的物质的量为(m + n)mol
2
【答案】B
【解析】A项,由图可知,K分子中含有如图*所示的手性碳原子: ,M分子中含有如图*所示的手性碳原子: ,故A正确;B项,由图
可知,K分子、L分子中的碳氧环断裂与二氧化碳发生加聚反应生成M,所以合成M的过程中会产生含五
元环的副产物,即: ,故B错误;C项,由图可知,M分子中含有的酯基在强酸或强碱溶液
中会发生水解反应,所以使用该材料时应避免接触强酸或强碱,故C正确;D项,根据反应可知,每生成
1molM,理论上消耗(m+n)molCO ,故D正确;故选B。
2
10.已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、苯胺、苯
甲酸混合溶液的流程如下。下列说法正确的是( )
A.苯胺既可与盐酸也可与 溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
【答案】C
【解析】由题给流程可知,向甲苯、苯胺、苯甲酸的混合溶液中加入盐酸,盐酸将微溶于水的苯胺转
化为易溶于水的苯胺盐酸盐,分液得到水相Ⅰ和有机相Ⅰ;向水相中加入氢氧化钠溶液将苯胺盐酸盐转化
为苯胺,分液得到苯胺粗品①;向有机相中加入水洗涤除去混有的盐酸,分液得到废液和有机相Ⅱ,向有
机相Ⅱ中加入碳酸钠溶液将微溶于水的苯甲酸转化为易溶于水的苯甲酸钠,分液得到甲苯粗品②和水相Ⅱ;向水相Ⅱ中加入盐酸,将苯甲酸钠转化为苯甲酸,经结晶或重结晶、过滤、洗涤得到苯甲酸粗品③。A项,
苯胺分子中含有的氨基能与盐酸反应,但不能与氢氧化钠溶液反应,故A错误;B项,得到苯胺粗品①的
分离方法为分液,得到苯甲酸粗品③的分离方法为结晶或重结晶、过滤、洗涤,获取两者的操作方法不同,
故B错误;C项,苯胺粗品、甲苯粗品、苯甲酸粗品依次由①、②、③获得,故C正确;D项,①、②为
液相,③为固相,都不是两相混合体系,故D错误;故选C。
11.(2025·山东省德州市高三联考)恒压下,将HCl和O 分别以不同的起始流速通入体积为7L的反应
2
器中,发生反应:2HCl(g)+ O(g) Cl(g)+HO(g),在T、T、T 温度下反应,通过检测流出气体成分绘
2 2 2 1 2 3
制HCl转化率(a)曲线,如图所示(较低流速下转化率可近似为平衡转化率)。下列说法错误的是( )
A.T>T>T
1 2 3
B.该反应在低温下可自发进行
C.加入高效催化剂或升温可提高M点转化率
D.若通气1h开始反应,则N点容器体积减少1.225L
【答案】D
【解析】根据题给信息,较低流速下转化率视为平衡转化率,则由图可以看出,P点以后,流速较大,
说明此时的转化率不是平衡转化率,此时反应未达到平衡状态。A项,P点以后,流速较高,反应未达平
衡状态,温度越高,反应速率越快,单位时间内氯化氢的转化率越高。在P点后,同一流速下, T 温度
1
下的氯化氢的转化率最大,T 温度下的氯化氢的转化率最小,说明温度T>T>T,A项正确;B项,根
3 1 2 3
据题给信息,较低流速下转化率近似为平衡转化率,在较低流速时,T 转化率最大,T 转化率最小,温度
3 1
T>T>T,则此反应是放热反应,并且ΔS<0,根据ΔG=ΔH-TΔS<0是自发进行,所以此反应必须在低
1 2 3
温下才能自发进行,B项正确;C项,M点未达到平衡状态,使用高效催化剂或升高温度,可以增大反应
速率,使M点HCl的转化率增加,故加入高效催化剂或升温可提高M点转化率,C项正确;D项,由图可知,N点气流流速为0.16mol/h,以1h为单位带入气体流量,可知n(HCl) 为0.16mol,则n(O ) 为
始 2 始
0.12mol。N点时HCl转化率为70%,N点时转化的HCl的物质的量=0.16mol×70%=0.112mol,根据“三段
式”有:
同温同压下,容器起始体积和N点时容器的体积关系为:
,V =6.3L,则N点容器体积减少7L-6.3L=0.7L,D项错误;
N
故选D。
12.中国科学院研发了一种以酚类化合物为原料,以水为唯一氢源/氧源电解合成己二酸的方法,本方
法中苯酚可高效转化为 (环己酮和环己醇的混合物), 再转化为己二酸。下列说法错误的是(
)
A.CuCo O 为阳极催化剂
2 4
B.PtAu合金催化剂上发生氧化反应
C.H+透过质子交换膜从 极向 极移动
D.环已酮在N极上的电极反应式为
【答案】B
【解析】根据题意该装置为电解池,M极上苯酚加氢还原成环己酮,PtAu合金催化剂上发生还原反应,
得电子为电解池的阴极,N极为电解池的阳极,故CuCo O 为阳极催化剂,电极反应为2HO-4e-=O↑+
2 4 2 2
4H+,发生氧化反应,环己酮再被O 氧化为己二酸,反应方程式为
2,H+从N极通过质子交换膜移向M极。A项,N极
为阳极,则CuCo O 为阳极催化剂,A正确;B项,该装置为电解池,M极上苯酚加氢还原成环己酮,
2 4
PtAu合金催化剂上发生还原反应,得电子为电解池的阴极,B错误;C项,H+从N极通过质子交换膜移向
M极,C正确;D项,环已酮在N极上的电极反应式为
,D正确;故选B。
13.超导现象一直吸引着广大科学家的关注。某超导材料的晶体结构属于四方晶系,其晶胞如图所示。
下列说法错误的是( )
A.两个O原子之间的最短距离为 B.与Ba2+最近且等距的Cu2+有4个
C.该超导材料的化学式为HgBa CuO D.该晶体的密度为
2 2 4
【答案】C
【解析】A项,氧原子位于棱上,则两个氧原子之间的最短距离为面对角线的一半,
,故A正确;B项,由图可知,Ba2+在内部,Cu2+在顶点,则与Ba2+最近且等距
的Cu2+有4个,故B正确;C项,根据均摊法,晶胞中含 个 ,2个Ba、 个个O,则该短导材料的化学式为HgBa CuO,故C错误;D项,晶胞中含 个 ,2个Ba、
2 4
个 个O,可知, ,故D正
确;故选C。
14.新戊醇可发生如下转化:
下列说法正确的是( )
A.产物C在NaOH醇溶液中加热能生成E
B.化合物B的结构为
C.由上述机理可知: (主产物)
D.化合物D到E反应的有机副产物是 、
【答案】D
【解析】A项,由题干信息可知,产物C与Br相邻的碳原子上没有H,不能在NaOH醇溶液中加热发
生消去反应,即不能生成E,A错误;B项,由题干信息可知,根据D的结构简式可知,化合物B的结构为 ,B错误;C项,由上述机理可知: (副产物) ,
(主产物) ,C错误;D项,由上述机理可知:化合物D到E反应即D发生消
去反应时,其有机副产物是 ,D正确;故选D。
15.25℃时,草酸(H C O)的电离常数为K =5.0×10-2,K =5.4×10-5;CaC O 的K =2.5×10-9;
2 2 4 a1 a2 2 4 sp
。常温下,下列说法不正确的是( )
A. 的KHC O 溶液呈酸性
2 4
B.若某溶液中cHC O-=cHC O,溶液的pH约为1.3
2 4 2 2 4
C.草酸钙饱和溶液中cC O2->cHC O-
2 4 2 4
D.NaC O 溶液中粒子浓度关系:c(OH―)-c(H+)<cHC O-+cHC O
2 2 4 2 4 2 2 4
【答案】D
【解析】A项,由电离常数可知,草酸氢根离子在溶液中的水解常数K = = =2.0×10—13<
h
K ,则草酸氢根离子在溶液中的电离程度大于水解程度,溶液呈酸性,故A正确;B项,由电离常数
a2
K (H C O)= 可知,溶液中cHC O-=cHC O时,溶液中c(H+)= K =5.0×10-2,则溶液
a1 2 2 4 2 4 2 2 4 a1
pH=2—lg5=1.3,故B正确;C项,草酸钙饱和溶液中,草酸根离子在溶液中分步水解,以一级水解为主,
则溶液中草酸根离子大于草酸氢根离子,故C正确;D项,草酸钠溶液中存在质子守恒关系c(OH―)=c(H+)
+cHC O-+2cHC O,则溶液中c(OH―)-c(H+)>cHC O-+cHC O,故D错误;故选D。
2 4 2 2 4 2 4 2 2 4
16.已知金属硫化物在“细菌氧化”时转化为硫酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的Au颗粒被FeS、FeAsS包裹),以提高金的浸出率并冶炼金,工艺流程如下。
2
下列说法中错误的是( )
A.“细菌氧化”过程中,体系的酸性增强
B.“细菌氧化”的优势为无需控温,可减少有害气体产生
C.“沉金”中Zn作还原剂,将[Au(CN) ]-还原为Au
2
D.“沉铁砷”时需加碱调节 ,生成Fe(OH) 胶体起絮凝作用,促进了含As微粒的沉降
3
【答案】B
【解析】矿粉中加入足量空气和HSO ,在pH=2时进行细菌氧化,金属硫化物中的S元素转化为硫
2 4
酸盐,过滤,滤液中主要含有Fe3+、硫酸根离子、As(Ⅵ),加碱调节pH值,Fe3+转化为Fe(OH) 胶体,可
3
起到絮凝作用,促进含As微粒的沉降,过滤可得到净化液;滤渣主要为Au,Au与空气中的O 和NaCN
2
溶液反应,得到含[Au(CN) ]-的浸出液,加入Zn进行“沉金”得到Au和含[Zn(CN) ]2-的滤液②。A项,根
2 4
据分析可知,“细菌氧化”过程中硫元素被氧化为硫酸,即有硫酸生成,体系的酸性增强,故A正确;B
项,“细菌氧化”的需要控温,保证细菌的活性,故B错误;C项,“沉金”中Zn的化合价升高,作还
原剂,将[Au(CN) ]-还原为Au,故C正确;D项,根据分析可知,“沉铁砷”时需加碱调节pH,生成
2
Fe(OH) 胶体起絮凝作用,促进了含As微粒的沉降,故D正确;故选B。
3
二、非选择题(本大题共4小题,共52分)
17.(16分)氮及其化合物对生命、生产生活意义重大。
(1)同周期第一电离能比 N大的元素有 (用元素符号表示);NO -的大π键可表示为
2
。
(2)三硝基甲苯可用来制作炸药TNT,试从分子结构中分析其易爆炸的原因 。
(3)下列说法不正确的是___________。
A.NCl 分子的极性比PCl 的大
3 3
B.碱性:NH OH>NH >N H >NH CH
2 3 2 4 2 3
C. 的熔点为2200℃,硬度高,推测它为共价晶体
D.NH BH 中存在配位键,提供空轨道的是B
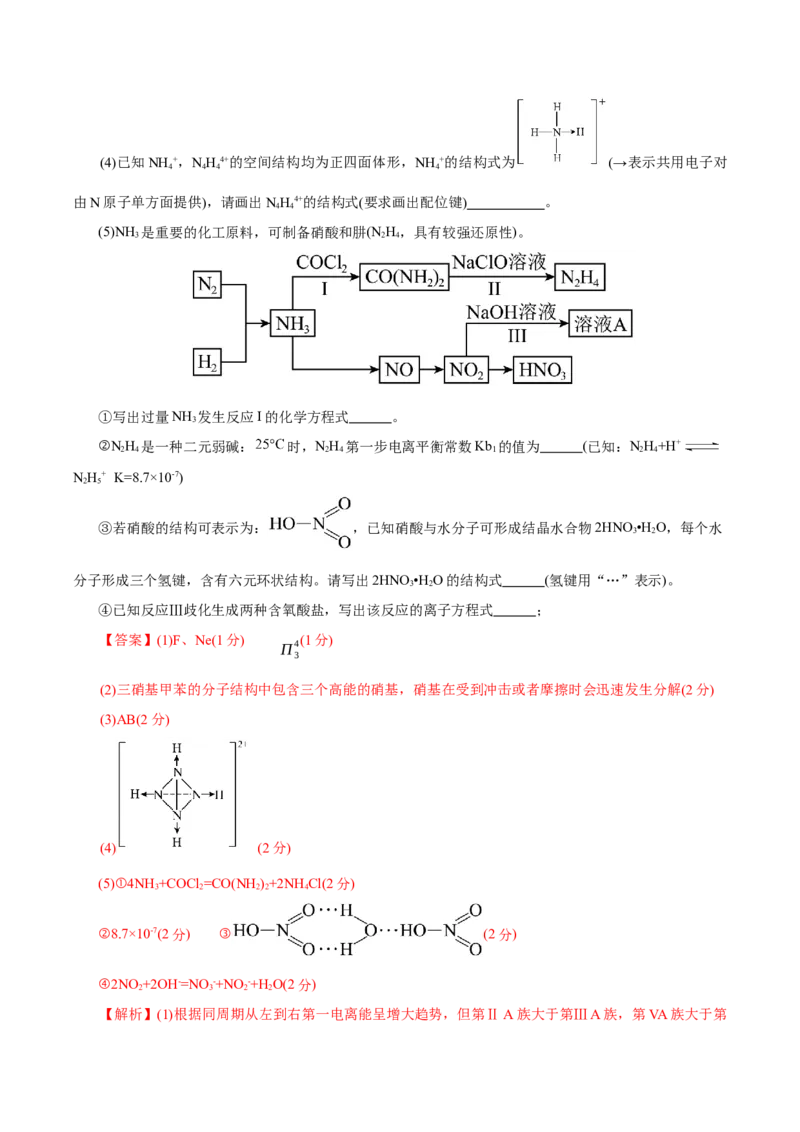
3 3(4)已知NH +,NH4+的空间结构均为正四面体形,NH +的结构式为 (→表示共用电子对
4 4 4 4
由N原子单方面提供),请画出NH4+的结构式(要求画出配位键) 。
4 4
(5)NH 是重要的化工原料,可制备硝酸和肼(N H,具有较强还原性)。
3 2 4
①写出过量NH 发生反应I的化学方程式 。
3
②NH 是一种二元弱碱: 时,NH 第一步电离平衡常数Kb 的值为 (已知:NH+H+
2 4 2 4 1 2 4
NH+ K=8.7×10-7)
2 5
③若硝酸的结构可表示为: ,已知硝酸与水分子可形成结晶水合物2HNO•H O,每个水
3 2
分子形成三个氢键,含有六元环状结构。请写出2HNO•H O的结构式 (氢键用“…”表示)。
3 2
④已知反应Ⅲ歧化生成两种含氧酸盐,写出该反应的离子方程式 ;
【答案】(1)F、Ne(1分) (1分)
Π4
3
(2)三硝基甲苯的分子结构中包含三个高能的硝基,硝基在受到冲击或者摩擦时会迅速发生分解(2分)
(3)AB(2分)
(4) (2分)
(5)①4NH +COCl =CO(NH )+2NHCl(2分)
3 2 2 2 4
②8.7×10-7(2分) ③ (2分)
④2NO +2OH-=NO-+NO-+H O(2分)
2 3 2 2
【解析】(1)根据同周期从左到右第一电离能呈增大趋势,但第ⅡA族大于第ⅢA族,第VA族大于第ⅥA族,则同周期第一电离能比N大的元素有F、Ne;NO -是“V”形结构,NO -的大π键中参与原子数为
2 2
3,氮原子剩余电子数5+1−2=4,O原子剩余电子数6-1=5,根据“单出1,偶除2”,则大π键可表示为
;(2)三硝基甲苯可用来制作炸药TNT,试从分子结构中分析其易爆炸的原因三硝基甲苯的分子结构中
Π4
3
包含三个高能的硝基,硝基在受到冲击或者摩擦时会迅速发生分解;(3)A项,氮的电负性比P的电负性大,
N与Cl的电负性差值小于P与Cl的电负性差值,因此NCl 分子的极性比PCl 的大,故A错误;B项,氮
3 3
的碱性是氮孤对电子起作用,电负性O>N>H>C,NH 为氨基取代,NH OH为羟基取代,NH CH 为甲基
2 4 2 2 3
取代,甲基是供电子基团,而吸引电子能力是羟基>氨基,则碱性:NH OH