文档内容
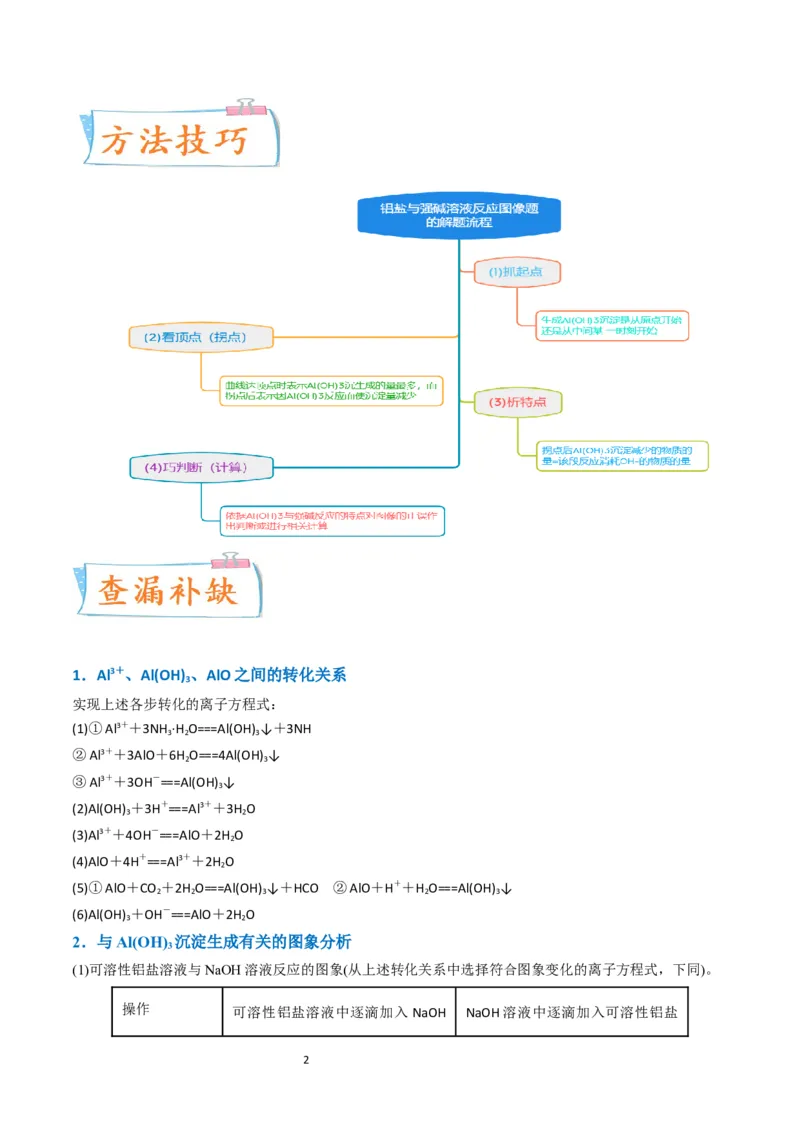
微专题12 数形结合思想突破“铝三角”图象与计算
1.(2023·浙江·高考真题)共价化合物 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
,下列说法不正确的是
A. 的结构式为 B. 为非极性分子
C.该反应中 的配位能力大于氯 D. 比 更难与 发生反应
2.(2023·山东·统考高考真题)鉴别浓度均为 的 、 三种溶液,仅用
下列一种方法不可行的是
A.测定溶液 B.滴加酚酞试剂
C.滴加 溶液 D.滴加饱和 溶液
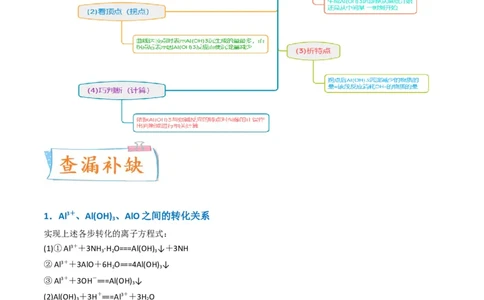
11.Al3+、Al(OH) 、AlO之间的转化关系
3
实现上述各步转化的离子方程式:
(1)①Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
②Al3++3AlO+6H O===4Al(OH) ↓
2 3
③Al3++3OH-===Al(OH) ↓
3
(2)Al(OH) +3H+===Al3++3H O
3 2
(3)Al3++4OH-===AlO+2H O
2
(4)AlO+4H+===Al3++2H O
2
(5)①AlO+CO +2H O===Al(OH) ↓+HCO ②AlO+H++H O===Al(OH) ↓
2 2 3 2 3
(6)Al(OH) +OH-===AlO+2H O
3 2
2.与Al(OH) 沉淀生成有关的图象分析
3
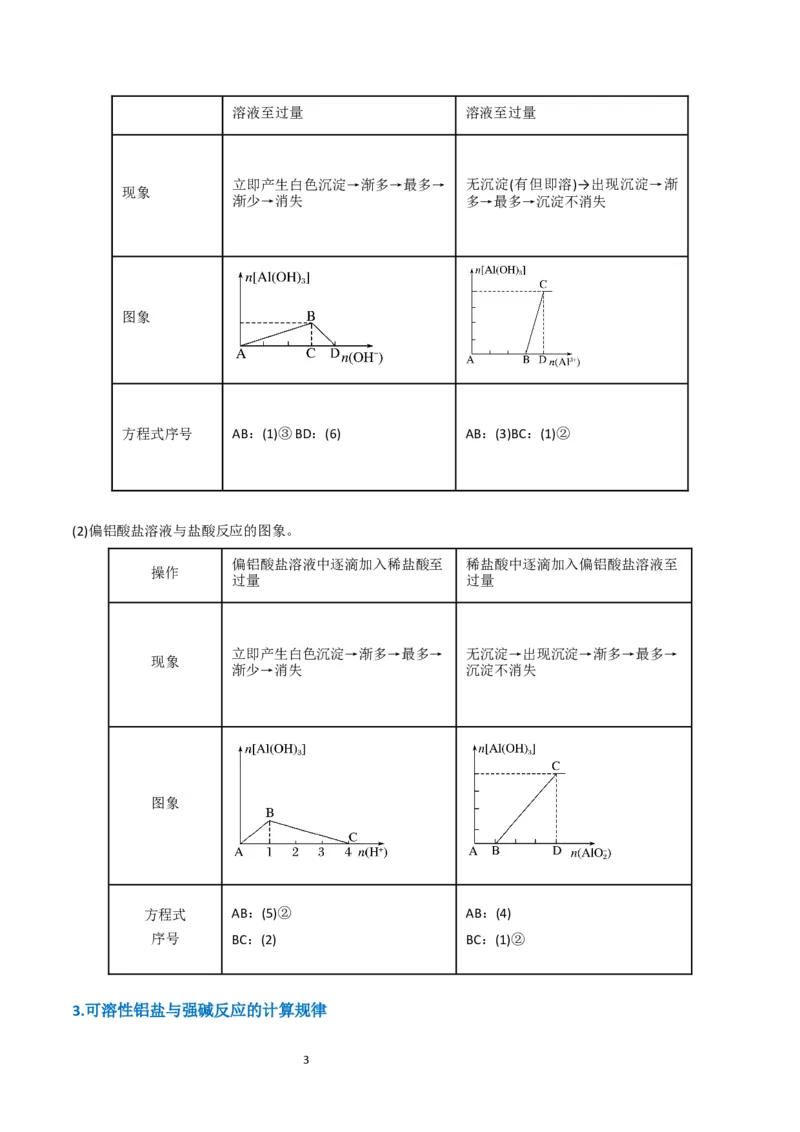
(1)可溶性铝盐溶液与NaOH溶液反应的图象(从上述转化关系中选择符合图象变化的离子方程式,下同)。
操作 可溶性铝盐溶液中逐滴加入NaOH NaOH溶液中逐滴加入可溶性铝盐
2溶液至过量 溶液至过量
立即产生白色沉淀→渐多→最多→ 无沉淀(有但即溶)→出现沉淀→渐
现象
渐少→消失 多→最多→沉淀不消失
图象
方程式序号 AB:(1)③BD:(6) AB:(3)BC:(1)②
(2)偏铝酸盐溶液与盐酸反应的图象。
偏铝酸盐溶液中逐滴加入稀盐酸至 稀盐酸中逐滴加入偏铝酸盐溶液至
操作
过量 过量
立即产生白色沉淀→渐多→最多→ 无沉淀→出现沉淀→渐多→最多→
现象
渐少→消失 沉淀不消失
图象
方程式 AB:(5)② AB:(4)
序号 BC:(2) BC:(1)②
3.可溶性铝盐与强碱反应的计算规律
3(1)求产物Al(OH) 的量
3
①当n(OH-)≤3n(Al3+)时,n[Al(OH) ]=n(OH-);
3
②当3n(Al3+)<n(OH-)<4n(Al3+)时,n[Al(OH) ]=
3
4n(Al3+)-n(OH-);
③当n(OH-)≥4n(Al3+)时,n[Al(OH) ]=0,无沉淀。
3
(2)求反应物碱的量
①若碱不足(Al3+未完全沉淀),n(OH-)=3n[Al(OH) ];
3
4.与Al3+、AlO有关的离子反应的一般规律
(1)当溶液中有多种离子时,要考虑离子之间的反应顺序,如向含有 H+、NH、Mg2+、Al3+的混合溶液中逐
滴加入NaOH溶液,OH-先与H+反应,再与Mg2+、Al3+反应生成沉淀,再与NH反应,最后才溶解Al(OH)
3
沉淀。
(2)AlO与HCO的反应不属于水解相互促进的反应,而是 HCO电离出的H+与AlO发生反应:AlO+HCO+
H O===Al(OH) ↓+CO。
2 3
1.(2020·江苏·高考真题)下列有关化学反应的叙述正确的是
A.室温下,Na在空气中反应生成Na O
2 2
B.室温下,Al与4.0 mol﹒L-1NaOH溶液反应生成NaAlO
2
C.室温下,Cu与浓HNO 反应放出NO气体
3
D.室温下,Fe与浓H SO 反应生成FeSO
2 4 4
1.(2023·广东·广州市第二中学校联考三模)下图为铝的生产原理示意图,下列相关说法不正确的是
A.冰晶石做助熔剂
4B.氧化铝属于过渡晶体
C.金属铁、铜的冶炼方法与铝类似
D.铝在工业上是一种很好的还原剂
2.(2023·湖南长沙·长郡中学校考模拟预测)学习小组用废弃的铝制易拉罐按如下流程制备明矾,并测定
明矾中结晶水的含量。
上述实验中不需要用到的操作是
A. B.
C. D.
3.(2022·北京朝阳·北京八十中校考模拟预测)某小组用如图装置探究铝片与酸碱的反应,实验如下:
①A为盐酸时,1分钟后有大量气泡产生
②A为NaOH时,20秒后有大量气泡产生
③A为硫酸时,3分钟后有极少量气泡产生,滴加1mLCuSO 溶液,立即产生大量气泡,Al表面有少量红色
4
固体。下列说法正确的是
A.对比①②说明氧化性NaOH>HCl
B.对比①③说明Cl-对铝表面的氧化膜破坏能力强
C.对比①②③说明Al在不同的环境中还原性不同
D.③中实验说明Al与Cu2+反应剧烈放热
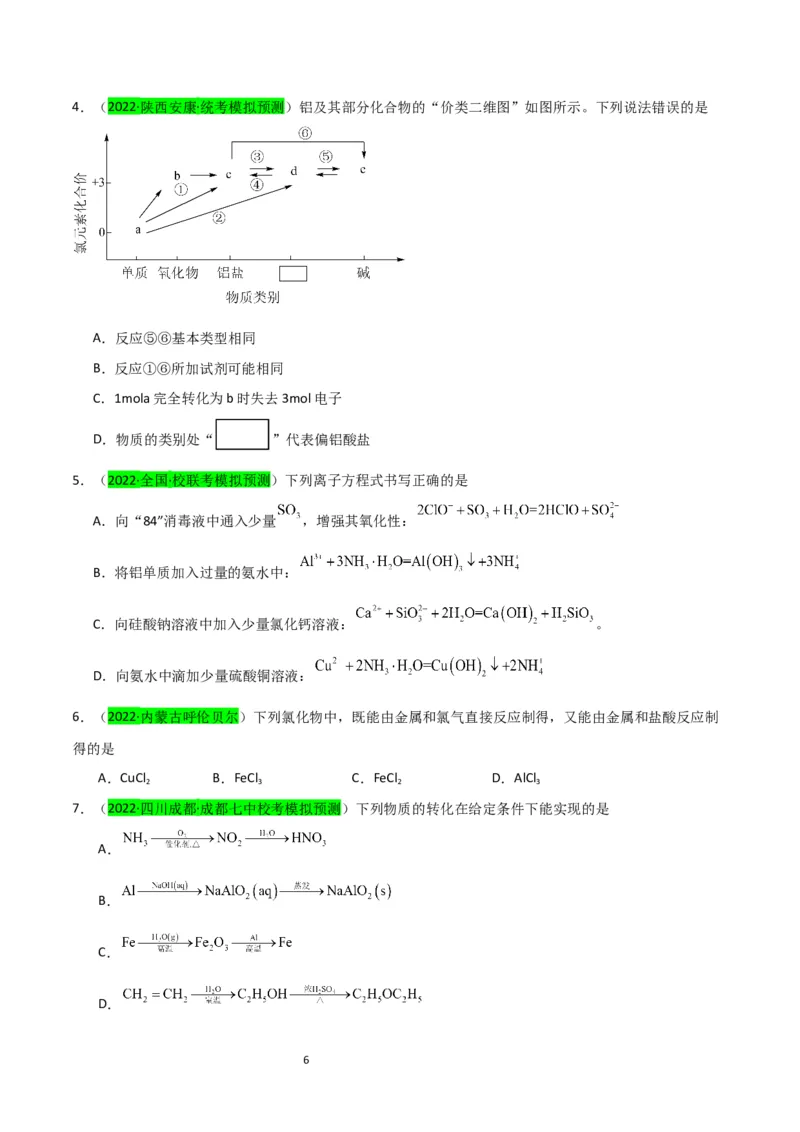
54.(2022·陕西安康·统考模拟预测)铝及其部分化合物的“价类二维图”如图所示。下列说法错误的是
A.反应⑤⑥基本类型相同
B.反应①⑥所加试剂可能相同
C.1mola完全转化为b时失去3mol电子
D.物质的类别处“ ”代表偏铝酸盐
5.(2022·全国·校联考模拟预测)下列离子方程式书写正确的是
A.向“84”消毒液中通入少量 ,增强其氧化性:
B.将铝单质加入过量的氨水中:
C.向硅酸钠溶液中加入少量氯化钙溶液: 。
D.向氨水中滴加少量硫酸铜溶液:
6.(2022·内蒙古呼伦贝尔)下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制
得的是
A.CuCl B.FeCl C.FeCl D.AlCl
2 3 2 3
7.(2022·四川成都·成都七中校考模拟预测)下列物质的转化在给定条件下能实现的是
A.
B.
C.
D.
68.(2022秋·广东东莞)相同质量的两份铝,分别放入足量的盐酸和氢氧化钠溶液中,放出的氢气在同温
同压下体积之比为
A.1:1 B.1:6 C.2:3 D.3:2
9.(2022秋·云南丽江)铝在空气中能稳定存在的原因是
A.铝的熔点比较小 B.铝的化学性质不活泼
C.铝的金属性比镁弱 D.铝表面能形成一层致密的氧化物薄膜
10.(2023秋·贵州铜仁)将某份镁铝合金均分为两份,一份加入足量盐酸,另一份加入足量NaOH溶液,
同温同压下产生的气体体积比为 ,则样品中镁、铝物质的量之比为
A. B. C. D.
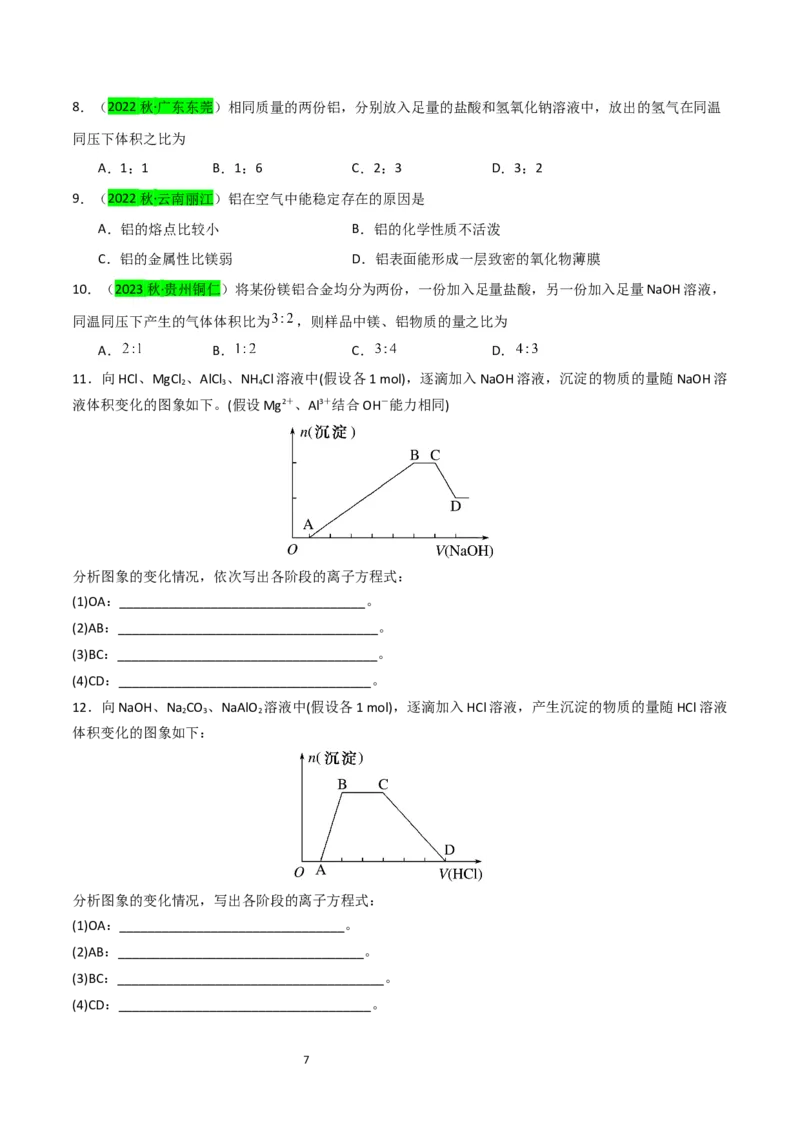
11.向HCl、MgCl 、AlCl 、NH Cl溶液中(假设各1 mol),逐滴加入NaOH溶液,沉淀的物质的量随NaOH溶
2 3 4
液体积变化的图象如下。(假设Mg2+、Al3+结合OH-能力相同)
分析图象的变化情况,依次写出各阶段的离子方程式:
(1)OA:___________________________________。
(2)AB:_____________________________________。
(3)BC:_____________________________________。
(4)CD:____________________________________。
12.向NaOH、Na CO 、NaAlO 溶液中(假设各1 mol),逐滴加入HCl溶液,产生沉淀的物质的量随HCl溶液
2 3 2
体积变化的图象如下:
分析图象的变化情况,写出各阶段的离子方程式:
(1)OA:________________________________。
(2)AB:___________________________________。
(3)BC:______________________________________。
(4)CD:____________________________________。
71.(2023春·山东泰安)下列有关 的图象不正确的是
A.图A是向氯化铝溶液中滴加氢氧化钠溶液 B.图B是向 中通入二氧化碳
C.图C是向氢氧化钠溶液中滴加氯化铝 D.图D是向氯化铝溶液中滴加氨水
2.(2022秋·陕西延安)下列有关Al(OH) 的图象不正确的是
3
A.图A是向氯化铝溶液中滴加氢氧化钠溶液 B.图B是向偏铝酸钠中通入二氧化碳
C.图C是向氢氧化钠溶液中滴加氯化铝 D.图D是向氯化铝溶液中滴加氨水
3.(2023秋·河南三门峡)甲、乙两个烧杯中分别盛有200mL4.0mol/L的盐酸和200mL4.0mol/LNaOH溶液,
向两个烧杯中均加入10.8g铝粉,在相同状况下产生气体的体积比为
A.1:1 B.2:1 C.3:2 D.2:3
4.(2023秋·广东广州)取两块大小一样的铝片,进行如下图的实验:
根据该实验,下列说法不正确的是
A.氧化铝有保护作用,因此烧杯Ⅰ中没有反应发生
B.烧杯Ⅰ中开始没有气泡,一段时间后才产生气泡;烧杯Ⅱ中立即产生气泡
C.两个烧杯中均发生反应:
8D.铝制餐具不宜长时间存放碱性食物
5.(2023春·河南洛阳·高三孟津县第一高级中学校考阶段练习)下列物质转化在给定条件下能实现的是
A.
B.
C.
D.
6.(2023秋·湖南益阳)把5.1 g镁铝合金的粉末放入过量的盐酸中,得到5.6 LH (标准状况),下列说法错
2
误的是
A.该合金的硬度比纯铝的大 B.该合金中铝的质量分数为50%
C.该合金中镁和铝的物质的量之比为1:1D.铝是地壳中含量最多的金属元素
7.(2023秋·辽宁铁岭)下列指定溶液中能大量共存的离子组是
A.澄清透明的溶液: 、 、 、
B.所含溶质为 的溶液加入: 、 、 、
C.插入铝片有气泡产生的溶液: 、 、 、
D.含有大量 的溶液: 、 、 、
8.(2023·全国·高三专题练习)甲、乙两烧杯中分别盛有 浓度均为 的盐酸与 溶液,
向两烧杯中分别加入等质量的铝粉,反应结束后测得同温同压下生成气体的体积之比为 ,则加入铝粉
的质量为
A. B. C. D.
9.(2023春·内蒙古呼伦贝尔)一定质量的铝铁合金溶于足量的NaOH溶液中,完全反应后产生3.36L(标
准状况下)气体;用同样质量的铝铁合金完全溶于足量的盐酸中,在标准状况下产生6.72L的气体,则该合
金中铝、铁的物质的量之比为
A.1 ∶1 B.2∶3 C.3∶2 D.1 ∶2
10.(2022秋·新疆巴音郭楞)在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡。然后将两
9球分别浸没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如图所示。下列说法正确的是
A.铝球表面有气泡产生,溶液澄清且杠杆不平衡
B.铝球表面有气泡产生,有白色沉淀;铁球表面有红色物质析出,溶液蓝色变浅,杠杆右边下沉
C.反应后去掉两烧杯,杠杆仍平衡
D.右边球上出现红色,左边溶液的c(OH-)增大
11.(2023秋·四川成都)Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有
很多转化关系,如表所列物质不能按如图关系(“→”表示一步完成)相互转化的是
选项 A B C D
a Na Al Fe
b NaOH
c NaCl CuO
A.A B.B C.C D.D
12.(2023秋·湖北襄阳)常温下,将等质量的 和 分别与等浓度、等体积的稀硫酸反应,产生气体的
体积(V)与时间(t)的关系如图所示。下列说法错误的是
A.曲线Ⅰ代表 与稀硫酸反应的变化曲线
B.参加反应的 和 的质量之比:
C.在 与稀硫酸的反应中,每转移0.6mol电子,同时生成气体的体积为6.72L(标准状况下)
D.上述发生的反应中,稀硫酸的量不足
1013.(2023秋·湖北襄阳)向 溶液中投入一小块金属钠(如图所示),反应完全后,过滤并洗涤,所
得沉淀干燥后在空气中完全灼烧。下列说法正确的是
A.所得沉淀为
B. 溶液可以导电,故 溶液是电解质
C.可以用手代替镊子直接取用金属钠进行该实验操作
D.灼烧后所得产物既能与稀的强酸溶液反应,也能与稀的强碱溶液反应
14.(2023·浙江·统考高考真题)某研究小组用铝土矿为原料制备絮凝剂聚合氯化铝(
)按如下流程开展实验。
已知:①铝土矿主要成分为 ,含少量 和 。用 溶液溶解铝土矿过程中 转变为难
溶性的铝硅酸盐。
② 的絮凝效果可用盐基度衡量,盐基度
当盐基度为0.60~0.85时,絮凝效果较好。
请回答:
(1)步骤Ⅰ所得滤液中主要溶质的化学式是 。
(2)下列说法不正确的是___________。
A.步骤I,反应须在密闭耐高压容器中进行,以实现所需反应温度
B.步骤Ⅱ,滤液浓度较大时通入过量 有利于减少 沉淀中的杂质
11C.步骤Ⅲ,为减少 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌
D.步骤Ⅳ中控制 和 的投料比可控制产品盐基度
(3)步骤V采用如图所示的蒸汽浴加热,仪器A的名称是 ;步骤V不宜用酒精灯直接加热的原
因是 。
(4)测定产品的盐基度。
的定量测定:称取一定量样品,配成溶液,移取 溶液于锥形瓶中,调 ,滴加指示
剂 溶液。在不断摇动下,用 标准溶液滴定至浅红色(有 沉淀),30秒
内不褪色。平行测试3次,平均消耗 标准溶液 。另测得上述样品溶液中
。
①产品的盐基度为 。
②测定 过程中溶液 过低或过高均会影响测定结果,原因是 。
12