文档内容
微专题13 Fe2+、Fe3+的性质及检验
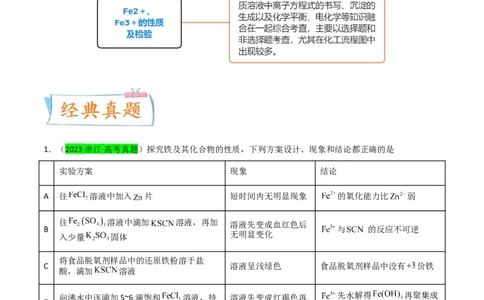
1.(2023·浙江·高考真题)探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是
实验方案 现象 结论
A 往 溶液中加入 片 短时间内无明显现象 的氧化能力比 弱
往 溶液中滴加 溶液,再加 溶液先变成血红色后
B 与 的反应不可逆
无明显变化
入少量 固体
将食品脱氧剂样品中的还原铁粉溶于盐
C 溶液呈浅绿色 食品脱氧剂样品中没有 价铁
酸,滴加 溶液
向沸水中逐滴加5~6滴饱和 溶液,持 溶液先变成红褐色再 先水解得 再聚集成
D
续煮沸 析出沉淀 沉淀
A.A B.B C.C D.D
2.(2023·浙江·统考高考真题)氯化铁是一种重要的盐,下列说法不正确的是
A.氯化铁属于弱电解质 B.氯化铁溶液可腐蚀覆铜板
C.氯化铁可由铁与氯气反应制得 D.氯化铁溶液可制备氢氧化铁胶体
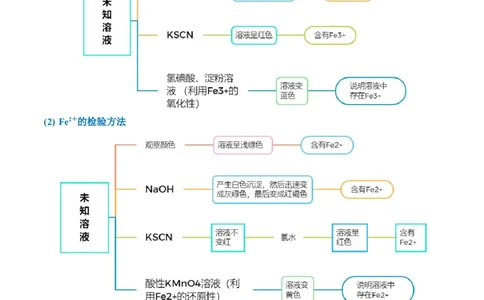
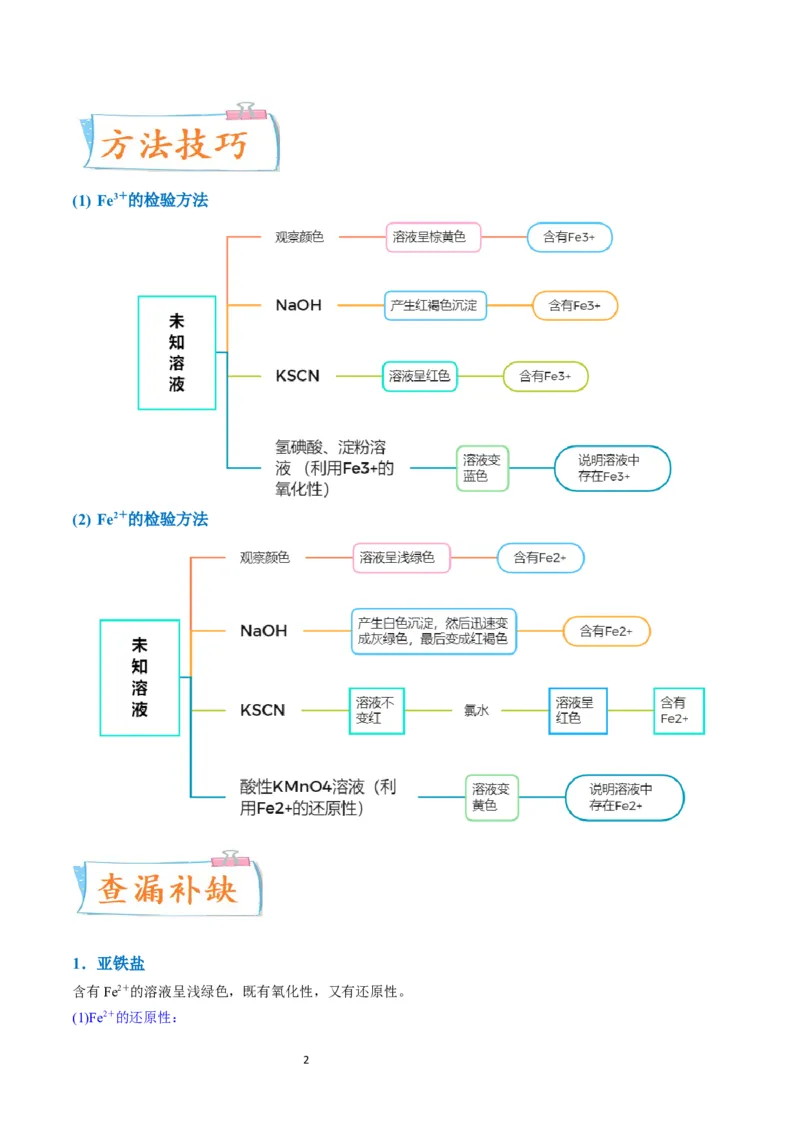
1(1) Fe3+的检验方法
(2) Fe2+的检验方法
1.亚铁盐
含有Fe2+的溶液呈浅绿色,既有氧化性,又有还原性。
(1)Fe2+的还原性:
2Fe2+的酸性溶液与HO 反应的离子方程式:
2 2
2Fe2++HO+2H+===2Fe3++2HO。
2 2 2
(2)Fe2+的弱氧化性:Fe2+ Fe
2.铁盐
含Fe3+的溶液呈棕黄色,Fe3+具有较强的氧化性。
写出下列转化的离子方程式:
(1)Fe3+ Fe2+:
2Fe3++SO+HO===2Fe2++SO+2H+
2
(2)Fe3+ Fe2+:2Fe3++2I-===2Fe2++I
2
3.Fe2+、Fe3+的检验方法
(1)用KSCN溶液和氯水
(2)用NaOH溶液
检验Fe3+也可用苯酚溶液,在FeCl 溶液中滴加苯酚溶液,溶液变紫色。
3
(3)含Fe2+、Fe3+的混合溶液中Fe3+、Fe2+的检验
―――――――→溶液变血红色,说明含有Fe3+
―――――→KMnO 溶液紫红色褪去,说明含有Fe2+。
4
(4)Fe2+的特征检验方法
溶液 产生蓝色沉淀,说明溶液中含有Fe2+,有关反应离子方程式为
3Fe2++2[Fe(CN) ]3-===Fe [Fe(CN) ]↓。
6 3 6 2
(5)盐溶液的配制与保存
(6)物质的制备
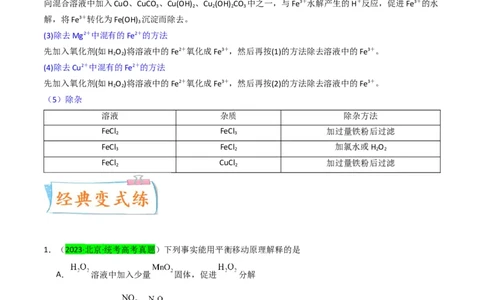
34.混合溶液中Fe3+、Fe2+除去的实验
(1)除去Mg2+中混有的Fe3+的方法
向混合溶液中加入MgO、MgCO 、Mg(OH) 中之一,与Fe3+水解产生的H+反应,促进Fe3+的水解,将Fe3+
3 2
转化为Fe(OH) 沉淀除去。
3
(2)除去Cu2+中混有的Fe3+的方法
向混合溶液中加入CuO、CuCO 、Cu(OH) 、Cu (OH) CO 中之一,与Fe3+水解产生的H+反应,促进Fe3+的水
3 2 2 2 3
解,将Fe3+转化为Fe(OH) 沉淀而除去。
3
(3)除去Mg2+中混有的Fe2+的方法
先加入氧化剂(如H O )将溶液中的Fe2+氧化成Fe3+,然后再按(1)的方法除去溶液中的Fe3+。
2 2
(4)除去Cu2+中混有的Fe2+的方法
先加入氧化剂(如H O )将溶液中的Fe2+氧化成Fe3+,然后再按(2)的方法除去溶液中的Fe3+。
2 2
(5)除杂
溶液 杂质 除杂方法
FeCl FeCl 加过量铁粉后过滤
2 3
FeCl FeCl 加氯水或H O
3 2 2 2
FeCl CuCl 加过量铁粉后过滤
2 2
1.(2023·北京·统考高考真题)下列事实能用平衡移动原理解释的是
A. 溶液中加入少量 固体,促进 分解
B.密闭烧瓶内的 和 的混合气体,受热后颜色加深
C.铁钉放入浓 中,待不再变化后,加热能产生大量红棕色气体
D.锌片与稀 反应过程中,加入少量 固体,促进 的产生
2.(2023·北京·统考高考真题)下列离子方程式与所给事实不相符的是
A. 制备84消毒液(主要成分是 ):
4B.食醋去除水垢中的 :
C.利用覆铜板制作印刷电路板:
D. 去除废水中的 :
3.(2023·浙江·统考高考真题)下列反应的离子方程式正确的是
A.碘化亚铁溶液与等物质的量的氯气:
B.向次氯酸钙溶液通入足量二氧化碳:
C.铜与稀硝酸:
D.向硫化钠溶液通入足量二氧化硫:
1.(2023·浙江·高三专题练习)已知硫酸亚铁溶液吸收 可生成硫酸亚硝酰合铁(分子式为
),下列说法不正确的是
A.硫酸亚硝酰合铁具有还原性
B.硫酸亚硝酰合铁水溶液呈中性
C.硫酸亚硝酰合铁是一种配合物,中心原子铁的配位数为6
D.硫酸亚铁溶液吸收 生成硫酸亚硝酰合铁的变化是化学变化
2.(2023春·天津南开·高三南开中学校考阶段练习)下列指定反应的离子方程式正确的是
A.用 溶液吸收少量 :
B. 通入足量的NaClO溶液中:
C. 溶液中加过量 溶液:
D. 溶液中加过量 溶液:
53.(2023·上海·高三专题练习)可用于检验 溶液是否少量变质的试剂
A.NaOH B.Fe C. D.KSCN
4.(2023·上海奉贤·统考二模)要除去 溶液中少量的 ,可行的方法是
A.滴入 溶液 B.通入氯气
C.加入适量铜粉并过滤 D.加入适量铁粉并过滤
5.(2023·湖南·校联考模拟预测)地壳表面分布很多阳离子,下列关于指定阳离子的检验方法正确的是
A. :向样品溶液中逐滴滴加氨水,先产生蓝色沉淀,然后沉淀消失,则有
B. :向样品溶液中滴加氯水,再加入 溶液,溶液血红色,则有
C. :向样品溶液中滴加 溶液,产生白色沉淀,再滴加稀盐酸,产生使澄清石灰水变浑浊
的气体,则有
D. :向样品溶液中滴加 溶液,产生使湿润的红色石蕊试纸变蓝的气体,则有
6.(2021秋·吉林·高三校考阶段练习)下列离子的检验方法合理的是
A.向某溶液中滴入硫氰化钾溶液呈红色,说明不含Fe2+
B.向某溶液中通入氯气,然后再加入硫氰化钾溶液变红色,说明原溶液中含有Fe2+
C.向某溶液中加入氢氧化钠溶液,得红褐色沉淀,说明溶液中含有Fe3+
D.向某溶液中加入氢氧化钠溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有
Fe2+,不含有Mg2+
7.(2022秋·安徽·高三校联考阶段练习)某褐色粉末样品,可能含有 、 、 和 中的若干
种,取少量样品进行如下实验:
①滴加过量稀硫酸,粉末溶解,有气体产生且溶液变浑浊,过滤;
②向①的上层清液中滴加过量氯化钡溶液,产生白色沉淀,过滤;
③向②的上层清液中滴加过量氯水,溶液变黄色。
该样品中确定存在的是
A. 和 B.只有
C. 、 和 D. 和
68.(2021·湖南·高考真题)下列实验设计不能达到实验目的的是
实验目的 实验设计
A 检验溶液中 是否被氧化 取少量待测液,滴加 溶液,观察溶液颜色变化
B 净化实验室制备的 气体依次通过盛有饱和 溶液、浓 的洗气瓶
C 测定 溶液的pH 将待测液滴在湿润的pH试纸上,与标准比色卡对照
D 工业酒精制备无水乙醇 工业酒精中加生石灰,蒸馏
A.A B.B C.C D.D
9.(2020·浙江·高考真题)黄色固体X,可能含有漂白粉、 、 、 、 之中的几种或
全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是
A.X中含 ,可能含有
B.X中含有漂白粉和
C.X中含有 ,Y中含有
D.用 酸化溶液Z,若有黄绿色气体放出,说明X中含有
10.(2020·海南·高考真题)下列实验操作或方法,目的可实现的是
操作或方法 实验目的
A 向未知弱酸性试液中滴加含有SCN- 的溶液 确证试液中Fe2+存在
B
等体积0.1 mol·L-1Ag+和[Ag(NH ) ]+溶液分别与大量1 判断多步过程中, 分步反
3 2
mol·L-1葡萄糖碱性溶液形成银镜 应速率与浓度的关系
C
稀H SO 酸化n(KBrO ): n(KBr)= 1 :5的混合液替代
2 4 3 降低液溴的贮存与使用风险
溴水
D
由浑浊情况测定单质硫的溶
向0.1 mol·L-1 Na S O 溶液中缓慢滴加0.2 mol·L-1盐酸
2 2 3 解度
7A.A B.B C.C D.D
1.(2023·河南安阳·统考三模)某化学实验小组设计如下实验探究Zn与溶液中Fe3+发生反应的原理。
实
试剂 现象
验
2 mL0.1 mol· L-1FeCl 溶液、过量
I 3 黄色溶液很快变浅,接着有无色气泡产生,固体中未检出铁单质
锌粉
2 mL1 mol· L-1FeCl 溶液 很快有大量气体产生,出现红褐色浑浊,30 min左右产生红褐色
Ⅱ 3
(pH≈0.70)、过量锌粉 沉淀,溶液颜色变浅,产生少量铁单质
下列说法错误的是
A.实验I说明Fe3+被还原为Fe2+
B.可用酸性高锰酸钾溶液检验实验I得到的溶液中含有Fe2+
C.实验Ⅱ发生了置换反应和复分解反应
D.实验说明Fe3+、H+与Zn的反应与离子浓度有关
2.(2023·广东·校联考模拟预测)下列反应的离子方程式书写正确的是
A.向氯化亚铁溶液中滴入 溶液:
B.向次氯酸钠溶液中通入足量二氧化硫:
C.将氯气通入冷的石灰乳中制漂白粉:
D.向磁性氧化铁粉末中加入稀盐酸:
3.(2023·浙江温州·乐清市知临中学校考二模)下列有关铁及其化合物的实验方案,对应的现象和结论都
正确的是
选
实验方案 现象 结论
项
将红热的铁与水蒸气在高温条件下反 反应结束后有黑色固体生成,且 铁与水蒸气在高温下
A
应,反应结束后,将磁铁靠近产物 该固体被磁铁吸引 反应,生成
为了验证 的还原性,取 溶液于
B 酸性高锰酸钾溶液紫色褪去 具有还原性
试管中,加入酸性高锰酸钾溶液
8取 溶液与试管中,逐滴加入
和 既发生氧
溶液至过量。再加入过量稀盐酸 加入稀盐酸前,溶液由黄色变为
化还原反应,也发生
C 和 溶液 红棕色。加入稀盐酸和 溶 双水解
液后产生白色沉淀
向少量蒸馏水的试管里滴加2滴
与 的配位能
D 溶液,然后再滴加2滴硫氰 溶液变血红色
力小于
化钾溶液
A.A B.B C.C D.D
4.(2023·山西·校联考模拟预测)下列实验操作、现象和结论都正确的是
选
实验操作和现象 结论
项
A 向FeBr 溶液中通入少量的氯气,再滴加少量苯,上层呈橙色 Fe3+的氧化性比Br 强
2 2
B 室温下,向碳酸氢钠溶液中加入适量盐酸,温度下降 碳酸氢钠和盐酸反应吸收热量
将少量BaSO 固体用饱和Na CO 溶液浸泡,过滤后,向滤渣中加盐 相同温度下,
C 4 2 3
酸,滤渣溶解,产生气泡 K (BaCO )