文档内容
(新高考)小题必练17:物质的检验、分离与提纯
主要考查物质的检验方法和原理、混合物的分离与提纯方法、相关实验操作及其注意事
项等。
1【. 2020年全国卷2】某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进行如
4 3
下实验:①混合物溶于水,得到澄清透明溶液;②做焰色反应,通过钴玻璃可观察到紫色;
③向溶液中加碱,产生白色沉淀。根据实验现象可判断其组成为( )
A.KCl、NaCl B.KCl、MgSO C.KCl、CaCO D.MgSO 、NaCl
4 3 4
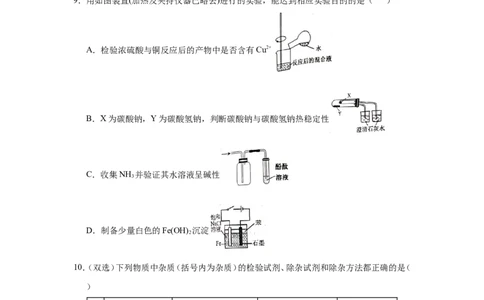
2.【2020年山东卷】实验室分离Fe3+和Al3+的流程如下:
知Fe3+在浓盐酸中生成黄色配离子[FeCl ]−,该配离子在乙醚(Et O,沸点34.6℃)中生成缔
4 2
合物 。下列说法错误的是( )
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
3.【2020年天津卷】检验下列物所选用的试剂正确的是( )
待检验物质 所用试剂
A 海水中的碘元素 淀粉溶液
B SO 气体 澄清石灰水
2
C 溶液中的Cu2+ 氨水D 溶液中的NH NaOH溶液,湿润的蓝色石蕊试纸
1.中国传统文化对人类文明贡献巨大,下列各文献中所记载的古代化学研究过程或成果不
涉及分离提纯操作的的是( )
A.《本草纲目》“(烧酒)自元时始创其法,用浓酒和精入甑,蒸令气上……其清如水,味极
浓烈,盖酒露也。”
B.(齐民要术》“凡酿酒失所味者,或初好后动未压者,皆宜翅(同“回”)作醋。”
C.《开宝本草》“(消石)所在山泽,冬月地上有霜扫取,以水淋汁,后乃煎炼而成。”
D.《本草行义》“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然
下垂如乳,尖长者为胜,平短者次之。”
2.“水飞”是传统中医中将不溶的药材与适量水共研细,取极细药材粉末的方法。《医学入
门》中记载提纯铜绿的方法:“水洗净,细研。水飞去石澄清,慢火熬干。”文中涉及的操
作方法是( )
A.洗涤、溶解、过滤、蒸发 B.洗涤、溶解、过滤、灼烧
C.洗涤、萃取、过滤、蒸馏 D.洗涤、萃取、过滤、蒸发
3.利用图中所示装置及试剂,能达到相应实验目的的是( )
试剂甲 试剂乙 实验目的
从Cl 和SO 的混
2 2
A 饱和食盐水 浓硫酸
合气体中分离出SO
2
B NaOH溶液 浓硫酸 除去乙烷中的HS
2
C 溴水 浓硫酸 除去C H 中的CH
2 4 4
D NaOH溶液 浓硫酸 除去NO 中的NO
2
4.从溴水中提取溴,下列方法中最适宜的是( )
A.蒸馏 B.过滤 C.萃取 D.结晶
5.雾霾含有大量的污染物SO 、NO。工业上变“废”为宝,吸收工业尾气SO 和NO,可获得
2 2
NaSO 和NH NO 产品的流程图如下(Ce为铈元素):
2 2 3 4 3下列说法错误的是( )
A.NaSO 中S元素的化合价为+3
2 2 4
B.装置Ⅱ消耗36g水生成4N 个H+(N 代表阿伏伽德罗常数)
A A
C.装置Ⅲ用甲烷燃料电池进行电解,当消耗24g甲烷时,理论上可再生10mol Ce4+
D.装置Ⅳ获得粗产品NH NO 的实验操作依次为蒸发浓缩、冷却结晶、过滤、洗涤等。
4 3
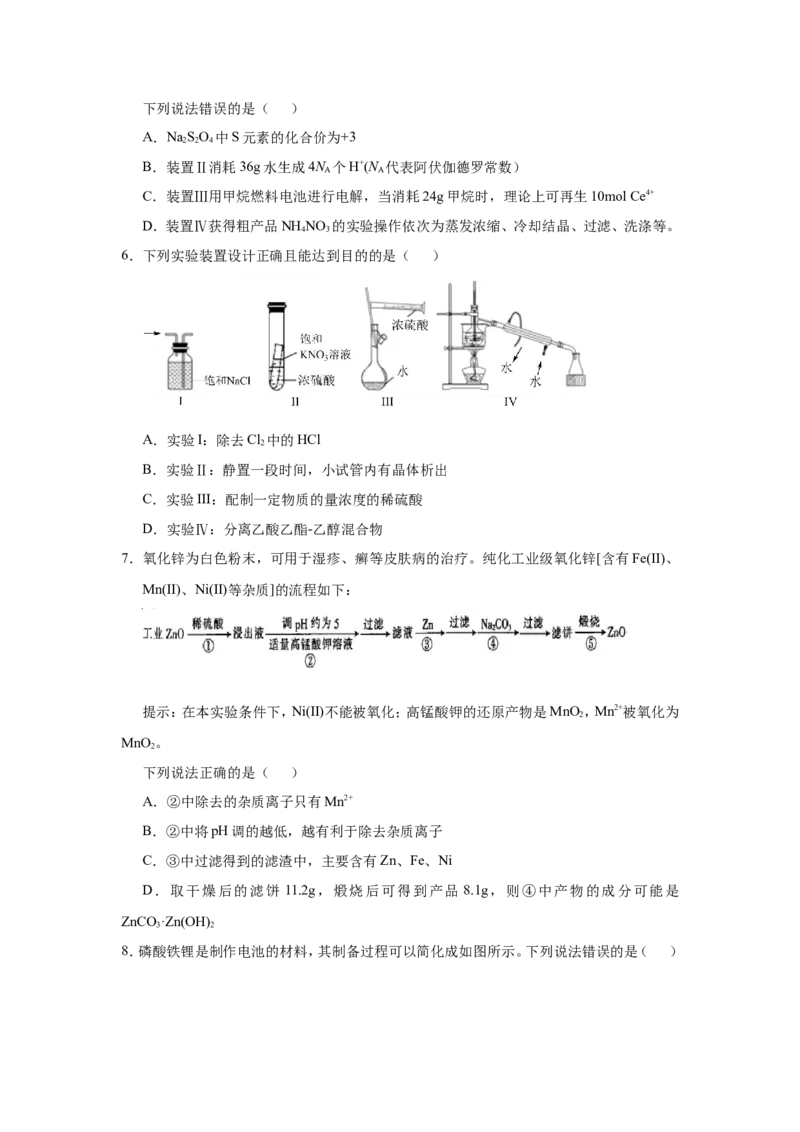
6.下列实验装置设计正确且能达到目的的是( )
A.实验I:除去Cl 中的HCl
2
B.实验Ⅱ:静置一段时间,小试管内有晶体析出
C.实验III:配制一定物质的量浓度的稀硫酸
D.实验Ⅳ:分离乙酸乙酯-乙醇混合物
7.氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌[含有Fe(II)、
Mn(II)、Ni(II)等杂质]的流程如下:
提示:在本实验条件下,Ni(II)不能被氧化;高锰酸钾的还原产物是MnO ,Mn2+被氧化为
2
MnO 。
2
下列说法正确的是( )
A.②中除去的杂质离子只有Mn2+
B.②中将pH调的越低,越有利于除去杂质离子
C.③中过滤得到的滤渣中,主要含有Zn、Fe、Ni
D.取干燥后的滤饼 11.2g,煅烧后可得到产品 8.1g,则④中产物的成分可能是
ZnCO ·Zn(OH)
3 2
8.磷酸铁锂是制作电池的材料,其制备过程可以简化成如图所示。下列说法错误的是( )A.蒸发需要的硅酸盐材料仪器有:烧杯、酒精灯、玻璃棒、泥三角
B.反应釜中反应的化学方程式为2HPO +LiCO=2LiHPO +HO+CO↑
3 4 2 3 2 4 2 2
C.分离的操作是过滤
D.烧结窑中氧化铁与炭黑发生氧化还原反应
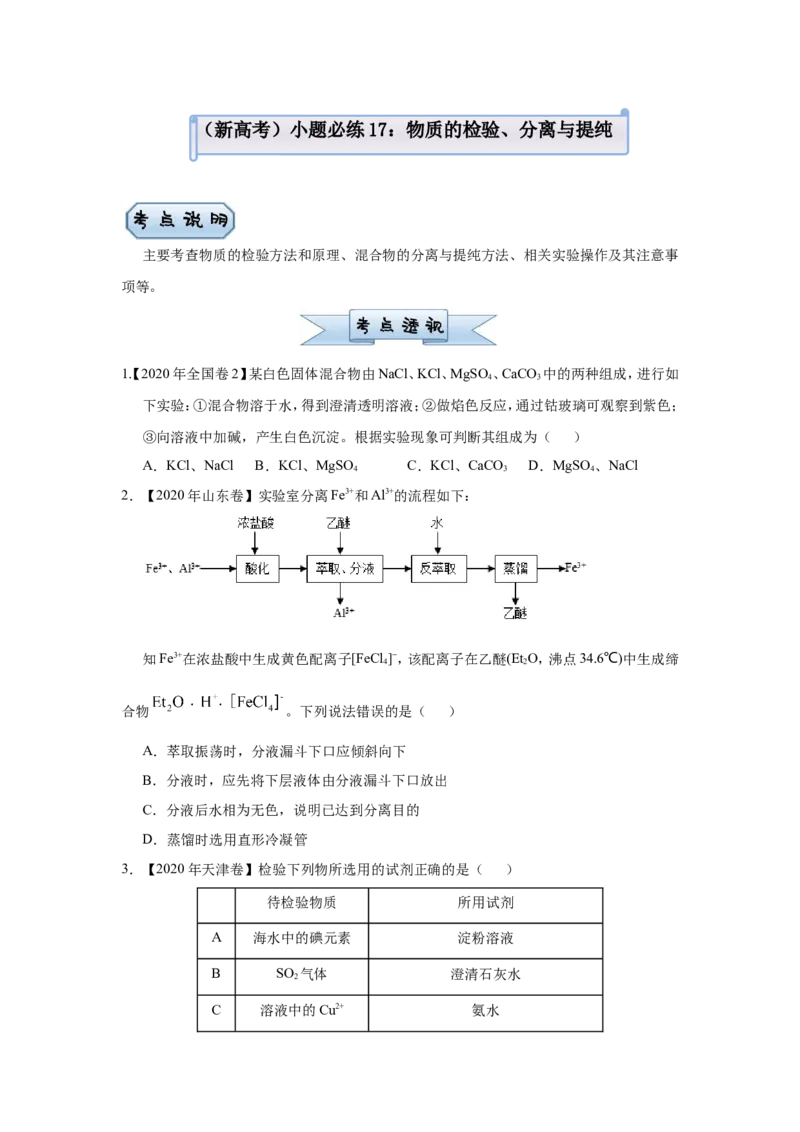
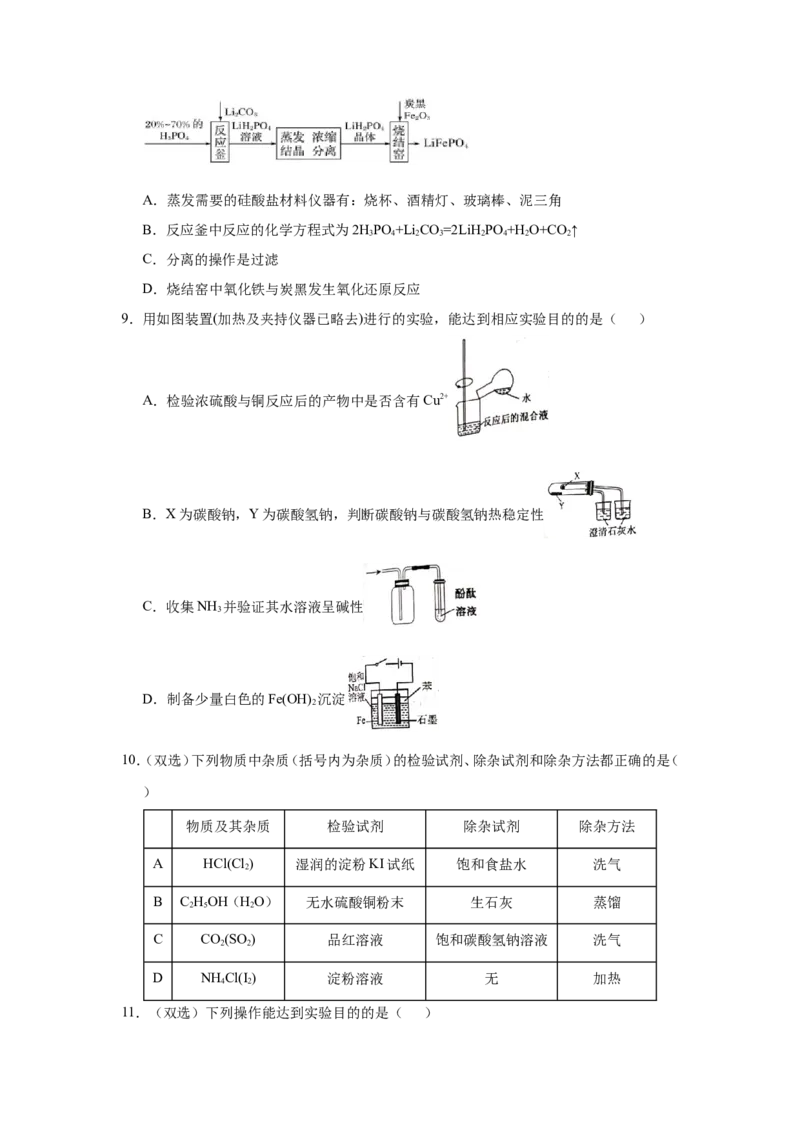
9.用如图装置(加热及夹持仪器已略去)进行的实验,能达到相应实验目的的是( )
A.检验浓硫酸与铜反应后的产物中是否含有Cu2+
B.X为碳酸钠,Y为碳酸氢钠,判断碳酸钠与碳酸氢钠热稳定性
C.收集NH 并验证其水溶液呈碱性
3
D.制备少量白色的Fe(OH) 沉淀
2
10.(双选)下列物质中杂质(括号内为杂质)的检验试剂、除杂试剂和除杂方法都正确的是(
)
物质及其杂质 检验试剂 除杂试剂 除杂方法
A HCl(Cl ) 湿润的淀粉KI试纸 饱和食盐水 洗气
2
B C HOH(HO) 无水硫酸铜粉末 生石灰 蒸馏
2 5 2
C CO(SO ) 品红溶液 饱和碳酸氢钠溶液 洗气
2 2
D NH Cl(I ) 淀粉溶液 无 加热
4 2
11.(双选)下列操作能达到实验目的的是( )目的 操作
A 除去苯中少量的苯酚 加入适量NaOH溶液,振荡、静置、分液
将盐酸与NaHCO 混合产生的
3
B 证明酸性:碳酸>苯酚
气体直接通入苯酚钠溶液
将尖嘴垂直向下,挤压胶
C 除去碱式滴定管胶管内的气泡
管内玻璃球将气泡排出
配制用于检验醛基 向试管中加入2mL 10% NaOH
D
的氢氧化铜悬浊液 溶液,再滴加数滴2% CuSO 溶液,振荡
4
12.(双选)用铁泥(主要成分为Fe O、FeO和少量Fe)制备超顺磁性(平均直径25nm)纳米
2 3
Fe O 的流程示意图如图:
3 4
下列叙述不正确的是( )
A.常用热的NaCO 溶液除去钢铁表面的油污
2 3
B.步骤②中,主要反应的离子方程式是2Fe3++Fe=3Fe2+
C.步骤④中,应加入过量的HO
2 2
D.步骤⑤中,得到的Fe O 粒子,是一种胶体
3 4
13.(双选)下列操作不能达到实验目的的是( )
目的 操作
用已知浓度的NaOH溶液滴定
A 证明草酸是二元酸
一定体积已知浓度的草酸溶液
B 除去甲烷中的少量乙烯 将气体通过酸性高锰酸钾溶液,再通过浓硫酸
C 检验绿矾是否氧化 取少量绿矾溶于蒸馏水,再加入K[Fe(CN) ]溶液
3 6
D 鉴别1-丙醇和2-丙醇 做核磁共振氢谱
14.化工催化剂中往往含有大量有用成分,其回收利用具有重要意义。以某种废镍催化剂(主
要成分为NiCO 和SiO,含少量Fe O、Cr O)为原料制备硫酸镍和重铬酸钾晶体的工业
3 2 2 3 2 3
流程如图:已知:①NiS、Ni(OH) 、Cr(OH) 均难溶于水;
2 3
②Cr(OH) 是两性氢氧化物,碱性溶液中以Cr(OH)形式存在,酸性溶液中以Cr3+形式存在;
3
③Ni(OH) 能溶于氨水生成[Ni(NH )]2+。
2 3 6
根据上述信息回答下列问题:
(1)滤渣I和滤渣II的主要成分分别为 、 。
(2)“碱析”中Cr元素转化的离子反应方程式为 。
(3)“氧化I”的离子方程式为 。
(4)进行“氧化II”时,所加KMnO 溶液须过量,原因是 。
4
(5)“系列操作b”包括___、___、过滤、洗涤、干燥。为了减少KCr O 晶体的损耗,最好选
2 2 7
用下列物质中的___作洗涤剂。
A.酒精 B.饱和氯化钠溶液 C.20℃蒸馏水 D.40℃蒸馏水
参考答案
考点透视
1.【答案】B
【解析】①混合物溶于水,得到澄清透明溶液,则不含CaCO ,排除C选项;②做焰色反应,
3
通过钴玻璃可观察到紫色,可确定含有钾元素,即含有KCl;③向溶液中加碱,产生白色沉淀,则应含有MgSO ,综合以上分析,混合物由KCl和MgSO 两种物质组成,选B。
4 4
【点睛】常用焰色反应来检验钠元素和钾元素。
2.【答案】A
【解析】A.萃取振荡时,分液漏斗下口应倾斜向上,A错误;B.分液时,密度大的液体在下
层,密度小的液体在上层,下层液体由分液漏斗下口放出,下层液体放完后,密度小的上层液
体从分液漏斗上口倒出,B正确;C.Fe3+在浓盐酸中生成黄色配离子,该离子在乙醚中生成缔
合物,乙醚与水不互溶,故分液后水相为无色,则水相中不再含有Fe3+,说明已经达到分离目
的,C正确;D.蒸馏时选用直形冷凝管,能使馏分全部转移到锥形瓶中,而不会残留在冷凝管
中,D正确;答案选A。
【点睛】常见的基本实验操作的考查,主要对学生的识记、应用的考查。
3.【答案】C
【解析】A.淀粉溶液可以检验碘单质,不能检验碘元素,故A错误;B.能使澄清石灰水变
浑浊的气体可以是二氧化硫或二氧化碳,应该用品红检验二氧化硫气体,故B错误;C.铜离
子遇到氨水会先产生氢氧化铜蓝色沉淀,继续加氨水会生成四氨合铜离子,检验铜离子可以
用氨水,故C正确;D.铵根离子遇氢氧化钠溶液(加热)生成氨气,氨气能使湿润的红色石蕊
试纸变蓝,不能使用湿润的蓝色石蕊试纸检验氨气,故D错误;答案选C。
【点睛】常常利用品红溶液来检验二氧化硫气体。
考点突破
1.【答案】B
【解析】A.由“浓酒和精入甑,蒸令气上”可知,该过程中所采用的是蒸馏法提高酒精浓
度,涉及分离提纯操作;B.由“酿酒”、“皆宜翅(同“回”)作醋”可知,其所描述的是酒精
转化为醋酸,未涉及分离提纯操作;C.由“有霜扫取,以水淋汁,后乃煎炼而成”可知,该过
程中所涉及溶解、蒸发结晶分离提纯操作;D.该过程所描述的是将生砒加热升华,然后砒烟
在容器上凝华,涉及升华、凝华分离提纯操作;综上所述,涉及分离提纯操作的是B项,故答
案为B。
2.【答案】A
【解析】提纯铜绿的方法:“水洗净,细研,水飞去石澄清,慢火熬干”,可知洗涤后,溶解
于水中,过滤后蒸发,因铜绿加热灼烧可发生分解,则不能灼烧,即文中涉及的操作方法是洗
涤、溶解、过滤、蒸发。故答案选:A。
3.【答案】B【解析】A.Cl 和SO 的混合气体在饱和食盐水中反应生成硫酸和盐酸,不能分离出SO ,
2 2 2
故A不符合题意;B.NaOH溶液与HS气体反应,乙烷不和NaOH溶液反应,浓硫酸干燥乙
2
烷气体,能达到实验目的,故B符合题意;C.溴水和C H 反应,不和CH 反应,需要保留的物
2 4 4
质被反应了,不能达到实验目的,故C不符合题意;D.2NO +2NaOH=NaNO +
2 2
NaNO +HO,NO+NO +2NaOH=2NaNO +HO,虽然NO已除去,但NO 也被反应了,不能达
3 2 2 2 2 2
到实验目的,故D不符合题意。综上所述,答案为B。
【点睛】主要涉及物质的除杂,一般注意除杂的原则,不能减少被提纯的物质,不能引入新
的杂质等。
4.【答案】C
【解析】萃取利用溶质在不同溶剂中溶解度不同,用一种溶剂把溶质从它与另一溶剂所组
成的溶液中提取出来,溴在水和有机溶剂中溶解度差异较大,可以采用萃取方法。故选C。
5.【答案】C
【解析】A.根据化合物中元素化合价代数和等于0,由于Na是+1价,O为-2价,所以
NaSO 中S元素的化合价为+3,A正确;B.36g水的物质的量是2mol,在装置II中发生反应:
2 2 4
NO+2H O+3Ce4+=3Ce3++NO+4H+,NO+H O+Ce4+=Ce3++NO+2H+,可见两个反应都是消耗
2 2
1mol HO,会产生2mol H+,则反应消耗2mol HO,就产生4mol H+,生成H+的数目等于4N
2 2 A
个,B正确;C.24g甲烷的物质的量为n(CH)=24g÷16g/mol=1.5mol,在碱性甲烷燃料电池中,
4
通入甲烷的电极为负极,失去电子发生氧化反应,电极反应式为: CH-8e−
4
+10OH−=CO+7H O,1mol甲烷反应失去8mol电子,则1.5mol甲烷完全反应转移电子的物质
2
的量为n(e−)=8×1.5mol=12mol,由于在同一闭合回路中电子转移数目相等,所以当消耗24g
甲烷时,理论上可再生12mol Ce4+,C错误;D.由于NH NO 高温易分解,因此从溶液中得到
4 3
粗产品NH NO 的实验操作依次为蒸发浓缩、冷却结晶、过滤、洗涤等,D正确;故合理选项
4 3
是C。
6.【答案】B
【解析】A.除去Cl 中的HCl可用饱和NaCl溶液洗气,进气方向为长进短出,A错误;B.
2
浓硫酸具有吸水性,导致饱和硝酸钾溶液中溶剂减少,因而有硝酸钾晶体析出,B正确;C.浓
硫酸不能在容量瓶中稀释,应在烧杯中稀释、冷却后转移到容量瓶中,C错误;D.蒸馏时温度
计水银球应该放在蒸馏烧瓶支管出口处,D错误。答案选B。
7.【答案】D
【解析】纯化工业级氧化锌和稀硫酸反应导致溶液中存在Fe2+、Mn2+、Zn2+和Ni2+,向浸出液中加入适量高锰酸钾溶液并调节溶液的pH约为5,Ni(Ⅱ)不能被氧化,Fe2+、Mn2+被氧化而
被除去,同时溶液中有MnO 生成,过滤后,向滤液中加入Zn过滤,Zn和Ni2+发生氧化还原
2
反应生成Ni,溶液中存在Zn2+,向滤液中加入碳酸钠溶液,生成碳酸锌沉淀,煅烧碳酸锌沉淀
生成ZnO。A.根据题意,Ni(Ⅱ)不能被氧化,反应②中除掉的杂质离子是Fe2+和Mn2+,故A错
误;B.加高锰酸钾溶液前,若pH较低,铁离子和锰离子不能生成沉淀,从而无法除去铁和锰
杂质,故B错误;C.反应③为锌与镍离子的发生反应得到锌离子和镍,反应类型为置换反应;
得到的滤渣中,除了过量的锌外还有金属镍,故 C 错误;D.根据关系式可知
xZnCO ·yZn(OH) ~(x+y)ZnO
3 2
解得x=y,所以④中产物的成分可能是ZnCO ·Zn(OH) ,故D正确;答案选D。
3 2
8.【答案】A
【解析】A.蒸发需要的硅酸盐材料仪器有:蒸发皿、酒精灯、玻璃棒,A项错误;B.强酸制
弱酸原理,反应釜中反应的化学方程式为2HPO +LiCO=2LiHPO +HO+CO↑,B项正确;
3 4 2 3 2 4 2 2
C.最后得到LiH PO 晶体,分离的操作是过滤,C项正确;D.铁的化合价下降,烧结窑中氧化
2 4
铁与炭黑发生氧化还原反应,D项正确;答案选A。
【点睛】坩埚常用于高温灼烧的操作中。
9.【答案】D
【解析】A.检验浓硫酸与铜反应后的产物中是否含有Cu2+,操作错误,因为产物中还残留
部分浓硫酸,应该是产物加入水中稀释,不是向产物中加水,故A错误;B.碳酸钠比碳酸氢
钠稳定,所以大试管内加入碳酸钠,小试管内加入碳酸氢钠,大试管温度高,小试管温度低,
碳酸氢钠受热分解,而碳酸钠受热不分解,才能比较碳酸钠和碳酸氢钠的热稳定性,故B错
误;C.收集NH 时,氨气的密度比空气密度小,用向上排空气法,因此收集氨气的导管是短
3
进长出,故C错误;D.制备少量白色的Fe(OH) 沉淀,电解饱和的食盐水,在阴极产生氢氧根
2
离子,阳极金属铁失电子变成二价亚铁离子,在无氧环境中,可以制备少量的白色的Fe(OH)
2
沉淀,故D正确;答案选:D。
10.【答案】BC
【解析】A.饱和食盐水除去的是氯化氢,不能除去氯气,故A错误;B.无水硫酸铜遇水变
为蓝色,可以检验水的存在,生石灰与水反应生成氢氧化钙,然后蒸馏即可得到无水乙醇,故
B正确;C.碳酸氢钠溶液不吸收二氧化碳,故C正确;D.氯化铵加热分解生成氨气和氯化氢,
不能除去碘,故D错误;故选BC。【点睛】明确物质的性质差异是解答的关键,注意物质提纯的原则:不增、不减、易复、易
分。所谓不增,不引进新的物质;不减指不能损耗或减少被提纯的物质;易复指被提纯物质转
化后易复原;易分指易使杂质与被提纯的物质分离。
11.【答案】AD
【解析】A.苯酚可与氢氧化钠溶液反应生成可溶于水的苯酚钠,最后与苯混合后互不相溶,
分层,该操作能达到实验目的,故A正确;B.盐酸易挥发,若将盐酸与碳酸氢钠溶液混合产
生的气体直接通入苯酚钠,可能挥发的HCl会与苯酚钠反应生成常温下难溶于水的苯酚,不
能证明是二氧化碳与其发生的反应,达不到实验目的,应该先除去二氧化碳中可能挥发的
HCl再进行实验操作,故B错误;C.除去碱式滴定管胶管内气泡时,尖嘴不应该垂直向下,应
向上挤压橡胶管,利用空气排出,该实验操作达不到实验目的,故C错误;D.为检验醛基,配
制氢氧化铜悬浊液时,碱需过量,保证醛基是在碱性条件下发生反应,该操作可达到实验目
的,故D正确;答案选AD。
12.【答案】CD
【解析】铁泥(主要成分为Fe O、FeO和少量Fe)与稀盐酸反应得到的滤液A溶质为氯化
2 3
铁、氯化亚铁、过量的稀盐酸,加入铁粉还原铁离子:2Fe3++Fe=3Fe2+,过滤过量的铁,滤液B
的溶质为氯化亚铁,加入氢氧化钠溶液,生成Fe(OH) 浑浊液,向浑浊液中加入双氧水氧化:
2
2Fe(OH)+H O=2FeOOH+2H O,反应完成后需再加热一段时间除去剩余HO,再与氯化亚
2 2 2 2 2 2
铁加热搅拌发生反应:2FeOOH+Fe2++2OH−=Fe O+2H O,过滤、洗涤、干燥得产品Fe O,以
3 4 2 3 4
此解答该题。A.钢铁表面的油污在碱性条件下可以发生水解反应,NaCO 是强碱弱酸盐溶
2 3
液,显碱性,热的NaCO 溶液可以让油脂水解,水解是吸热的,温度升高,水解平衡向吸热的
2 3
方向移动,水解效果越好,选项A正确;B.滤液A溶质为氯化铁、氯化亚铁、过量的稀盐酸,
加入铁粉还原铁离子和反应过量的盐酸:2Fe3++Fe=3Fe2+,选项B正确;C.步骤④中,防止其
在步骤⑤中继续氧化+2价铁元素,反应完成后需再加热一段时间除去剩余HO,故不要加
2 2
入过量的HO,选项C不正确;D.超顺磁性的Fe O 粒子平均直径25nm,属于纯净物而不是
2 2 3 4
胶体,选项故D不正确;答案选CD。
13.【答案】BC
【解析】A.用已知浓度的NaOH溶液滴定一定体积已知浓度的草酸溶液,可根据消耗的
NaOH溶液的体积来计算出NaOH与草酸的化学计量数,从而可得出草酸是否为二元酸,故
A不选;B.乙烯能被酸性高锰酸钾氧化成二氧化碳和水,二氧化碳既不溶液浓硫酸也不与农
浓硫酸反应,则产生的二氧化碳不能被除去,故选B;C.绿矾为十二水硫酸亚铁,溶液水后含亚铁离子,亚铁离子能与K[Fe(CN) ]反应生成蓝色沉淀,但若只有部分被氧化,同样也有该
3 6
实验现象,则不能用K[Fe(CN) ]检验明矾是否变质,故选C;D.1-丙醇和2-丙醇的H原子所
3 6
在环境不同,在核磁共振氢谱图中的吸收峰也就不同,故D不选。答案选BC
【点睛】检验某种物质是否变质,应该检测的是假如变质后产生的离子,根据其选择相应
的试剂。
14.【答案】(1)SiO Fe(OH)
2 3
(2)Cr3++3OH−=Cr(OH) ↓和Cr(OH) +OH−=Cr(OH)
3 3
(3)3NiS+8H++8NO=3Ni2++3SO+8NO↑+4H O
2
(4)溶液中有过量的Cl−会消耗高锰酸钾
(5)蒸发浓缩(或加热浓缩) 冷却结晶 A
【解析】废镍催化剂(主要成分为NiCO 和SiO,含少量Fe O、Cr O)为原料制备硫酸镍,
3 2 2 3 2 3
加入20%的硫酸酸溶、过滤,滤渣Ⅰ为SiO,滤液加入KOH溶液进行一次碱析,滤液Ⅰ含有
2
CrO,加入盐酸酸化,生成Cr3+,加入高锰酸钾溶液,Cr3+被氧化成重铬酸根离子,蒸发浓缩,
冷却结晶获得重铬酸钾;沉淀加入氯化铵、氨水缓冲液,由信息②可知滤渣Ⅱ为氢氧化铁,过
滤得到的滤液含有[Ni(NH )]2+,“净化”时加入的HS,将镍元素转化为NiS沉淀,加入硝酸
3 6 2
氧化,可生成S和Ni2+,加入氢氧化钠生成Ni(OH) ,过滤后加入硫酸可得到硫酸镍,经蒸发
2
浓度、冷却结晶得到晶体。(1)NiCO 、Fe O 和Cr O 均溶于硫酸,SiO 不溶于硫酸,“滤渣
3 2 3 2 3 2
Ⅰ”的主要成分为SiO,沉淀加入氯化铵、氨水缓冲液,由信息②可知滤渣Ⅱ为Fe(OH) ;(2)
2 3
三氧化铬溶于硫酸生成硫酸铬和水,加入氢氧化钾溶液后生成Cr(OH) 和KCr(OH) ,反应的
3 4
离子方程式是Cr3++3OH−=Cr(OH) ↓和Cr(OH) +OH−=Cr(OH);(3)镍离子遇到硫化氢生成硫化
3 3
镍沉淀,加稀硝酸氧化产生硫酸镍,一氧化氮和水,反应的离子方程式是 3NiS+8H+
+8NO=3Ni2++3SO+8NO↑+4H O;(4)进行“氧化II”时,所加KMnO 溶液须过量,原因是溶液
2 4
中有过量的Cl−会消耗高锰酸钾,故答案为:溶液中有过量的Cl−会消耗高锰酸钾;(5)从溶液
中获得重铬酸钾晶体,需要蒸发浓缩(或加热浓缩)、冷却结晶、过滤、洗涤、干燥,洗涤时为了
减少KCr O 晶体的损耗,降低重铬酸钾的溶解度,最好选用有机溶剂,故答案为:蒸发浓缩
2 2 7
(或加热浓缩);冷却结晶;A。