文档内容
大题优练 12
以推断元素为背景的物质结构与性质
优 选 例 题
例:熟记元素周期表,熟知元素周期律对于化学学习是至关重要的:现有 A、B、C、D、E、F原子序数依次
增大的六种元素,它们分别位于元素周期表的前四周期。B元素含有3个能级,且每个能级所含的电子数
相同;D的原子核外有8个运动状态不同的电子,B、C、D均可与A形成10电子微粒,E元素与F元素
处于同一周期相邻的族,它们的原子序数相差 3,且E元素的基态原子有4个未成对电子。请回答下列问
题:
(1)请写出F基态原子的电子排布式:___________,F元素位于周期表的___区。
(2)B、C、D基态原子第一电离能由小到大的顺序为_____________(用元素符号表示)。
(3)已知(BC) 是直线型分子,并有对称性,且分子中每个原子最外层都达到8电子稳定结构,则(BC) 中σ
2 2
键和π键的个数比为_____________。
(4)E的单质和C的氢化物在640°C可发生置换反应,产物之一的晶胞结构如图1所示,写出该反应的化学
方程式: 。
(5)立方硫化锌晶胞与金刚石晶胞类似,结构如图 2,其中a代表S2−,b代表Zn2+。则该晶胞中S2−的配位
数为_______,若晶体的密度为ρ g·cm−3,则晶胞的体积为 cm3(用N 表示阿伏加德罗常数数值)。
A
【答案】(1)[Ar]3d104s1 ds
(2)C”或“<”),电负性C____D(“>”或“<”) 。
(3)CD中心原子杂化方式_____,CA 立体构型_____。
3
(4)E元素的焰色反应呈黄色,金属元素能产生焰色反应的微观原因为________。
(5)已知B元素的某种单质结构如图所示,且晶胞边长为a pm,B原子的摩尔质量为M g/mol,N 为阿伏加
A
德罗常数,则两个最近的B原子之间的距离为__________pm,该晶体的密度为__________g/cm3。
【答案】(1)3d54s1 共价键、离子键
(2)> <
(3)sp2杂化 三角锥
(4)电子从较高能级的激发态跃迁到较低能级的激发态乃至基态时,会以光的形式释放能量
(5)
【解析】A、B、C、D、E、F为前四周期原子序数依次增大的六种元素,已知 A元素的某种核素没有中
子,A为H元素;B元素基态原子中有3个不同能级且各能级中的电子数相等,B为C元素;D元素的最外
层电子数是其电子层数的3倍,D为O元素;因原子序数依次增大,则C为N元素;E元素的焰色反应呈黄
色,E为Na元素;F元素是第四周期未成对电子数最多的元素,其原子的价层电子排布式应该是 3d54s1,F
为Cr元素。(1)F是Cr元素,原子的价层电子排布式为3d54s1,O与Na元素形成的NaO 是由钠离子和过氧
2 2
离子构成,过氧离子中的两个O原子以共价键相结合,则NaO 所含化学键的类型是离子键和共价键;(2)同
2 2
周期从左到右,基态原子第一电离能呈增大趋势,但N元素的原子为半充满的稳定结构,第一电离能大于O
元素;同周期从左到右,元素的电负性逐渐增大,则电负性 N<O;(3)NO中心原子的价层电子对数为:3+=3,则NO中心原子的杂化方式为sp2;NH 的中心原子价层电子对数为:3+ =3+1=4,
3
含有1个孤电子对,所以其立体构型为三角锥形;(4)Na元素的焰色反应呈黄色,金属元素能产生焰色反应的
微观原因为:电子从较高能级的激发态跃迁到较低能级的激发态乃至基态时,会以光的形式释放能量;(5)据
图可知,晶胞中两个最近的C原子之间的距离为该晶胞体对角线长度的 ,晶胞边长为a pm,则两个最近的
C 原子之间的距离为: pm;晶胞中所含的原子个数为:4+8× +6× =8,晶胞的体积为:
(a×10−10)3cm3,则该晶体的密度为: g/cm3= g/cm3。
3.A、X、Y、B、C、D、E、M是前30号元素,原子序数依次增加。A原子是周期表中半径最小的原子;X
的基态原子次外层有2个电子,最外层有3个未成对电子;Y原子的2p轨道上有1个电子的自旋方向与
其它电子相反;B的价层电子排布式为ns1,C和Y形成的化合物是引起酸雨的主要大气污染物,常温下,
D的单质是一种黄绿色的气体;E的+3价离子的3d轨道为半充满状态,M与E元素位于同一周期,且为
ⅠB族元素。
(1)B、Y、C分别形成的简单离子的半径由大到小顺序为(填离子符号)_________。
(2)元素D基态原子的核外电子排布式为________,其同周期元素中,第一电离能最大的是______(写
元素符号)。
(3)M与D形成的一种化合物的立方晶胞如图所示。
①该化合物的化学式为_______。②此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_______,其中配位
体为_______分子(填“极性”或“非极性”)。
(4)基态C原子电子占据最高能级的电子云轮廓图为_______形。将AC通入ED 溶液中反应的离子方
2 3
程式为_________________。
(5)用200mL 1mol·L−1的BYA溶液吸收4.48L(标准状况)CY 所得溶液的pH<7,溶液中离子浓度由大
2
到小的顺序为_______________________。
(6)工业上用电化学法治理酸性废液中XY的原理如图,阴极的电极反应式为_______。
【答案】(1)S2−>O2−>Na+
(2)1s22s22p63s23p5或[Ne]3s23p5 Ar
(3)CuCl [Cu(NH )]2+ 极性
3 4
(4)哑铃 HS+2Fe3+=2Fe2++S↓+2H+
2
(5)c(Na+)>c(HSO)>c(H+)>c(SO)>c(OH−)
(6)2NO+10e−+12H+=N ↑+6H O
2 2
【解析】A原子是周期表中半径最小的原子,所以A为H元素;X的基态原子次外层有2个电子,最外层
有3个未成对电子,则X的核外电子排布式为1s22s22p3,X为N元素;Y原子的2p轨道上有1个电子的自旋
方向与其它电子相反,则Y的2p轨道电子排布式为2p4,所以Y为O元素;常温下,D的单质是一种黄绿色
的气体,则D为Cl元素;C和Y形成的化合物是引起酸雨的主要大气污染物,且C的原子序数大于O小于
Cl,所以C为S;B的价层电子排布式为ns1,其原子序数大于O且小于S,则其价层电子排布式为3s1,所以
B为Na元素;E的+3价离子的3d轨道为半充满状态,则其原子的价层电子排布为3d64s2,为Fe元素;M与
E元素位于同一周期,且为ⅠB族元素,则M为Cu元素。(1)B、Y、C形成的简单离子为Na+、O2−、S2−,离
子核外电子层数越多半径越大,电子层数相同,核电荷数越小半径越大,所以离子半径由大到小顺序为:S2−>O2−>Na+;(2)Cl元素为17号元素,原子的基态原子核外电子排布式为1s22s22p63s23p5或[Ne]3s23p5;同周期
元素中自左至右第一电离能呈增大趋势,Ar元素为该周期最右端元素,且其最外层电子为全满状态,所以第
一电离能最大;(3)①根据均摊法,该晶胞中Cl原子数目为 =4,Cu原子数目为4,所以该化合物
的化学式为CuCl;②此化合物的氨水溶液遇到空气则被氧化为深蓝色,说明Cu+被氧化成Cu2+,继而与NH
3
形成配离子:[Cu(NH )]2+;配位体为NH ,其空间构型为三角锥形,正负电荷中心不重合,为极性分子;(4)
3 4 3
基态S原子电子占据最高能级为3p能级,电子云轮廓图为哑铃形;将HS通入FeCl 溶液中,Fe3+可将-2价的
2 3
S元素氧化成S,自身被还原成Fe2+,离子方程式为:HS+2Fe3+=2Fe2++S↓+2H+;(5)用200mL 1mol·L−1的
2
NaOH溶液吸收4.48L(标准状况)即0.2mol SO 溶液所得溶液中的溶质为NaHSO,溶液pH<7,说明HSO的电
2 3
离程度大于水解程度,所以溶液中离子浓度由大到小为:c(Na+)>c(HSO)>c(H+)>c(SO)>c(OH−);(6)电解时阴
极上NO发生得电子的还原反应生成N,则其阴极的反应式为2NO+12H++10e−=N ↑+6H O。
2 2 2
4.X、Y、Z、R、W均为元素周期表中前四周期的元素,其原子序数依次增大;X2−和Y+有相同的核外电子
排布;Z的氢化物的沸点比其上一周期同族元素氢化物的沸点低;R的基态原子在前四周期元素的基态原
子中单电子最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实
验室制取Z的气态单质。回答下列问题(相关问题均用元素符号或化学式表示):
(1)R的基态原子的核外电子排布式是___________________。
(2)Z的氢化物的沸点比其上一周期同族元素氢化物的沸点低的原因是_______________。
(3)X与Z中电负性较大的是_________;Z的某种含氧酸盐常用于实验室中X单质的制取,此酸根离子的
空间构型是__________,此离子中含有的化学键类型是__________;X—Z—X的键角______109°28'(填“>”
“<”或“=”)。
(4)X与Y形成的化合物YX的晶胞如图。其中X离子的配位数为_______,以距离一个X离子最近的所
2
有Y离子为顶点构成的几何体为________。该化合物与MgO相比,熔点较高的是____________。
(5)已知该化合物的晶胞边长为a pm,则该化合物的密度为_________g/cm3。(列算式,不必计算出数值,阿伏伽德罗常数的数值为N )
A
【答案】(1)[Ar]3d54s1
(2)HF分子间形成氢键,HCl分子间不存在氢键
(3)O 三角锥形 共价键 <
(4)8 正方体 MgO
(5)
【解析】X、Y、Z、R、W均为周期表中前四周期的元素,其原子序数依次增大;X2−和Y+有相同的核外
电子排布,则X在Y上一周期,且X位于第VIA族、Y位于第IA族;Z的氢化物的沸点比其上一周期同族
元素氢化物的沸点低,则Z氢化物中不含氢键,其上一周期同一主族元素氢化物有氢键;R的基态原子在前
四周期元素的基态原子中单电子数最多,则R为Cr元素;X位于第二周期,为O元素;Y、Z位于第三周期,
Y为Na元素;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制
取Z的气态单质,实验室用浓盐酸和二氧化锰制取氯气,所以 W为Mn元素,Z为Cl元素。(1)R为Cr元素,
其原子核外有 24 个电子,根据构造原理书写 R 的基态原子的核外电子排布式为[Ar]3d54s1,故答案为
[Ar]3d54s1;(2)Z为Cl元素,氢化物的熔沸点与相对分子质量成正比,但含有氢键的氢化物熔沸点较高,HCl
中不含氢键而HF中含有氢键,所以HF熔沸点高于HCl,故答案为HF分子间存在氢键、HCl分子间不存在
氢键;(3)X是O、Z是Cl,X与Z中电负性较大的是O;Z的某种含氧酸盐常用于实验室中X的单质的制取,
实验室用氯酸钾制取氧气,ClO中中心原子价层电子对个数=3+ =4且含有一个孤电子对,根据价
层电子对互斥理论判断此酸根离子的空间构型为三角锥形;此离子中含有的化学键类型是共价键;孤电子对
和成键电子对之间的排斥力大于成键电子对之间的排斥力,所以其键角小于109°28′,故答案为O;三角锥形;
共价键;<;(4)O与Na形成的化合物NaO,根据晶胞结构可知,黑球为钠离子(Y),白球为氧离子(X),则
2
该晶胞中氧离子的配位数为8;以距离一个氧离子最近的所有钠离子为顶点构成的几何体为正方体;离子化
合物中,化合物的熔沸点与晶格能成正比,晶格能与离子半径成反比、与电荷成正比,钠离子半径大于镁离
子,而电荷小于镁离子,所以氧化钠熔沸点低于MgO,故答案为8;正方体;MgO;(5)该化合物的晶胞边长为a pm,其体积=(a×10−10cm)3,该晶胞中钠离子个数为8、氧离子个数=8× +6× =4,则该化合物的密度为
= g·cm−3,故答案为 。
5.已知A、B、R、D都是周期表中前四周期的元素,它们的原子系数依次增大。其中A元素基态原子第一
电离能比B元素基态原子的第一电离能大,B的基态原子的L层、R基态原子的M层均有2个单电子,D
是第Ⅷ族中原子序数最小的元素。
(1)写出基态D原子的电子排布式__________。
(2)已知高纯度R的单质在现代信息技术与新能源开发中具有极为重要的地位。工业上生产高纯度R的单
质过程如下:
写出过程③的反应方程式___________,已知RHCl 的沸点是31.5oC,则该物质的晶体类型是__________,
3
中心原子的轨道杂化类型为__________,该物质的空间构型是______。
(3)A的第一电离能比B的第一电离能大的原因是_________,A、B两元素分别与R形成的共价键中,极
性较强的是________。A、B两元素间能形成多种二元化合物,其中与A互为等电子体的物质的化学式为
_______。
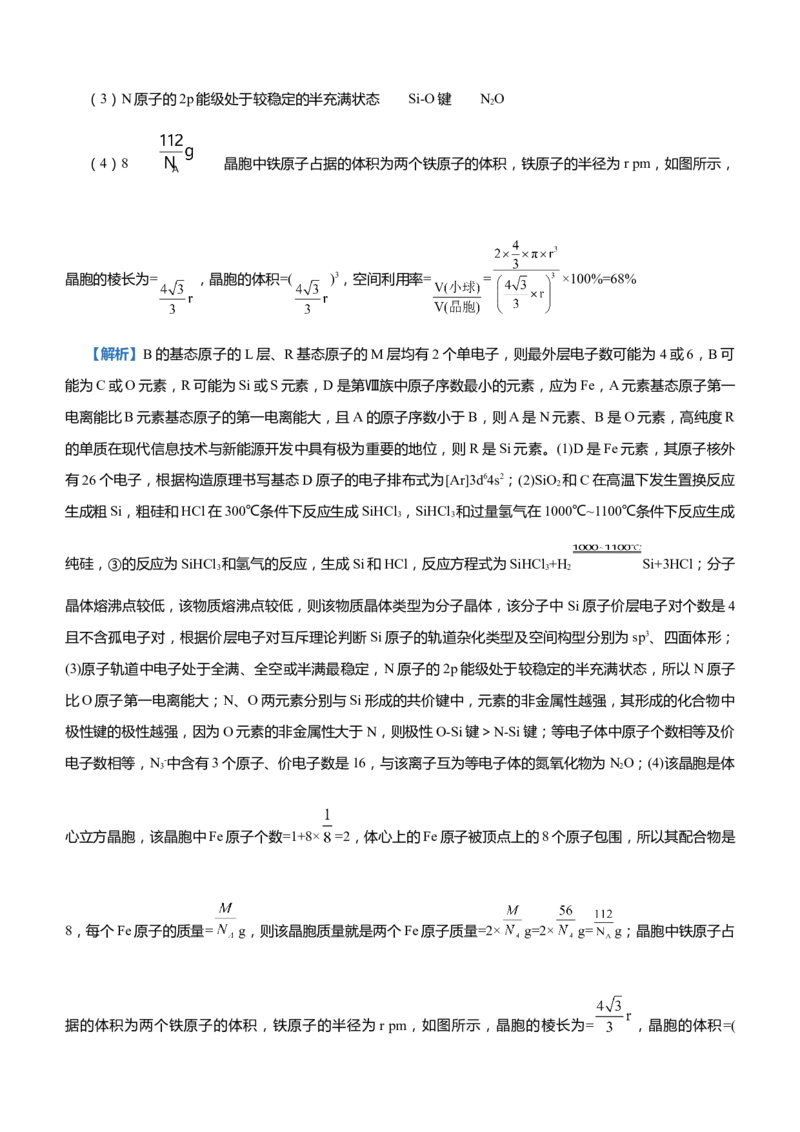
(4)已知D单质的晶胞如图所示,则晶体中D原子的配位数为______,一个D的晶胞质量为____,已知D
原子半径为r pm,则该晶胞的空间利用率为_____________(写出计算过程)。
【答案】(1)[Ar]3d64s2
(2)SiHCl +H Si+3HCl 分子晶体 sp3 四面体形
3 2(3)N原子的2p能级处于较稳定的半充满状态 Si-O键 NO
2
(4)8 晶胞中铁原子占据的体积为两个铁原子的体积,铁原子的半径为r pm,如图所示,
晶胞的棱长为= ,晶胞的体积=( )3,空间利用率= = ×100%=68%
【解析】B的基态原子的L层、R基态原子的M层均有2个单电子,则最外层电子数可能为4或6,B可
能为C或O元素,R可能为Si或S元素,D是第Ⅷ族中原子序数最小的元素,应为Fe,A元素基态原子第一
电离能比B元素基态原子的第一电离能大,且A的原子序数小于B,则A是N元素、B是O元素,高纯度R
的单质在现代信息技术与新能源开发中具有极为重要的地位,则R是Si元素。(1)D是Fe元素,其原子核外
有26个电子,根据构造原理书写基态D原子的电子排布式为[Ar]3d64s2;(2)SiO 和C在高温下发生置换反应
2
生成粗Si,粗硅和HCl在300℃条件下反应生成SiHCl ,SiHCl 和过量氢气在1000℃~1100℃条件下反应生成
3 3
纯硅,③的反应为SiHCl 和氢气的反应,生成Si和HCl,反应方程式为SiHCl +H Si+3HCl;分子
3 3 2
晶体熔沸点较低,该物质熔沸点较低,则该物质晶体类型为分子晶体,该分子中 Si原子价层电子对个数是4
且不含孤电子对,根据价层电子对互斥理论判断Si原子的轨道杂化类型及空间构型分别为sp3、四面体形;
(3)原子轨道中电子处于全满、全空或半满最稳定,N原子的2p能级处于较稳定的半充满状态,所以N原子
比O原子第一电离能大;N、O两元素分别与Si形成的共价键中,元素的非金属性越强,其形成的化合物中
极性键的极性越强,因为O元素的非金属性大于N,则极性O-Si键>N-Si键;等电子体中原子个数相等及价
电子数相等,N-中含有3个原子、价电子数是16,与该离子互为等电子体的氮氧化物为NO;(4)该晶胞是体
3 2
心立方晶胞,该晶胞中Fe原子个数=1+8× =2,体心上的Fe原子被顶点上的8个原子包围,所以其配合物是
8,每个Fe原子的质量= g,则该晶胞质量就是两个Fe原子质量=2× g=2× g= g;晶胞中铁原子占
据的体积为两个铁原子的体积,铁原子的半径为r pm,如图所示,晶胞的棱长为= ,晶胞的体积=()3,空间利用率= = ×100%=68%。