文档内容
大题优练 7
以元素性质为主线串联反应原理
优 选 例 题
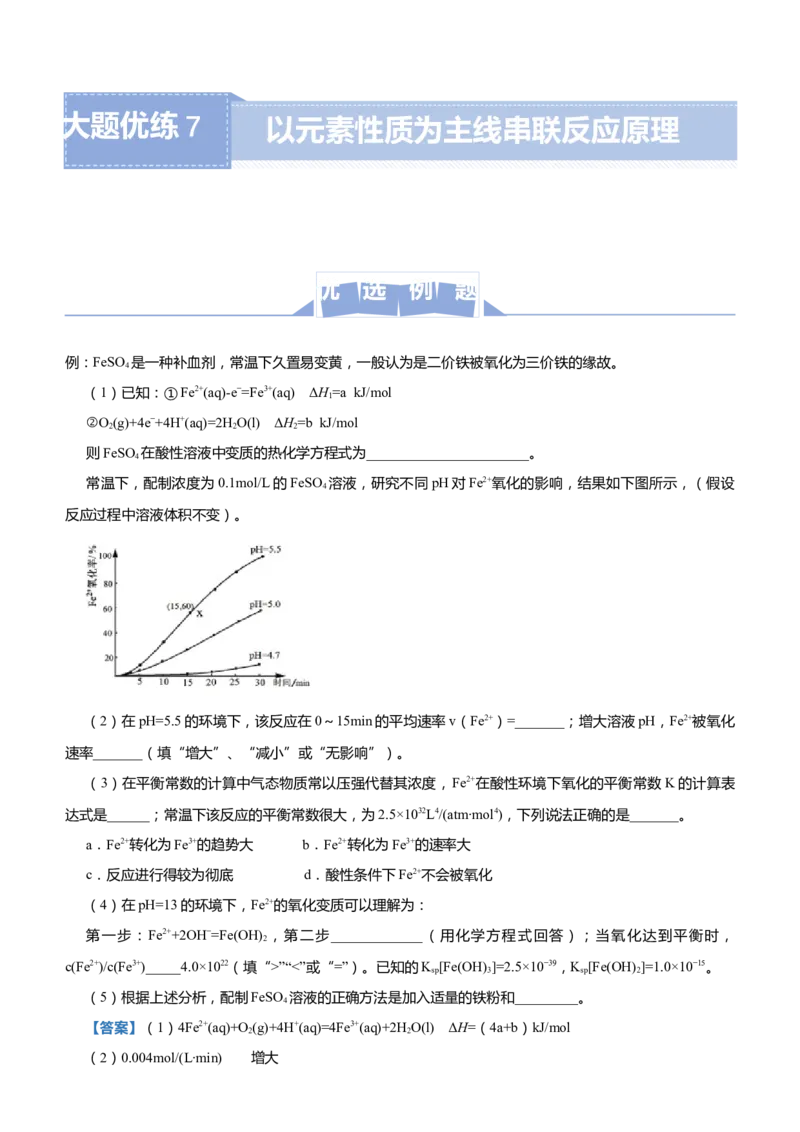
例:FeSO 是一种补血剂,常温下久置易变黄,一般认为是二价铁被氧化为三价铁的缘故。
4
(1)已知:①Fe2+(aq)-e−=Fe3+(aq) ΔH=a kJ/mol
1
②O (g)+4e−+4H+(aq)=2H O(l) ΔH=b kJ/mol
2 2 2
则FeSO 在酸性溶液中变质的热化学方程式为_______________________。
4
常温下,配制浓度为0.1mol/L的FeSO 溶液,研究不同pH对Fe2+氧化的影响,结果如下图所示,(假设
4
反应过程中溶液体积不变)。
(2)在pH=5.5的环境下,该反应在0~15min的平均速率v(Fe2+)=_______;增大溶液pH,Fe2+被氧化
速率_______(填“增大”、“减小”或“无影响”)。
(3)在平衡常数的计算中气态物质常以压强代替其浓度,Fe2+在酸性环境下氧化的平衡常数K的计算表
达式是______;常温下该反应的平衡常数很大,为2.5×1032L4/(atm∙mol4),下列说法正确的是_______。
a.Fe2+转化为Fe3+的趋势大 b.Fe2+转化为Fe3+的速率大
c.反应进行得较为彻底 d.酸性条件下Fe2+不会被氧化
(4)在pH=13的环境下,Fe2+的氧化变质可以理解为:
第一步:Fe2++2OH−=Fe(OH) ,第二步_____________(用化学方程式回答);当氧化达到平衡时,
2
c(Fe2+)/c(Fe3+)_____4.0×1022(填“>”“<”或“=”)。已知的K [Fe(OH) ]=2.5×10−39,K [Fe(OH) ]=1.0×10−15。
sp 3 sp 2
(5)根据上述分析,配制FeSO 溶液的正确方法是加入适量的铁粉和_________。
4
【答案】(1)4Fe2+(aq)+O (g)+4H+(aq)=4Fe3+(aq)+2H O(l) ΔH=(4a+b)kJ/mol
2 2
(2)0.004mol/(L∙min) 增大(3)c4(Fe3+)/c4(Fe2+)∙c4(H+)∙p(O ) ac
2
(4)4Fe(OH) +O +2H O=4Fe(OH) =
2 2 2 3
(5)HSO
2 4
【解析】(1)①Fe2+(aq)-e−= Fe3+(aq) ΔH=a kJ/mol
1
②O (g)+4e−+4H+(aq)=2H O(l) ΔH=b kJ/mol
2 2 2
根据盖斯定律,①×4+②可得,4Fe2+(aq)+O (g)+4H+(aq)=4Fe3+(aq)+2H O(l) ΔH=(4a+b)kJ/mol,故答案
2 2
为 4Fe2+(aq)+O (g)+4H+(aq)=4Fe3+(aq)+2H O(l) ΔH= ( 4a+b ) kJ/mol 。 ( 2 )
2 2
v(Fe2+)=(0.1mol/L×60%)/15min=0.004
mol/(L∙min),根据图示分析,增大溶液pH,Fe2+氧化率增大,所以Fe2+被氧化速率增大,故答案为0.004mol/
(L∙min);增大。(3)根据4Fe2+(aq)+O (g)+4H+(aq)=4Fe3+(aq)+2H O(l),可知Fe2+在酸性环境下氧化的平衡常
2 2
数K=c4(Fe3+)/c4(Fe2+)∙c4(H+)∙p(O );a.因为常温下该反应的平衡常数很大,故Fe2+转化为Fe3+的趋势大,a故
2
正确;b.K值越大,表示反应进行得越完全,故 b错误;c.K值越大,表示反应进行得越完全,越彻底,
故c正确;d.在酸性条件下Fe2+会被氧化,故d错误;故答案为c4(Fe3+)/c4(Fe2+)∙c4(H+)∙p(O );ac。(4)在
2
pH=13的环境下,Fe2++2OH−=Fe(OH) ,接着Fe(OH) 被空气中的氧气氧化为Fe(OH) ,反应的化学方程式为:
2 2 3
4Fe(OH) +O +2H O=4Fe(OH) ; 根 据 pH=13 , 可 知 c(OH−)=10−1mol/L ,
2 2 2 3
K [Fe(OH) ]=2.5×10−39=c(Fe3+)∙c3(OH−) , c(Fe3+)=2.5×10−36 , K [Fe(OH) ]=1.0×10−15=c(Fe2+)c2(OH−) ,
sp 3 sp 2
c(Fe2+)=1.0×10−13,c(Fe2+)/c(Fe3+)=1.0×10−13/2.5×10−36
=4.0×1022,故答案为4Fe(OH) +O +2H O=4Fe(OH) ;=。(5)由于Fe2+在酸性环境下易被氧化为Fe3+,在碱
2 2 2 3
性环境中易被氧化成 Fe(OH) ,所以配制 FeSO 溶液的正确方法是加入适量的铁粉和 HSO ,故答案为
3 4 2 4
HSO 。
2 4模 拟 优 练
1.环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
(1)某温度,等物质的量的碘和环戊烯( )在刚性容器内发生反应 (g)+I(g)= (g)+2HI(g) ΔH>
2
0,起始总压为 105Pa,平衡时总压增加了 20%,环戊烯的转化率为_________,该反应的平衡常数
K=________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有___________(填标号)。
p
A.通入惰性气体 B.提高温度 C.增加环戊烯浓度 D.增加碘浓度
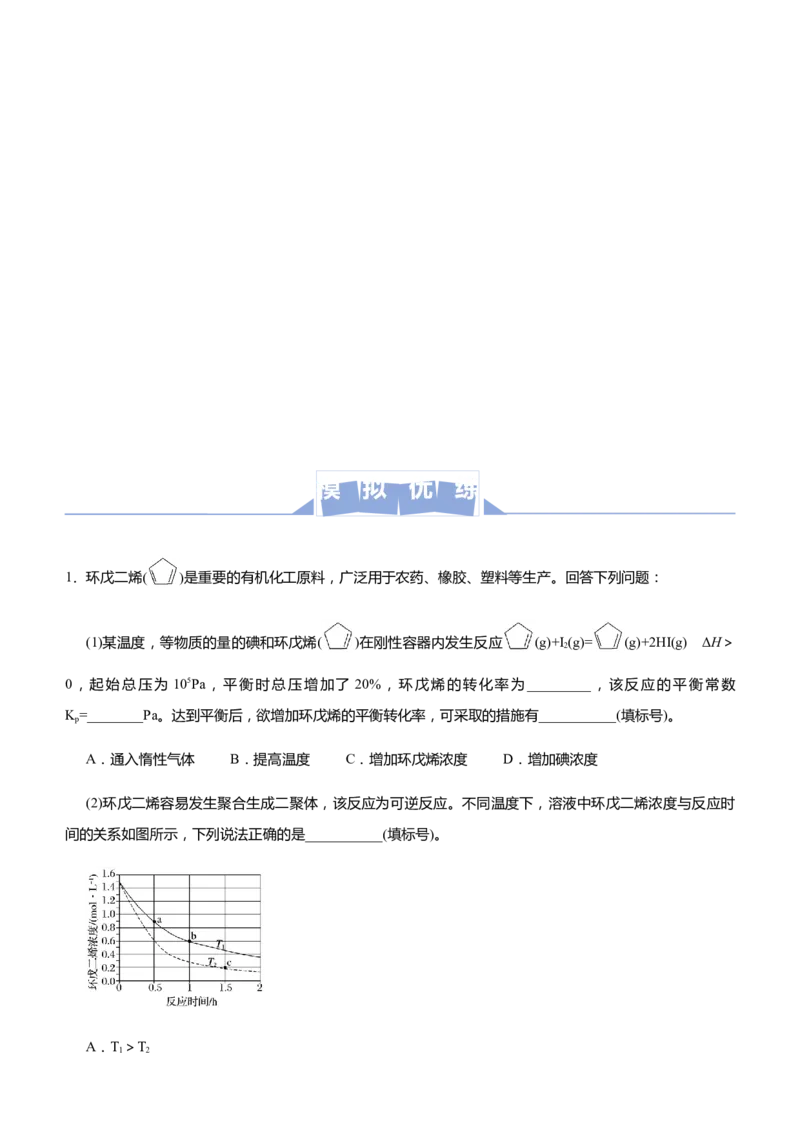
(2)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时
间的关系如图所示,下列说法正确的是___________(填标号)。
A.T>T
1 2B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45mol·L−1
【答案】(1)40% 3.56×104 BD
(2)CD
【解析】(1)设容器中起始加入I(g)和环戊烯的物质的量均为a,平衡时转化的环戊烯的物质的量为x,列
2
出三段式:
C H(g) + I (g) C H(g) + 2HI(g)
5 8 2 5 6
恒温恒容时,压强之比等于气体物质的量之比,平衡时总压强增加了 20%,则 ,
解得x=0.4a,则环戊烯的转化率为 40%,平衡时 (g)、I(g), (g)、HI(g)的分压分别为
2
、 、 、 ,则 K= ,根据 p =1.2×105Pa,可得 K=
p 总 p
×1.2×105Pa≈3.56×104Pa;通入惰性气体,对反应的平衡无影响,环戊烯的平衡转化率不变,故 A不符合题意;
反应为吸热反应,提高温度,平衡正向移动,可提高环戊烯的平衡转化率,故B符合题意;增加环戊烯浓度,
平衡正向移动,能提高I(g)的平衡转化率,但环戊烯的平衡转化率降低,故C不符合题意;增加I(g)的浓度,
2 2
平衡正向移动,能提高环戊烯的平衡转化率,故D符合题意。(2)A.相同时间内,环戊二烯浓度减小量越大,
反应速率越快,由图可知,T <T ,故A错误;B.影响反应速率的因素有温度和环戊二烯的浓度等,a点时
1 2
温度较低,但环戊二烯浓度较大,c点时温度较高,但环戊二烯浓度较小,故无法比较a点和c点的反应速率
大小,故B错误;C.a点和b点温度相同,a点时环戊二烯的浓度大于b点时环戊二烯的浓度,即a点的正
反应速率大于b点的正反应速率,因为b点时反应未达到平衡,b点的正反应速率大于逆反应速率,故a点的
正反应速率大于b点的逆反应速率,故C正确;D.b点时,环戊二烯的浓度减小0.9mol·L−1,结合生成的二聚体浓度为环戊二烯浓度变化量的 ,可知二聚体的浓度为0.45mol·L−1,故D正确。
2.CO 的回收与利用是科学家研究的热点课题。
2
(1)由CO 转化为羧酸是CO 资源化利用的重要方法。在催化作用下CO 和CH 合成CHCOOH的化学方程
2 2 2 4 3
式为_______________________。在合成CHCOOH的反应中,下列有关说法正确的是_______。(填字母)
3
A.利用催化剂可以使反应的平衡常数增大
B.CH→CHCOOH过程中,有C-H键发生断裂
4 3
C.有22.4L CH 参与反应时转移4mol电子
4
D.该反应为放热反应
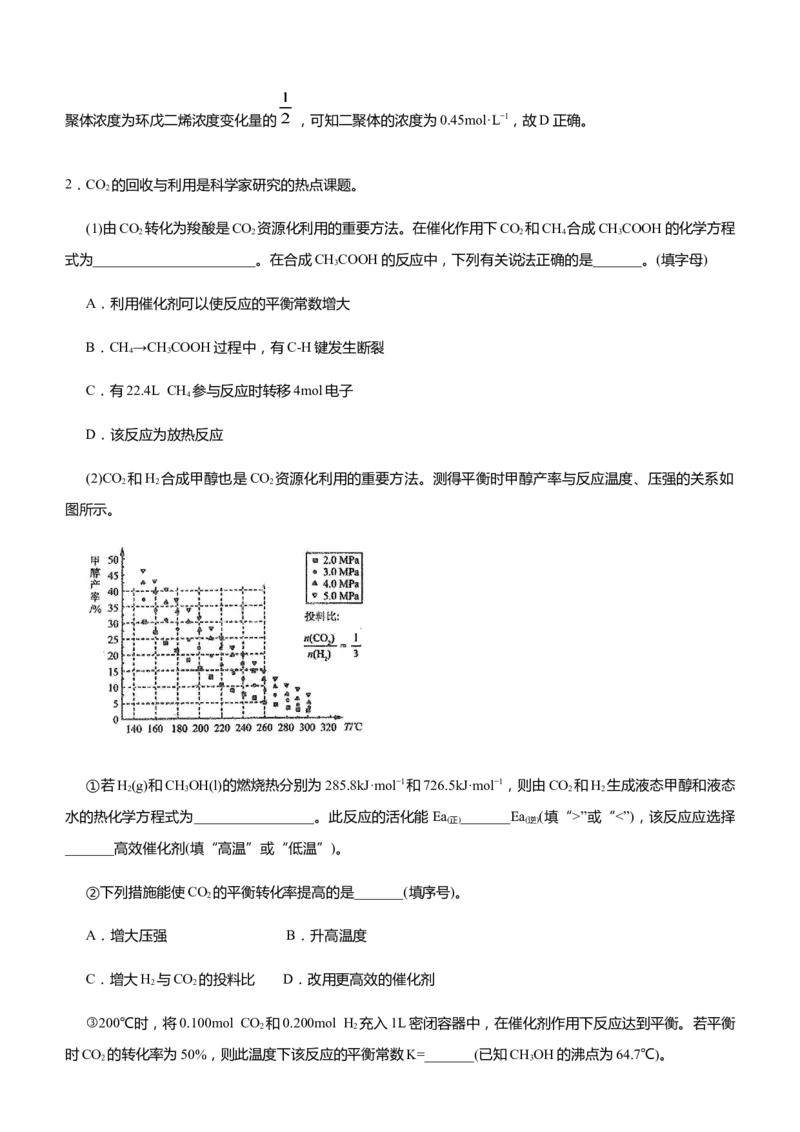
(2)CO 和H 合成甲醇也是CO 资源化利用的重要方法。测得平衡时甲醇产率与反应温度、压强的关系如
2 2 2
图所示。
①若H(g)和CHOH(l)的燃烧热分别为285.8kJ·mol−1和726.5kJ·mol−1,则由CO 和H 生成液态甲醇和液态
2 3 2 2
水的热化学方程式为_________________。此反应的活化能Ea _______Ea (填“>”或“<”),该反应应选择
(正) (逆)
_______高效催化剂(填“高温”或“低温”)。
②下列措施能使CO 的平衡转化率提高的是_______(填序号)。
2
A.增大压强 B.升高温度
C.增大H 与CO 的投料比 D.改用更高效的催化剂
2 2
③200℃时,将0.100mol CO 和0.200mol H 充入1L密闭容器中,在催化剂作用下反应达到平衡。若平衡
2 2
时CO 的转化率为50%,则此温度下该反应的平衡常数K=_______(已知CHOH的沸点为64.7℃)。
2 3(3)可利用电解的方法将CO 转化为CHOH,请写出在酸性条件下的阴极反应式_______。
2 3
【答案】(1)CO+CH =====CHCOOH BD
2 4 3
(2)CO(g)+3H(g)=CH OH(g)+H O(l) ΔH=-130.9kJ·mol−1 < 低温 AC 400
2 2 3 2
(3)CO+6e−+6H+=CH OH+H O
2 3 2
【解析】(1)根据反应物生成物可直接得出答案为CO+CH =====CHCOOH;A中平衡常数只与温度有关,
2 4 3
催化剂不能改变平衡常数,A错误;CH 有C-H键发生断裂形成甲基,B正确;C未说明温度压强,C错误;
4
该反应是熵减的反应,反应能发生,则 <0,可得出ΔH<0,故该反应为放热反应,D正确。
(2)①由H(g)和CHOH(l)的燃烧热分别为285.8kJ·mol−1和726.5kJ·mol−1可得出式①H(g)+1/2O (g)=HO(l)
2 3 2 2 2
ΔH=-285.8kJ·mol−1和式②CHOH(l)+3/2O(g)=CO (g)+2HO(l) ΔH=-726.5kJ·mol−1;3 ①-②即可得出CO(g)
3 2 2 2 2
+3H (g)=CH OH(g)+H O(l) ΔH=-130.9kJ·mol−1,ΔH=Ea -Ea <0可得出Ea ”、“<”或“=”)图中纵坐标为___的转化率;图中A、B、C三点对
1 2 1 2
应的NOCl体积分数最大的是____(填“A”、“B”或“C”)。
②若容器容积为1L,经过10min到达A点,该时间段内化学反应速率v(NO)=__________。
③若在温度为T ,容积为1L的容器中,充入0.5mol NO、1mol Cl 、2mol NOCl,此时平衡将向___移动
1 2
(填“左”、“右”或“不移动”)。【答案】(1)2ΔH-ΔH
2 1
(2)ad 增大
(3)< Cl A 右
2
【解析】(1)根据盖斯定律可知,Ⅲ=2×Ⅱ-Ⅰ,即ΔH=2ΔH-ΔH ,则K = ,故答案为:2ΔH-ΔH ;
3 2 1 3 2 1
;(2)①a.反应Ⅱ、Ⅲ中,二氧化氮和氯气有颜色,当反应体系中混合气体的颜色保持不变,说明反应Ⅱ、Ⅲ
均达到平衡状态,a项正确;b.焓变只与反应起始和终止的物质有关,不可以判断反应Ⅱ、Ⅲ是否达到平衡
状态,b项错误;c.同等条件下,反应Ⅱ的速率远远大于反应Ⅲ,说明反应Ⅱ的活化能小,但无法判断焓变
大小,c项错误;d.达平衡后,向反应体系中再通入一定量NOCl(g),反应Ⅱ、Ⅲ均向逆向移动,则NO (g)
2
和NO(g)的百分含量均增大,d项正确;综上,正确的为ad,故答案为:ad;②反应Ⅱ正反应方向气体减少、
Ⅲ反应前后体积不变,恒容密闭容器中,平衡后,向反应体系中充入少量 ,则反应Ⅲ中NO会减少,平衡
逆向移动,消耗NOCl(g),促使反应Ⅱ正向移动,再次平衡时,NO 的转化率将增大,故答案为:增大;
2
(3)①ΔH<0,为放热反应,根据勒夏特列原理可得,升高温度,反应逆向移动,则 T