文档内容
第 58 讲 沉淀溶解平衡图像的分析
[复习目标] 1.熟知常考沉淀溶解平衡图像的类型,能用沉淀溶解平衡原理解释曲线变化的
原因。2.会选取特殊点利用数据进行有关K 的计算。
sp
分析沉淀溶解平衡曲线图像的一般思路
1.明确图像中横、纵坐标的含义。
2.分析曲线上或曲线外的点对应的溶液是否为饱和溶液时,要明确点所对应的溶液中,若
Q>K ,能形成沉淀,则该点所对应的溶液为过饱和溶液;若Q<K ,不能形成沉淀,则该
sp sp
点所对应的溶液为不饱和溶液。
3.分析曲线上指定点的离子浓度时,需根据 K 计算或抓住K 的特点,结合选项分析判断。
sp sp
溶液在蒸发时,离子浓度的变化分两种情况:原溶液不饱和时,离子浓度都增大;原溶液饱
和时,离子浓度都不变。溶度积常数只是温度的函数,与溶液中的离子浓度无关,在同一曲
线上的点,溶度积常数都相同。
类型一 溶解度曲线
1.图像举例
如图为A、B、C三种物质的溶解度随温度变化曲线。
2.信息解读
(1)曲线上各点的意义:曲线上任一点都表示饱和溶液,曲线上方的任一点均表示过饱和溶
液,此时有沉淀析出,曲线下方的任一点均表示不饱和溶液。
(2)曲线的变化趋势:A曲线表示溶解度随温度升高而增大;B曲线表示溶解度随温度升高而
减小;C曲线表示溶解度随温度升高变化不大。
(3)分离提纯:A(C):蒸发浓缩、冷却结晶、过滤、洗涤、干燥;C(A):蒸发结晶、趁热过
滤。
(4)计算K :对于难溶电解质来说,若知道溶解度的值S g,可求出难溶电解质饱和溶液时
sp
的浓度c= mol·L-1,进而求出K 。
sp
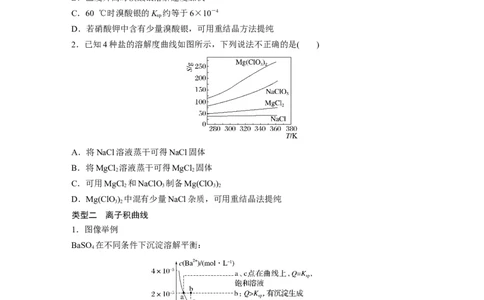
1.(2014·全国卷 Ⅰ,11)溴酸银(AgBrO )溶解度随温度变化曲线如图所示,下列说法错误的
3
是( )A.溴酸银的溶解是放热过程
B.温度升高时溴酸银溶解速度加快
C.60 ℃时溴酸银的K 约等于6×10-4
sp
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
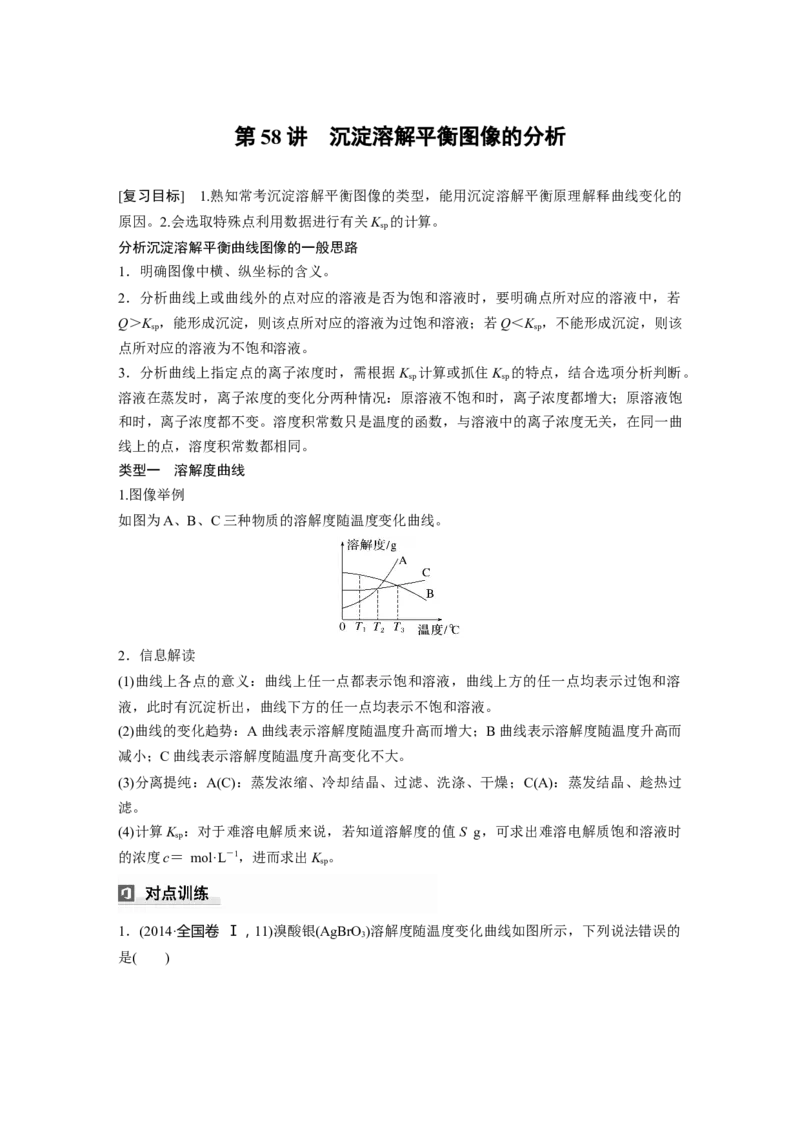
2.已知4种盐的溶解度曲线如图所示,下列说法不正确的是( )
A.将NaCl溶液蒸干可得NaCl固体
B.将MgCl 溶液蒸干可得MgCl 固体
2 2
C.可用MgCl 和NaClO 制备Mg(ClO)
2 3 3 2
D.Mg(ClO) 中混有少量NaCl杂质,可用重结晶法提纯
3 2
类型二 离子积曲线
1.图像举例
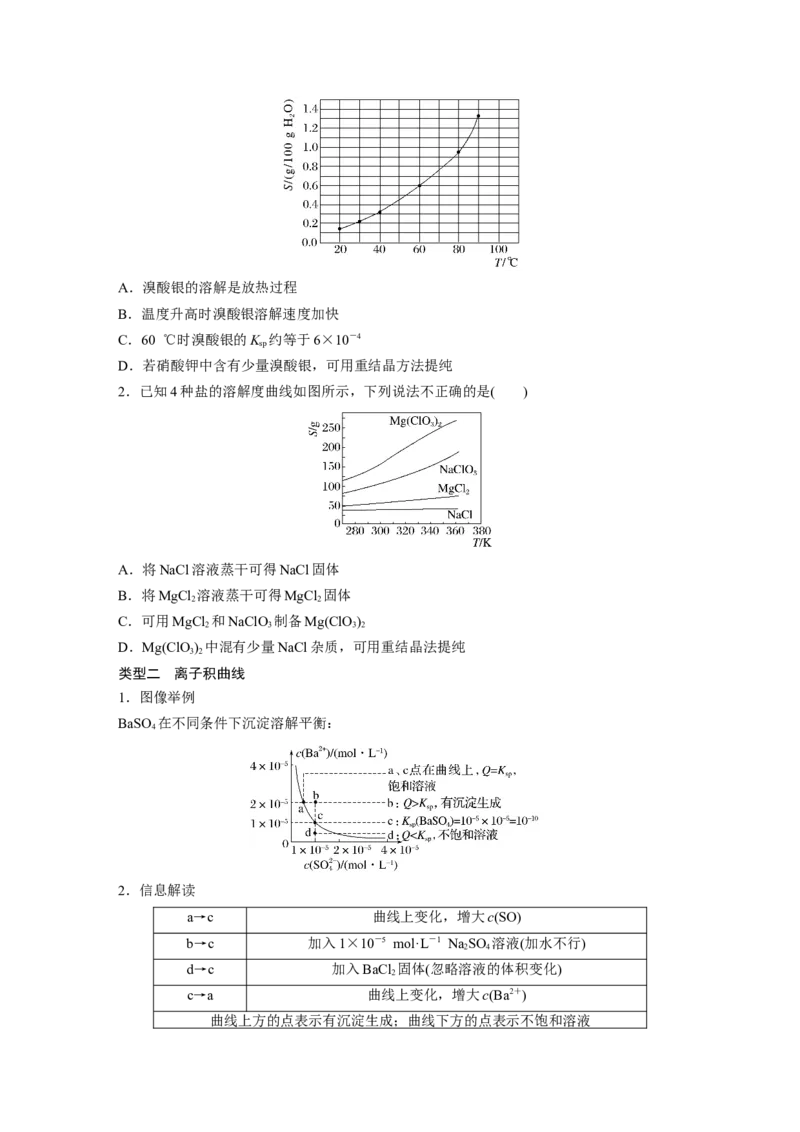
BaSO 在不同条件下沉淀溶解平衡:
4
2.信息解读
a→c 曲线上变化,增大c(SO)
b→c 加入1×10-5 mol·L-1 Na SO 溶液(加水不行)
2 4
d→c 加入BaCl 固体(忽略溶液的体积变化)
2
c→a 曲线上变化,增大c(Ba2+)
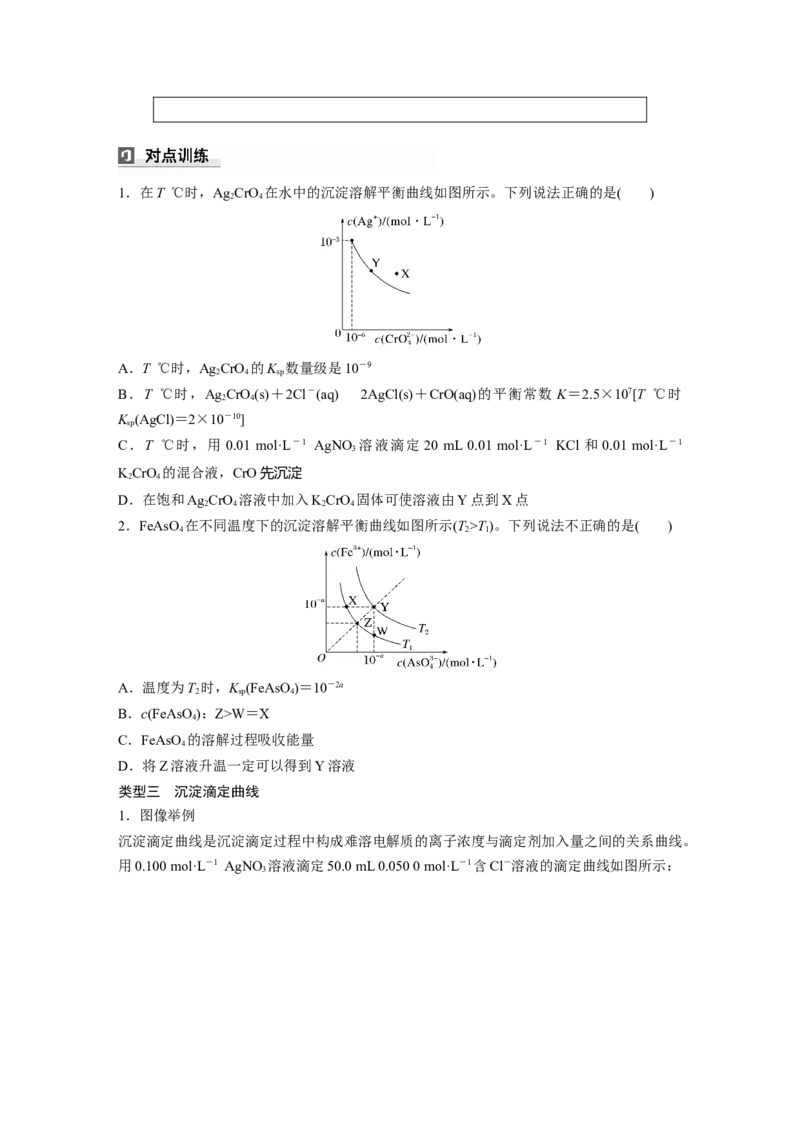
曲线上方的点表示有沉淀生成;曲线下方的点表示不饱和溶液1.在T ℃时,Ag CrO 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
2 4
A.T ℃时,Ag CrO 的K 数量级是10-9
2 4 sp
B.T ℃时,Ag CrO(s)+2Cl-(aq)2AgCl(s)+CrO(aq)的平衡常数 K=2.5×107[T ℃时
2 4
K (AgCl)=2×10-10]
sp
C.T ℃时,用 0.01 mol·L-1 AgNO 溶液滴定 20 mL 0.01 mol·L-1 KCl 和 0.01 mol·L-1
3
KCrO 的混合液,CrO先沉淀
2 4
D.在饱和Ag CrO 溶液中加入KCrO 固体可使溶液由Y点到X点
2 4 2 4
2.FeAsO 在不同温度下的沉淀溶解平衡曲线如图所示(T>T)。下列说法不正确的是( )
4 2 1
A.温度为T 时,K (FeAsO)=10-2a
2 sp 4
B.c(FeAsO):Z>W=X
4
C.FeAsO 的溶解过程吸收能量
4
D.将Z溶液升温一定可以得到Y溶液
类型三 沉淀滴定曲线
1.图像举例
沉淀滴定曲线是沉淀滴定过程中构成难溶电解质的离子浓度与滴定剂加入量之间的关系曲线。
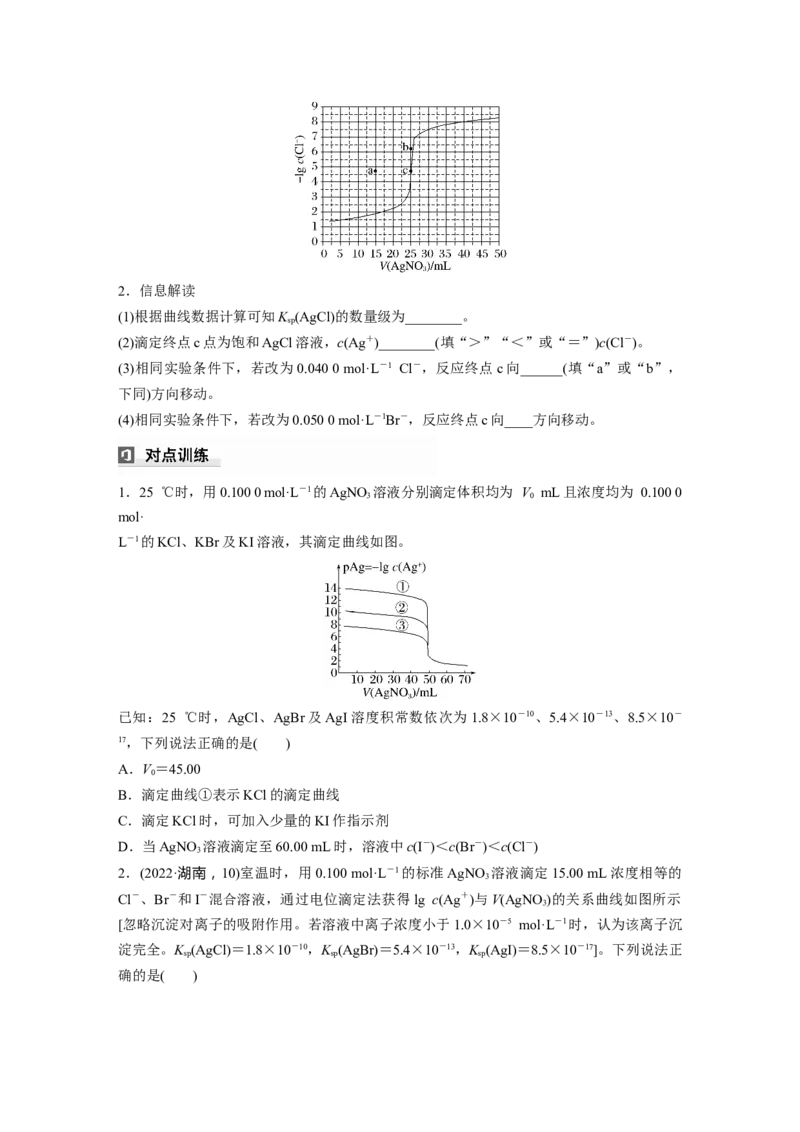
用0.100 mol·L-1 AgNO 溶液滴定50.0 mL 0.050 0 mol·L-1含Cl-溶液的滴定曲线如图所示:
32.信息解读
(1)根据曲线数据计算可知K (AgCl)的数量级为________。
sp
(2)滴定终点c点为饱和AgCl溶液,c(Ag+)________(填“>”“<”或“=”)c(Cl-)。
(3)相同实验条件下,若改为0.040 0 mol·L-1 Cl-,反应终点c向______(填“a”或“b”,
下同)方向移动。
(4)相同实验条件下,若改为0.050 0 mol·L-1Br-,反应终点c向____方向移动。
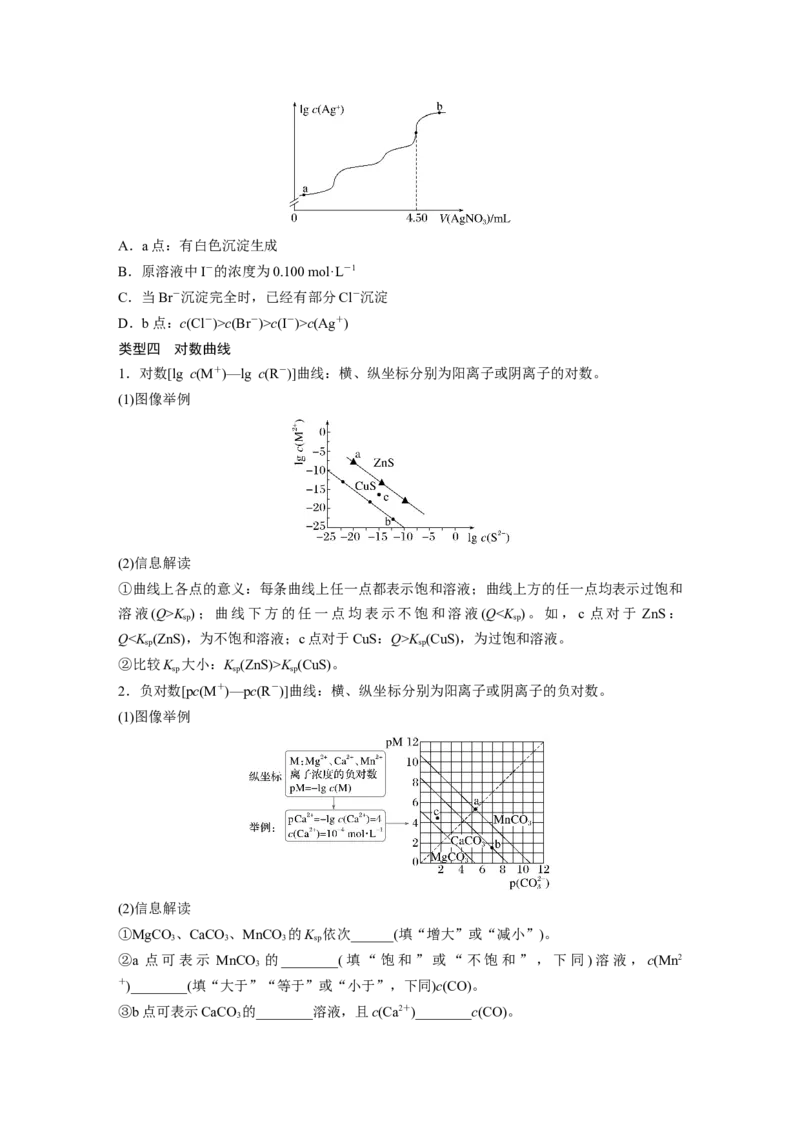
1.25 ℃时,用0.100 0 mol·L-1的AgNO 溶液分别滴定体积均为 V mL且浓度均为 0.100 0
3 0
mol·
L-1的KCl、KBr及KI溶液,其滴定曲线如图。
已知:25 ℃时,AgCl、AgBr及AgI溶度积常数依次为1.8×10-10、5.4×10-13、8.5×10-
17,下列说法正确的是( )
A.V=45.00
0
B.滴定曲线①表示KCl的滴定曲线
C.滴定KCl时,可加入少量的KI作指示剂
D.当AgNO 溶液滴定至60.00 mL时,溶液中c(I-)<c(Br-)<c(Cl-)
3
2.(2022·湖南,10)室温时,用0.100 mol·L-1的标准AgNO 溶液滴定15.00 mL浓度相等的
3
Cl-、Br-和I-混合溶液,通过电位滴定法获得 lg c(Ag+)与V(AgNO)的关系曲线如图所示
3
[忽略沉淀对离子的吸附作用。若溶液中离子浓度小于1.0×10-5 mol·L-1时,认为该离子沉
淀完全。K (AgCl)=1.8×10-10,K (AgBr)=5.4×10-13,K (AgI)=8.5×10-17]。下列说法正
sp sp sp
确的是( )A.a点:有白色沉淀生成
B.原溶液中I-的浓度为0.100 mol·L-1
C.当Br-沉淀完全时,已经有部分Cl-沉淀
D.b点:c(Cl-)>c(Br-)>c(I-)>c(Ag+)
类型四 对数曲线
1.对数[lg c(M+)—lg c(R-)]曲线:横、纵坐标分别为阳离子或阴离子的对数。
(1)图像举例
(2)信息解读
①曲线上各点的意义:每条曲线上任一点都表示饱和溶液;曲线上方的任一点均表示过饱和
溶液(Q>K );曲线下方的任一点均表示不饱和溶液(QK (CuS),为过饱和溶液。
sp sp
②比较K 大小:K (ZnS)>K (CuS)。
sp sp sp
2.负对数[pc(M+)—pc(R-)]曲线:横、纵坐标分别为阳离子或阴离子的负对数。
(1)图像举例
(2)信息解读
①MgCO 、CaCO 、MnCO 的K 依次______(填“增大”或“减小”)。
3 3 3 sp
②a 点可表示 MnCO 的________(填“饱和”或“不饱和”,下同)溶液,c(Mn2
3
+)________(填“大于”“等于”或“小于”,下同)c(CO)。
③b点可表示CaCO 的________溶液,且c(Ca2+)________c(CO)。
3④c点可表示MgCO 的________溶液,且c(Mg2+)________c(CO)。
3
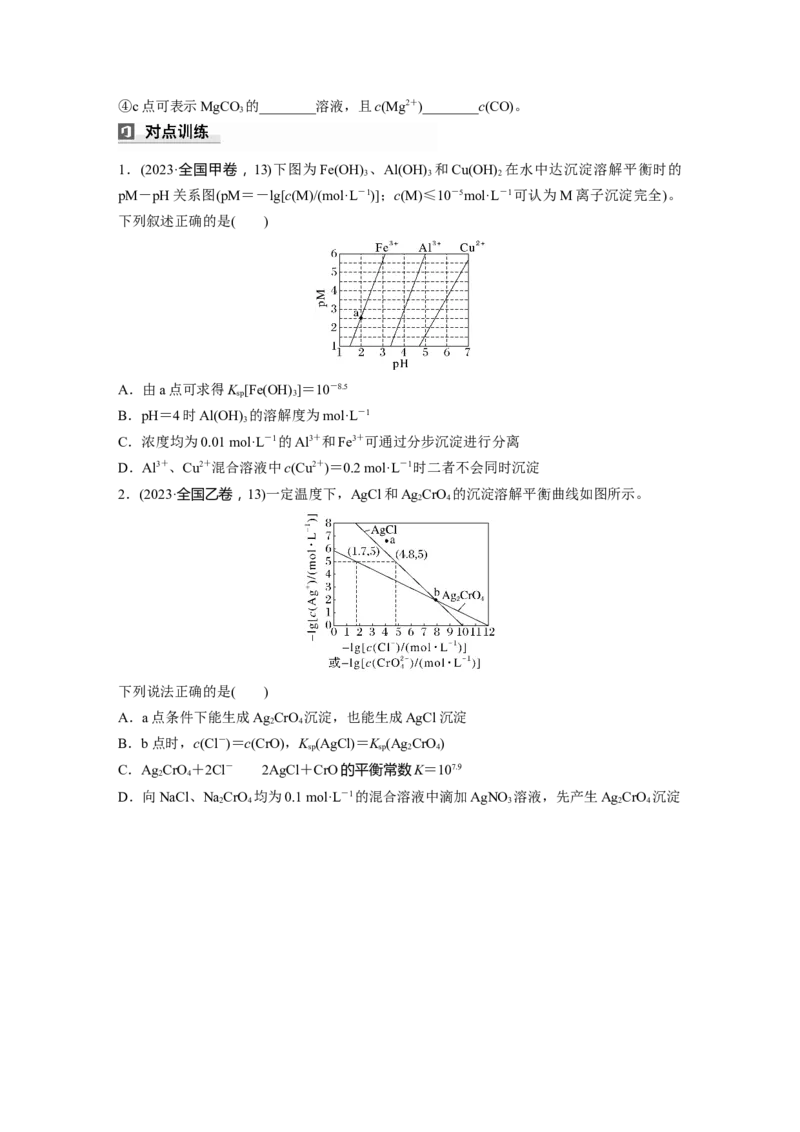
1.(2023·全国甲卷,13)下图为Fe(OH) 、Al(OH) 和Cu(OH) 在水中达沉淀溶解平衡时的
3 3 2
pM-pH关系图(pM=-lg[c(M)/(mol·L-1)];c(M)≤10-5mol·L-1可认为M离子沉淀完全)。
下列叙述正确的是( )
A.由a点可求得K [Fe(OH) ]=10-8.5
sp 3
B.pH=4时Al(OH) 的溶解度为mol·L-1
3
C.浓度均为0.01 mol·L-1的Al3+和Fe3+可通过分步沉淀进行分离
D.Al3+、Cu2+混合溶液中c(Cu2+)=0.2 mol·L-1时二者不会同时沉淀
2.(2023·全国乙卷,13)一定温度下,AgCl和Ag CrO 的沉淀溶解平衡曲线如图所示。
2 4
下列说法正确的是( )
A.a点条件下能生成Ag CrO 沉淀,也能生成AgCl沉淀
2 4
B.b点时,c(Cl-)=c(CrO),K (AgCl)=K (Ag CrO)
sp sp 2 4
C.Ag CrO+2Cl-2AgCl+CrO的平衡常数K=107.9
2 4
D.向NaCl、NaCrO 均为0.1 mol·L-1的混合溶液中滴加AgNO 溶液,先产生Ag CrO 沉淀
2 4 3 2 4