文档内容
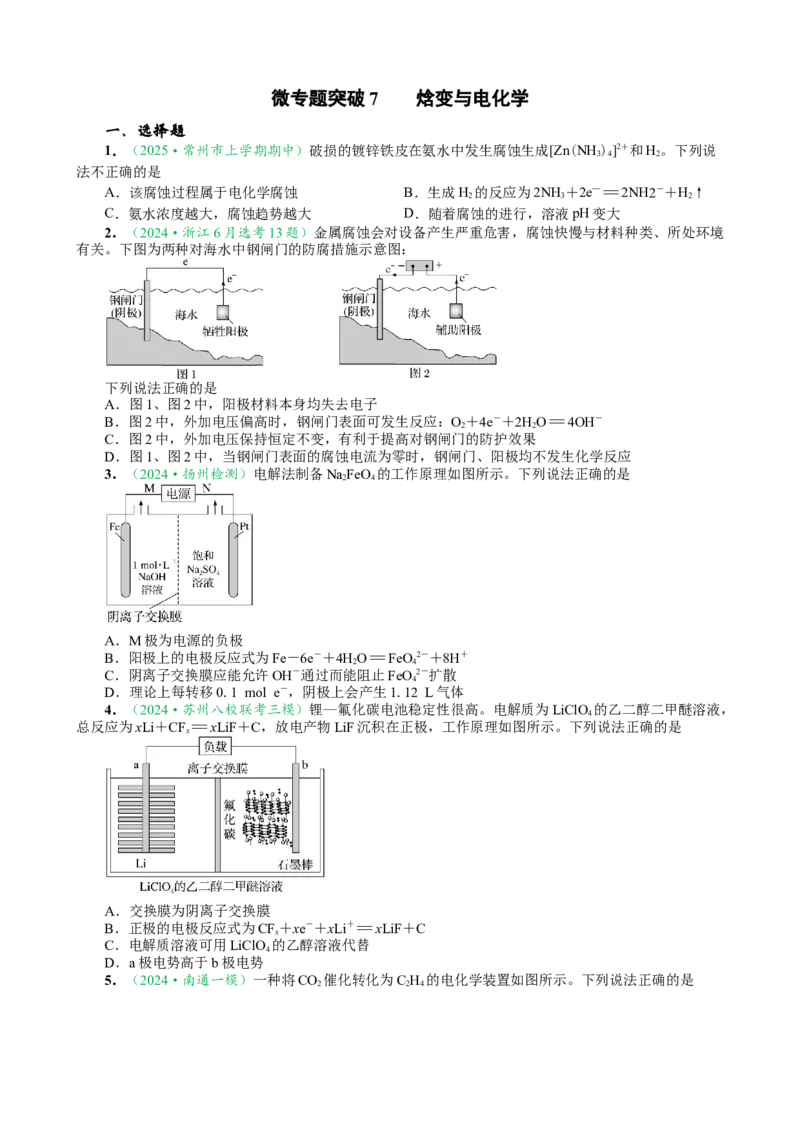
微专题突破7 焓变与电化学
一、选择题
1.(2025·常州市上学期期中)破损的镀锌铁皮在氨水中发生腐蚀生成[Zn(NH )]2+和H。下列说
3 4 2
法不正确的是
A.该腐蚀过程属于电化学腐蚀 B.生成H 的反应为2NH +2e—=2NH2-+H↑
2 3 2
C.氨水浓度越大,腐蚀趋势越大 D.随着腐蚀的进行,溶液pH变大
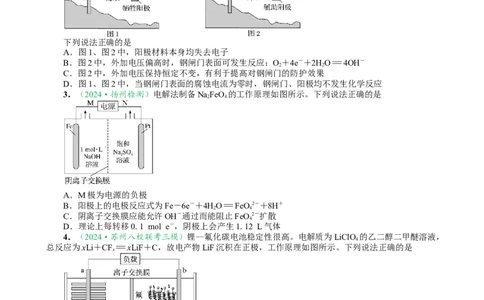
2.(2024·浙江6月选考13题)金属腐蚀会对设备产生严重危害,腐蚀快慢与材料种类、所处环境
有关。下图为两种对海水中钢闸门的防腐措施示意图:
下列说法正确的是
A.图1、图2中,阳极材料本身均失去电子
B.图2中,外加电压偏高时,钢闸门表面可发生反应:O+4e-+2HO=4OH-
2 2
C.图2中,外加电压保持恒定不变,有利于提高对钢闸门的防护效果
D.图1、图2中,当钢闸门表面的腐蚀电流为零时,钢闸门、阳极均不发生化学反应
3.(2024·扬州检测)电解法制备NaFeO 的工作原理如图所示。下列说法正确的是
2 4
A.M极为电源的负极
B.阳极上的电极反应式为Fe-6e-+4HO=FeO2-+8H+
2 4
C.阴离子交换膜应能允许OH-通过而能阻止FeO2-扩散
4
D.理论上每转移0.1 mol e-,阴极上会产生1.12 L气体
4.(2024·苏州八校联考三模)锂—氟化碳电池稳定性很高。电解质为LiClO 的乙二醇二甲醚溶液,
4
总反应为xLi+CF=xLiF+C,放电产物LiF沉积在正极,工作原理如图所示。下列说法正确的是
x
A.交换膜为阴离子交换膜
B.正极的电极反应式为CF+xe-+xLi+=xLiF+C
x
C.电解质溶液可用LiClO 的乙醇溶液代替
4
D.a极电势高于b极电势
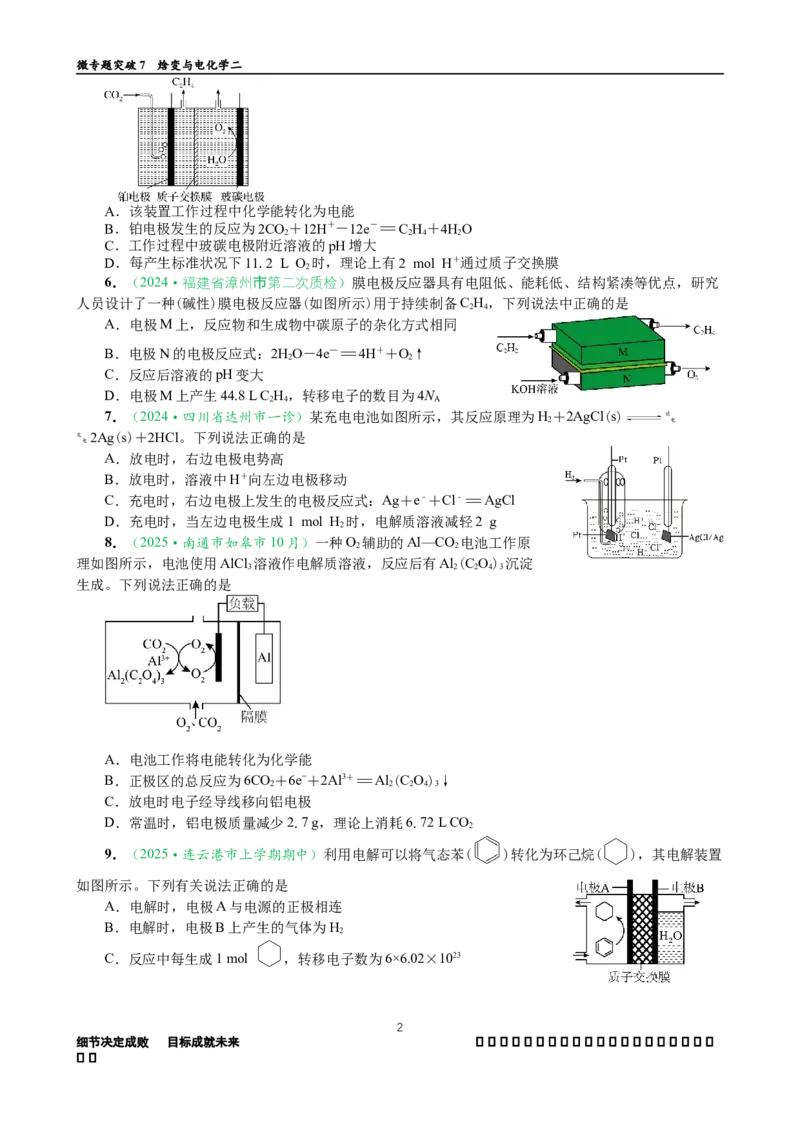
5.(2024·南通一模)一种将CO 催化转化为C H 的电化学装置如图所示。下列说法正确的是
2 2 4微专题突破7 焓变与电化学二
A.该装置工作过程中化学能转化为电能
B.铂电极发生的反应为2CO+12H+-12e-=C H+4HO
2 2 4 2
C.工作过程中玻碳电极附近溶液的pH增大
D.每产生标准状况下11.2 L O 时,理论上有2 mol H+通过质子交换膜
2
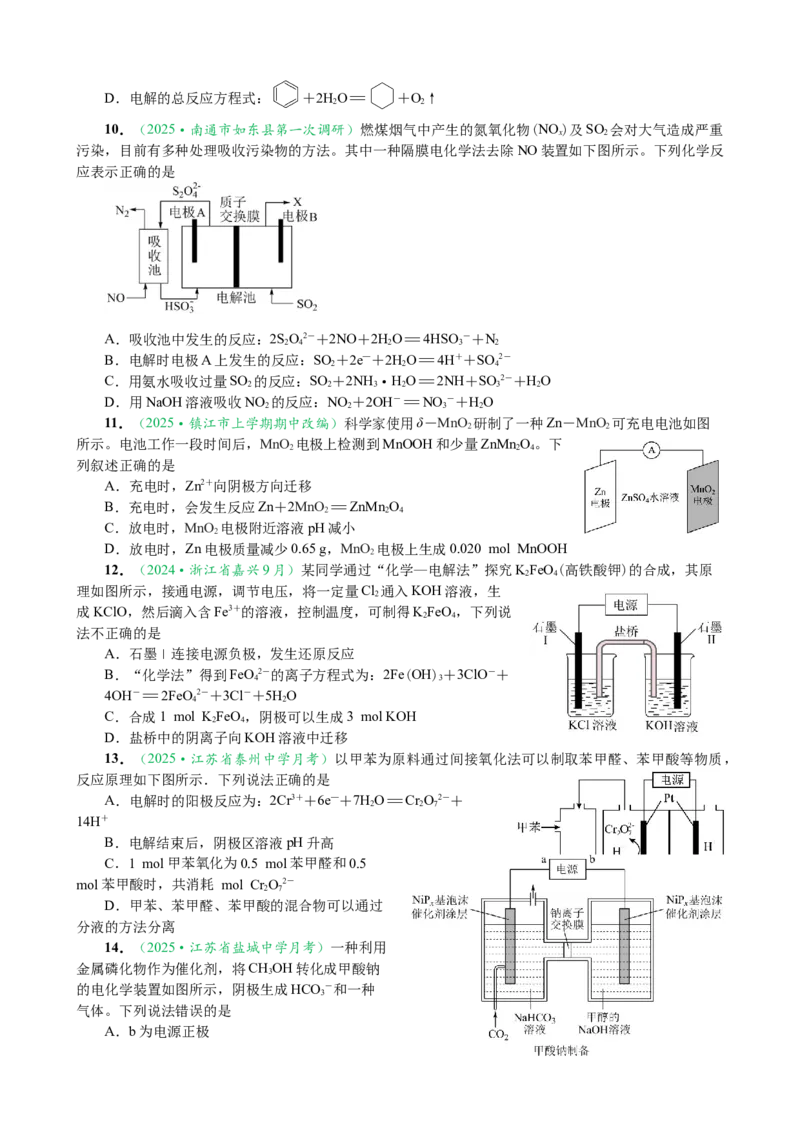
6.(2024·福建省漳州市第二次质检)膜电极反应器具有电阻低、能耗低、结构紧凑等优点,研究
人员设计了一种(碱性)膜电极反应器(如图所示)用于持续制备C H,下列说法中正确的是
2 4
A.电极M上,反应物和生成物中碳原子的杂化方式相同
B.电极N的电极反应式:2HO-4e—=4H++O↑
2 2
C.反应后溶液的pH变大
D.电极M上产生44.8 L C H,转移电子的数目为4N
2 4 A
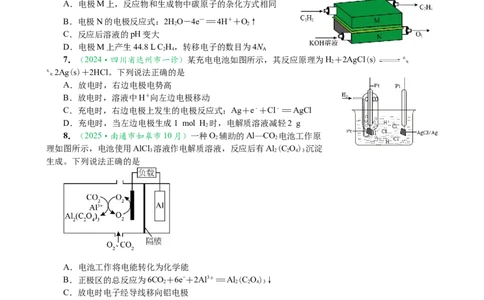
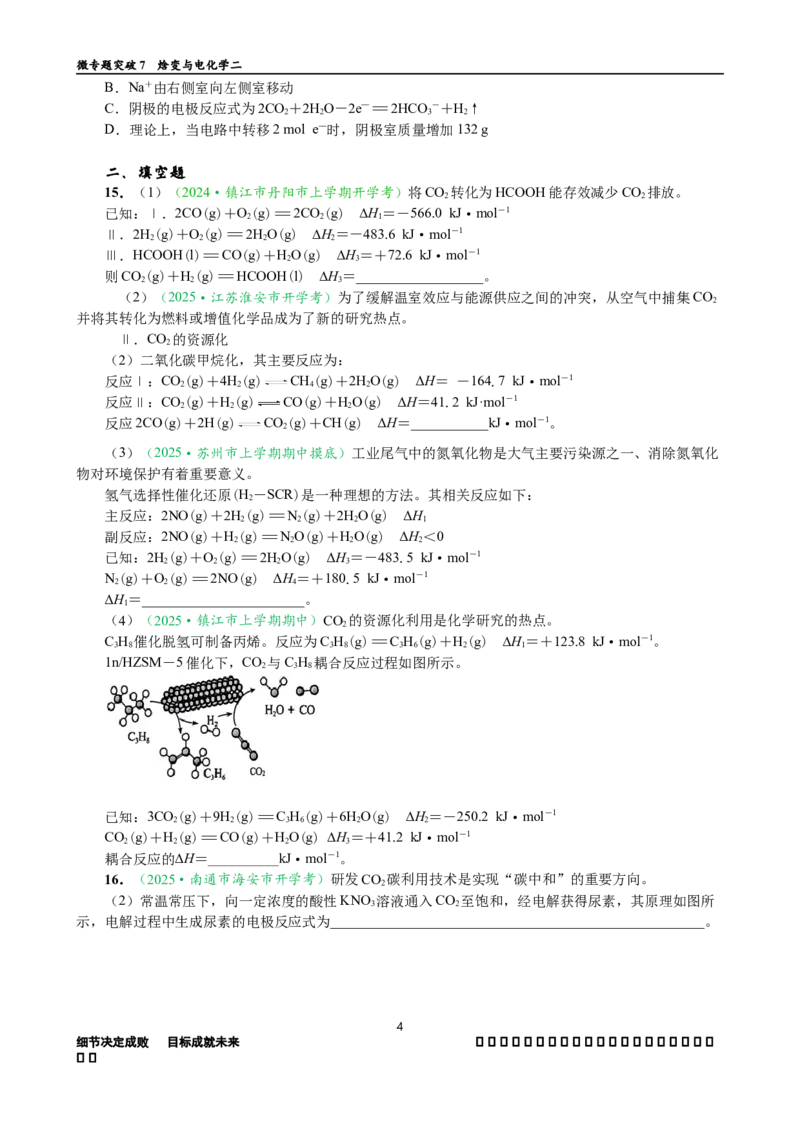
7.(2024·四川省达州市一诊)某充电电池如图所示,其反应原理为H+2AgCl(s) 放
2 电
充 2Ag(s)+2HCl。下列说法正确的是
电
A.放电时,右边电极电势高
B.放电时,溶液中H+向左边电极移动
C.充电时,右边电极上发生的电极反应式:Ag+e﹣+Cl﹣=AgCl
D.充电时,当左边电极生成1 mol H 时,电解质溶液减轻2 g
2
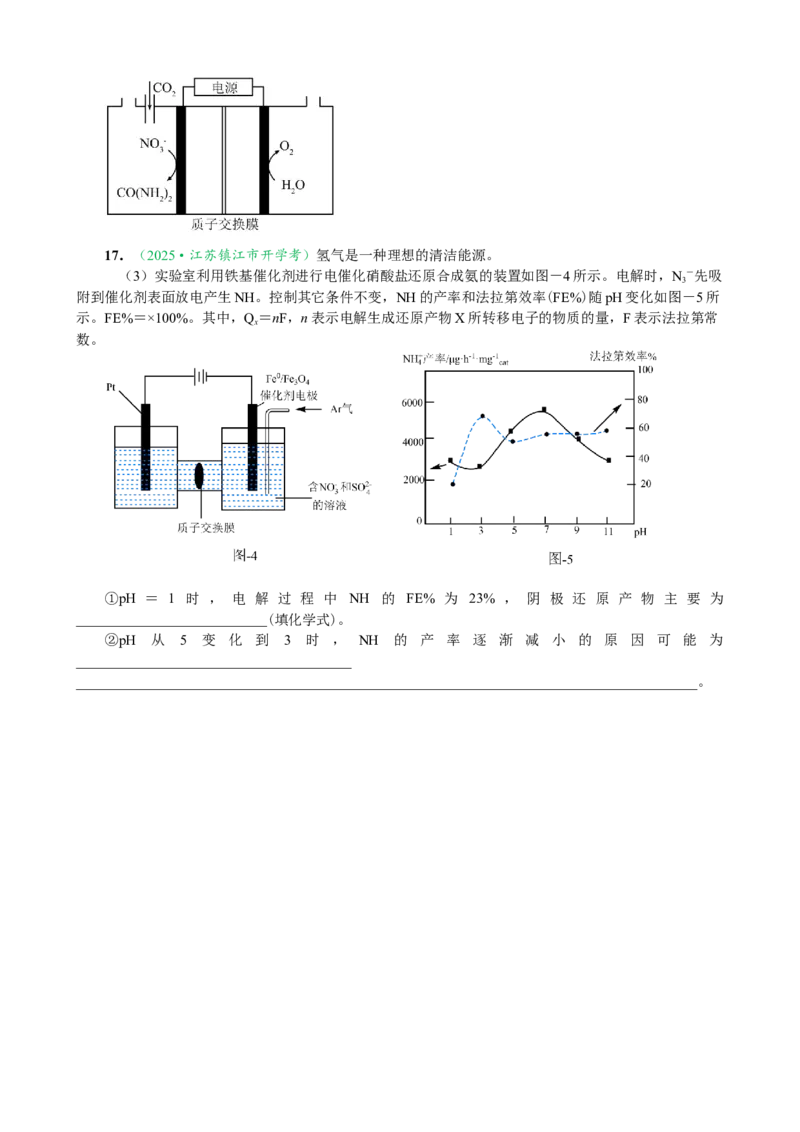
8.(2025·南通市如皋市10月)一种O 辅助的Al—CO 电池工作原
2 2
理如图所示,电池使用AlCl 溶液作电解质溶液,反应后有Al (C O) 沉淀
3 2 2 4 3
生成。下列说法正确的是
A.电池工作将电能转化为化学能
B.正极区的总反应为6CO+6e−+2Al3+=Al (C O)↓
2 2 2 4 3
C.放电时电子经导线移向铝电极
D.常温时,铝电极质量减少2.7 g,理论上消耗6.72 L CO
2
9.(2025·连云港市上学期期中)利用电解可以将气态苯( )转化为环己烷( ),其电解装置
如图所示。下列有关说法正确的是
A.电解时,电极A与电源的正极相连
B.电解时,电极B上产生的气体为H
2
C.反应中每生成1 mol ,转移电子数为6×6.02×1023
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找D.电解的总反应方程式: +2HO= +O↑
2 2
10.(2025·南通市如东县第一次调研)燃煤烟气中产生的氮氧化物(NO)及SO 会对大气造成严重
x 2
污染,目前有多种处理吸收污染物的方法。其中一种隔膜电化学法去除NO装置如下图所示。下列化学反
应表示正确的是
A.吸收池中发生的反应:2SO2-+2NO+2HO=4HSO -+N
2 4 2 3 2
B.电解时电极A上发生的反应:SO +2e—+2HO=4H++SO 2-
2 2 4
C.用氨水吸收过量SO 的反应:SO +2NH ·HO=2NH+SO2-+HO
2 2 3 2 3 2
D.用NaOH溶液吸收NO 的反应:NO +2OH-=NO -+HO
2 2 3 2
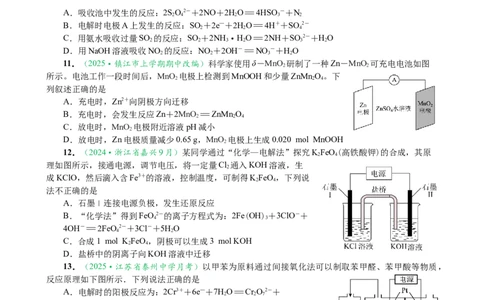
11.(2025·镇江市上学期期中改编)科学家使用δ-MnO 研制了一种Zn-MnO 可充电电池如图
2 2
所示。电池工作一段时间后,MnO 电极上检测到MnOOH和少量ZnMnO。下
2 2 4
列叙述正确的是
A.充电时,Zn2+向阴极方向迁移
B.充电时,会发生反应Zn+2MnO =ZnMnO
2 2 4
C.放电时,MnO 电极附近溶液pH减小
2
D.放电时,Zn电极质量减少0.65 g,MnO 电极上生成0.020 mol MnOOH
2
12.(2024·浙江省嘉兴9月)某同学通过“化学—电解法”探究KFeO(高铁酸钾)的合成,其原
2 4
理如图所示,接通电源,调节电压,将一定量Cl 通入KOH溶液,生
2
成KClO,然后滴入含Fe3+的溶液,控制温度,可制得KFeO,下列说
2 4
法不正确的是
A.石墨Ⅰ连接电源负极,发生还原反应
B.“化学法”得到FeO2-的离子方程式为:2Fe(OH)+3ClO-+
4 3
4OH-=2FeO2-+3Cl-+5HO
4 2
C.合成1 mol KFeO,阴极可以生成3 mol KOH
2 4
D.盐桥中的阴离子向KOH溶液中迁移
13.(2025·江苏省泰州中学月考)以甲苯为原料通过间接氧化法可以制取苯甲醛、苯甲酸等物质,
反应原理如下图所示.下列说法正确的是
A.电解时的阳极反应为:2Cr3++6e—+7HO=Cr O2-+
2 2 7
14H+
B.电解结束后,阴极区溶液pH升高
C.1 mol甲苯氧化为0.5 mol苯甲醛和0.5
mol苯甲酸时,共消耗 mol Cr O2-
2 7
D.甲苯、苯甲醛、苯甲酸的混合物可以通过
分液的方法分离
14.(2025·江苏省盐城中学月考)一种利用
金属磷化物作为催化剂,将CHOH转化成甲酸钠
3
的电化学装置如图所示,阴极生成HCO -和一种
3
气体。下列说法错误的是
A.b为电源正极微专题突破7 焓变与电化学二
B.Na+由右侧室向左侧室移动
C.阴极的电极反应式为2CO+2HO-2e—=2HCO -+H↑
2 2 3 2
D.理论上,当电路中转移2 mol e—时,阴极室质量增加132 g
二、填空题
15.(1)(2024·镇江市丹阳市上学期开学考)将CO 转化为HCOOH能存效减少CO 排放。
2 2
已知:Ⅰ.2CO(g)+O(g)=2CO(g) ∆H=-566.0 kJ·mol-1
2 2 1
Ⅱ.2H(g)+O(g)=2HO(g) ∆H=-483.6 kJ·mol-1
2 2 2 2
Ⅲ.HCOOH(l)=CO(g)+HO(g) ∆H=+72.6 kJ·mol-1
2 3
则CO(g)+H(g)=HCOOH(l) ∆H=__________________。
2 2 3
(2)(2025·江苏淮安市开学考)为了缓解温室效应与能源供应之间的冲突,从空气中捕集CO
2
并将其转化为燃料或增值化学品成为了新的研究热点。
Ⅱ.CO 的资源化
2
(2)二氧化碳甲烷化,其主要反应为:
反应Ⅰ:CO(g)+4H(g) CH(g)+2HO(g) ΔH= -164.7 kJ·mol-1
2 2 4 2
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH=41.2 kJ·mol-1
2 2 2
反应2CO(g)+2H(g) CO(g)+CH(g) ΔH=___________kJ·mol-1。
2
(3)(2025·苏州市上学期期中摸底)工业尾气中的氮氧化物是大气主要污染源之一、消除氮氧化
物对环境保护有着重要意义。
氢气选择性催化还原(H-SCR)是一种理想的方法。其相关反应如下:
2
主反应:2NO(g)+2H(g)=N(g)+2HO(g) ΔH
2 2 2 1
副反应:2NO(g)+H(g)=NO(g)+HO(g) ΔH<0
2 2 2 2
已知:2H(g)+O(g)=2HO(g) ΔH=-483.5 kJ·mol-1
2 2 2 3
N(g)+O(g)=2NO(g) ΔH=+180.5 kJ·mol-1
2 2 4
ΔH=_______________________。
1
(4)(2025·镇江市上学期期中)CO 的资源化利用是化学研究的热点。
2
C H 催化脱氢可制备丙烯。反应为C H(g)=C H(g)+H(g) ∆H=+123.8 kJ·mol-1。
3 8 3 8 3 6 2 1
1n/HZSM-5催化下,CO 与C H 耦合反应过程如图所示。
2 3 8
已知:3CO(g)+9H(g)=C H(g)+6HO(g) ∆H=-250.2 kJ·mol-1
2 2 3 6 2 2
CO(g)+H(g)=CO(g)+HO(g) ∆H=+41.2 kJ·mol-1
2 2 2 3
耦合反应的∆H=__________kJ·mol-1。
16.(2025·南通市海安市开学考)研发CO 碳利用技术是实现“碳中和”的重要方向。
2
(2)常温常压下,向一定浓度的酸性KNO 溶液通入CO 至饱和,经电解获得尿素,其原理如图所
3 2
示,电解过程中生成尿素的电极反应式为_____________________________________________________。
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找17.(2025·江苏镇江市开学考)氢气是一种理想的清洁能源。
(3)实验室利用铁基催化剂进行电催化硝酸盐还原合成氨的装置如图-4所示。电解时,N-先吸
3
附到催化剂表面放电产生NH。控制其它条件不变,NH的产率和法拉第效率(FE%)随pH变化如图-5所
示。FE%=×100%。其中,Q=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常
x
数。
①pH = 1 时 , 电 解 过 程 中 NH 的 FE% 为 23% , 阴 极 还 原 产 物 主 要 为
___________________________(填化学式)。
②pH 从 5 变 化 到 3 时 , NH 的 产 率 逐 渐 减 小 的 原 因 可 能 为
_______________________________________
________________________________________________________________________________________。