文档内容
微专题突破6 焓变与电化学
辛勤的蜜蜂永没有时间悲哀。——布莱克
目标定位
1.能应用盖斯定律进行有关计算。
2.能准确书写电极反应式及判断所给电极反应式的正误。
教学重点难点
1.盖斯定律应用。
2.原电池及电解的电极反应式的书写。
教学方法
讨论、归纳
教学过程
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
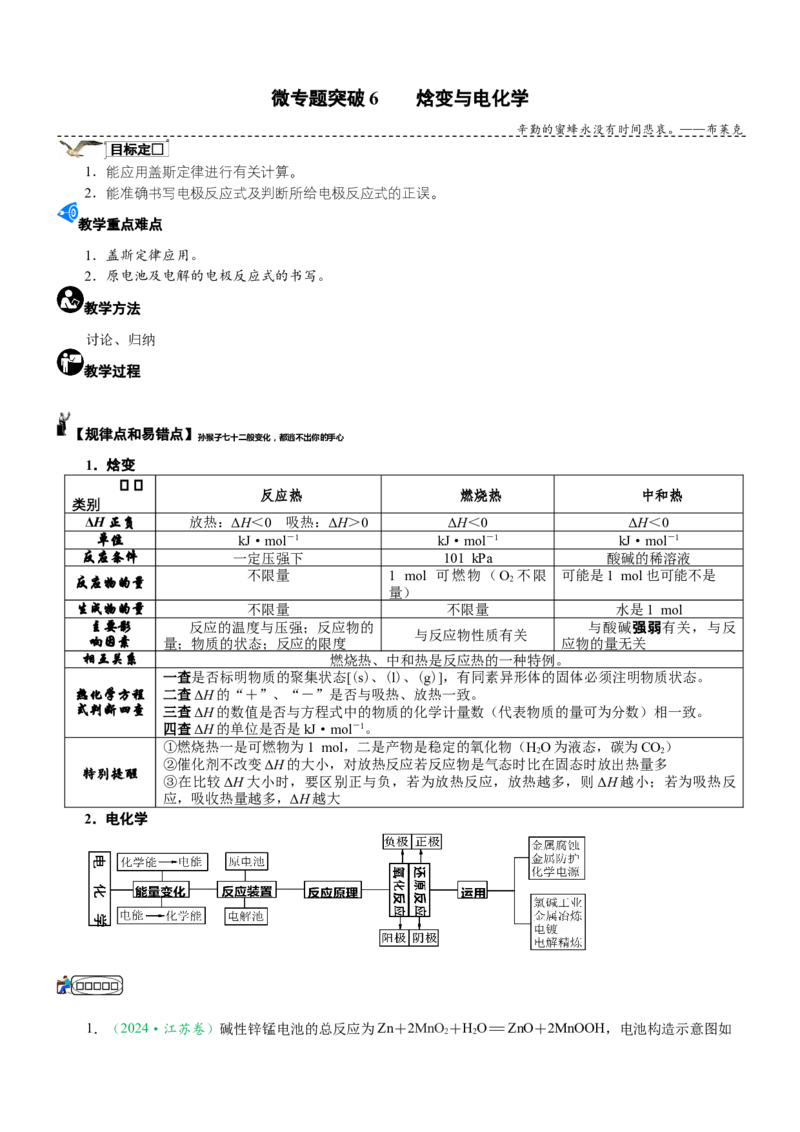
1.焓变
名 名
反应热 燃烧热 中和热
类别
ΔH正负 放热:ΔH<0 吸热:ΔH>0 ΔH<0 ΔH<0
单位 kJ·mol-1 kJ·mol-1 kJ·mol-1
反应条件 一定压强下 101 kPa 酸碱的稀溶液
不限量 1 mol 可燃物(O 不限 可能是1 mol也可能不是
反应物的量 2
量)
生成物的量 不限量 不限量 水是1 mol
主要影 反应的温度与压强;反应物的 与酸碱强弱有关,与反
与反应物性质有关
响因素 量;物质的状态;反应的限度 应物的量无关
相互关系 燃烧热、中和热是反应热的一种特例。
一查是否标明物质的聚集状态[(s)、(l)、(g)],有同素异形体的固体必须注明物质状态。
热化学方程 二查ΔH的“+”、“-”是否与吸热、放热一致。
式判断四查 三查ΔH的数值是否与方程式中的物质的化学计量数(代表物质的量可为分数)相一致。
四查ΔH的单位是否是kJ·mol-1。
①燃烧热一是可燃物为1 mol,二是产物是稳定的氧化物(HO为液态,碳为CO)
2 2
②催化剂不改变ΔH的大小,对放热反应若反应物是气态时比在固态时放出热量多
特别提醒
③在比较ΔH大小时,要区别正与负,若为放热反应,放热越多,则ΔH越小;若为吸热反
应,吸收热量越多,ΔH越大
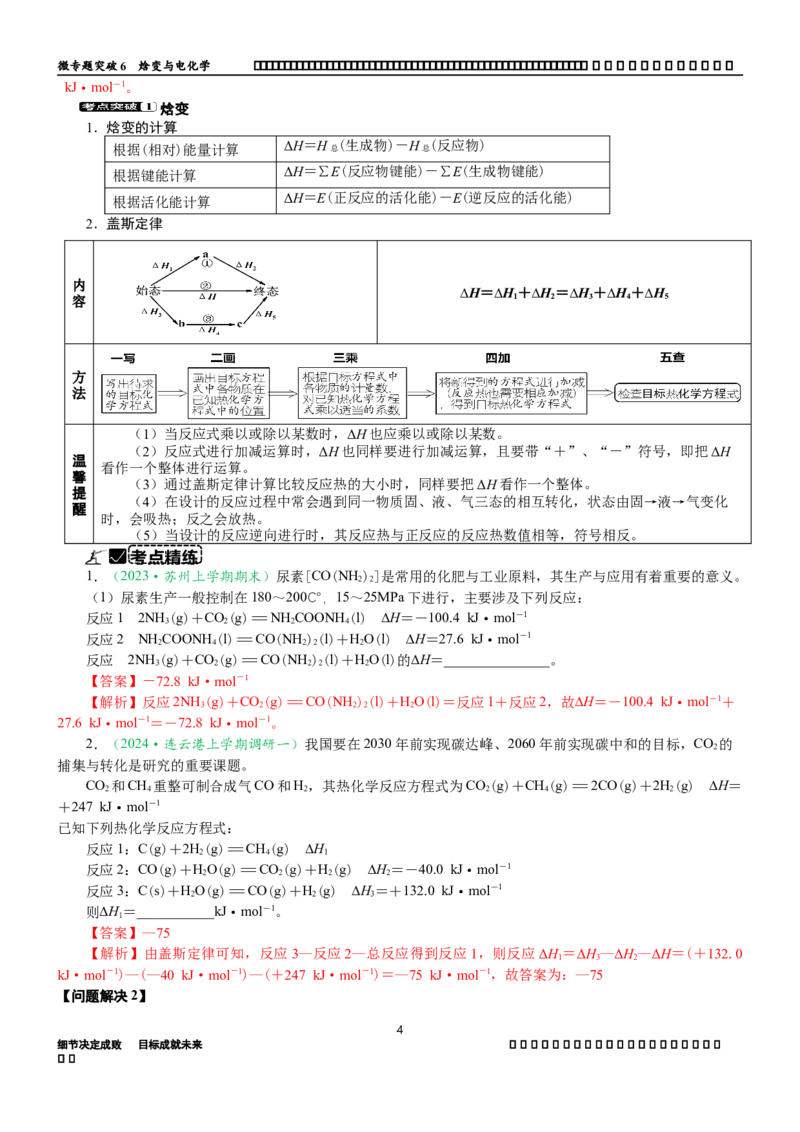
2.电化学
位位位位位
1.(2024·江苏卷)碱性锌锰电池的总反应为Zn+2MnO +HO=ZnO+2MnOOH,电池构造示意图如
2 2微专题突破6 焓变与电化学 名名名名名名名名名名名
图所示。下列有关说法正确的是
A.电池工作时,MnO 发生氧化反应
2
B.电池工作时,OH-通过隔膜向正极移动
C.环境温度过低,不利于电池放电
D.反应中每生成1 mol MnOOH,转移电子数为2×6.02×1023
【答案】C
【解析】Zn为负极,电极反应式为:Zn-2e—+2OH-=ZnO+HO,MnO 为正极,电极反应式为:MnO
2 2 2
+e—+HO=MnOOH+OH-。
2
A项,电池工作时,MnO 为正极,得到电子,发生还原反应,错误;B项,电池工作时,OH-通过隔膜向
2
负极移动,错误;C项,环境温度过低,化学反应速率下降,不利于电池放电,正确;D项,由电极反应式
MnO +e—+HO=MnOOH+OH-可知,反应中每生成1 mol MnOOH,转移电子数为6.02×1023,错误。
2 2
2.(2023·江苏)催化电解吸收CO 的KOH溶液可将CO 转化为有机物。在相同条件下,恒定通过电解
2 2
池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。
FE%=×100%
其中,Q =nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
X
①当电解电压为UV时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为______(填化学式)。
1
②当电解电压为UV时,阴极由HCO生成CH 的电极反应式为___________________________________。
2 4
③ 当 电 解 电 压 为 UV 时 , 电 解 生 成 的 C H 和 HCOO - 的 物 质 的 量 之 比 为
3 2 4
________________________________
_________________________________________________(写出计算过程)。
【答案】①H ②HCO+8e-+6HO=CH↑+9OH- ③每生成1 mol C H 转移12 mol e-,每生成1 mol
2 2 4 2 4
HCOO-转移2 mol e-,故电解生成的C H 和HCOO-的物质的量之比为∶=1∶2
2 4
【解析】①当电解电压为UV时,电解过程中含碳还原产物的FE%为0,说明二氧化碳未得电子,为HO
1 2
放电变成氢气。②当电解电压为UV时,根据得失电子守恒、原子守恒和电荷守恒可知碱性条件下阴极由 HCO
2
生成CH 的电极反应式为HCO+8e-+6HO=CH↑+9OH-。③当电解电压为UV时,电解过程中还原产物
4 2 4 3
C H 的FE%为24%,还原产物HCOO-的FE%为8%,每生成1 mol C H 转移12 mol e-,每生成1 mol HCOO-
2 4 2 4
转移2 mol e-,故电解生成的C H 和HCOO-的物质的量之比为∶=1∶2。
2 4
3.(2022·江苏卷)氢气是一种清洁能源,绿色环保制氢技术研究具有重要意义。
(1)“CuClHO热电循环制氢”经过溶解、电解、热水解和热分解4个步骤,其过程如图1所示。
2
2
细节决定成败 目标成就未来 名名名名名名名名名名名名名名名名名名名名
名名①电解在质子交换膜电解池中进行。阳极区为酸性CuCl溶液,阴极区为盐酸,电解过程中CuCl转化为
CuCl。电解时阳极发生的主要电极反应为__________________________________(用电极反应式表示)。
②电解后,经热水解和热分解的物质可循环使用。在热水解和热分解过程中,发生化合价变化的元素有
__________(填元素符号)。
【答案】①CuCl+2Cl--e-=CuCl ②Cu、O
【解析】①电解在质子交换膜电解池中进行,H+可自由通过,阳极区为酸性CuCl溶液,电解过程中CuCl
转化为CuCl,电解时阳极发生的主要电极反应为CuCl+2Cl--e-=CuCl;②电解后,经热水解得到的HCl和
热分解得到的CuCl等物质可循环使用,从图中可知,热分解产物还有 O ,又进入热水解的物质有CuCl,故发
2
生化合价变化的元素有Cu、O。
【问题解决1】
1.(2024·南通市如皋2月)二氧化碳的综合利用具有重要意义。
(1)工业上以CO和CH 为原料可以制取合成气(CO和H)。
4 2
①已知CH、H、CO的燃烧热分别为890.3 kJ·mol-1、285.8 kJ·mol-1、283 kJ·mol-1,则反应CH(g)
4 2 4
+CO(g)=2CO(g)+2H(g)的∆H=_______________。
2 2
②将CO 和CH 以体积比1∶1混合后,通过装有催化剂的反应管。下列措施有利于提高CH 转化率的是
2 4 4
________(填字母)。
a.将反应管控制在催化剂的最大活性温度范围内
b.延长混合气体通过反应管的时间
c.向反应管中加入少量炭粉
【答案】(1)①247.3 kJ·mol-1 ②ab
【解析】①根据CH、H、CO的燃烧热分别为890.3 kJ·mol-1、285.8 kJ·mol-1、283 kJ·mol-1,则有:
4 2
CH(g)+2O(g)=CO(g)+2HO(l) ∆H=-890.3 kJ·mol-1……①
4 2 2 2
CO(g)+O(g)=CO(g) ∆H=-283 kJ·mol-1……②
2 2
H(g)+O(g)=HO(l) ∆H=-285.8 kJ·mol-1……③
2 2 2
根据盖斯定律,①-(②+③)×2 可得:CH(g)+CO(g)=2CO(g)+2H(g) ΔH,则∆H=-890.3
4 2 2
kJ·mol-1-(-283 kJ·mol-1+-285.8 kJ·mol-1)×2=+247.3 kJ·mol-1,故答案为:+247.3;②反应为
CH(g)+CO(g)=2CO(g)+2H(g),将CO 和CH 以体积比1∶1混合后,通过装有催化剂的反应管:a项,
4 2 2 2 4
将反应管控制在催化剂的最大活性温度范围内,此时催化剂活性最大,可以提高未平衡前一段时间内的 CH 转
4
化率;b项,延长混合气体通过反应管的时间,让反应逐渐达到平衡,也就是CH 转化率最大时,因此可以提
4
高CH 转化率;c项,向反应管中加入少量炭粉,对反应并没有影响,不能改变 CH 转化率,综上所述选ab;
4 4
故答案为:ab。
2.(2024·南通市海门市第一次调研)TiCl₄制备提纯过程中涉及以下两个反应:
TiCl (s)+2H(g)=Ti(s)+4HCl(g) ∆H
4 2 5
Ti(s)+2Cl=TiCl (s) ∆H=-763 kJ·mol-1
2 4 6
已知:部分共价键的键能如下表所示:
H-H Cl-Cl Cl-H
键能/kJ·mol-1 436 243 431
依据以上信息可得∆H=___________kJ·mol-1。
5
【答案】397
【解析】根据数据可知Cl(g)+H(g)=2HCl(g)的∆H=436 kJ·mol-1+243 kJ·mol-1-2×431 kJ·mol
2 2
-1=-183 kJ·mol-1,由盖斯定律可知∆H =2∆H-∆H =2×(-183 kJ·mol-1)-( -763 kJ·mol-1)=+379
5 6微专题突破6 焓变与电化学 名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名
kJ·mol-1。
焓变
1.焓变的计算
根据(相对)能量计算
ΔH=H
总
(生成物)-H
总
(反应物)
根据键能计算
ΔH=∑E(反应物键能)-∑E(生成物键能)
根据活化能计算
ΔH=E(正反应的活化能)-E(逆反应的活化能)
2.盖斯定律
内
∆H=∆H+∆H=∆H+∆H+∆H
容 1 2 3 4 5
方
法
(1)当反应式乘以或除以某数时,ΔH也应乘以或除以某数。
(2)反应式进行加减运算时,ΔH也同样要进行加减运算,且要带“+”、“-”符号,即把ΔH
温
看作一个整体进行运算。
馨
(3)通过盖斯定律计算比较反应热的大小时,同样要把ΔH看作一个整体。
提
(4)在设计的反应过程中常会遇到同一物质固、液、气三态的相互转化,状态由固→液→气变化
醒
时,会吸热;反之会放热。
(5)当设计的反应逆向进行时,其反应热与正反应的反应热数值相等,符号相反。
考点精练
1.(2023·苏州上学期期末)尿素[CO(NH )]是常用的化肥与工业原料,其生产与应用有着重要的意义。
2 2
(1)尿素生产一般控制在180~200℃,15~25MPa下进行,主要涉及下列反应:
反应1 2NH (g)+CO(g)=NH COONH(l) ∆H=-100.4 kJ·mol-1
3 2 2 4
反应2 NH COONH(l)=CO(NH )(l)+HO(l) ∆H=27.6 kJ·mol-1
2 4 2 2 2
反应 2NH (g)+CO(g)=CO(NH )(l)+HO(l)的∆H=_______________。
3 2 2 2 2
【答案】-72.8 kJ·mol-1
【解析】反应2NH (g)+CO(g)=CO(NH )(l)+HO(l)=反应1+反应2,故∆H=-100.4 kJ·mol-1+
3 2 2 2 2
27.6 kJ·mol-1=-72.8 kJ·mol-1。
2.(2024·连云港上学期调研一)我国要在2030年前实现碳达峰、2060年前实现碳中和的目标,CO 的
2
捕集与转化是研究的重要课题。
CO 和CH 重整可制合成气CO和H,其热化学反应方程式为CO(g)+CH(g)=2CO(g)+2H(g) ∆H=
2 4 2 2 4 2
+247 kJ·mol-1
已知下列热化学反应方程式:
反应1:C(g)+2H(g)=CH(g) ∆H
2 4 1
反应2:CO(g)+HO(g)=CO(g)+H(g) ∆H=-40.0 kJ·mol-1
2 2 2 2
反应3:C(s)+HO(g)=CO(g)+H(g) ∆H=+132.0 kJ·mol-1
2 2 3
则∆H=___________kJ·mol-1。
1
【答案】—75
【解析】由盖斯定律可知,反应3—反应2—总反应得到反应1,则反应ΔH =ΔH—ΔH—ΔH=(+132.0
1 3 2
kJ·mol-1)—(—40 kJ·mol-1)—(+247 kJ·mol-1)=—75 kJ·mol-1,故答案为:—75
【问题解决2】
4
细节决定成败 目标成就未来 名名名名名名名名名名名名名名名名名名名名
名名(2024·连云港一模)用如图所示的新型电池可以处理含CN-的碱性废水,同时还可以淡化海水。
下列说法正确的是
A.a极电极反应式:2CN-+10e—+12OH-=2CO2-+N↑+6HO
3 2 2
B.电池工作一段时间后,右室溶液的pH减小
C.交换膜Ⅰ为阳离子交换膜,交换膜Ⅱ为阴离子交换膜
D.若将含有26 g CN-的废水完全处理,理论上可除去NaCl的质量为292.5 g
【答案】D
【解析】由图可知,a电极CN-在碱性条件下失去电子生成氮气,电极反应为2CN--10e—+12OH-=
2CO2-+N↑+6HO,a为负极,则b为正极,电极反应为:2H++2e—=H↑,以此解题。
3 2 2 2
A项,由分析可知,a极电极反应式:2CN--10e—+12OH-=2CO2-+N↑+6HO,错误;B项,由分
3 2 2
析可知,b为正极,电极反应为:2H++2e—=H↑,则消耗氢离子,pH增大,错误;C项,由A分析可知,a
2
电极附近负电荷减少,则阴离子通过交换膜Ⅰ向左移动,由B分析可知,b电极附近正电荷减少,则阳离子通
过交换膜Ⅱ向右移动,错误;D项,26 g CN-的物质的量为1 mol,根据选项A分析可知,消耗1 mol CN-时转
移5 mol电子,根据电荷守恒可知,可同时处理5 mol NaCl,其质量为292.5 g,正确。
原电池工作原理
原电池 ①放热的氧化还原反应都可以设计成原电池;②原电池的电极不一定参加电极反应
微粒 电子由负极导线—\s\up 4()用电器导线—\s\up 4()正极(溶液中无电子迁移!)
—→ —→
迁移方向 阳离子—→正极,阴离子—→负极(同性恋!)
①较活泼金属不一定做负极。
温 ②电子是旱鸭子,不会游泳!即在电池与电
电极反应式 馨 解池的内部无电子通过!
书写 提 ③电极反应式书写:酸性溶液不能出现OH-,
醒
碱性溶液不能出现H+,水溶液中不能出现O2-
考点精练
(2024·无锡上学期期中)一种浓差电池的放电原理是利用电解质溶液的浓度不同而产生电流。某浓差电
池装置示意图如图所示,该电池使用前将开关K先与a连接一段时间后再与b连接。下列说法不正确的是
A.交换膜应当选择阳离子交换膜
B.K与a连接的目的是形成两电极区溶液的浓度差
C.K与b连接时,电极B上发生的反应为Cu2++2e—=Cu
D.K与b连接时,导线中通过2 mol电子,约有1 mol离子通过交换膜
【答案】A
【解析】由题干信息可知,将开关K先与a连接后则电极B为阳极,电极反应为Cu-2e—=Cu2+,电极A微专题突破6 焓变与电化学 名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名
为阴极,电极反应为:Cu2++2e—=Cu,一段时间后右侧溶液中Cu2+浓度增大,而左侧溶液中Cu2+浓度减小,
为了保持Cu2+的浓度差必须保证Cu2+不能通过半透膜,故交换膜是阴离子交换膜,一段时间后与b连接,电极
A为负极,电极反应为:Cu-2e—=Cu2+,电极B为正极,电极反应为:Cu2++2e—=Cu,据此分析解题。
A项,由分析可知,交换膜应当选择阴离子交换膜,阻止阳极Cu2+通过以保证两侧溶液中有Cu2+浓度差,
错误;B项,由分析可知,K与a连接是电极B为阳极,电极反应为Cu-2e—=Cu2+,电极A为阴极,电极反
应为:Cu2++2e—=Cu,其目的是形成两电极区溶液的浓度差,正确;C项,由分析可知,K与b连接时,电
极B为正极,其上发生的反应为Cu2++2e—=Cu,正确;D项,由分析可知,离子交换膜为阴离子交换膜,故
K与b连接时,导线中通过2 mol电子,约有1 mol离子即SO 2-通过交换膜,正确。
4
【问题解决3】
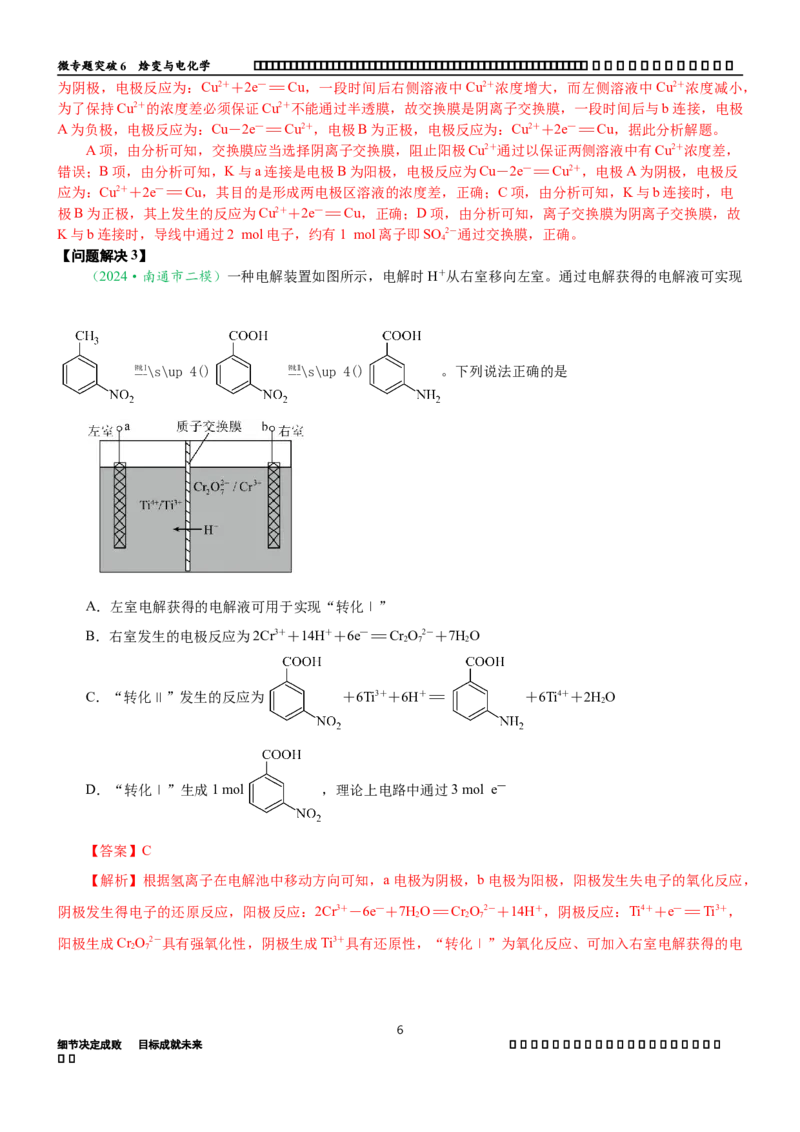
(2024·南通市二模)一种电解装置如图所示,电解时H+从右室移向左室。通过电解获得的电解液可实现
转化Ⅰ\s\up 4() 转化Ⅱ\s\up 4() 。下列说法正确的是
——— ———
A.左室电解获得的电解液可用于实现“转化Ⅰ”
B.右室发生的电极反应为2Cr3++14H++6e—=Cr O2-+7HO
2 7 2
C.“转化Ⅱ”发生的反应为 +6Ti3++6H+= +6Ti4++2HO
2
D.“转化Ⅰ”生成1 mol ,理论上电路中通过3 mol e—
【答案】C
【解析】根据氢离子在电解池中移动方向可知,a电极为阴极,b电极为阳极,阳极发生失电子的氧化反应,
阴极发生得电子的还原反应,阳极反应:2Cr3+-6e—+7HO=Cr O2-+14H+,阴极反应:Ti4++e—=Ti3+,
2 2 7
阳极生成Cr O2-具有强氧化性,阴极生成Ti3+具有还原性,“转化Ⅰ”为氧化反应、可加入右室电解获得的电
2 7
6
细节决定成败 目标成就未来 名名名名名名名名名名名名名名名名名名名名
名名解液氧化实现,“转化II”为还原反应,可加入左室电解获得的电解液还原实现, +6Ti3++6H+
= +6Ti4++2HO。
2
A项,根据分析,“转化Ⅰ”为氧化反应,应加入氧化剂,左室电解液含Ti3+,右室电解液含Cr O2-,所
2 7
以实现“转化Ⅰ”需右室电解获得电解液,错误;B项,根据分析,右室发生的电极反应:2Cr3+-6e—+7HO
2
=Cr O2-+14H+,错误;C项,“转化II”为还原反应,可加入左室电解获得的电解液还原实现,
2 7
+6Ti3++6H+= +6Ti4++2HO,正确;D项,“转化Ⅰ”为 -6e—+
2
2HO= +6H+,根据得失电子守恒,生成1 mol 理论上电路中通过6 mol e—,错误。
2
电解原理
电 电极
解 反应
规 式书
律 写
①充电反应正好是放电
微 反应的逆反应。看清
粒 电子:电源负极导线—\s\up 4()阴极、阳极 二 “充电、放电”的方
—→
迁 导线—\s\up 4()正极 次 向,放电时为原电池,
—→
移 离子:阳离子—→阴极,阴离子—→阳 电 充电时则是电解池,右
方 极 池 图是二次电池充电装
向 置。
②记忆:正正负负
①K+、Ca2+、Na+、Mg2+、Al3+离子在溶液中不放电!是水电离的H+放电!
温馨提醒 ②电镀是特殊的电解,阳极——镀层金属 阴极——镀件 电解液——含镀层金属阳离子
③记乙:阴得(阴德)——阴极得电子;痒痒——阳极发生氧化反应
铜的电解精炼:粗铜中通常含有Zn、Fe、Ni、Ag、Au等。
电极名称 电极材料 电极反应式 电解质溶液 溶液浓度
阳极 粗铜板 Cu-2e-=Cu2+ Fe-2e-=Fe2+ Ni-2e-=Ni2+ CuSO 溶液(加
4 略有下降
阴极 纯铜板 Cu2++2e-=Cu 入一定量的硫酸)
考点精练微专题突破6 焓变与电化学 名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名
换题(2024·江苏省南通市、盐城市二模)“太阳水”电池装置如图所示,该电池由三个电极组成,其中
a为TiO 电极,b为Pt电极,c为WO 电极,电解质溶液为pH=3的LiSO -HSO 溶液。锂离子交换膜将电池
2 3 2 4 2 4
分为A、B两个区,A区与大气相通,B区为封闭体系并有N 保护。下列关于该电池的说法错误的是
2
A.若用导线连接a、c,则a为负极,该电极附近pH减小
B.若用导线连接a、c,则c电极的电极反应式为HWO-xe一=WO+xH+
x 3 3
C.若用导线先连接a、c,再连接b、c,可实现太阳能向电能转化
D.若用导线连接b、c,b电极的电极反应式为O+4H++4e一=2HO
2 2
【答案】B
【解析】A项,有图可知,连接a、c时,a极上水失去电子生成氧气,发生氧化反应,则a极是负极,电
极反应式是2HO-4e-=O+4H+,生成氢离子,a极附近pH减少,不符合题意;B项,有图可知,用导线连
2 2
接a、c,a极上水失去电子生成氧气,发生氧化反应,则a极是负极,c极是正极,则c电极的电极反应式为
WO +xH++xe 一=HWO ,符合题意;C 项,若用导线先连接 a、c,则 c 电极是正极,发生 WO 生成
3 x 3 3
HWO ,将太阳能转化为化学能储存,再连接b、c,b极发生氧气生成水,为正极,则c电极是负极,实现化
x 3
学能转化为电能,对外供电,不符合题意;D项,用导线连接b、c,b电极发生氧气生成水为正极,电极反应
式为O+4H++4e一=2HO,不符合题意。
2 2
【问题解决4】
(2024·南京市二模)一种电解乙酰基吡嗪废水中的(NH )SO 制备(NH )SO 的电化学装置如题所示。
4 2 4 4 2 2 8
下列说法正确的是
A.石墨电极与直流电源正极相连
B.电解时,铂网电极附近pH增大
C.离子交换膜应选择性透过阴离子
D.阴极上的电极反应为2SO 2-+2e—=SO2-
4 2 8
【答案】B
【解析】电解乙酰基吡嗪废水中的(NH )SO 制备(NH )SO ,由图可知,铂网电极上(NH )SO 失去电子
4 2 4 4 2 2 8 4 2 4
发生氧化反应生成(NH )SO,为阳极,则石墨电极为阴极;
4 2 2 8
A项,石墨电极为阴极,与直流电源负极相连,错误;B项,电解时,铂网电极为阳极,(NH )SO 失去电
4 2 4
子发生氧化反应生成(NH )SO ,电极反应式为2SO 2--2e—=SO2-,阴极反应式为2H++2e—=H↑,则
4 2 2 8 4 2 8 2
右侧氢离子通过阳离子交换进入左侧,使得铂网电极附近pH增大,正确;C项,由B分析可知,离子交换膜应
选择性透过氢离子,错误;D项,阴极上的电极反应为2H++2e—=H↑,错误。
2
电化学原理的应用
8
细节决定成败 目标成就未来 名名名名名名名名名名名名名名名名名名名名
名名1.金属的腐蚀与防护
类型 ①析氢腐蚀:强酸性;②吸氧腐蚀:弱酸性、中性或碱性
保护 ①牺牲阳极的阴极保护法——原电池原理;②外加电源的阴极保护法——电解池原理
温馨提醒 铁作电极时通常转化为Fe2+!
2.制备物质、治理污染
考点精练
1.(2024·扬州市高三下学期开学考)臭氧催化氧化是降解水体中有机污染物的常用方法。
(1)一种电解法制备O 的装置如图所示。阳极生成O 的电极反应式为_______________________。O 广
3 3 3
泛用于食品、环境的消毒与水体处理,主要原因有_____________________________________________________
___________________。
【答案】①3HO-6e-=O↑+6H+ ②氧化性强;还原产物无污染;过量的O 会分解,分解产物是O,
2 3 3 2
无残留污染
【解析】和电源正极相连的是阳极,阳极发生氧化反应,阳极生成O 的电极反应式为:3HO-6e-=O↑
3 2 3
+6H+;O 具有很强的氧化性,且还原产物对环境无污染,过量的O 也会分解,分解产物是O 无残留,因此广
3 3 2
泛用于食品、环境的消毒与水体处理。
2.(2024·南通市如皋二模)以甲苯为原料通过间接氧化法可以制取苯甲醛、苯甲酸等物质,反应原理如
下图所示.下列说法正确的是
A.电解时的阳极反应为:2Cr3++6e—+7HO=Cr O2-+14H+
2 2 7
B.电解结束后,阴极区溶液pH升高
C.1 mol甲苯氧化为0.5 mol苯甲醛和0.5 mol苯甲酸时,共消耗 mol Cr O2-
2 7
D.甲苯、苯甲醛、苯甲酸的混合物可以通过分液的方法分离
【答案】C
【解析】由图可知,左侧电极为阳极,水分子作用下铬离子在阳极失去电子发生氧化反应生成重铬酸根离
子和氢离子,电极反应式为2Cr3+-6e—+7HO=Cr O2-+14H+,阳极槽外中重铬酸根离子与甲苯在酸性条件
2 2 7
下反应生成苯甲醛或苯甲酸,反应的离子方程式为 3C H -CH +2Cr O2-+16H+=3C H -CHO+4Cr3++
6 5 3 2 7 6 5
11HO,C H-CH+Cr O2-+8H+=C H-COOH +2Cr3++5HO,电解时,氢离子通过阳离子交换膜由阳极
2 6 5 3 2 7 6 5 2
区进入阴极区,右侧电极为电解池的阴极,阴极氢离子放电,电极反应为:2H++2e—=H↑,据此作答。
2
A项,电解时的阳极发生氧化反应,电极反应为:2Cr3+-6e—+7HO=Cr O2-+14H+,错误;B项,阳
2 2 7
极区产生的氢离子透过质子交换膜进入阴极区,阴极上氢离子放电,电极反应为:2H++2e—=H↑,电极上
2
每消耗2 mol H+,就有2 mol H+进入阴极区,故电极电解结束后,阴极区溶液pH不变,错误;C项,结合
3C H-CH+2Cr O2-+16H+=3C H-CHO+4Cr3++11HO,0.5 mol甲苯氧化为0.5 mol苯甲醛时消耗 mol
6 5 3 2 7 6 5 2微专题突破6 焓变与电化学 名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名
Cr O2-,根据C H-CH+Cr O2-+8H+=C H-COOH+2Cr3++5HO,0.5 mol甲苯氧化为0.5 mol苯甲酸
2 7 6 5 3 2 7 6 5 2
时消耗0.5 mol Cr O2-,则1 mol甲苯氧化为0.5 mol苯甲醛和0.5 mol苯甲酸时,共消耗 mol Cr O2-,正确;
2 7 2 7
D项,甲苯、苯甲醛、苯甲酸的混合物是互溶的液体,不可以通过分液的方法分离,错误。
对于原电池原理的分析,需围绕电子为核心:定性抓电子的流向;定量抓电子的流量。
电极反应式步骤:(1)依据通式;(2)关注介质;(3)遵循守恒
成功体验
1.(2024··江苏扬州高三下开学考试)如图为一种酶生物电池,可将葡萄糖(C H O)转化为葡萄糖内
6 12 6
酯(C H O),两个碳纳米管电极材料由石墨烯片层卷曲而成。下列说法不正确的是
6 10 6
A.图中的离子交换膜为阳离子交换膜
B.负极区发生的电极反应主要为C H O-2e—=C H O+2H+
6 12 6 6 10 6
C.碳纳米管有良好导电性能,且能高效吸附气体
D.理论上消耗标况下2.24 L O,可生成葡萄糖内酯0.2 mol
2
【答案】D
【解析】由图可知,右侧碳纳米管为正极,电极反应式为O+4e-+4H+=2HO,左侧碳纳米管为负极,
2 2
电极反应式为H-2e-=2H+,C H O-2e-=2H++C H O,据此作答。
2 6 12 6 6 10 6
【解析】A项,图中离子交换膜能让氢离子透过,故离子交换膜为阳离子交换膜,正确;B项,由分析可
知,负极区发生的电极反应主要为C H O-2e—=C H O+2H+,正确;C项,碳纳米管电极材料由石墨烯片
6 12 6 6 10 6
层卷曲而成,有良好导电性能,且能高效吸附气体,正确;D项,由分析可知,理论上消耗标况下2.24 L O,
2
得到0.4 mol e-,由于负极区有H 和C H O 两种物质失电子,所以生成葡萄糖内酯小于0.2 mol,错误。
2 6 12 6
2.(2024·江苏徐州模拟预测)氯、溴、碘及其化合物在自然界广泛存在且具有重要应用。氯、溴主要存
在于海水中,工业常通,过电解NaCl饱和溶液制备Cl,Cl 可用于制取漂白粉、氯化氢(H-H、Cl-Cl、H-
2 2
Cl的键能分别为436 kJ·mol-1、243 kJ·mol-1、432 kJ·mol-1)。卤水中Br-可通过Cl 氧化、NaCO 溶液吸
2 2 3
收,BrCl能发生水解反应。锂碘电池可供电心脏起搏器。一种Li-I 二次电池正极界面反应机理如图所示,下
2
列化学反应表示正确的是
10
细节决定成败 目标成就未来 名名名名名名名名名名名名名名名名名名名名
名名A.LiI 电池正极放电时的电极反应有:I—+2e—=2I-+I-
2 5 3
B.Br (g)用NaCO 溶液吸收:Br +CO2-=Br-+BrO-+CO
2 2 3 2 3 3 2
C.BrCl与HO反应:BrCl+HO=HCl+Br++OH-
2 2
D.氯气制氯化氢:H(g)+Cl(g)=2HCl(g) ∆H=185 kJ·mol-1
2 2
【答案】A
【解析】A项,LiI 电池正极放电时是由I—得到电子生成 -,然后 -继续得电子生成I-,第一步放电的电
2 5 3 3
极反应为:I—+2e—=2I-+I-,正确;B项,Br (g)用NaCO 溶液吸收的方程式前后没有原子守恒,正确的
5 3 2 2 3
离子方程式为3Br +3CO2-=5Br-+BrO-+3CO,错误;C项,BrCl与HO反应类似于卤素单质和水反应,
2 3 3 2 2
因此反应方程式为:BrCl+HO=HCl+HBrO,错误;D项,氯气制氯化氢反应方程式为:H(g)+Cl(g)=
2 2 2
2HCl(g),由题可知反应物和生成物化学键的键能,因此∆H=反应物的键能–生成物的键能=-185 kJ·mol-
1,错误。
3.(2024·苏州调研期初)氨硼烷—HO 燃料电池装置示意如图所示,该电池在常温下即可工作,总反
2 2
应为NH •BH+3HO=NH BO+4HO,下列说法不正确的是
3 3 2 2 4 2 2
A.氨硼烷与水分子间可形成氢键,故易溶于水
B.a电极上的反应为:NH •BH+2HO+6e—=NH+BO2-+6H+
3 3 2
C.放电过程中1molH O 参与反应时,转移的电子数约为2×6.02×1023
2 2
D.其他条件不变,向HO 溶液中加入适量硫酸能增大电流强度
2 2
【答案】B
【解析】由总反应方程式可知,放电时,a电极为燃料电池的负极,水分子作用下氨硼烷在负极失去电子
发生氧化反应生成偏硼酸铵和氢离子,电极反应式为 NH ·BH +2HO-6e—=NH+BO2-+6H+,b电极为正
3 3 2
极,酸性条件下过氧化氢在正极得到电子发生还原反应生成水,电极反应式为HO+2e—+2H+=2HO。
2 2 2
A项,氨硼烷分子中含有氮氢键,能与水分子形成分子间氢键,所以氨硼烷易溶于水,正确;B项,由分
析可知,放电时,a电极为燃料电池的负极,水分子作用下氨硼烷在负极失去电子发生氧化反应生成偏硼酸铵
和氢离子,电极反应式为NH ·BH+2HO-6e—=NH+BO2-+6H+,错误;C项,由分析可知,b电极为正
3 3 2
极,酸性条件下过氧化氢在正极得到电子发生还原反应生成水,电极反应式为HO+2e—+2H+=2HO,则1
2 2 2
mol过氧化氢参与反应时,转移的电子数约为2×6.02×1023,正确;D项,硫酸为强电解质,加入适量的硫酸,
可以增大溶液中离子浓度,增强导电能力,增大电流强度,正确。
4.(2024·南通市海安市)捕集并转化CO 可以有效实现碳达峰、碳中和。
2
Ⅰ.工业上利用两种温室气体CH 和CO 催化重整制取H 和CO,主要反应为
4 2 2
反应①:CH(g)+CO(g) 2CO(g)+2H(g) ∆H=+247.4 kJ·mol-1
4 2 2 1
过程中还发生三个副反应:
反应②:CO(g)+H(g) CO(g)+HO(g) ∆H=+41.2 kJ·mol-1
2 2 2 2
反应③:2CO(g) CO(g)+C(s) ∆H=-171.0 kJ·mol-1
2 3
反应④:CH(g) 2H(g)+C(s) ∆H
4 2 4
∆H=___________。
4
【答案】+76.4 kJ·mol-1
【解析】由盖斯定律可知,反应①+反应③得到反应④,则反应ΔH =(+247.4 kJ·mol-1)+(—171.0
4
kJ·mol-1)=+76.4 kJ·mol-1,故答案为:+76.4 kJ·mol-1。
5.(2024·江苏南京市、盐城市一模)“碳中和”目标如期实现的关键技术之一是CO 的再资源化利用。
2
催化电解吸收CO 的KOH溶液可将CO 转化为有机物。
2 2微专题突破6 焓变与电化学 名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名名
①HCO -在阴极放电生成CHCOO-的电极反应式为______________________________________________。
3 3
②碱性溶液有利于抑制阴极上副产物的产生,该副产物的化学式为___________。
【答案】①11HCO -+8e—=CHCOO-+9CO2-+4HO ②H
3 3 3 2 2
【解析】①催化电解吸收CO 的KOH溶液可将CO 转化为有机物,HCO -在阴极放电生成CHCOO-,电
2 2 3 3
极反应式为11HCO -+8e—=CHCOO-+9CO2-+4HO,故答案为11HCO -+8e—=CHCOO-+9CO2-+
3 3 3 2 3 3 3
4HO;②电解时,H+可在阴极得到电子生成H,碱性溶液有利于抑制H 的产生,故答案为H。
2 2 2 2
12
细节决定成败 目标成就未来 名名名名名名名名名名名名名名名名名名名名
名名