文档内容
微专题突破8 化学反应速率与化学平衡
一、选择题
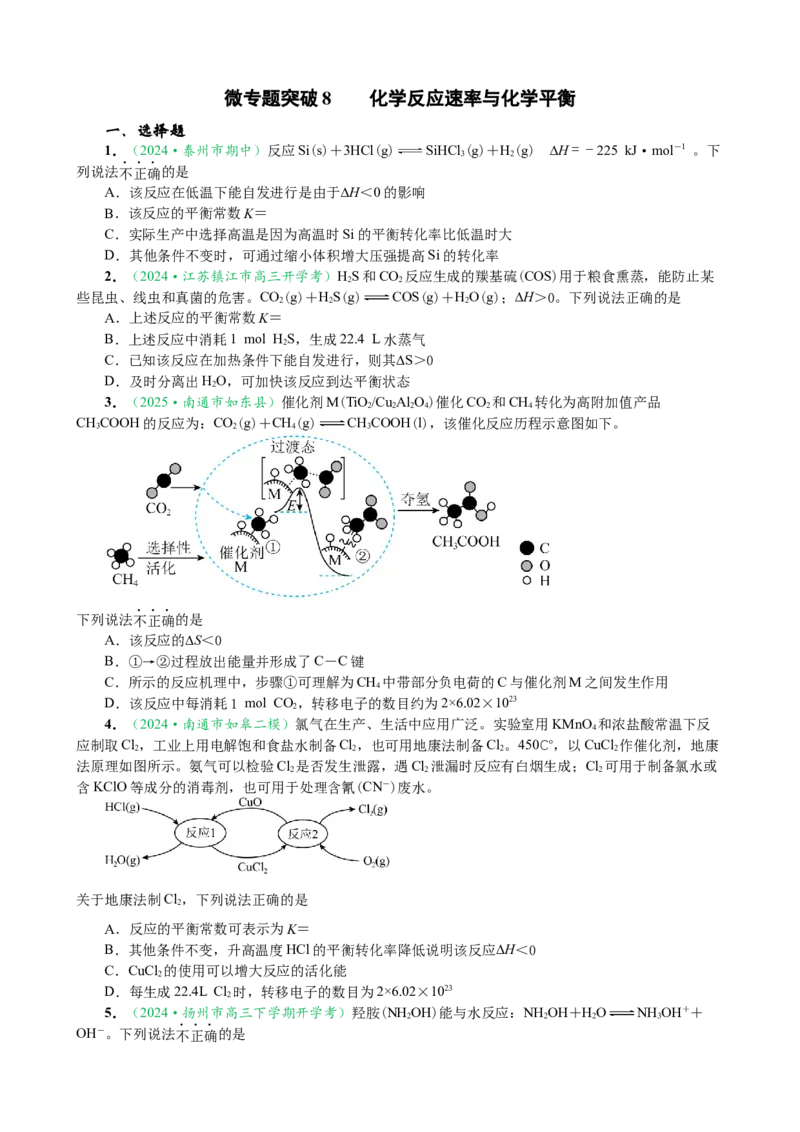
1.(2024·泰州市期中)反应Si(s)+3HCl(g) SiHCl (g)+H(g) ∆H=-225 kJ·mol-1 。下
3 2
列说法不正确的是
A.该反应在低温下能自发进行是由于∆H<0的影响
B.该反应的平衡常数K=
C.实际生产中选择高温是因为高温时Si的平衡转化率比低温时大
D.其他条件不变时,可通过缩小体积增大压强提高Si的转化率
2.(2024·江苏镇江市高三开学考)HS和CO 反应生成的羰基硫(COS)用于粮食熏蒸,能防止某
2 2
些昆虫、线虫和真菌的危害。CO(g)+HS(g) COS(g)+HO(g);∆H>0。下列说法正确的是
2 2 2
A.上述反应的平衡常数K=
B.上述反应中消耗1 mol HS,生成22.4 L水蒸气
2
C.已知该反应在加热条件下能自发进行,则其∆S>0
D.及时分离出HO,可加快该反应到达平衡状态
2
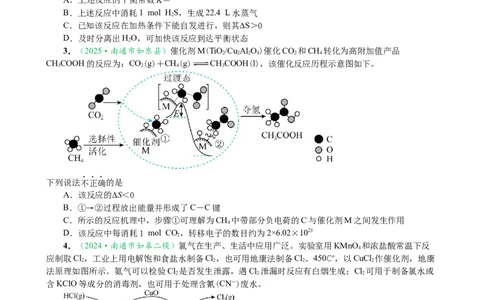
3.(2025·南通市如东县)催化剂M(TiO/Cu Al O)催化CO 和CH 转化为高附加值产品
2 2 2 4 2 4
CHCOOH的反应为:CO(g)+CH(g) CHCOOH(l),该催化反应历程示意图如下。
3 2 4 3
下列说法不正确的是
A.该反应的∆S<0
B.①→②过程放出能量并形成了C-C键
C.所示的反应机理中,步骤①可理解为CH 中带部分负电荷的C与催化剂M之间发生作用
4
D.该反应中每消耗1 mol CO,转移电子的数目约为2×6.02×1023
2
4.(2024·南通市如皋二模)氯气在生产、生活中应用广泛。实验室用KMnO 和浓盐酸常温下反
4
应制取Cl,工业上用电解饱和食盐水制备Cl,也可用地康法制备Cl。450℃,以CuCl 作催化剂,地康
2 2 2 2
法原理如图所示。氨气可以检验Cl 是否发生泄露,遇Cl 泄漏时反应有白烟生成;Cl 可用于制备氯水或
2 2 2
含KClO等成分的消毒剂,也可用于处理含氰(CN-)废水。
关于地康法制Cl,下列说法正确的是
2
A.反应的平衡常数可表示为K=
B.其他条件不变,升高温度HCl的平衡转化率降低说明该反应∆H<0
C.CuCl 的使用可以增大反应的活化能
2
D.每生成22.4L Cl 时,转移电子的数目为2×6.02×1023
2
5.(2024·扬州市高三下学期开学考)羟胺(NH OH)能与水反应:NH OH+HO NH OH++
2 2 2 3
OH-。下列说法不正确的是微专题突破8 化学反应速率与化学平衡
A.反应的平衡常数K=
B.NH OH能与水反应是因为分子中氮原子存在孤电子对
2
C.NH OH溶液能吸收CO 气体
2 2
D.向羟胺溶液中滴加过量稀HSO ,可生成(NH OH)SO
2 4 3 2 4
6.(2024·徐州上学期期中)汽车安装尾气净化装置也可除去NO,反应方程式为2NO (g)+
x 2
4CO(g) N(g)+4CO(g),关于反应2NO (g)+4CO(g) N(g)+4CO(g),下列说法正确的是
2 2 2 2 2
A.该反应的∆S>0
B.选择合适的催化剂,可以使NO 完全转化成N
2 2
C.及时移除N、CO,正反应速率增大,平衡向正反应方向移动
2 2
D.上述反应中每生成0.1 mol N,转移电子的数目约为0.8×6.02×1023
2
7.(2024·苏锡常镇一模)对于反应2SO(g)+O(g) 2SO(g),下列有关说法正确的是
2 2 3
A.该反应的∆S>0
B.该反应平衡常数的表达式为K=
C.反应中每消耗22.4 L O(标准状况),转移电子数约为2×6.02×1023
2
D.温度不变,提高c (O)或增大反应压强,均能提高反应速率和SO 的转化率
起始 2 2
8.(2024·南通市二模)CuO-TiO 可用于低温下催化氧化HCHO:HCHO(g)+
x 2
O(g)==========CO(g)+HO(l)。下列关于CuO-TiO 催化氧化甲醛的反应说法正确的是
2 2 2 x 2
A.该反应∆H<0,∆S<0
B.HCHO、CO、HO均为极性分子
2 2
C.升高温度,υ 增大,υ 减小
逆 正
D.使用CuO-TiO 催化剂降低了该反应的焓变
x 2
9.(2024·南京市二模)制备光电子功能材料ZnS可通过自发反应ZnO(s)+HS(g)=ZnS(s)+
2
HO(g) ∆H>0。下列说法正确的是
2
A.该反应的ΔS<0
B.其他条件相同,缩小容器体积,达到新平衡时减小
C.其他条件相同,升高体系温度,HS的平衡转化率增大
2
D.其他条件相同,使用催化剂加快正反应速率,减慢逆反应速率
10.(2025·南通市海安市开学考)工业上由粗硅制备高纯晶体硅流程中的一步反应为SiHCl(g)+
3
H(g) Si(s)+3HCl(g)。下列说法正确的是
2
A.该反应∆S<0
B.该反应的平衡常数K=
C.用E表示键能,该反应∆H=3E(Si-Cl)+E(Si-H)+E(H-H)-3E(H-Cl)-2E(Si-Si)
D.该过程需要在无水条件下进行的原因:SiHCl 与水反应生成HSiO 和HCl两种物质
3 2 3
11.(2024·苏锡常镇一模)采用热分解法脱除沼气中的HS过程中涉及的主要反应为
2
反应Ⅰ:2HS(g)=2H(g)+S(g) ∆H=169.8 kJ·mol-1
2 2 2 1
反应Ⅱ:CH(g)+S(g)=CS(g)+2H(g) ∆H=63.7 kJ·mol-1
4 2 2 2 1
保持100 kPa不变,将HS与CH 按2∶1体积比投料,并用N 稀释,在不同温度下反应达到平衡时,
2 4 2
所得H、S 与CS 的体积分数如图所示。下列说法正确的是
2 2 2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
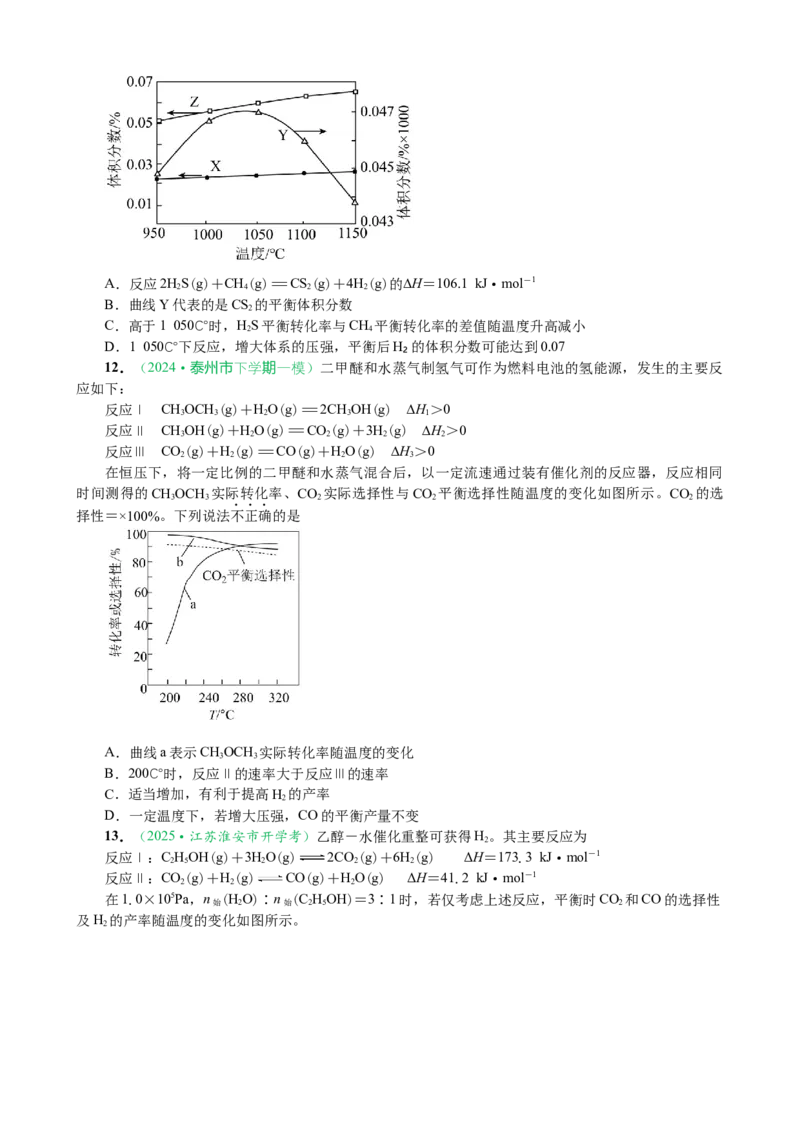
找找A.反应2HS(g)+CH(g)=CS(g)+4H(g)的∆H=106.1 kJ·mol-1
2 4 2 2
B.曲线Y代表的是CS 的平衡体积分数
2
C.高于1 050℃时,HS平衡转化率与CH 平衡转化率的差值随温度升高减小
2 4
D.1 050℃下反应,增大体系的压强,平衡后H₂的体积分数可能达到0.07
12.(2024·泰州市下学期一模)二甲醚和水蒸气制氢气可作为燃料电池的氢能源,发生的主要反
应如下:
反应Ⅰ CHOCH (g)+HO(g)=2CHOH(g) ∆H>0
3 3 2 3 1
反应Ⅱ CHOH(g)+HO(g)=CO(g)+3H(g) ∆H>0
3 2 2 2 2
反应Ⅲ CO(g)+H(g)=CO(g)+HO(g) ∆H>0
2 2 2 3
在恒压下,将一定比例的二甲醚和水蒸气混合后,以一定流速通过装有催化剂的反应器,反应相同
时间测得的CHOCH 实际转化率、CO 实际选择性与CO 平衡选择性随温度的变化如图所示。CO 的选
3 3 2 2 2
择性=×100%。下列说法不正确的是
A.曲线a表示CHOCH 实际转化率随温度的变化
3 3
B.200℃时,反应Ⅱ的速率大于反应Ⅲ的速率
C.适当增加,有利于提高H 的产率
2
D.一定温度下,若增大压强,CO的平衡产量不变
13.(2025·江苏淮安市开学考)乙醇-水催化重整可获得H。其主要反应为
2
反应Ⅰ:C HOH(g)+3HO(g) 2CO(g)+6H(g) ΔH=173.3 kJ·mol-1
2 5 2 2 2
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH=41.2 kJ·mol-1
2 2 2
在1.0×105Pa,n (HO)∶n (C HOH)=3∶1时,若仅考虑上述反应,平衡时CO 和CO的选择性
始 2 始 2 5 2
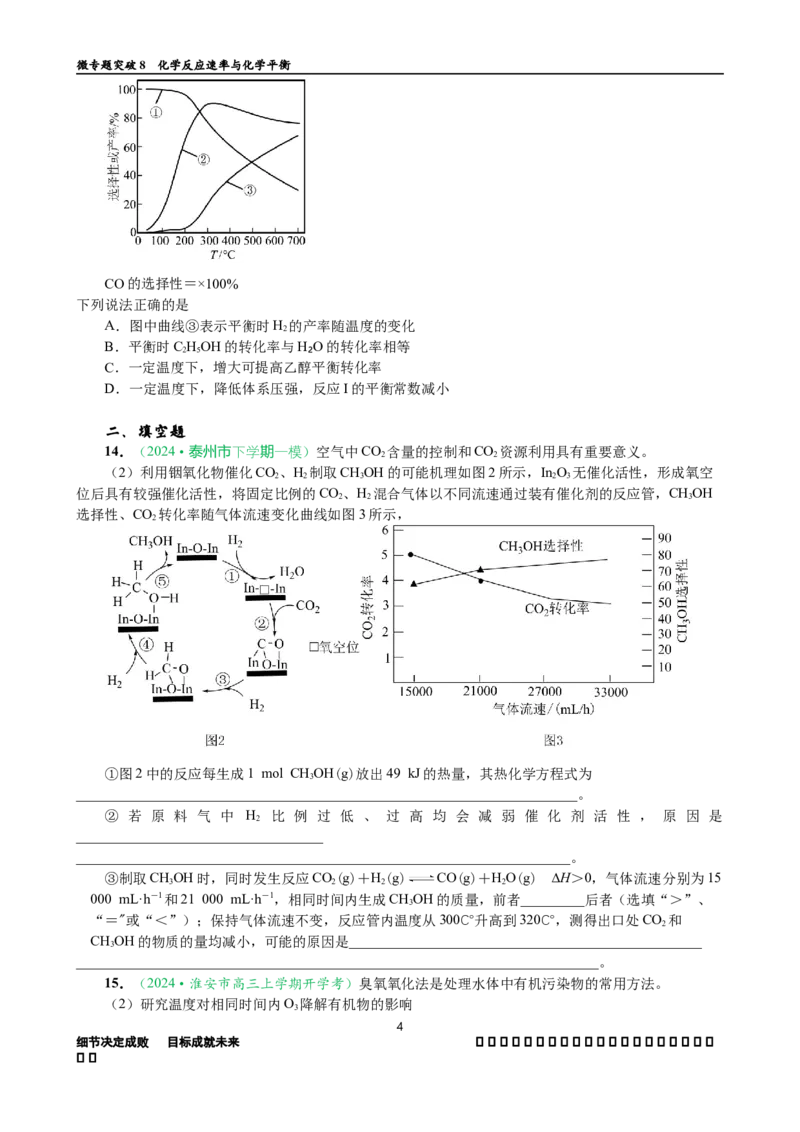
及H 的产率随温度的变化如图所示。
2微专题突破8 化学反应速率与化学平衡
CO的选择性=×100%
下列说法正确的是
A.图中曲线③表示平衡时H 的产率随温度的变化
2
B.平衡时C HOH的转化率与H₂O的转化率相等
2 5
C.一定温度下,增大可提高乙醇平衡转化率
D.一定温度下,降低体系压强,反应I的平衡常数减小
二、填空题
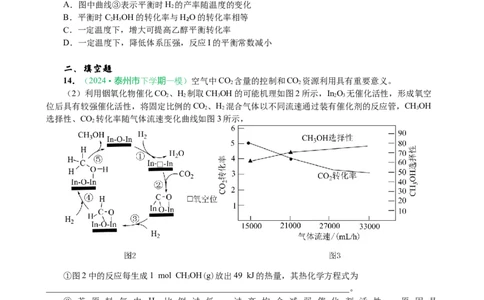
14.(2024·泰州市下学期一模)空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
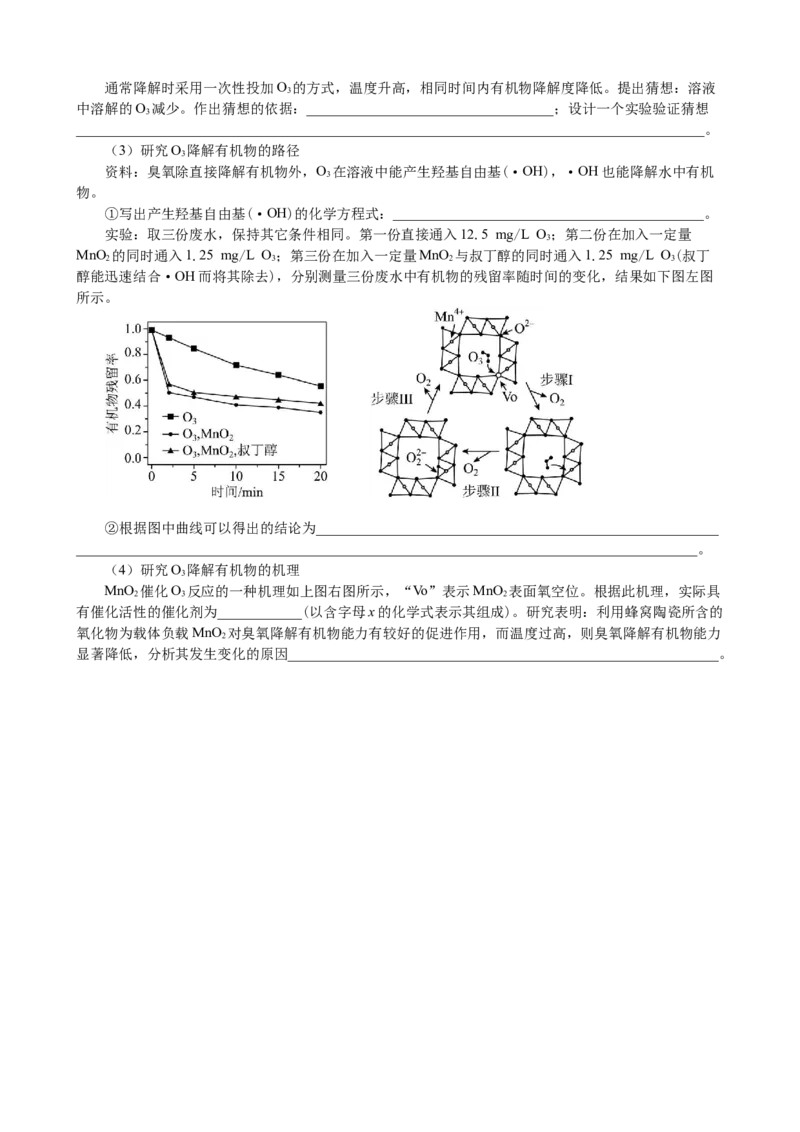
(2)利用铟氧化物催化CO、H 制取CHOH的可能机理如图2所示,InO 无催化活性,形成氧空
2 2 3 2 3
位后具有较强催化活性,将固定比例的CO、H 混合气体以不同流速通过装有催化剂的反应管,CHOH
2 2 3
选择性、CO 转化率随气体流速变化曲线如图3所示,
2
①图2中的反应每生成1 mol CHOH(g)放出49 kJ的热量,其热化学方程式为
3
_______________________________________________________________________。
② 若 原 料 气 中 H 比 例 过 低 、 过 高 均 会 减 弱 催 化 剂 活 性 , 原 因 是
2
___________________________________
______________________________________________________________________。
③制取CHOH时,同时发生反应CO(g)+H(g) CO(g)+HO(g) ∆H>0,气体流速分别为15
3 2 2 2
000 mL·h-1和21 000 mL·h-1,相同时间内生成CHOH的质量,前者_________后者(选填“>”、
3
“="或“<”);保持气体流速不变,反应管内温度从300℃升高到320℃,测得出口处CO 和
2
CHOH的物质的量均减小,可能的原因是__________________________________________________
3
__________________________________________________________________________。
15.(2024·淮安市高三上学期开学考)臭氧氧化法是处理水体中有机污染物的常用方法。
(2)研究温度对相同时间内O 降解有机物的影响
3
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找通常降解时采用一次性投加O 的方式,温度升高,相同时间内有机物降解度降低。提出猜想:溶液
3
中溶解的O 减少。作出猜想的依据:___________________________________;设计一个实验验证猜想
3
_________________________________________________________________________________________。
(3)研究O 降解有机物的路径
3
资料:臭氧除直接降解有机物外,O 在溶液中能产生羟基自由基(·OH),·OH也能降解水中有机
3
物。
①写出产生羟基自由基(·OH)的化学方程式:____________________________________________。
实验:取三份废水,保持其它条件相同。第一份直接通入12.5 mg/L O;第二份在加入一定量
3
MnO 的同时通入1.25 mg/L O;第三份在加入一定量MnO 与叔丁醇的同时通入1.25 mg/L O(叔丁
2 3 2 3
醇能迅速结合·OH而将其除去),分别测量三份废水中有机物的残留率随时间的变化,结果如下图左图
所示。
②根据图中曲线可以得出的结论为_________________________________________________________
________________________________________________________________________________________。
(4)研究O 降解有机物的机理
3
MnO 催化O 反应的一种机理如上图右图所示,“Vo”表示MnO 表面氧空位。根据此机理,实际具
2 3 2
有催化活性的催化剂为____________(以含字母x的化学式表示其组成)。研究表明:利用蜂窝陶瓷所含的
氧化物为载体负载MnO 对臭氧降解有机物能力有较好的促进作用,而温度过高,则臭氧降解有机物能力
2
显著降低,分析其发生变化的原因_____________________________________________________________。