文档内容
微专题突破13 化学基础实验考点透视
一、选择题
1.(2025·江苏苏州市开学考)实验室模拟侯氏制碱法制备NaCO,下列装置与原理均正确的是
2 3
A.制取CO B.制取NH C.制取NaHCO D.制取NaCO
2 3 3 2 3
A.A B.B C.C D.D
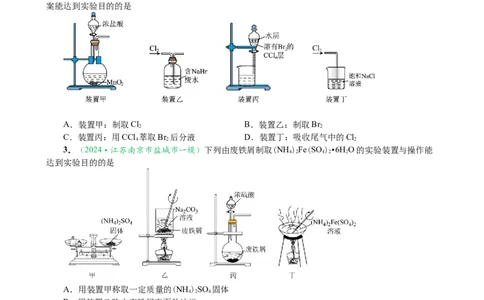
2.(2024·南通市如皋市高三上学期开学考)下列制取Cl 并从含NaBr的废水中提取Br 的实验方
2 2
案能达到实验目的的是
A.装置甲:制取Cl B.装置乙:制取Br
2 2
C.装置丙:用CCl 萃取Br 后分液 D.装置丁:吸收尾气中的Cl
4 2 2
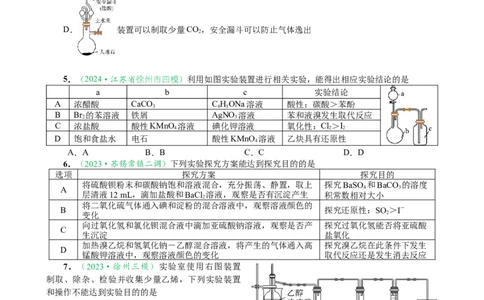
3.(2024·江苏南京市盐城市一模)下列由废铁屑制取(NH )Fe(SO )•6HO的实验装置与操作能
4 2 4 2 2
达到实验目的的是
A.用装置甲称取一定质量的(NH )SO 固体
4 2 4
B.用装置乙除去废铁屑表面的油污
C.用装置丙将废铁屑充分溶解
D.用装置丁蒸干溶液得到(NH )Fe(SO )•6HO晶体
4 2 4 2 2
4.(2024·江苏省南通市、盐城市二模)下列实验能实现的是
A. 装置左侧用于检验氯化铵受热分解出的氨气微专题突破13 化学基础实验考点透视
B. 装置用于分离碘单质和高锰酸钾固体混合物
C. 装置中若a处有红色物质生成,b处变蓝,证明X一定是H
2
D. 装置可以制取少量CO,安全漏斗可以防止气体逸出
2
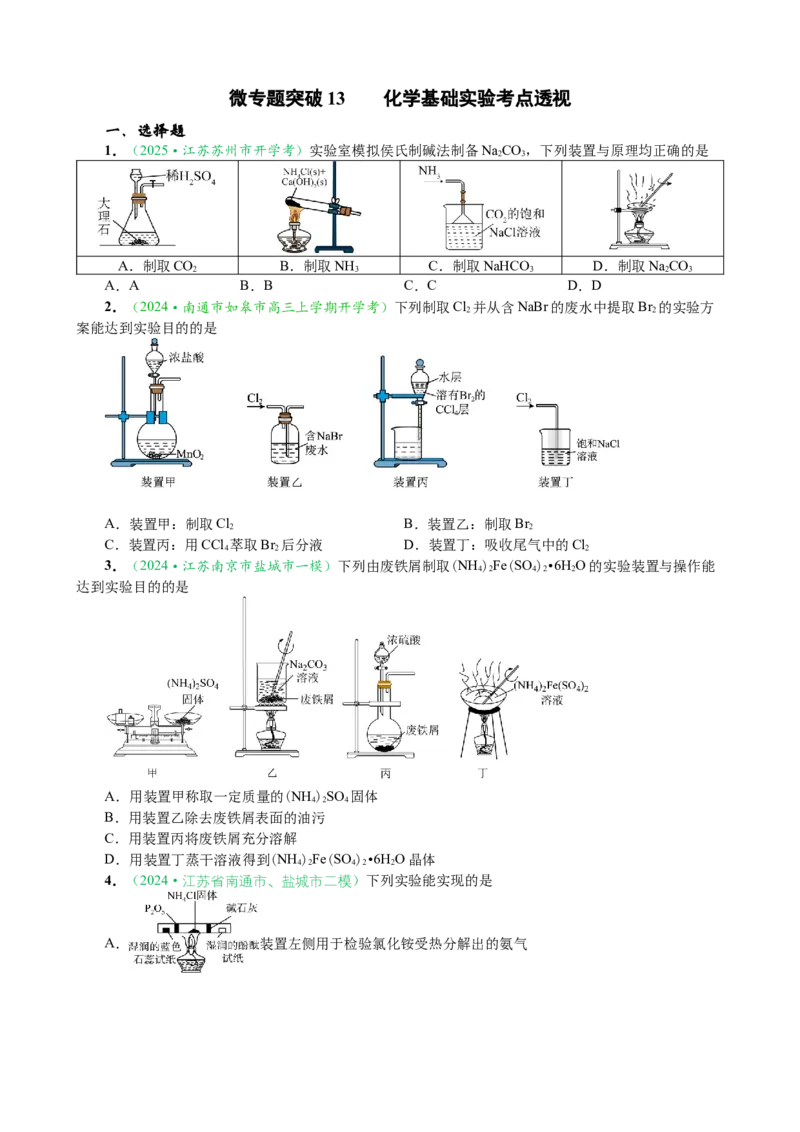
5.(2024·江苏省徐州市四模)利用如图实验装置进行相关实验,能得出相应实验结论的是
a b c 实验结论
A 浓醋酸 CaCO C HONa溶液 酸性:碳酸>苯酚
3 6 5
B Br 的苯溶液 铁屑 AgNO 溶液 苯和液溴发生取代反应
2 3
C 浓盐酸 酸性KMnO 溶液 碘化钾溶液 氧化性:Cl>I
4 2 2
D 饱和食盐水 电石 酸性KMnO 溶液 乙炔具有还原性
4
A.A B.B C.C D.D
6.(2023·苏锡常镇二调)下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
将硫酸钡粉末和碳酸钠饱和溶液混合,充分振荡、静置,取上 探究BaSO 和BaCO 的溶度
A 4 3
层清液12 mL,滴加盐酸和BaCl 溶液,观察是否有沉淀产生 积常数相对大小
2
将二氧化硫气体通入碘和淀粉的混合溶液中,观察溶液颜色的
B 探究还原性:SO >I-
变化 2
向过氧化氢和氯化钡混合液中滴加亚硫酸钠溶液,观察是否产 探究过氧化氢能否将亚硫酸
C
生沉淀 盐氧化
加热溴乙烷和氢氧化钠-乙醇混合溶液,将产生的气体通入高 探究溴乙烷在此条件下发生
D
锰酸钾溶液中,观察溶液颜色的变化 取代反应还是发生消去反应
7.(2023·徐州三模)实验室使用右图装置
制取、除杂、检验并收集少量乙烯,下列实验装置
和操作不能达到实验目的的是
A.用装置甲制取乙烯
B.用装置乙除去乙烯中的SO 气体
2
C.用装置丙检验乙烯
D.用装置丁收集乙烯
8.(2023·南京、盐城调研)下列探究方案能达到探究目的的是
选项 探究方案 探究目的
室温下,测定浓度均为0.1 mol·L-1
A 比较室温下CHCOOH和NH ·HO的电离能力
CHCOONa、NH Cl溶液的pH 3 3 2
3 4
将浓硫酸和灼热的木炭反应产生的气体依次
B 通过品红溶液、饱和NaHCO 溶液、澄清石 浓硫酸和木炭反应产生SO 和CO 气体
3 2 2
灰水,观察现象
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找将少量Fe O 溶于过量热浓盐酸中,再滴加
C 3 4 Fe O 中含Fe2+
几滴KMnO 溶液,观察溶液颜色变化 3 4
4
向含有少量乙酸的乙酸乙酯中加入过量
D 提纯含有少量乙酸的乙酸乙酯
NaOH溶液,振荡后静置分液
9.(2023·江苏四校联考)利用下列装置进行实验,能达到相应实验目的的是
A.装置甲可用于由FeSO 溶液制备FeSO ·7HO
4 4 2
B.装置乙可用于实验室制备少量Fe(OH)
2
C.装置丙中滴加KSCN溶液,溶液不变红,可证明锌比铁活泼
D.装置丁的肥皂液中产生无色气泡,可证明铁粉与水蒸气反应生成O
2
10.(2024·江苏省南通市、盐城市二模)根据下列实验操作和现象所得出的结论正确的是
选项 实验操作和现象 结论
A 向苯酚浊液中滴加NaCO 溶液,浊液变清 苯酚的酸性强于HCO 的酸性
2 3 2 3
将溴乙烷和氢氧化钠的乙醇溶液共热后产生的气体通入溴
B 溴乙烷发生消去反应
的四氯化碳溶液,溶液褪色
C SO 通入KMnO 溶液,溶液褪色 SO 有漂白性
2 4 2
向NaCl、NaI的混合稀溶液中滴入少量稀AgNO 溶液,有
D 3 K (AgCl)>K (AgI)
黄色沉淀生成 sp sp
A.A B.B C.C D.D
11.(2024·苏锡常镇二模)常温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 实验操作和现象 实验结论
将铁锈溶于浓盐酸,再滴入几滴酸性KMnO 溶液,振
A 4 铁锈中不含二价铁
荡,溶液中未出现红色
向FeSO 溶液中滴加几滴新制氯水,振荡,再滴加KSCN
4
B FeSO 溶液已经变质
溶液,溶液变 血为红色 4
向含有KSCN的Fe (SO ) 溶液中加入少量KSO 固体,
C 2 4 3 2 4 Fe (SO ) 与KSCN的反应不可逆
振荡,溶液颜色未变化 2 4 3
分别向等浓度的FeSO 和CuSO 溶液中通入HS气体至饱
D 4 4 2 K (FeS)>K (CuS)
和,前者无明显现象,后者出现黑色沉淀 sp sp
A.A B.B C.C D.D
12.(2024·南通市海安市高三上学期开学考)下列实验能达到目的的是
选项 实验目的 实验方法或操作
A 测定中和反应的反应热 酸碱中和滴定的同时,用温度传感器采集锥形瓶内溶液的温度
探究浓度对化学反应速率 室温下,量取等体积不同浓度的NaClO溶液,分别加入等体积
B
的影响 等浓度的KI溶液,观察溶液颜色变化
向2 mL FeCl 溶液中滴加2~3滴酸性KMnO 溶液,观察溶液
C Fe2+是否具有还原性 2 4
颜色变化
D 检验淀粉是否发生了水解 向淀粉水解液中加入碘水
A.A B.B C.C D.D
13.(2024·泰州市下学期一模)室温下,下列实验探究方案能够边到探究目的的是
选项 探究方案 探究目的
将1-溴丁烷与NaOH的乙醇溶液混合后加热,生成的气体 1-溴丁烷能否发生消去反应生成
A
通入Br 的CCl 溶液中,观察现象 烯烃
2 4
B 将SO 气体通入紫色石蕊溶液中,观察溶液颜色变化 SO 是否具有漂白性
2 2
比较 NaCO 与 NaHCO 在水中
C 向饱和NaCO 溶液中通入足量CO 气体,观察现象 2 3 3
2 3 2 溶解度的大小
D 向Fe(NO 3 ) 3 溶液中滴加淀粉,再通入 气体,观察现象 比较Fe3+与I 2 氧化性的强弱微专题突破13 化学基础实验考点透视
A.A B.B C.C D.D
14.(2024·南通市如皋二模)室温下,探究0.1 mol·L-1 KClO溶液的性质,下列实验方案能达到
探究目的的是
选项 探究目的 实验方案
用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,透过蓝色钴玻
A 溶液中是否含KClO
璃观察火焰的颜色
B ClO-有氧化性 向淀粉KI试纸上滴加几滴KClO溶液,观察试纸颜色变化
C 比较F-和ClO-的水解能力大小 测定KClO溶液、KF溶液的pH,比较pH的大小
向稀盐酸和浓盐酸中分别加入等量的KClO溶液,观察溶液
D H+浓度对ClO-氧化性的影响
颜色变化
A.A B.B C.C D.D
15.(2024·浙江省嘉兴9月)探究钠及其化合物的性质,下列方案设计、现象和结论都正确的是
实验方案 现象 结论
分别测定NaHCO 和NaCO 溶液 两者都大于7,且
A 3 2 3 CO2-的水解能力强于HCO -
的pH NaCO 溶液的pH大 3 3
2 3
B 对某未知溶液进行焰色试验 火焰呈黄色 该溶液中含有钠盐
用形状和质量相同的钠,分别和等 钠与乙醇反应比与苯 乙醇中羟基的活性强于苯酚中羟
C
物质的量的苯酚和乙醇反应 酚反应剧烈 基的活性
向饱和NaHCO 溶液中滴加一定量 溶液变浑浊同时产生 发生的反应:Ba2++2HCO -=
D 3 3
的浓BaCl 溶液 气泡 BaCO ↓+CO↑+HO
2 3 2 2
A.A B.B C.C D.D
二、填空题
16.(2024·南外、金陵中学、海安中学三校最后一卷节选)氧化亚铜(Cu O)主要用于制造杀虫剂、
2
分析试剂和红色玻璃等。Cu O在酸性溶液中歧化为二价
2
铜和铜单质。以黄铜矿(主要成分为 CuFeS ,含有杂质
2
SiO)为原料制取Cu O的一种工艺流程如图所示:
2 2
(1)写出“浸泡”时CuFeS 发生反应的离子方程式
2
_______________________________________。
(2)判断“操作1”反应已完成的实验操作及现象
为______________________________________________
__________________________。
(3)“热还原”时,将新制NaSO 溶液和CuSO 溶液按一定量混合,加热至90 ℃并不断搅拌反应
2 3 4
得到Cu O粉末。制备装置如图所示:
2
反应时A装置原料反应配比为n(NaSO )∶n(CuSO )=3∶2,B装置的作
2 3 4
用是吸收反应产生的酸性气体,防止污染环境,A装置中反应的化学方程式为:
__________________________________________________________。
(4)实际反应中不断滴加NaOH溶液的原因:_____________________
_________________________________________________________________。
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找