文档内容
专项训练 微型工业流程题
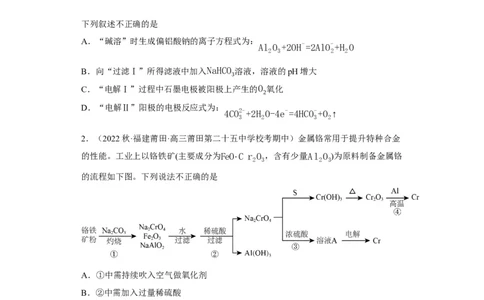
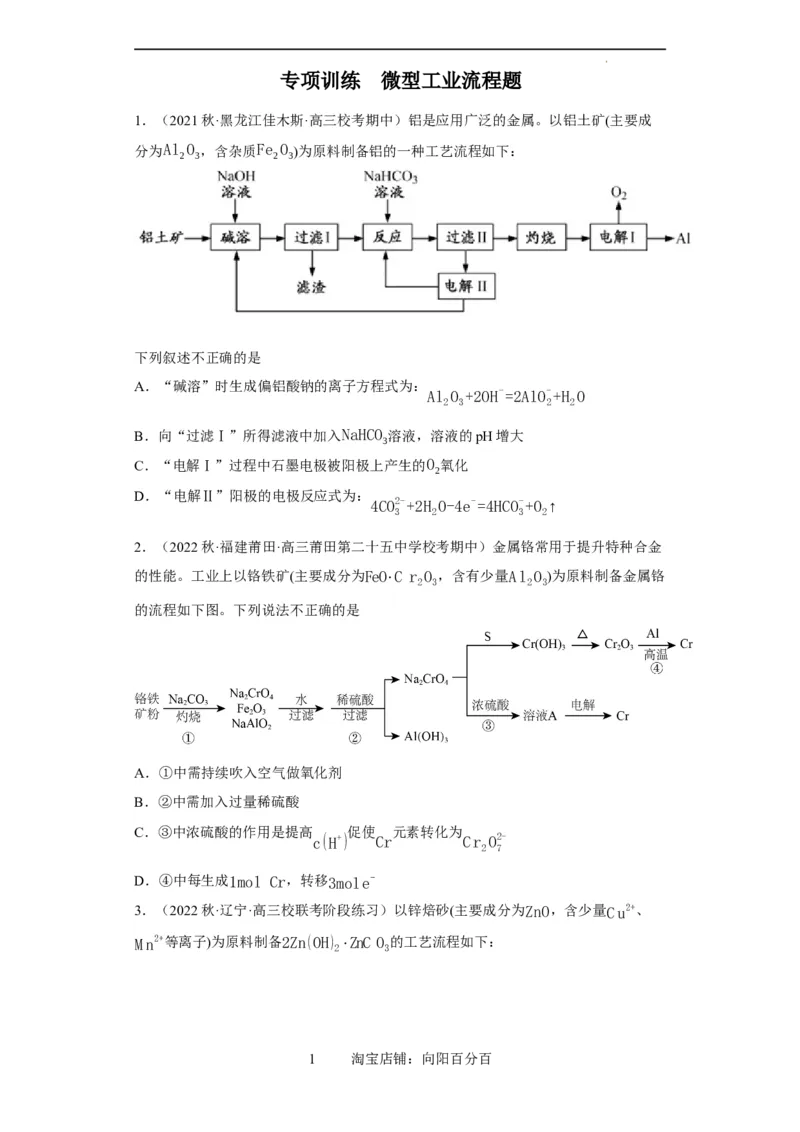
1.(2021秋·黑龙江佳木斯·高三校考期中)铝是应用广泛的金属。以铝土矿(主要成
分为Al O ,含杂质Fe O )为原料制备铝的一种工艺流程如下:
2 3 2 3
下列叙述不正确的是
A.“碱溶”时生成偏铝酸钠的离子方程式为:
Al O +2OH-=2AlO-+H O
2 3 2 2
B.向“过滤Ⅰ”所得滤液中加入NaHCO 溶液,溶液的pH增大
3
C.“电解Ⅰ”过程中石墨电极被阳极上产生的O 氧化
2
D.“电解Ⅱ”阳极的电极反应式为:
4CO2-+2H O-4e-=4HCO-+O ↑
3 2 3 2
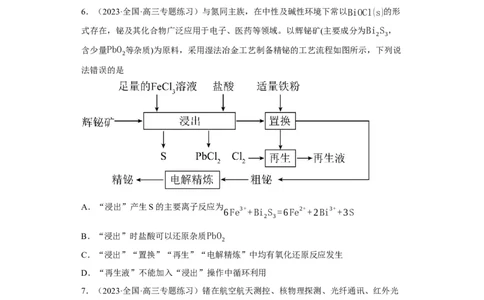
2.(2022秋·福建莆田·高三莆田第二十五中学校考期中)金属铬常用于提升特种合金
的性能。工业上以铬铁矿(主要成分为FeO⋅C r O ,含有少量Al O )为原料制备金属铬
2 3 2 3
的流程如下图。下列说法不正确的是
A.①中需持续吹入空气做氧化剂
B.②中需加入过量稀硫酸
C.③中浓硫酸的作用是提高 促使 元素转化为
c(H+) Cr Cr O2-
2 7
D.④中每生成1mol Cr,转移3mole-
3.(2022秋·辽宁·高三校联考阶段练习)以锌焙砂(主要成分为ZnO,含少量Cu2+、
Mn2+等离子)为原料制备2Zn(OH) ⋅ZnC O 的工艺流程如下:
2 3
1 淘宝店铺:向阳百分百
学科网(北京)股份有限公司以下说法错误的是
A.“浸取”过程为加快反应速率应适当加热,但温度不宜过高
B.“除杂”步骤也可选择Na S或K S为沉淀剂,沉淀杂质离子
2 2
C.“沉锌”过程发生反应后释放的气体A为CO
2
D.“过滤3”所得滤液可循环使用,其主要成分的化学式是(NH ) SO
4 2 4
4.(2023秋·湖南·高三校联考阶段练习)大力推广锂电池新能源汽车对实现“碳达
峰”和“碳中和”具有重要意义。Li Ti O 与LiFePO 都是锂离子电池的电极材料,
4 5 12 4
可利用钛铁矿(主要成分为FeTiO ,还有少量MgO、SiO 等杂质)来制备,工艺流程如
3 2
下:
已知:“酸浸”后,钛主要以 形式存在,
TiOCl2−
4
。下列说法不正确的是。
FeTiO +4H++4Cl−=Fe2++TiOCl2−+2H O
3 4 2
A.在制备TiO ⋅xH O时需要加入水,同时加热,促使水解反应趋于完全
2 2
B.在制备Li Ti O 的过程中会生成Li Ti O (Ti为+4价),则Li Ti O 中过氧键的
4 5 12 2 5 15 2 5 15
数目为8
C.滤液②中的阳离子有Fe2+、Mg2+、H+
D.高温煅烧反应中氧化剂与还原剂物质的量之比为2∶1
5.(2023秋·新疆·高三校联考期末)碳酸锂是制备高纯锂化合物和锂合金的主要原料,
在玻璃和陶瓷制造、医药、有色金属冶炼、锂电池电极材料等领域具有广阔的应用前
景。某化学小组在实验室用含锂废渣(主要含LiO,还含有少量其他能溶于盐酸的金属
2
氧化物及少量碳单质)制备碳酸锂的流程如图所示:
试卷第2页,共13页下列说法错误的是
A.“浸渣”的主要成分是碳单质
B.“萃取”和“反萃取”均应在烧杯中进行
C.“蒸发浓缩”的目的之一是除去过量的HCl
D.“沉锂”后所得母液中含有NaCl
6.(2023·全国·高三专题练习)与氮同主族,在中性及碱性环境下常以BiOCl(s)的形
式存在,铋及其化合物广泛应用于电子、医药等领域。以辉铋矿(主要成分为Bi S ,
2 3
含少量PbO 等杂质)为原料,采用湿法冶金工艺制备精铋的工艺流程如图所示,下列说
2
法错误的是
A.“浸出”产生S的主要离子反应为
6Fe3++Bi S =6Fe2++2Bi3++3S
2 3
B.“浸出”时盐酸可以还原杂质PbO
2
C.“浸出”“置换”“再生”“电解精炼”中均有氧化还原反应发生
D.“再生液”不能加入“浸出”操作中循环利用
7.(2023·全国·高三专题练习)锗在航空航天测控、核物理探测、光纤通讯、红外光
学、化学催化剂、生物医学等领域有广泛而重要的应用。一种从二氧化锗粗品(主要含
GeO 、As O )中制备锗的工艺流程如下:
2 2 3
已知:i.GeO 与Al O 的性质相似;
2 2 3
ii.GeCl 易水解,GeCl 的沸点为86.6℃;
4 4
3 淘宝店铺:向阳百分百
学科网(北京)股份有限公司iii.As O +2NaOH= 2NaAsO +H O,NaAsO 与盐酸反应生成有毒的AsCl 。
2 3 2 2 2 3
下列说法正确的是
A.“蒸馏”时改用1mol⋅L−1盐酸可节省原料,同时不影响产率
B.工业上对高纯GeO 和SiO 的混合物进行电解制备硅锗合金,则产品在阳极区生成
2 2
C.“水解”反应的化学方程式为GeCl +(n+2)H O=GeO ⋅nH O↓+4HCl
4 2 2 2
D.若“氧化”的目的是将NaAsO 氧化为Na AsO ,则该反应中氧化剂与还原剂的物
2 3 4
质的量之比为3∶1
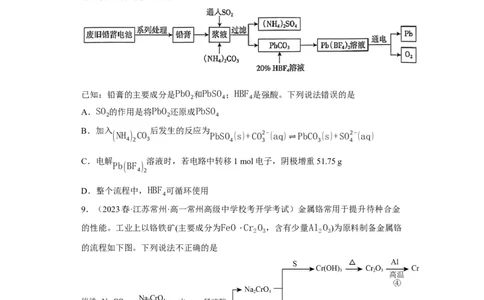
8.(2023春·山东临沂·高二统考阶段练习)废旧铅蓄电池会导致铅污染,利用RSR工
艺回收铅的流程如图所示。
已知:铅膏的主要成分是PbO 和PbSO ;HBF 是强酸。下列说法错误的是
2 4 4
A.SO 的作用是将PbO 还原成PbSO
2 2 4
B.加入 后发生的反应为
(NH
4
)
2
CO
3
PbSO
4
(s)+CO
3
2− (aq)⇌ PbCO
3
(s)+SO2
4
− (aq)
C.电解 溶液时,若电路中转移1 mol电子,阴极增重51.75 g
Pb(BF )
4 2
D.整个流程中,HBF 可循环使用
4
9.(2023春·江苏常州·高一常州高级中学校考开学考试)金属铬常用于提升待种合金
的性能。工业上以铬铁矿(主要成分为FeO⋅Cr O ,含有少量Al O )为原料制备金属铬
2 3 2 3
的流程如下图。下列说法不正确的是
A.①中需持续吹入空气做氧化剂
高温
B.①中Al
2
O
3
参与的反应为Al
2
O
3
+Na
2
CO
3
¿2NaAlO
2
+CO
2
↑
¿
C.②中需加入过量稀硫酸
D.④中每生成1molCr,转移3mole−
10.(2023·全国·高三统考专题练习)“太空金属”钛广泛应用于新型功能材料等方面,
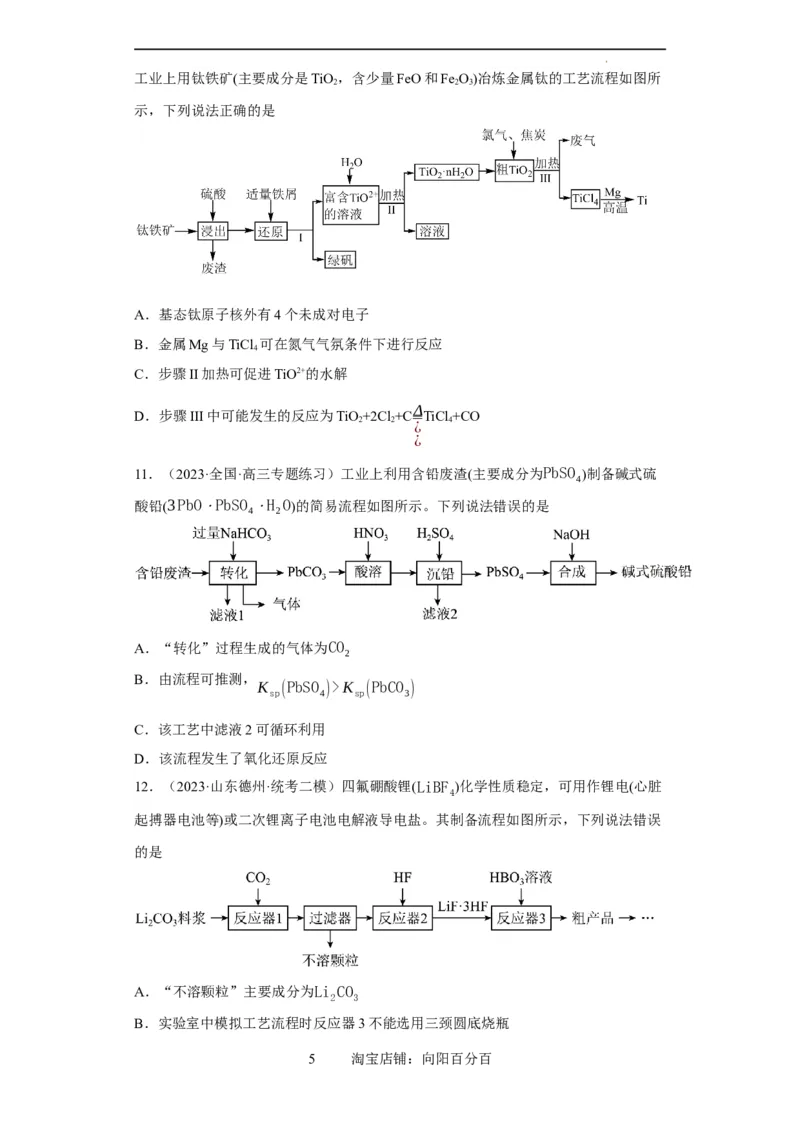
试卷第4页,共13页工业上用钛铁矿(主要成分是TiO,含少量FeO和Fe O)冶炼金属钛的工艺流程如图所
2 2 3
示,下列说法正确的是
A.基态钛原子核外有4个未成对电子
B.金属Mg与TiCl 可在氮气气氛条件下进行反应
4
C.步骤II加热可促进TiO2+的水解
Δ
D.步骤III中可能发生的反应为TiO+2Cl+C TiCl +CO
2 2 4
¿
¿
11.(2023·全国·高三专题练习)工业上利用含铅废渣(主要成分为PbSO )制备碱式硫
4
酸铅(3PbO⋅PbSO ⋅H O)的简易流程如图所示。下列说法错误的是
4 2
A.“转化”过程生成的气体为CO
2
B.由流程可推测,
K (PbSO )>K (PbCO )
sp 4 sp 3
C.该工艺中滤液2可循环利用
D.该流程发生了氧化还原反应
12.(2023·山东德州·统考二模)四氟硼酸锂(LiBF )化学性质稳定,可用作锂电(心脏
4
起搏器电池等)或二次锂离子电池电解液导电盐。其制备流程如图所示,下列说法错误
的是
A.“不溶颗粒”主要成分为Li CO
2 3
B.实验室中模拟工艺流程时反应器3不能选用三颈圆底烧瓶
5 淘宝店铺:向阳百分百
学科网(北京)股份有限公司C.反应器2中反应为LiHCO +4HF=LiF⋅3HF+H O+CO
3 2 2
D.粗产品经过负压下浓缩、冷却结晶即可得到纯净的四氟硼酸锂
13.(2023·全国·高三统考专题练习)钛酸钡(BaTiO )是电子陶瓷基础母体原料,超细
3
微BaTiO 粉体的制备方法如下。
3
❑
已知:TiCl +(x+2)H O
⇌
TiO ⋅xH O+4HCl
4 2 2 2
❑
下列说法不正确的是
A.向TiCl 中先加入H C O ,可防止其水解生成TiO ⋅xH O
4 2 2 4 2 2
B.得到溶液1的反应:
TiCl +2H C O +6NH ⋅H O=(NH ) TiO(C O ) +4NH Cl+5H O
4 2 2 4 3 2 4 2 2 4 2 4 2
C.加入过量氨水,有利于提高BaTiO(C O ) ⋅4H O的产率
2 4 2 2
D.“煅烧”得到的气体A是CO、CO 和H O的混合物
2 2
14.(2020秋·宁夏石嘴山·高三石嘴山市第三中学校考阶段练习)以高硫铝土矿(主
要成分为Al O、Fe O,还含有少量FeS)为原料,生产氧化铝并获得Fe O 的部分工
2 3 2 3 2 3 4
艺流程如图,下列叙述错误的是( )
A.烧渣分离可以选择用磁铁将烧渣中的Fe O 分离出来
3 4
B.隔绝空气焙烧时理论上反应消耗的n(FeS )∶n(Fe O)=1∶5
2 2 3
C.向滤液中通入过量CO、过滤、洗涤、灼烧沉淀可制得Al O
2 2 3
D.加入CaO可以减少SO 的排放同时生成建筑材料CaSO
2 4
15.(2021秋·甘肃嘉峪关·高三嘉峪关市第一中学校考阶段练习)工业上用铝土矿
(主要成分为Al O,还含有Fe O、FeO、SiO)制备铝的某种化合物的工艺流程如下,
2 3 2 3 2
下列有关说法不正确的是( )
试卷第6页,共13页A.向滤液A中加入KSCN溶液,溶液一定会变红
B. 的离子反应方程式为
② SiO +2OH−=SiO2−+H O
2 3 2
C.③漂白液的目的是氧化除铁,该过程中涉及的氧化还原反应为
2Fe2++ClO−+5H O=2Fe(OH)↓+Cl−+4H+
2 3
D.③中漂白液要适量,若过量则可能产生有毒的气体氯气
16.(2022·内蒙古呼和浩特·统考模拟预测)铝氢化钠(NaAlH )是有机合成中的一种重
4
要还原剂。以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂质)为原料制备铝氢化钠
2 3 2 2 3
的一种工艺流程如图:
下列说法中错误的是
A.为了提高“碱溶”效率,在“碱溶”前对铝土矿进行粉碎
B.“反应I”的部分化学原理与泡沫灭火器的原理相同
C.“滤渣1”的主要成分为氧化铁
D.“反应III”的化学方程式为4NaH+AlCl =NaAlH+3NaCl
3 4
17.(2022秋·河北保定·高三校考期中)金属铬常用于制备特种合金。工业上以铬铁
矿(主要成分为FeO⋅Cr O ,含有少量Al O )为原料,电解Na Cr O 制备金属铬的流
2 3 2 3 2 2 7
程如图。下列说法正确的是
A.过程①会生成CO 气体
2
B.过程②需加入过量稀硫酸
C.物质A的化学式为Fe(OH)
3
7 淘宝店铺:向阳百分百
学科网(北京)股份有限公司D.过程③生成金属 的电极反应式为
Cr Cr O2−+7H O+12e−=2Cr+14OH−
2 7 2
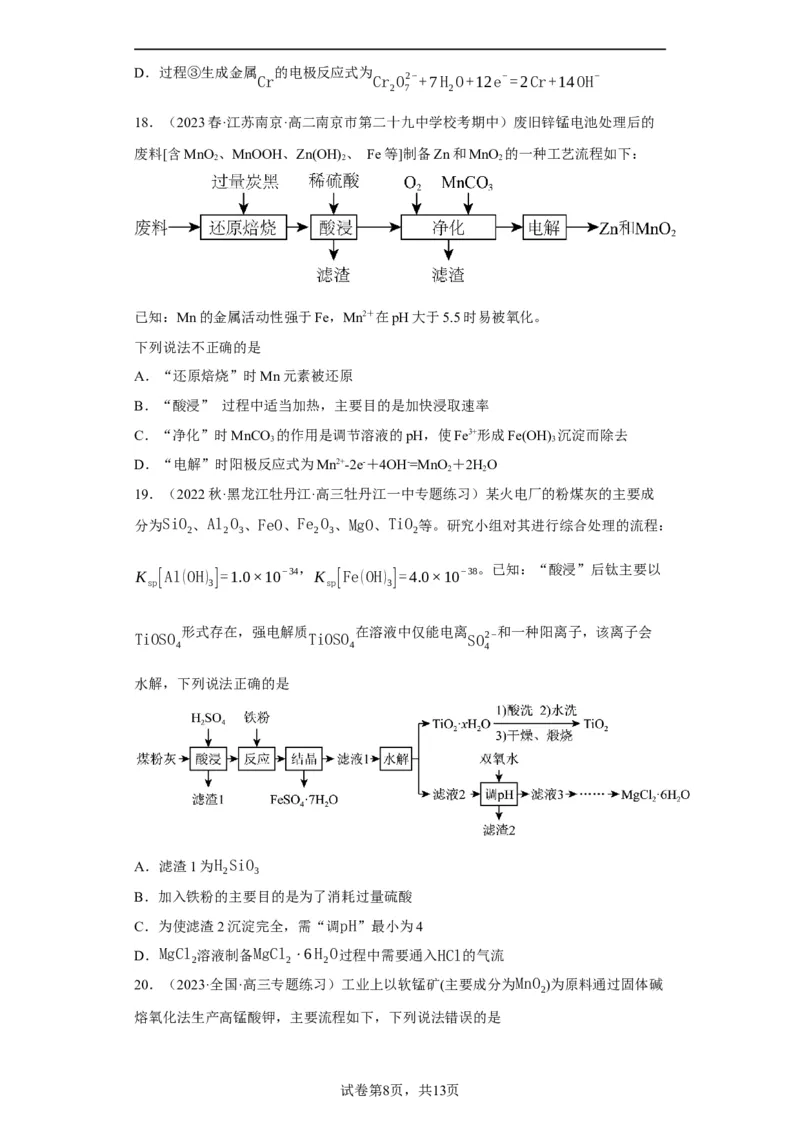
18.(2023春·江苏南京·高二南京市第二十九中学校考期中)废旧锌锰电池处理后的
废料[含MnO 、MnOOH、Zn(OH) 、 Fe等]制备Zn和MnO 的一种工艺流程如下:
2 2 2
已知:Mn的金属活动性强于Fe,Mn2+在pH大于5.5时易被氧化。
下列说法不正确的是
A.“还原焙烧”时Mn元素被还原
B.“酸浸” 过程中适当加热,主要目的是加快浸取速率
C.“净化”时MnCO 的作用是调节溶液的pH,使Fe3+形成Fe(OH) 沉淀而除去
3 3
D.“电解”时阳极反应式为Mn2+-2e-+4OH-=MnO+2HO
2 2
19.(2022秋·黑龙江牡丹江·高三牡丹江一中专题练习)某火电厂的粉煤灰的主要成
分为SiO 、Al O 、FeO、Fe O 、MgO、TiO 等。研究小组对其进行综合处理的流程:
2 2 3 2 3 2
, 。已知:“酸浸”后钛主要以
K [Al(OH) ]=1.0×10−34 K [Fe(OH) ]=4.0×10−38
sp 3 sp 3
形式存在,强电解质 在溶液中仅能电离 和一种阳离子,该离子会
TiOSO TiOSO SO2−
4 4 4
水解,下列说法正确的是
A.滤渣1为H SiO
2 3
B.加入铁粉的主要目的是为了消耗过量硫酸
C.为使滤渣2沉淀完全,需“调pH”最小为4
D.MgCl 溶液制备MgCl ⋅6H O过程中需要通入HCl的气流
2 2 2
20.(2023·全国·高三专题练习)工业上以软锰矿(主要成分为MnO )为原料通过固体碱
2
熔氧化法生产高锰酸钾,主要流程如下,下列说法错误的是
试卷第8页,共13页A.“熔融氧化”应在铁坩埚中进行
B.“锰酸钾歧化(锰元素化合价既升高又降低)”可以用H SO 代替CO
2 4 2
C.该流程中可循环使用的物质是MnO
2
D.“滤液蒸发结晶”过程中加热蒸发至有较多晶体析出时停止加热
21.(2023春·山西忻州·高二校联考阶段练习)四水合磷酸锌[Zn (PO ) ⋅4H O,
3 4 2 2
难溶于水]是一种性能优良的绿色环保防锈颜料。实验室以锌灰(含Zn、ZnO、PbO、
CuO、FeO、Fe O 、SiO 等)为原料制备Zn (PO ) ⋅4H O的流程如下:
2 3 2 3 4 2 2
已知: , 。
K (ZnS)=1.6×10−24 K (CuS)=6.4×10−16
sp sp
下列说法错误的是
A.滤渣工的主要成分是SiO
2
B.步骤I中,调节溶液的pH约为5后加KMnO 溶液反应的离子方程式为
4
MnO−+3Fe2++7H O=MnO ↓+3Fe(OH) ↓+5H+
4 2 2 3
C.若试剂a为ZnS,反应ZnS(s)+Cu2+ (aq)=Zn2+ (aq)+CuS(s)的K=2.5×1011
D.为提高锌元素的利用率,可将分离出四水合磷酸锌的母液收集、循环使用
22.(2023春·重庆北碚·高一西南大学附中校考阶段练习)一种高硫锰矿的主要成分
为MnCO ,主要杂质为SiO 、CaCO ,还含有少量MnS、FeS、CuS、NiS、FeCO 等,
3 2 3 3
其中FeCO 含量较大。研究人员设计了如下流程,制得了金属锰。下列说法错误的是
3
已知:SiO 为酸性氧化物。铁元素除杂一般是转化为Fe(OH) 。
2 3
9 淘宝店铺:向阳百分百
学科网(北京)股份有限公司A.滤渣1为SiO
2
催化剂
B.脱硫的方程式为4FeS+6H O+3O ¿4S+4Fe(OH)
2 2 3
¿
C.若未经脱硫直接酸浸,会产生的污染物是H S
2
D.酸浸时,MnO 的主要作用是作氧化剂
2
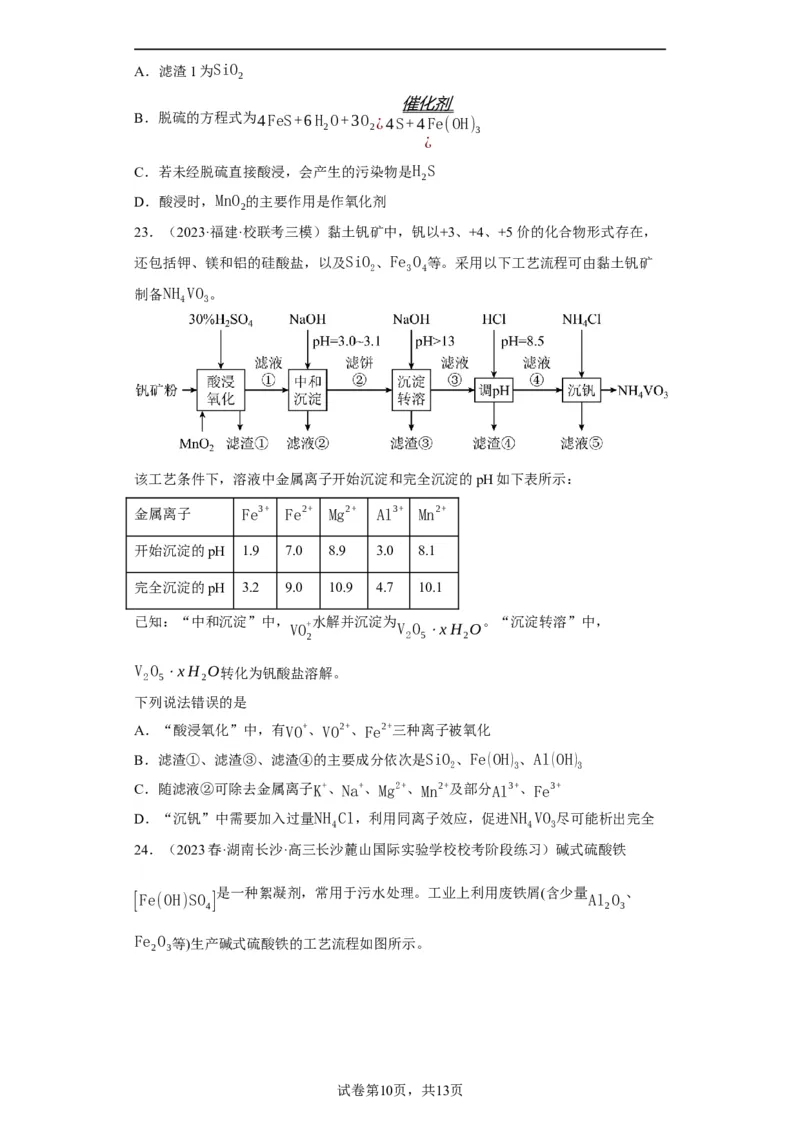
23.(2023·福建·校联考三模)黏土钒矿中,钒以+3、+4、+5价的化合物形式存在,
还包括钾、镁和铝的硅酸盐,以及SiO 、Fe O 等。采用以下工艺流程可由黏土钒矿
2 3 4
制备NH VO 。
4 3
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Mg2+ Al3+ Mn2+
开始沉淀的pH 1.9 7.0 8.9 3.0 8.1
完全沉淀的pH 3.2 9.0 10.9 4.7 10.1
已知:“中和沉淀”中, 水解并沉淀为 。“沉淀转溶”中,
VO+ V O ⋅xH O
2 2 5 2
V O ⋅xH O转化为钒酸盐溶解。
2 5 2
下列说法错误的是
A.“酸浸氧化”中,有VO+、VO2+、Fe2+三种离子被氧化
B.滤渣①、滤渣③、滤渣④的主要成分依次是SiO 、Fe(OH) 、Al(OH)
2 3 3
C.随滤液②可除去金属离子K+、Na+、Mg2+、Mn2+及部分Al3+、Fe3+
D.“沉钒”中需要加入过量NH Cl,利用同离子效应,促进NH VO 尽可能析出完全
4 4 3
24.(2023春·湖南长沙·高三长沙麓山国际实验学校校考阶段练习)碱式硫酸铁
是一种絮凝剂,常用于污水处理。工业上利用废铁屑(含少量 、
[Fe(OH)SO ] Al O
4 2 3
Fe O 等)生产碱式硫酸铁的工艺流程如图所示。
2 3
试卷第10页,共13页下列说法不正确的是
A.“反应I”中包含的反应类型有置换反应、复分解反应和化合反应
B.“过滤”所得滤液中溶质主要是
Fe (SO )
2 4 3
C.“反应II”对应的离子方程式
Fe2++NO−+2H+=Fe3++NO↑+H O
2 2
D.合理处理废铁屑有利于环境保护和资源再利用
25.(2023秋·江苏盐城·高一盐城市第一中学校联考期末)废弃物的综合利用有利于
节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备
ZnSO·7H O和CuSO ·5H O的部分实验步骤如下:
4 2 4 2
下列说法正确的是
A.滤液I中存在的主要阳离子有Zn2+、H+、Cu2+
B.操作I为了尽可能多的得到CuSO ·5H O晶体,应该将溶液蒸干
4 2
C.溶解II过程发生反应的离子方程式为:Cu + H O + 2H+ = Cu2+ + 2H O
2 2 2
D.不可用操作I的方法从滤液I中提取ZnSO·7H O
4 2
26.(2023·辽宁·统考高考真题)某工厂采用如下工艺制备Cr(OH) ,已知焙烧后Cr元
3
素以+6价形式存在,下列说法错误的是
A.“焙烧”中产生CO B.滤渣的主要成分为Fe(OH)
2 2
11 淘宝店铺:向阳百分百
学科网(北京)股份有限公司C.滤液①中 元素的主要存在形式为 D.淀粉水解液中的葡萄糖起还原作用
Cr CrO2−
4
27.(2022秋·河北保定·高三河北省唐县第一中学校考阶段练习)钯(Pd)的性质与铂相
似,一种从废钯催化剂(主要成分为Pd、α-Al O 和活性炭,还含少量Fe、Cu等元素)
2 3
中回收海绵钯的工艺流程如图:
已知:阴、阳离子交换树脂的基本工作原理分别为R-Cl+M-❑R-M+Cl-、R-Na+N+
⇌
❑R-N+Na+。下列说法错误的是
⇌
A.“灼烧”的主要目的是除去活性炭
B.“酸浸”过程中温度不宜过高
C.“离子交换”所用树脂为阳离子交换树脂
D.“还原”过程中氧化剂与还原剂的物质的量之比为1∶2
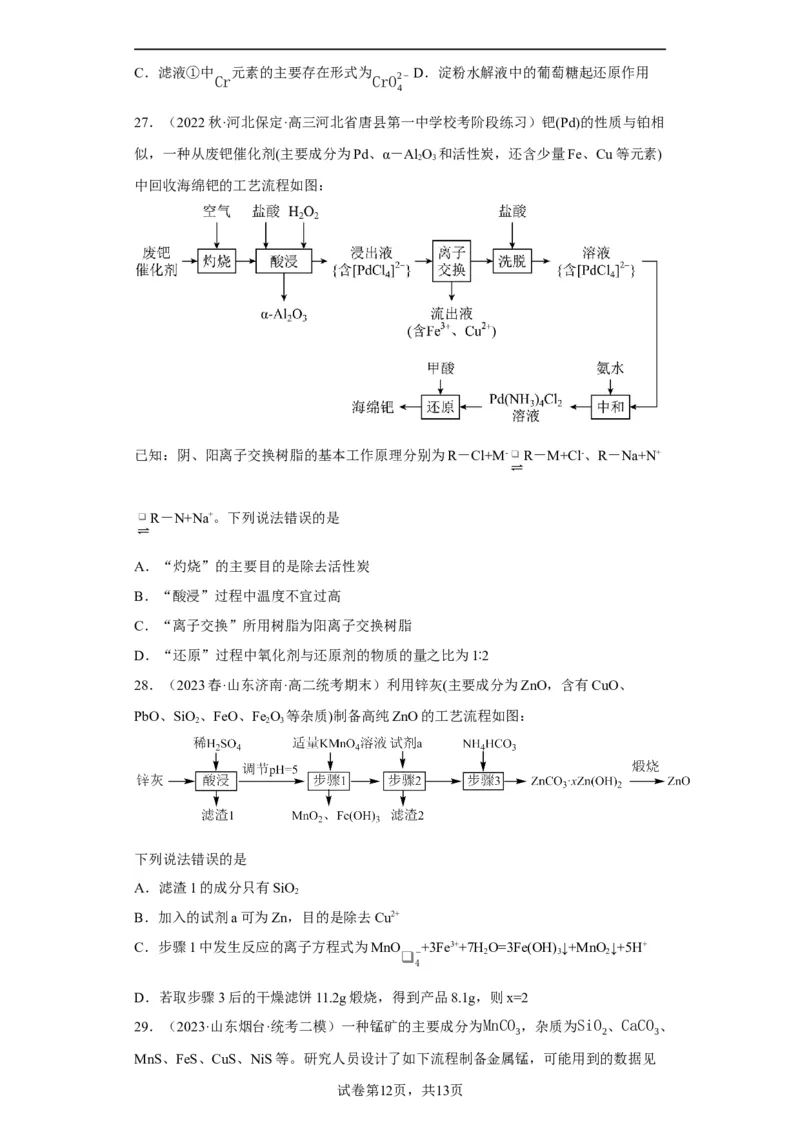
28.(2023春·山东济南·高二统考期末)利用锌灰(主要成分为ZnO,含有CuO、
PbO、SiO、FeO、Fe O 等杂质)制备高纯ZnO的工艺流程如图:
2 2 3
下列说法错误的是
A.滤渣1的成分只有SiO
2
B.加入的试剂a可为Zn,目的是除去Cu2+
C.步骤1中发生反应的离子方程式为MnO +3Fe3++7H O=3Fe(OH) ↓+MnO↓+5H+
− 2 3 2
❑
4
D.若取步骤3后的干燥滤饼11.2g煅烧,得到产品8.1g,则x=2
29.(2023·山东烟台·统考二模)一种锰矿的主要成分为MnCO ,杂质为SiO 、CaCO 、
3 2 3
MnS、FeS、CuS、NiS等。研究人员设计了如下流程制备金属锰,可能用到的数据见
试卷第12页,共13页下表。
Fe(OH) Cu(OH) Ni(OH) Mn(OH)
3 2 2 2
开始沉淀pH 1.9 4.2 6.5 7.6
沉淀完全pH 3.2 6.7 8.5 9.8
下列说法正确的是
A.“脱硫”过程中FeS发生反应:4FeS+3O +6H O=4S+4Fe(OH)
2 2 3
B.物质X为H SiO ,滤渣Y为Fe(OH)
2 3 3
C.上述流程表明:K (CuS)>K (MnS),K (NiS)>K (MnS)
sp sp sp sp
D.“电解”所得阳极产物均可循环利用
30.(2023·全国·高三专题练习)高纯碳酸锰在电子工业中有重要的应用,湿法浸出软
锰矿(主要成分为MnO ,含少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的实验过程
2
如下:其中除杂过程包括:①向浸出液中加入一定量的X,调节浸出液的pH为
3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…。下列说法正确的是
已知室温下:K [Mg(OH) ]=1.8×10-11,K [Al(OH) ]=3.0×10-34,K [Fe(OH) ]=4.0×10-38)
sp 2 sp 3 sp 3
A.试剂X可以是MnO、MnCO 等物质
3
B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质
C.浸出时加入植物粉的作用是作为还原剂
D.为提高沉淀MnCO 步骤的速率可以持续升高温度
3
13 淘宝店铺:向阳百分百
学科网(北京)股份有限公司