文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
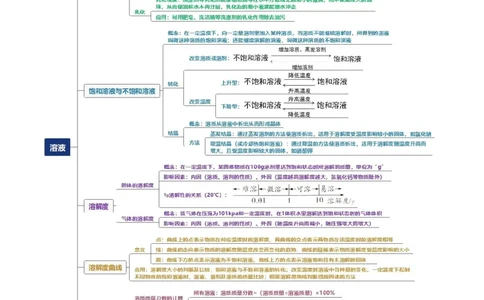
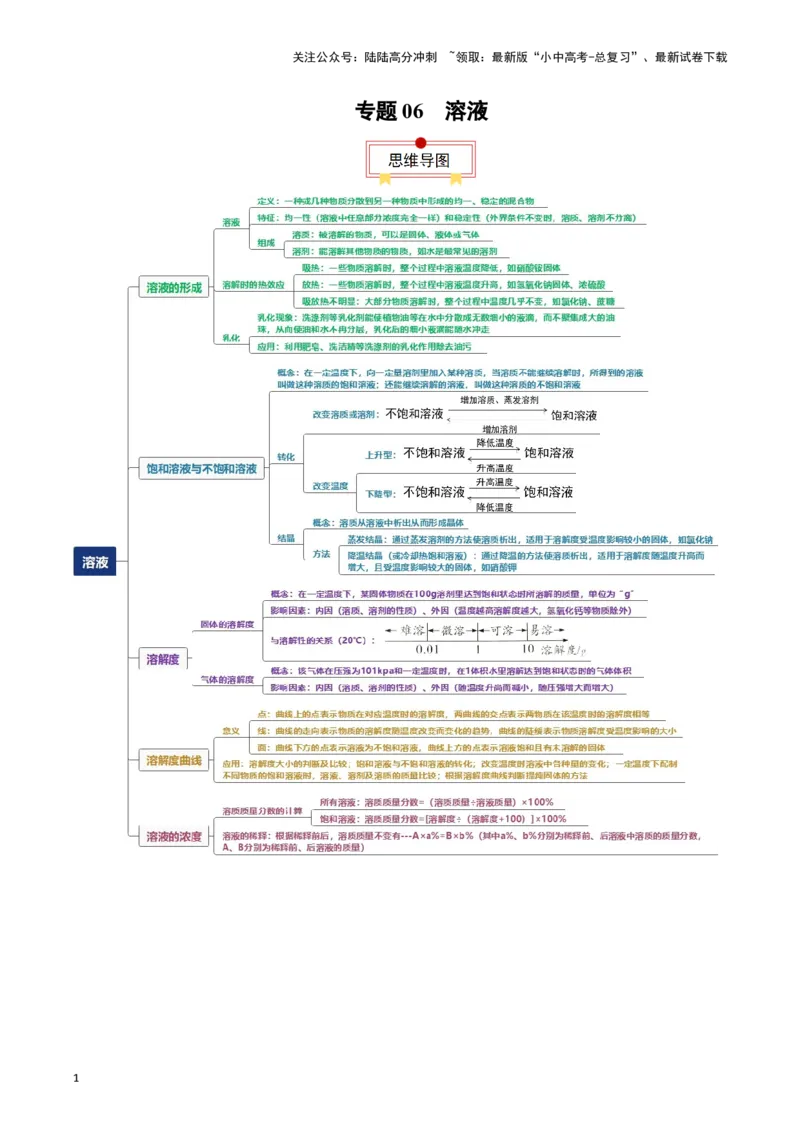
专题 06 溶液
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
知识01 溶液的形成 方法01 溶解度曲线的应用
知识02 饱和溶液和不饱和溶液 方法02 溶液的配制
知识03 溶解度
知识04 溶解度曲线
知识05 溶液的浓度
知识 01 溶液的形成
一、概念
一种或几种物质分散到另一种物质里形成的均一的、稳定的混合物。
二、溶液的特征
均一性:溶液各部分组成和性质完全相同。
稳定性:只要外界条件(如温度)不改变,溶剂和溶质不会分离
混合物:溶液由溶质和溶剂两部分物质组成。
三、溶液的组成
溶质:被溶解的物质,可以是固体、液体、气体。
溶剂:能溶解其他物质的物质,常用水、汽油、酒精等液体。
四、溶解性
影响溶解能力的因素:内因:溶质溶剂性质;外因:温度
影响溶解速率的因素:溶质溶剂的性质、温度、溶质的颗粒大小、是否搅拌。
五、溶液的应用
1. 在溶液中进行化学反应能加快反应的速率。
2. 医疗上的多种注射液也是溶液。
3. 溶液对动植物和人的生理活动有重要意义。(如营养液无土栽培)
六、溶解时的热现象
溶于水放热:氢氧化钠NaOH、浓硫酸HSO
2 4
溶于水吸热:硝酸铵NH NO
4 3
溶于水温度无明显变化:氯化钠NaCl
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【例1】(2023·湖南湘潭·统考中考真题)把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是(
)
A.蔗糖 B.面粉 C.植物油 D.大理石
知识 0 2 饱和溶液和不饱和溶液
一、饱和溶液和不饱和溶液
饱和溶液 不饱和溶液
在一定温度下,向一定量的溶剂里加入某种溶
在一定温度下,向一定量的溶剂里加入某种溶质,
质,溶质还能继续溶解所得到的该溶质的溶
溶质不能继续溶解所得到的该溶质的溶液。
液。
当溶剂量、温度确定时,某溶液的饱和状态表示该溶质溶解的量达到最大值。
(1)判断某溶液是否饱和的方法:
①观察法:观察底部有无不能继续溶解的溶质。若有且不继续溶解,则是饱和溶液。若无,则可能是
不饱和溶液或恰好饱和的溶液(注意恰好饱和和不饱和的溶液看起来都是澄清透明的,外观无法区
别,实验法区别)
②实验法:取样,在该温度下,向溶液里继续加入该种溶质,充分混合,观察溶质是否继续溶解。溶
质不能继续溶解,则是恰好饱和溶液,若溶解,则是不饱和溶液。
(2)饱和溶液和不饱和溶液的转化
(3)饱和溶液和不饱和溶液与稀溶液浓溶液的区别与联系
是否饱和:比较在一定温度下一定量溶剂里溶解溶质的质量是否达到最大限度。
浓稀程度:比较的是在一定量的溶液里溶质质量的相对大小(溶质的质量分数)。
相同温度下,同种溶质的饱和溶液比不饱和溶液浓。
二、结晶与除杂
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
结晶
①降温结晶/冷却热饱和溶液结晶:(通过改变温度降低溶解度
析出晶体)适用于溶解度随温度升高而增大且受温度影响变化
较大的固体溶质
注意:
②蒸发结晶:(通过减少溶剂量使晶体析出)
析出晶体后的母液(又名苦卤)一定
适用于溶解度受温度影响不大的固体溶质
是该晶体溶质的饱和溶液。
除杂 ①硝酸钾中含有少量氯化钠→冷却热饱和溶液法(降温结晶
原则:不增加新杂质、不减少原物 法)
质、易分离杂质、易复原原物质状态 ②氯化钠中含有少量硝酸钾→蒸发溶剂法(蒸发结晶)
【例2】(2023·海南海口·海口市校考二模)在室温的条件下,试管里盛有一种无色透明的溶液,将试管放
入盛有热水的烧杯中,可观察到试管里的溶液变浑浊。下列说法正确的是( )
A.该溶液中的溶质可能是硝酸钾
B.该溶液中的溶质可能是氢氧化钙
C.放入热水前的无色透明溶液一定是饱和溶液
D.变浑浊后过滤出来的溶液一定是浓溶液
知识 0 3 溶解度
一、气体的溶解度
1. 定义
常指气体在压强为101KPa和一定温度时,在1体积水里溶解达到饱和状态时的气体体积。
2. 影响气体溶解度的因素
内因:气体和溶剂的性质;
外因:①压强——气体溶解度随压强增大而增大。
②温度——气体溶解度随温度升高而减小。
二、固体的溶解度S
1. 定义
在一定温度下,某固态物质在100g溶剂(不指明溶剂,通常指水)里达到饱和状态时所溶解的质量。
2. 理解定义四要素
(1)条件:一定温度,固体溶质的溶解度随温度的变化而变化,只有指明温度,溶解度才有意义。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)标准:100g溶剂,固体物质的溶解量随溶剂量的增大而增大,限度100g溶剂的量便于统一标准后比
较。
(3)状态:达到饱和状态,只有达到最大溶解量时才是确定的值。
(4)单位:为g,溶解度其实就是溶质的质量,是在特定量溶剂和一定温度下的溶质质量。
3. 溶解度的意义
如20℃时,氯化钠溶解度为36g的意义为:
(1)在20℃时,100g水中最多能溶解(即达饱和)36gNaCl。
(2)在20℃时,100g水中溶解36g氯化钠形成饱和溶液。
(3)在20℃时,要完全溶解36g氯化钠,最少需要水100g。
(4)在20℃时,136g氯化钠溶液中有100g水,36g氯化钠。
三、溶解度和溶解性的关系
溶解性是根据20℃时,固体物质的溶解度的大小划分的。
【例3】(2023·四川巴中·统考中考真题)生活在盐碱湖附近的人们习惯“夏天晒盐,冬天捞碱”,结合下
表数据,下列说法正确的是
温度
溶解
0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃ 70℃
度
物质
氯化
35.7g 35.8g 36.0g 36.3g 36.6g 37.0g 37.3g 37.8g
钠
碳酸
7.0g 12.2g 21.8g 39.7g 49.0g 48.7g 46.5g 45.8g
钠
A.碳酸钠的溶解度比氯化钠大
B.“夏天晒盐,冬天捞碱”分别利用了蒸发结晶和降温结晶的原理
C.20℃时,将20g氯化钠加入50g水中,形成的溶液质量为70g
D.碳酸钠的溶解度随温度升高而增大
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
知识 0 4 溶解度曲线
溶解度的表示方法
1.列表法 从表格中找出物质的溶解度值
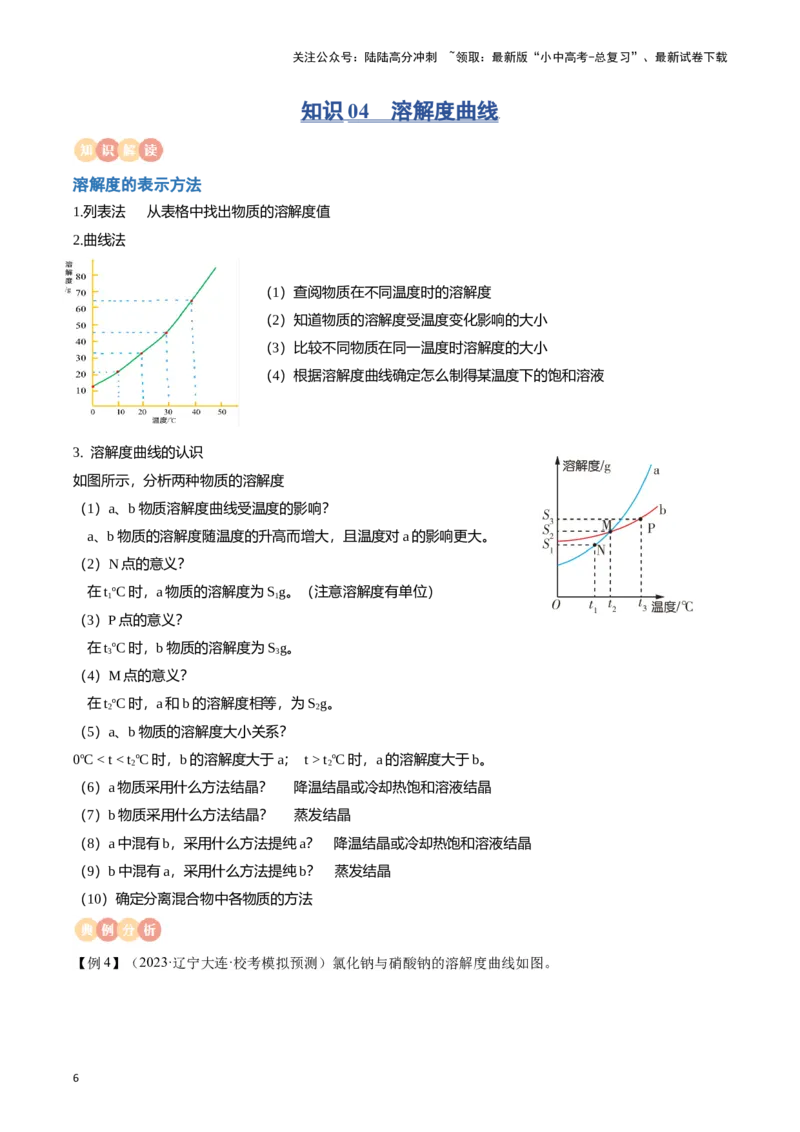
2.曲线法
(1)查阅物质在不同温度时的溶解度
(2)知道物质的溶解度受温度变化影响的大小
(3)比较不同物质在同一温度时溶解度的大小
(4)根据溶解度曲线确定怎么制得某温度下的饱和溶液
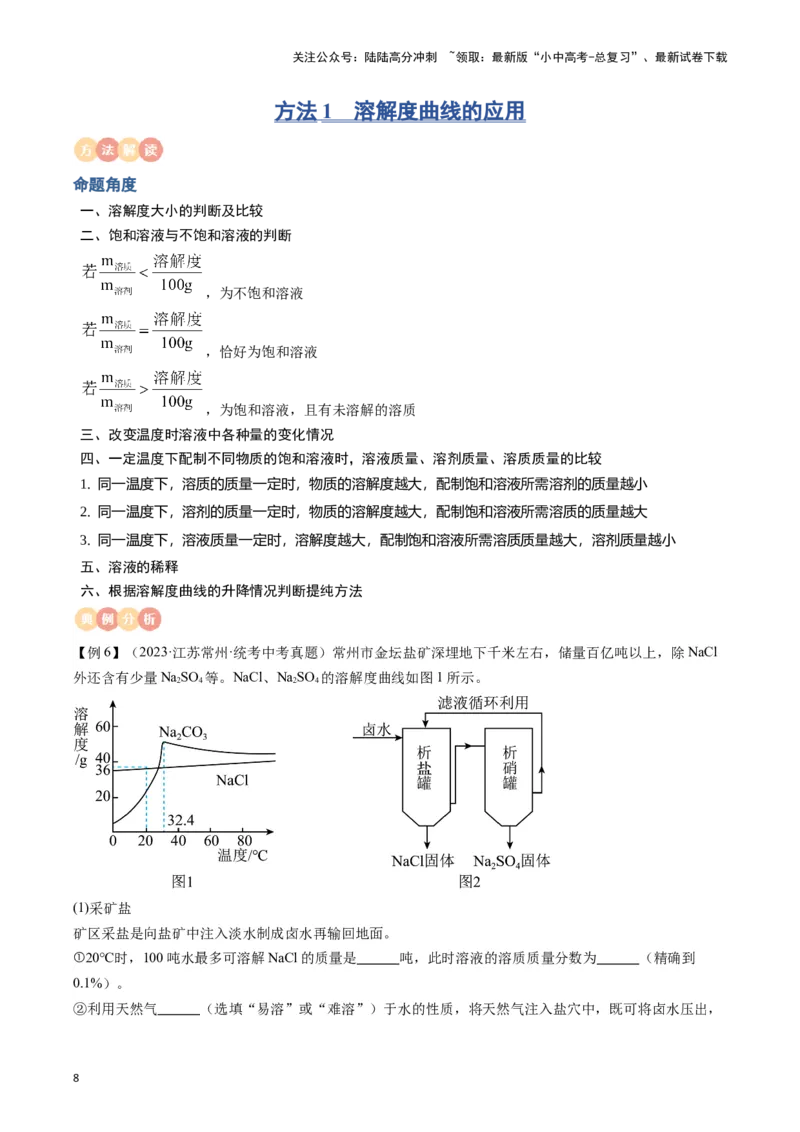
3. 溶解度曲线的认识
如图所示,分析两种物质的溶解度
(1)a、b物质溶解度曲线受温度的影响?
a、b物质的溶解度随温度的升高而增大,且温度对a的影响更大。
(2)N点的意义?
在toC时,a物质的溶解度为Sg。(注意溶解度有单位)
1 1
(3)P点的意义?
在toC时,b物质的溶解度为Sg。
3 3
(4)M点的意义?
在toC时,a和b的溶解度相等,为Sg。
2 2
(5)a、b物质的溶解度大小关系?
0oC < t < t oC时,b的溶解度大于a; t > t oC时,a的溶解度大于b。
2 2
(6)a物质采用什么方法结晶? 降温结晶或冷却热饱和溶液结晶
(7)b物质采用什么方法结晶? 蒸发结晶
(8)a中混有b,采用什么方法提纯a? 降温结晶或冷却热饱和溶液结晶
(9)b中混有a,采用什么方法提纯b? 蒸发结晶
(10)确定分离混合物中各物质的方法
【例4】(2023·辽宁大连·校考模拟预测)氯化钠与硝酸钠的溶解度曲线如图。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)20℃时溶解度较小的物质是 。
(2)20℃时硝酸钠饱和溶液中溶质与溶剂质量比为 ,将该饱和溶液变为不饱和溶液,可以 。
(3)除去硝酸钠溶液中少量的氯化钠应采取的方法是 。
知识 0 5 溶液的浓度
溶液的浓度——溶质质量分数
1. 溶质质量分数定义:溶质的质量与溶液的质量之比
2. 溶质质量分数计算公式:
3. 饱和溶液的溶质质量分数计算公式:
【例5】(2023·上海黄浦·统考一模)建立模型是解决问题的一种方法。图是 的蔗糖溶液,其中
“・”表示所含的蔗糖分子。在该溶液中加入一定量的水,成为 的蔗糖溶液。能表示稀释后蔗糖溶液
模型的是( )( 的蔗糖溶液的密度近似等于水的密度)
A. B. C. D.
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
方法 1 溶解度曲线的应用
命题角度
一、溶解度大小的判断及比较
二、饱和溶液与不饱和溶液的判断
,为不饱和溶液
,恰好为饱和溶液
,为饱和溶液,且有未溶解的溶质
三、改变温度时溶液中各种量的变化情况
四、一定温度下配制不同物质的饱和溶液时,溶液质量、溶剂质量、溶质质量的比较
1. 同一温度下,溶质的质量一定时,物质的溶解度越大,配制饱和溶液所需溶剂的质量越小
2. 同一温度下,溶剂的质量一定时,物质的溶解度越大,配制饱和溶液所需溶质的质量越大
3. 同一温度下,溶液质量一定时,溶解度越大,配制饱和溶液所需溶质质量越大,溶剂质量越小
五、溶液的稀释
六、根据溶解度曲线的升降情况判断提纯方法
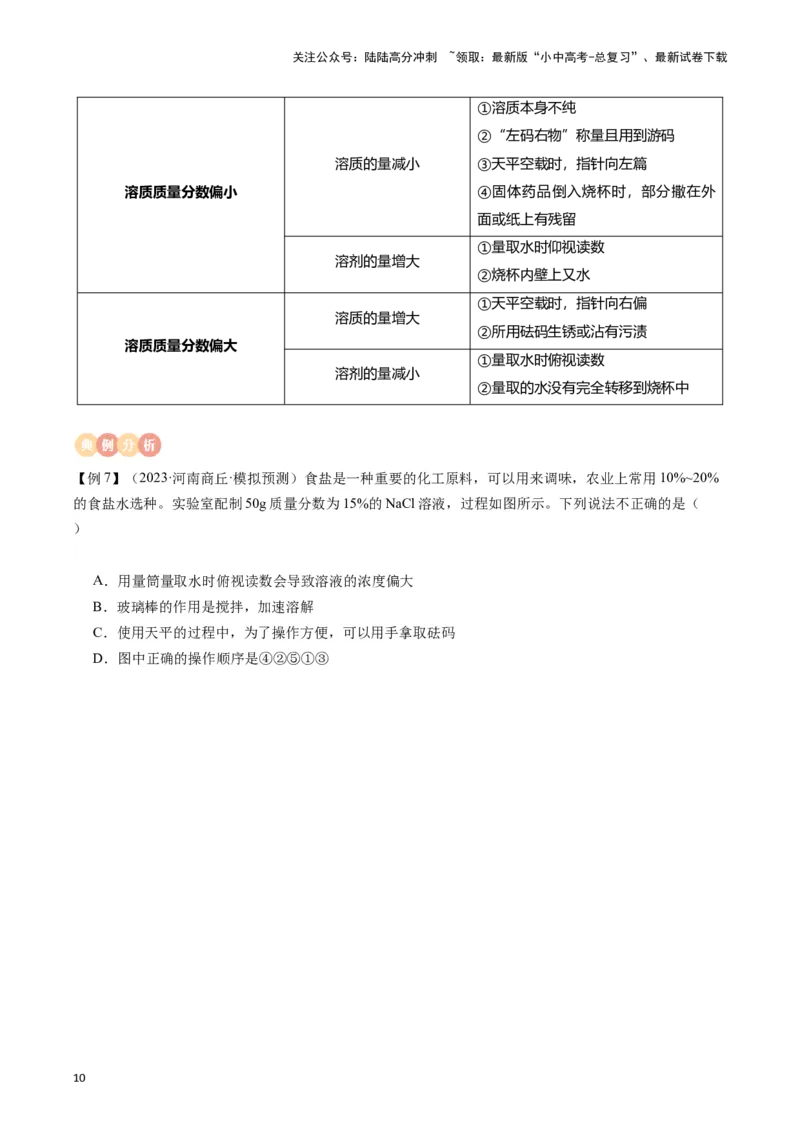
【例6】(2023·江苏常州·统考中考真题)常州市金坛盐矿深埋地下千米左右,储量百亿吨以上,除NaCl
外还含有少量NaSO 等。NaCl、NaSO 的溶解度曲线如图1所示。
2 4 2 4
(1)采矿盐
矿区采盐是向盐矿中注入淡水制成卤水再输回地面。
①20℃时,100吨水最多可溶解NaCl的质量是 吨,此时溶液的溶质质量分数为 (精确到
0.1%)。
②利用天然气 (选填“易溶”或“难溶”)于水的性质,将天然气注入盐穴中,既可将卤水压出,
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
又可把盐穴作为西气东输的中转站储存天然气。
(2)运盐水
抽出的卤水检验合格后通过管道送往厂区。为防止冬季管道堵塞,检验时合格的卤水必须是该温度下的
(选填“饱和”或“不饱和”)溶液。
(3)制精盐
如图2是金坛盐厂采用的NaCl、NaSO 联产工艺流程。析盐罐内真空减压蒸发水,温度宜控制为 ℃,
2 4
析硝罐中出来的滤液所含的溶质有 。
方法 2 溶液的配制
1.实验仪器
托盘天平(带砝码)、镊子、药匙、量筒、胶头滴管、烧杯、玻璃棒
2.实验装置
3.实验步骤
(1)用固体配制溶液
计算:计算所需的固体质量和液体体积
称量和量取:用托盘天平称取一定质量的固体,用量筒量取一定体积的水
溶解:将固体倒入烧杯,再将量取的水倒入烧杯,用玻璃棒搅拌均匀
装瓶:将配制好的溶液装入试剂瓶,贴上标签
【注意】①溶质质量=溶液质量×溶质质量分数
②溶剂质量=溶液质量–溶质质量
(2)用浓溶液配制稀溶液
①步骤:计算→量取→混匀→装瓶贴标签
②相关计算
加入水的质量=稀溶液的质量–浓溶液的质量
4. 偏差分析
偏差 原因 举例
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①溶质本身不纯
②“左码右物”称量且用到游码
溶质的量减小 ③天平空载时,指针向左篇
溶质质量分数偏小 ④固体药品倒入烧杯时,部分撒在外
面或纸上有残留
①量取水时仰视读数
溶剂的量增大
②烧杯内壁上又水
①天平空载时,指针向右偏
溶质的量增大
②所用砝码生锈或沾有污渍
溶质质量分数偏大
①量取水时俯视读数
溶剂的量减小
②量取的水没有完全转移到烧杯中
【例7】(2023·河南商丘·模拟预测)食盐是一种重要的化工原料,可以用来调味,农业上常用10%~20%
的食盐水选种。实验室配制50g质量分数为15%的NaCl溶液,过程如图所示。下列说法不正确的是(
)
A.用量筒量取水时俯视读数会导致溶液的浓度偏大
B.玻璃棒的作用是搅拌,加速溶解
C.使用天平的过程中,为了操作方便,可以用手拿取砝码
D.图中正确的操作顺序是④②⑤①③
10