文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 06 溶液
考点01 溶液的形成
考点02 溶质质量分数
考点03 配制一定溶质质量分数的溶液
考点04 溶解度
考点01 溶液的形成
1.(2024·湖北·中考真题)把少量下列物质加入水中,充分搅拌,能形成溶液的是( )
A.泥土 B.蜡烛 C.蔗糖 D.汽油
【答案】C
【解析】A、泥土不溶于水,与水混合形成不均一不稳定的悬浊液,不符合题意;
B、蜡烛不溶于水,不能形成溶液,不符合题意;
C、蔗糖易溶于水,形成均一稳定的混合物,属于溶液,符合题意;
D、汽油不溶于水,与水混合形成不均一不稳定的乳浊液,不符合题意;
故选:C。
2.(2024·江苏苏州·中考真题)下列有关溶液的说法正确的是( )
A.溶液由溶质和溶剂组成 B.碘酒中,碘是溶剂,酒精是溶质
C.溶液的溶质只能是一种 D.所有溶液均是无色、澄清的液体
【答案】A
【解析】A、溶液是由溶质和溶剂组成的混合物,A正确;
B、碘酒中,碘是溶质,酒精是溶剂,B错误;
C、溶液的溶质可以是一种,也可以是多种,C错误;
D、溶液不一定是无色的液体,如蓝色的CuSO 溶液、浅绿色的FeSO 溶液等,D错误。
4 4
故选:A。
3.(2024·广西·中考真题)下列家务劳动中,涉及乳化作用的是( )
A.用洗涤剂清洗衣物的油污 B.用自来水冲洗地上的灰尘
C.用食醋清除水壶内的水垢 D.用洁厕灵除去厕所的污垢
【答案】A
【解析】A、用洗涤剂清洗衣物的油污利用了洗洁精的乳化作用,故A正确;
B、用自来水冲洗地上的灰尘,可将灰尘冲刷掉,故B错误;
C、用食醋溶解水壶里的水垢,利用了化学反应的原理,故C错误;
D、用洁厕灵除去厕所的污垢,利用了化学反应的原理,故D错误。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选A。
4.(2024·湖南·中考真题)化学世界绚丽多彩。下列溶液中,有一种与其他三种颜色不同,这种溶液是(
)
A.硝酸钾溶液 B.硫酸钠溶液 C.稀硫酸 D.硫酸铜溶液
【答案】D
【解析】A.硝酸钾溶液是无色溶液;错误;
B.硫酸钠溶液是无色溶液;错误;
C.稀硫酸是无色溶液;错误;
D.硫酸铜溶液是蓝色溶液;正确;
故选D。
5.(2023·江苏南京·中考真题)下列物质加入一定量的水中,能使液体温度明显降低的是( )
A.浓硫酸 B.氯化钠 C.硝酸铵 D.氢氧化钠
【答案】C
【解析】A、浓硫酸加入一定量的水中,放出大量的热,溶液温度升高,故A错误;
B、氯化钠溶于水时温度几乎不变,故B错误;
C、硝酸铵溶于水时吸收热量,溶液温度降低,故C正确;
D、氢氧化钠溶于水放出大量的热,溶液温度升高,故D错误。
故选C。
6.(2023·江苏无锡·中考真题)下列化肥不能配成绿植“水培溶液”的是( )
A.氯化钾 B.氯化铵 C.硝酸钠 D.磷矿粉
【答案】D
【解析】A、氯化钾溶于水能形成均一稳定的溶液,不符合题意;
B、氯化铵 溶于水能形成均一稳定的溶液,不符合题意;
C、硝酸钠 溶于水能形成均一稳定的溶液,不符合题意;
D、磷矿粉属于磷肥,磷肥难溶于水,因此无法配制成溶液,符合题意;
故选:D
7.(2023·湖南湘潭·中考真题)下列固体物质加入适量水中,溶液的温度明显降低的是( )
A. B. C. D.
【答案】A
【解析】A、硝酸铵溶解在水中时吸热,溶液温度降低,符合题意;
B、氧化钙和水反应生成氢氧化钙,放热,溶液温度升高,不符合题意;
C、氯化钠溶解在水中时无明显吸放热,溶液温度不变,不符合题意;
D、氢氧化钠溶解在水中时放热,溶液温度升高,不符合题意;
故选A。
8.(2023·湖南长沙·中考真题)在体育中考期间,班主任为同学们准备了很多食物,其中属于溶液的是(
)
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.稀饭 B.番茄蛋汤 C.酸奶 D.淡盐水
【答案】D
【解析】A、稀饭不均一、不稳定,不属于溶液,故选项不符合题意;
B、番茄蛋汤不均一、不稳定,不属于溶液,故选项不符合题意;
C、酸奶是不溶性的小液滴等分散到液体中形成的,不均一、不稳定,不属于溶液,故选项不符合题意;
D、淡盐水是均一、稳定的混合物,属于溶液,故选项符合题意。
故选D。
9.(2022·辽宁鞍山·中考真题)把少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是(
)
A.面粉 B.硫酸铁 C.汽油 D.蔗糖
【答案】D
【解析】A. 面粉放入水中,会以细小固体颗粒形式分散于水中,形成的是悬浊液,不是溶液,故A错
误;
B. 硫酸铁放入水中,会以离子形式均匀分散到水中,形成均一、稳定的硫酸铁溶液,但硫酸铁溶液是黄
色的,故B错误;
C. 汽油放入水中,会以小液滴形式分散于水中,形成乳浊液,不是溶液,故C错误;
D. 蔗糖放入水中,会以分子形式均匀分散到水中,形成均一、稳定的无色蔗糖溶液,故D正确。
故选:D。
10.(2022·辽宁朝阳·中考真题)夏日里想随时喝到凉爽的饮料,可以自制化学“冰箱”,即把一种固体
物质放入一定量的水中,就可以形成低温小环境。这种固体可以是( )
A.食盐 B.硝酸铵 C.氧化钙 D.氢氧化钠
【答案】B
【解析】A、食盐溶于水,温度变化不大,不能形成低温环境,不符合题意;
B、硝酸铵溶于水吸热,溶液温度降低,能形成低温环境,符合题意;
C、氧化钙与水反应生成氢氧化钙,放出大量的热,不能形成低温环境,不符合题意;
D、氢氧化钠溶于水放出大量的热,不能形成低温环境,不符合题意。
故选B。
考点02 溶质质量分数
11.(2024·重庆·中考真题)已知KCl的溶解度随温度升高而增大,在40℃时KCl的溶解度为40g,在该
温度下,依据下表所示的数据,进行KCl溶于水的实验探究。下列说法中正确的是( )
实验编号 ① ② ③
KCl的质量/g 10 20 30
水的质量/g 50 60 70
A.在上述实验所得的溶液中,溶质质量分数①>②
B.实验③所得溶液中,溶质与溶剂的质量比为3:7
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.将实验②、③的溶液分别降温,一定都有晶体析出
D.将实验①、③的溶液按一定比例混合可得到与②浓度相等的溶液
【答案】D
【解析】A、在40℃时KCl的溶解度为40g,即100g水中最多能溶解40g氯化钾,则50g水中最多能溶解
氯化钾,60g水中最多能溶解 氯化钾,①中水的质量为50g,加入氯化钾
的质量为10g,可以完全溶解,得到不饱和溶液,溶质质量分数为: ,②中水的
质量为60g,加入氯化钾的质量为20g,可以完全溶解,得到不饱和溶液溶质质量分数为:
,故溶质质量分数①<②,故A说法错误;
B、在40℃时KCl的溶解度为40g,即100g水中最多能溶解40g氯化钾,则70g水中最多能溶解
氯化钾,③中水的质量为70g,加入氯化钾的质量为30g>28g,只能溶解28g氯化钾,得
到饱和溶液,则实验③所得溶液中,溶质与溶剂的质量比为28g:70g=2:5,故B说法错误;
C、由上可知,②为该温度下的不饱和溶液,③为该温度下的饱和溶液,KCl的溶解度随温度升高而增
大,将实验②、③的溶液分别降温,②不一定有晶体析出,③一定有晶体析出,故C说法错误;
D、将实验①、③的溶液按一定比例混合,即按照1:1混合,则得到的溶液中水的质量为
50g+70g=120g,加入氯化钾的质量为10g+30g=40g,可以完全溶解,溶质与溶剂的质量比为40g:
120g=1:3,②中溶质与溶剂的质量比也为20g:60g=1:3,即将实验①、③的溶液按一定比例(1:1)混
合可得到与②浓度相等的溶液,故D说法正确;
故选:D。
12.(2023·河北·中考真题) 和 时 的溶解度分别为 和 ,下图所示为对 进行
的溶解实验。下列分析错误的是( )
A.①中溶液为 的饱和溶液
B.②中溶液的质量为
C.溶液中溶质的质量:①<②=③
D.溶液中溶质的质量分数:①<②=③
【答案】D
【解析】A.20°C 时 KCl 的溶解度分别为 34.0g,即100g水中最多溶解34.0gKCl达到饱和,10.0g水中最
多溶解3.4gKCl达到饱和,加入5.0gKCl不能完全溶解,因此,①中溶液为 KCl 的饱和溶液,故选项说法
正确,不符合题意;
B.②是在①的基础上又加入10.0g水,使未溶解的KCl固体继续溶解,溶液的质量为:
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
10.0g+5.0g+10.0g=25.0g,故选项说法正确,不符合题意;
C.②到③的过程中温度升高,没加KCl固体,所以溶质质量②和③相等,①中有未溶解的KCl固体,溶质
质量小于②,所以溶液中溶质的质量:①<②=③,故选项说法正确,不符合题意;
D.溶液②升温的过程中没有加入溶质,没有加入溶剂,但升温可能导致水分的蒸发,使③中溶剂质量减
少,溶液质量减少,最终使③的溶质质量分数大于②,故选项说法错误,符合题意;
故选D。
13.(2024·云南·中考真题)实验室中存放有如图所示的氯化钾溶液。下列说法错误的是( )
A.该溶液中的溶剂是水 B.该溶液的溶质质量分数为6%
C.配制100g该溶液需要6gKCl D.该溶液取出一半后,溶质质量分数变为3%
【答案】D
【解析】A、该溶液是氯化钾溶液,溶质是氯化钾,溶剂是水,不符合题意;
B、标签上注明的是溶液名称和溶质质量分数,故该溶液的溶质质量分数为6%,不符合题意;
C、配制100g该溶液需要氯化钾的质量为: ,不符合题意;
D、溶液具有均一性,该溶液取出一半后,溶质质量分数仍然是6%,符合题意。
故选D。
(2023·北京·中考真题) 时,按下表数据配制 溶液。完成下面小题。
溶液序号 ① ② ③ ④
资料卡片
的质量/g 6 16 26 36
时, 的溶解度为 ;
10 10 时, 的溶解度为 。
水的质量/g 100 100
0 0
14.溶质与溶剂的质量比为 的溶液是( )
A.① B.② C.③ D.④
15.①中溶质的质量分数约为( )
A. B. C. D.
16.下列关于④的说法正确的是( )
A.所得溶液为不饱和溶液
B.向④中加水,溶液的质量变大
C.将④加热至 ,溶质的质量变大
D.向④中加 固体,溶质的质量分数变大
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【答案】14.B 15.A 16.B
【解析】14.A、20°C 时, NaCl 的溶解度为 36.0g ,溶液①中溶质与溶剂的质量比为6g:100g=3:
50,不符合题意;
B、溶液②中溶质与溶剂的质量比为16g:100g=4:25,符合题意;
C、溶液③中溶质与溶剂的质量比为26g:100g=13:50,不符合题意;
D、溶液④中溶质与溶剂的质量比为36g:100g=9:25,不符合题意;
故选B;
15.20°C 时, NaCl 的溶解度为 36.0g ,溶液①中溶的质量为6g,溶剂的质量为100g,故①中溶质的质
量分数为: ,故选A;
16.A、20°C 时, NaCl 的溶解度为 36.0g ,溶液④中溶质的质量为36g,溶剂的质量为100g,所得溶
液恰好为20℃氯化钠的饱和溶液,故A说法错误;
B、向④中加水,溶剂增多,故溶液的质量变大,故B说法正确;
C、20°C时,NaCl的溶解度为36.0g,50°C时, NaCl 的溶解度为37.0g,将④加热至 50°C ,氯化钠的
溶解度增大,④溶液变为不饱和溶液,但是溶液的组成不变,所以溶质的质量不变,故C说法错误;
D、④恰好为20℃氯化钠的饱和溶液,所以向④中加 NaCl 固体,不能再继续溶解氯化钠固体,故溶质的
质量分数不变,故D说法错误;
故选B。
17.(2022·山东青岛·中考真题)医生常用生理盐水(溶质质量分数为0.9%)给患者输液。下列对生理盐
水的理解不正确的是( )
A.生理盐水中氯化钠是溶质,水是溶剂
B.生理盐水中氯化钠与水的质量比为9:1000
C.每输入100g生理盐水,进入患者体内的氯化钠质量为0.9g
D.输液时,输液管中和输液瓶中生理盐水的溶质质量分数相同
【答案】B
【解析】A、生理盐水即溶质质量分数为0.9%的氯化钠溶液,故氯化钠是溶质,水是溶剂,不符合题意;
B、 ,故生理盐水中氯化钠与水的质量比为9:991,符合题意;
C、每输入100g生理盐水,进入患者体内的氯化钠质量为 ,不符合题意;
D、输液时,上方的输液瓶中生理盐水受重力随着输液管流到病人血管中,输液管中的生理盐水来自于输
液瓶,两者是同一溶液,故其溶质质量分数相同,不符合题意。
故选B。
18.(2022·辽宁鞍山·中考真题)实验室用质量分数为5%的过氧化氢溶液和适量二氧化锰混合制取氧气。
请计算(写出计算过程):
(1)制取1.6g氧气,需要质量分数为5%的过氧化氢溶液的质量是多少?
(2)将20g质量分数为30%的过氧化氢溶液,稀释成质量分数为5%的过氧化氢溶液,需要加入水的质量
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
是多少?
【答案】(1)68g
(2)100g
【解析】(1)解:设需要过氧化氢溶液的质量为x
答: 需要质量分数为5%的过氧化氢溶液的质量是68g。
(2)解:设需要加入水的质量为x
20g×30%=5%×(20g+x)
x=100g
答:需要加入水的质量是100g。
考点3 配制一定溶质质量分数的溶液
19.(2024·甘肃临夏·中考真题)如图所示是某同学配制一定质量分数的氯化钠溶液的部分实验操作,其
中错误的是( )
A.取用 B.称量 C.量取 D.溶解
【答案】B
【解析】A、氯化钠通常保存在广口瓶里,取用氯化钠时拿下瓶塞,倒放在桌面,用药匙取出。A正确;
B、托盘天平的两个托盘上放等大的纸片,氯化钠放在纸片上称量,应左盘放氯化钠,右盘放砝码。B错
误;
C、读取量筒的读数时,把量筒放在水平桌面上,视线与量筒内液体凹液面的最低处保持水平。C正确;
D、溶解氯化钠时,应用玻璃棒按一个方向搅拌。D正确。
综上所述:选择B。
20.(2024·重庆·中考真题)用密度为 的质量分数为6%的NaCl溶液配制50g质量分数为3%的
NaCl溶液,下列实验步骤①计算 ②称量 ③量取 ④溶解 ⑤混匀,正确的组合是( )
A.①②④ B.①③⑤ C.①③④ D.③④⑤
【答案】B
【解析】用浓溶液配制稀溶液,实验步骤为:计算、量取、混匀、装瓶贴标签,故顺序为:①③⑤。
故选B。
21.(2024·河南·中考真题)某同学在实验室配制一定溶质质量分数的氯化钠溶液,若其他操作均正确,
量取水时俯视量筒读数,会导致所配制溶液的质量分数( )
A.偏大 B.偏小 C.不变 D.无法判断
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【答案】A
【解析】用量筒量取蒸馏水时俯视读数,实际量取蒸馏水的体积偏小,最终配制的溶液中溶剂的质量偏
小,溶液的溶质质量分数偏大,故选:A。
22.(2024·江苏扬州·中考真题)实验室用 固体和蒸馏水配制50g15%的 溶液时,不需要使用的
仪器是( )
A.烧杯 B.玻璃棒 C.量筒 D.坩埚钳
【答案】D
【解析】实验室用 NaCl 固体和蒸馏水配制50g15%的 NaCl 溶液时,实验操作步骤分别是:计算、称
量、量取、溶解,托盘天平用于称取固体氯化钠、量筒与胶头滴管用于准确量取水、烧杯用于完成溶解操
作、玻璃棒用于溶解时的搅拌,无需使用坩埚钳;
故选:D。
23.(2023·海南·中考真题)某实验小组做“配制一定溶质质量分数的氯化钠溶液”实验的部分操作如
下,其中错误的是( )
A.取用固体 B.称量 C.量取液体 D.溶解
【答案】C
【解析】A、应用药匙取用粉末状药品,且瓶塞应倒放,图中操作正确,不符合题意;
B、用托盘天平称量物品时,应遵循“左物右码”的原则,图中操作正确,不符合题意;
C、常用量筒量取一定体积的液体,读数时,视线应与液体凹液面的最低处保持水平,图中操作错误,符
合题意;
D、溶解时,应用玻璃棒不断搅拌,加速溶解,不符合题意。
故选C。
24.(2023·山东菏泽·中考真题)某化学兴趣小组按如图操作配制一定溶质质量分数的氯化钠溶液。下列
说法不正确的是( )
A.③中玻璃棒的作用是加速溶解
B.⑥读数时视线与凹液面最低点保持水平
C.①~⑥项实验操作均正确
D.实验操作顺序为④②①⑥⑤③
【答案】C
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【解析】A、③是溶解,玻璃棒的作用是搅拌,加速固体的溶解,故正确;
B、⑥读数时应该平视,视线与凹液面最低点保持水平,操作正确,故正确;
C、②操作中,用天平称量药品时,应该称量物放左盘,砝码放右盘,图示操作错误,故错误;
D、用固体配制一定溶质质量分数的溶液,实验步骤为:计算、称量、量取、溶解、装瓶贴标签,实验操
作顺序为④②①⑥⑤③,故正确;
故选:C。
25.(2023·山东泰安·中考真题)实验室用固体氯化钠配制50g溶质质量分数为6%的氯化钠溶液。下列说
法正确的是( )
A.所需固体氧化钠的质量是
B.固体氯化钠可以直接放在托盘天平的左盘上称量
C.溶解固体氯化钠时,用玻璃棒搅拌能增大氯化钠的溶解度
D.用量筒量取所需水时仰视读数,会导致配制的溶液溶质质量分数偏大
【答案】A
【解析】A、氯化钠质量=50g×6%=3.0g,正确;
B、天平称量遵循左物右码原则,氯化钠会使托盘腐蚀,不能直接放于托盘天平托盘上直接称量,需要利
用称量纸或烧杯,错误;
C、玻璃搅拌可以加快溶解,不能增加物质溶解度,错误;
D、仰视读数,造成溶剂体积偏大,溶剂质量偏大,导致溶质质量分数变小,错误。
故选A。
26.(2022·湖南邵阳·中考真题)实验室配制50g溶质质量分数为10%的氯化钠溶液,下列说法正确的是
( )
A.计算得出所需氯化钠固体的质量为5g
B.将氯化钠固体直接放在托盘天平的右盘进行称量
C.溶解氯化钠时用玻璃棒搅拌,其目的是增大氯化钠的溶解度
D.将配制好的溶液装瓶时,有少量液体洒出,会造成溶液的溶质质量分数偏小
【答案】A
【解析】A、所需氯化钠固体的质量为:50g×10%=5g,符合题意;
B、用托盘天平称量物品时,应遵循“左物右码”的原则,氯化钠应放在左盘上进行称量,且氯化钠固体
不能直接放在托盘上进行称量,应放在称量纸上进行称量,不符合题意;
C、溶解氯化钠时用玻璃棒搅拌,其目的是加快溶解速率,不能增大溶解度,不符合题意;
D、将配制好的溶液装瓶时,有少量液体洒出,溶液具有均一性,不会影响溶液的溶质质量分数的大小,
不符合题意。
故选A。
27.(2024·四川乐山·中考真题)实验室现有质量分数为8%的氯化钠溶液,但在实验中需要 质量分数
为4%的氯化钠溶液,某同学准备用8%的氯化钠溶液和蒸馏水(密度为 )进行配制.
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
回答下列问题:
(1)计算配制时需要8%的氯化钠溶液的质量为 g.
(2)量取蒸馏水时应选择量程为 (选填“10”、“20”或“50”) 的量筒.
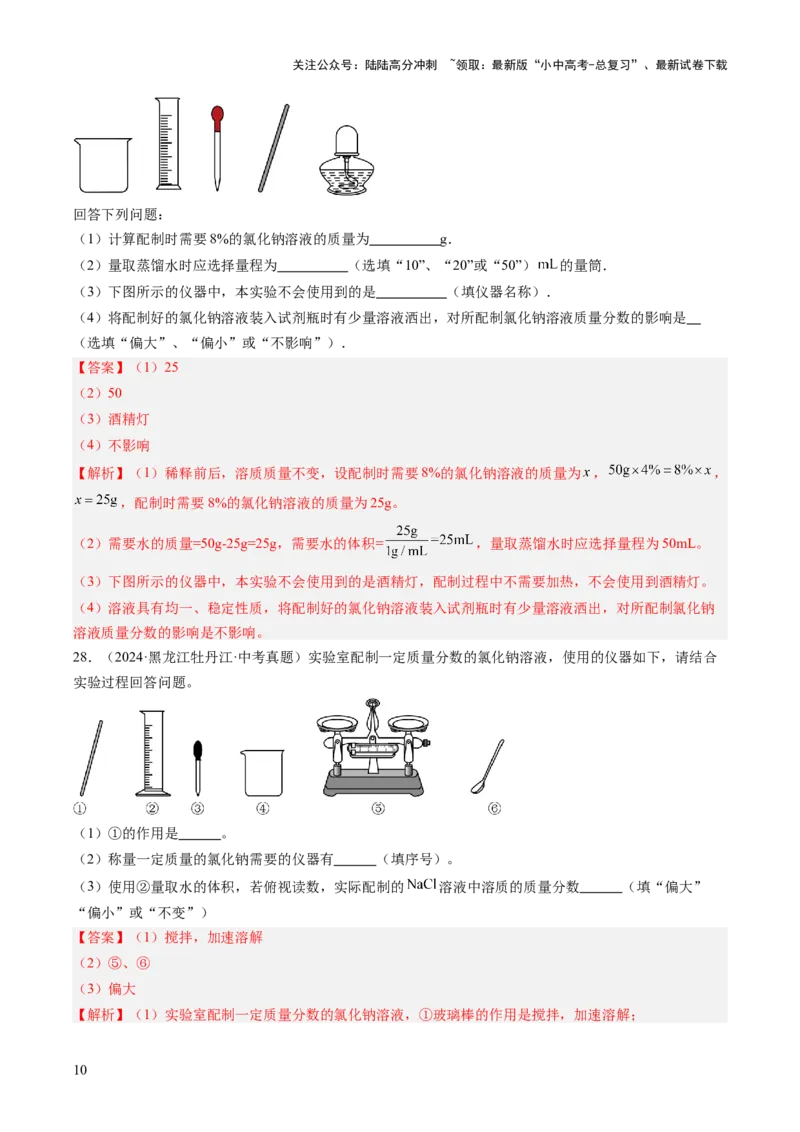
(3)下图所示的仪器中,本实验不会使用到的是 (填仪器名称).
(4)将配制好的氯化钠溶液装入试剂瓶时有少量溶液洒出,对所配制氯化钠溶液质量分数的影响是
(选填“偏大”、“偏小”或“不影响”).
【答案】(1)25
(2)50
(3)酒精灯
(4)不影响
【解析】(1)稀释前后,溶质质量不变,设配制时需要8%的氯化钠溶液的质量为 , ,
,配制时需要8%的氯化钠溶液的质量为25g。
(2)需要水的质量=50g-25g=25g,需要水的体积= ,量取蒸馏水时应选择量程为50mL。
(3)下图所示的仪器中,本实验不会使用到的是酒精灯,配制过程中不需要加热,不会使用到酒精灯。
(4)溶液具有均一、稳定性质,将配制好的氯化钠溶液装入试剂瓶时有少量溶液洒出,对所配制氯化钠
溶液质量分数的影响是不影响。
28.(2024·黑龙江牡丹江·中考真题)实验室配制一定质量分数的氯化钠溶液,使用的仪器如下,请结合
实验过程回答问题。
(1)①的作用是 。
(2)称量一定质量的氯化钠需要的仪器有 (填序号)。
(3)使用②量取水的体积,若俯视读数,实际配制的 溶液中溶质的质量分数 (填“偏大”
“偏小”或“不变”)
【答案】(1)搅拌,加速溶解
(2)⑤、⑥
(3)偏大
【解析】(1)实验室配制一定质量分数的氯化钠溶液,①玻璃棒的作用是搅拌,加速溶解;
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)称量一定质量的氯化钠需要的仪器有⑤托盘天平和⑥药匙;
(3)使用②量取水的体积,若俯视读数,读数偏大,则实际量取的水的体积偏小,导致实际配制的NaCl
溶液中溶质的质量分数偏大。
29.(2023·山东淄博·中考真题)某实验小组利用如下仪器配制500g10%的氯化钠溶液。回答下列问题:
(1)上图中缺少一种必须用到的玻璃仪器,它是 。
(2)配制500g10%的氯化钠溶液需要氯化钠的质量为 g。氯化钠溶液中的微观粒子有 (填粒
子符号)。
(3)配制好的氯化钠溶液取用一半后,剩余溶液中溶质的质量分数是 。
【答案】(1)烧杯
(2)50 Na+、Cl-、HO
2
(3)10%
【解析】(1)用固体配制一定溶质质量分数的溶液,实验步骤及所需仪器为:计算、称量(托盘天平、
药匙)、量取(量筒、胶头滴管)、溶解(烧杯、玻璃棒)、装瓶贴标签,故上图中缺少一种必须用到的
玻璃仪器,它是烧杯;
(2)需要氯化钠的质量为: ;
氯化钠溶液中含钠离子、氯离子、水分子,离子的表示方法:在该离子元素符号的右上角标上该离子所带
的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是在元素符号前面加
上相应的数字;故钠离子、氯离子表示为:Na+、Cl-,分子用化学式表示,故水分子表示为:HO;
2
(3)溶液具有均一性,配制好的氯化钠溶液取用一半后,剩余溶液中溶质的质量分数是10%。
30.(2022·辽宁朝阳·中考真题)某同学欲配制120g质量分数为10%的氯化钠溶液,请回答下列问题:
(1)需称取氯化钠的质量为 g。
(2)图示实验中,正确的操作顺序为 (填序号)。
(3)①若量取水的体积时仰视读数,其他操作均正确,则所配制溶液的溶质质量分数 (选填“偏
大”、“偏小”或“无影响”)。
②若称量氯化钠固体时托盘天平指针向右偏转,则应 直到天平平衡。
(4)欲配制60g质量分数为5%的氯化钠溶液,需要10%的氯化钠溶液的质量为 。
【答案】(1)12
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)②④⑤③①
(3)偏小 往左盘添加氯化钠
(4)30g
【解析】(1)由 可知,配制120g质量分数为10%的氯化钠溶液,需
称取氯化钠的质量为 。
(2)配制氯化钠溶液的步骤为首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取
水,最后进行溶解,故正确的操作顺序为②④⑤③①。
(3)①由 可知,若量取水的体积时仰视读数,读数偏小,实
际量取的水的体积偏大,配制的溶液的质量偏大,溶质质量不变,其他操作均正确,则所配制溶液的溶质
质量分数偏小。
②称量氯化钠固体时先要加好砝码,调节好游码,若称量氯化钠固体时托盘天平指针向右偏转,说明氯化
钠固体的量偏少,则应往左盘添加氯化钠直到天平平衡。
(4)溶液稀释前后溶质质量不变,配制60g质量分数为5%的氯化钠溶液,氯化钠的质量为
,需要10%的氯化钠溶液的质量为 。
考点04 溶解度
31.(2024·甘肃兰州·中考真题)如图是甲、乙两种物质在水中的溶解度曲线(不含结晶水),下列说法
正确的是( )
A.甲和乙的溶解度相等
B. ℃时,把20g乙加到50g水中,形成饱和溶液
C.若甲中混有少量的乙可采用蒸发结晶的方法提纯甲
D. ℃时甲的饱和溶液降温至 ℃,溶液中溶质的质量分数不变
【答案】B
【解析】A、由溶解度曲线图可知, ℃时甲和乙的溶解度相等,说法错误,不符合题意;
B、由溶解度曲线图可知, ℃时乙的溶解度为30g,则此温度下把20g乙加到50g水中,最多能溶解15g
乙,形成乙的饱和溶液,说法正确,符合题意;
C、由溶解度曲线图可知,甲的溶解度受温度变化影响较大,乙的溶解度受温度变化影响较小,若甲中混
有少量的乙可采用降温结晶的方法提纯甲,说法错误,不符合题意;
D、 ℃时甲的饱和溶液降温至 ℃,甲的溶解度减小,有晶体析出,甲的饱和溶液仍为饱和溶液,但溶
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
液中溶质质量分数变为 ℃时甲的饱和溶液的溶质质量分数,因此降温后溶液的溶质质量分数减小,说法
错误,不符合题意。
故选:B。
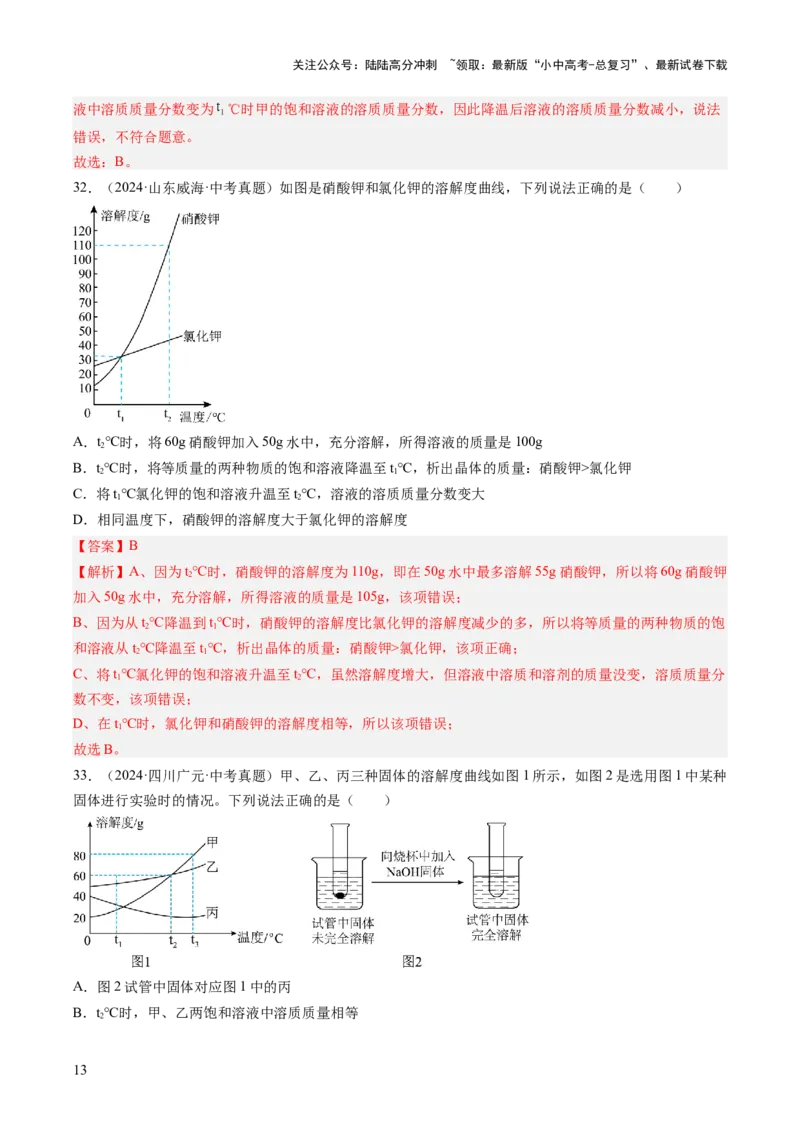
32.(2024·山东威海·中考真题)如图是硝酸钾和氯化钾的溶解度曲线,下列说法正确的是( )
A.t℃时,将60g硝酸钾加入50g水中,充分溶解,所得溶液的质量是100g
2
B.t℃时,将等质量的两种物质的饱和溶液降温至t℃,析出晶体的质量:硝酸钾>氯化钾
2 1
C.将t℃氯化钾的饱和溶液升温至t℃,溶液的溶质质量分数变大
1 2
D.相同温度下,硝酸钾的溶解度大于氯化钾的溶解度
【答案】B
【解析】A、因为t℃时,硝酸钾的溶解度为110g,即在50g水中最多溶解55g硝酸钾,所以将60g硝酸钾
2
加入50g水中,充分溶解,所得溶液的质量是105g,该项错误;
B、因为从t℃降温到t℃时,硝酸钾的溶解度比氯化钾的溶解度减少的多,所以将等质量的两种物质的饱
2 1
和溶液从t℃降温至t℃,析出晶体的质量:硝酸钾>氯化钾,该项正确;
2 1
C、将t℃氯化钾的饱和溶液升温至t℃,虽然溶解度增大,但溶液中溶质和溶剂的质量没变,溶质质量分
1 2
数不变,该项错误;
D、在t℃时,氯化钾和硝酸钾的溶解度相等,所以该项错误;
1
故选B。
33.(2024·四川广元·中考真题)甲、乙、丙三种固体的溶解度曲线如图1所示,如图2是选用图1中某种
固体进行实验时的情况。下列说法正确的是( )
A.图2试管中固体对应图1中的丙
B.t℃时,甲、乙两饱和溶液中溶质质量相等
2
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.t℃时,将40g甲加入到50g水中,所得溶液的溶质质量分数为80%
3
D.将等质量的甲、乙、丙饱和溶液从t℃降温到t℃,得到溶液的质量:丙>乙>甲
2 1
【答案】D
【解析】A、氢氧化钠固体溶于水放热,使温度升高,试管内的原来剩余的固体完全溶解,说明该物质的
溶解度随着温度的升高而增大,图2试管中固体对应的不可能是图1中的丙,故A错误;
B、选项说法没有指明饱和溶液的质量,则t℃时甲、乙两饱和溶液中溶质质量不一定相等,故B错误;
2
C、t℃时,甲的溶解度为80g,将40g甲加入到50g水中,最多能溶解40g,所得溶液的溶质质量分数
3
为: ,故C错误;
D、将等质量的甲、乙、丙饱和溶液从t℃降温到t℃,甲、乙的溶解度减小,有晶体析出,t℃时乙的溶
2 1 1
解度大于甲,甲析出晶体的质量大于乙,丙的溶解度随温度的降低而增大,没有晶体析出,则得到溶液的
质量:丙>乙>甲,故D正确。
故选:D。
34.(2024·河北·中考真题)如表是 和 在不同温度时的溶解度,小明用其中一种物质(X)进
行了如图所示的实验(水蒸发忽略不计)。下列分析错误的是( )
温度/℃ 20 40 60
31.6 63.9 110
溶解度/g
88.0 103 125
A.X为 B.③中溶液为X的不饱和溶液
C.④中溶液的质量为 D.溶液中溶质的质量分数:②=③>④
【答案】C
【解析】A、根据表格中的数据可知,40℃时,KNO 溶解度为63.9g,NaNO 溶解度为103g,根据分析可
3 3
知,X为NaNO ,说法正确,不符合题意;
3
B、根据分析可知,X为NaNO ,40℃时,NaNO 溶解度为103g,100g水加入100gNaNO 形成不饱和溶
3 3 3
液,分成两等分,其中一份是溶液③,则③中溶液为X的不饱和溶液,说法正确,不符合题意;
C、溶液④在降温之前是溶液②分成两等份中的其中一份,降温前的溶液中溶剂质量=100g× =50g,溶质
质量=100g× =50g,20℃时,NaNO 溶解度为88g,根据溶解度概念可知,20℃时,50g水中最多溶解
3
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
44gNaNO , 则的④中溶液的质量=50g+44g=94g,说法错误,符合题意;
3
D、溶液②中溶质的质量分数= ,溶液③是溶液②的一部分,根据溶液的均一性,
溶液③溶质质量分数=溶液②中溶质的质量分数=50%,根据C选项分析可知,溶液④中溶液质量=94g,溶
质质量=44g,溶质的质量分数= ,因此溶液中溶质的质量分数:②=③>④,说
法正确,不符合题意。
故选C。
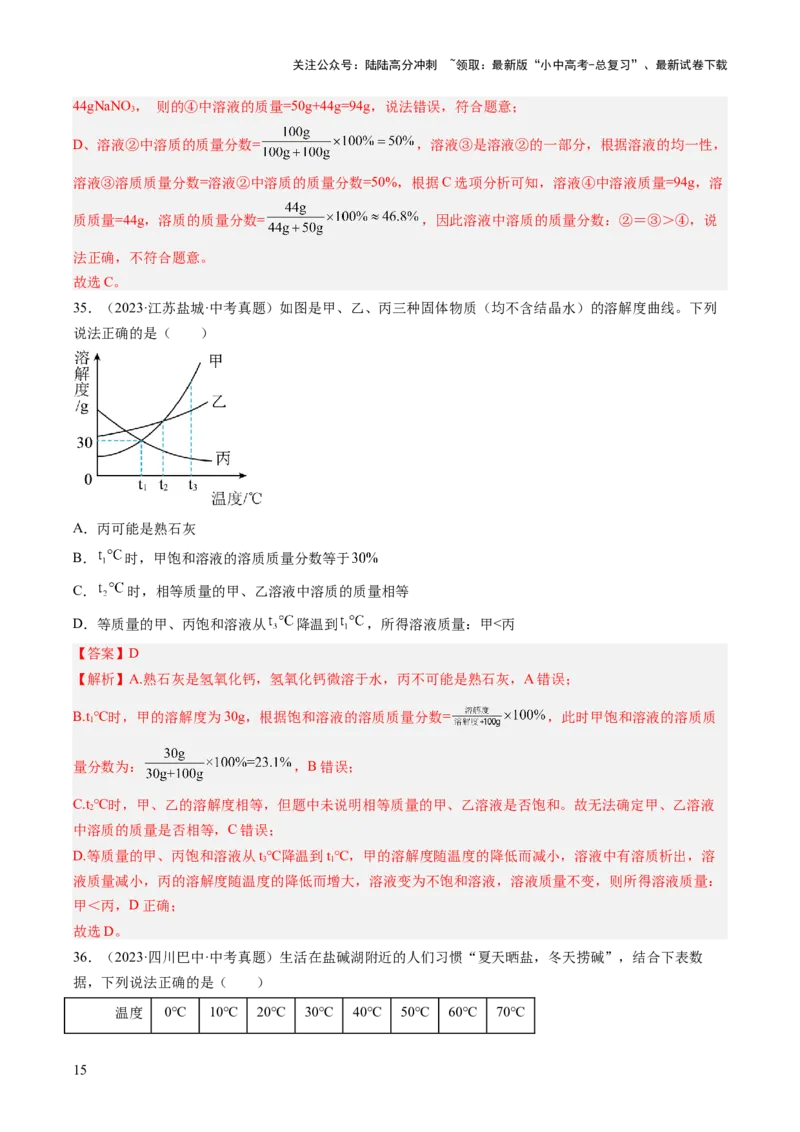
35.(2023·江苏盐城·中考真题)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。下列
说法正确的是( )
A.丙可能是熟石灰
B. 时,甲饱和溶液的溶质质量分数等于
C. 时,相等质量的甲、乙溶液中溶质的质量相等
D.等质量的甲、丙饱和溶液从 降温到 ,所得溶液质量:甲<丙
【答案】D
【解析】A.熟石灰是氢氧化钙,氢氧化钙微溶于水,丙不可能是熟石灰,A错误;
B.t℃时,甲的溶解度为30g,根据饱和溶液的溶质质量分数= ,此时甲饱和溶液的溶质质
1
量分数为: ,B错误;
C.t℃时,甲、乙的溶解度相等,但题中未说明相等质量的甲、乙溶液是否饱和。故无法确定甲、乙溶液
2
中溶质的质量是否相等,C错误;
D.等质量的甲、丙饱和溶液从t℃降温到t℃,甲的溶解度随温度的降低而减小,溶液中有溶质析出,溶
3 1
液质量减小,丙的溶解度随温度的降低而增大,溶液变为不饱和溶液,溶液质量不变,则所得溶液质量:
甲<丙,D正确;
故选D。
36.(2023·四川巴中·中考真题)生活在盐碱湖附近的人们习惯“夏天晒盐,冬天捞碱”,结合下表数
据,下列说法正确的是( )
温度 0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃ 70℃
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
溶解度物
质
氯化钠 35.7g 35.8g 36.0g 36.3g 36.6g 37.0g 37.3g 37.8g
碳酸钠 7.0g 12.2g 21.8g 39.7g 49.0g 48.7g 46.5g 45.8g
A.碳酸钠的溶解度比氯化钠大
B.“夏天晒盐,冬天捞碱”分别利用了蒸发结晶和降温结晶的原理
C.20℃时,将20g氯化钠加入50g水中,形成的溶液质量为70g
D.碳酸钠的溶解度随温度升高而增大
【答案】B
【解析】A、由表中数据知,温度小于20℃时,碳酸钠的溶解度比氯化钠小,温度大于20℃时,碳酸钠的
溶解度比氯化钠大,故A不符合题意;
B、由表中数据知,氯化钠的溶解度受温度影响较小,夏天温度高,水分蒸发快,氯化钠易结晶析出,碳
酸钠的溶解度受温度影响较大,冬天温度低,碳酸钠的溶解度减小,碳酸钠易结晶析出,所以“夏天晒
盐,冬天捞碱”分别利用了蒸发结晶和降温结晶的原理,故B符合题意;
C、由表中数据知,20℃时,氯化钠的溶解度为36g,则将20g氯化钠加入50g水中,只能溶解18g氯化
钠,形成的溶液质量为68g,故C不符合题意;
D、由表中数据知,40℃时碳酸钠的溶解度最大,温度小于40℃时,碳酸钠的溶解度随温度升高而增大,
温度大于40℃时,碳酸钠的溶解度随温度升高而减小,故D不符合题意。
故选B。
37.(2022·四川广元·中考真题)溶解度曲线反映了溶解度随温度的变化规律。如图是甲、乙、丙三种固
体物质(不含结晶水)的溶解度曲线图,下列说法正确的是( )
A. ℃时,甲、乙两种物质的溶液中溶质的质量分数相等
B. ℃时,100g甲的饱和溶液中甲的质量为25g
C.将丙的饱和溶液转化为不饱和溶液可采用升温的方法
D.将 ℃时等质量的甲、乙、丙三种物质的饱和溶液降温到 ℃,析出晶体最多的是甲
【答案】D
【解析】A、t℃时,甲、乙两种物质溶解度相同,其饱和溶液的溶质质量分数相同,选项未标明甲、乙两
2
物质是否饱和状态,故选项错误;
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B、t℃时,甲物质的溶解度为25g,100g甲的饱和溶液中的甲的质量为: ,
1
故选项计算错误;
C、根据丙物质的溶解度曲线可知,随温度升高溶解度下降,将丙的饱和溶液转化为不饱和溶液应采用降
温的方法,故选项错误;
D、由图可知,将t℃时等质量的甲、乙、丙三种物质的饱和溶液降温到t℃,丙物质溶解度升高,溶质无
2 1
析出,甲、乙两物质溶解度下降,有溶质析出,其中甲溶解度下降幅度大,因此析出晶体最多的是甲,故
选项正确。
故选D。
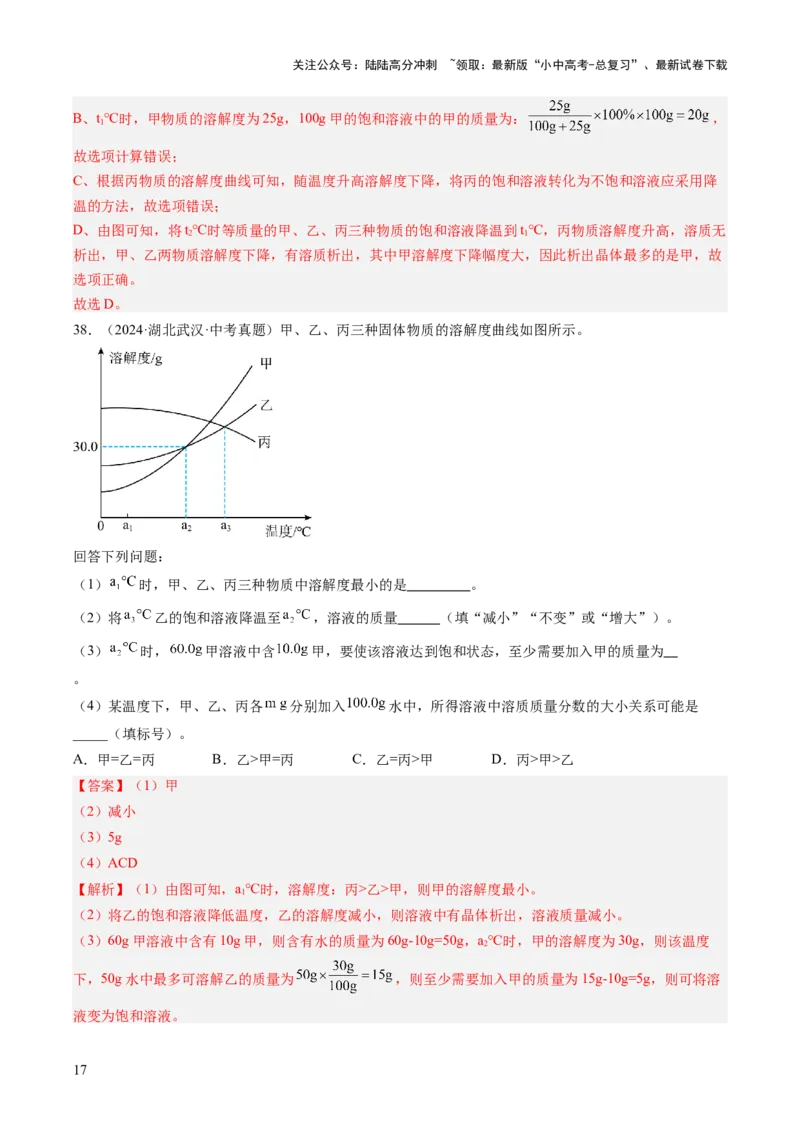
38.(2024·湖北武汉·中考真题)甲、乙、丙三种固体物质的溶解度曲线如图所示。
回答下列问题:
(1) 时,甲、乙、丙三种物质中溶解度最小的是 。
(2)将 乙的饱和溶液降温至 ,溶液的质量 (填“减小”“不变”或“增大”)。
(3) 时, 甲溶液中含 甲,要使该溶液达到饱和状态,至少需要加入甲的质量为
。
(4)某温度下,甲、乙、丙各 分别加入 水中,所得溶液中溶质质量分数的大小关系可能是
_____(填标号)。
A.甲=乙=丙 B.乙>甲=丙 C.乙=丙>甲 D.丙>甲>乙
【答案】(1)甲
(2)减小
(3)5g
(4)ACD
【解析】(1)由图可知,a℃时,溶解度:丙>乙>甲,则甲的溶解度最小。
1
(2)将乙的饱和溶液降低温度,乙的溶解度减小,则溶液中有晶体析出,溶液质量减小。
(3)60g甲溶液中含有10g甲,则含有水的质量为60g-10g=50g,a℃时,甲的溶解度为30g,则该温度
2
下,50g水中最多可溶解乙的质量为 ,则至少需要加入甲的质量为15g-10g=5g,则可将溶
液变为饱和溶液。
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)A、若加入的固体完全溶解,则所得溶液中溶质质量分数相等,该选项符合题意;
B、当温度低于a℃时,乙的溶解度小于丙,当温度高于a℃时,乙的溶解度小于甲,则所得溶液中,不
3 2
可能乙的溶解度最大,该选项不符合题意;
C、当温度低于a℃时,溶解度:丙>乙>甲,则若甲中固体没有完全溶解,乙、丙中固体完全溶解,则溶
2
质质量分数:乙=丙>甲,该选项符合题意;
D、由图可知,当温度刚大于a℃时,溶解度丙>甲>乙,则所得溶液的溶质质量分数可能为丙>甲>乙,该
2
选项符合题意。
故选ACD。
39.(2024·天津·中考真题)溶液与人类的生产、生活密切相关。
(1)下列物质分别放入水中,能形成溶液的是______(填序号)。
A.食盐 B.面粉 C.泥沙
(2)氯化铵和硝酸钾在不同温度时的溶解度如表。
温度/℃ 10 20 30 40 50 60 70
NH Cl 33.3 37.2 41.4 45.8 50.4 55.2 60.2
4
溶解度/g
KNO 20.9 31.6 45.8 63.9 85.5 110 138
3
①10℃时,氯化铵的溶解度为 g。
②20℃时,将20g氯化铵加入到100g水中,充分搅拌后所得溶液为 溶液(填“饱和”或“不饱
和”)。
③60℃时,将60g硝酸钾溶于50g水中,充分溶解后,所得溶液的质量为 g。
④将60℃相同质量的氯化铵饱和溶液和硝酸钾饱和溶液分别降温至20℃时,析出晶体的质量:氯化铵
硝酸钾(填“大于”、“等于”或“小于”)。
⑤20℃时,向50g质量分数为12%的硝酸钾溶液中加入5g硝酸钾固体,完全溶解,所得溶液中溶质的质量
分数为 。
【答案】(1)A
(2)33.3 不饱和 105 小于 20%
【解析】(1)A、食盐溶于水,形成溶液,故A正确;
B、面粉不溶于水,形成悬浊液,故B错误;
C、泥沙不溶于水,形成悬浊液,故C错误;
故选A;
(2)①从表中可知:10℃时,氯化铵的溶解度为33.3g;
②20℃时,氯化铵的溶解度为37.2g,即100g水中最多能溶解氯化铵37.2g,将20g氯化铵加入到100g水
中,得到不饱和溶液;
③60℃时,氯化铵的溶解度为110g,即100g水中最多能溶解氯化铵110g,将60g氯化铵加入到50g水
中,最多能溶解55g,所得溶液的质量为55g+50g=105g;
④从表中可知,硝酸钾的溶解度受温度影响变化较大,氯化铵的溶解度受温度影响变化较小,故将60℃相
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
同质量的氯化铵饱和溶液和硝酸钾饱和溶液分别降温至20℃时,析出晶体的质量:氯化铵小于硝酸钾;
⑤所得溶液中溶质的质量分数为 。
40.(2023·四川甘孜·中考真题) 和 在不同温度时的溶解度如下表:
温度 20 30 40 50 60
37.2 41.4 45.8 50.4 55.2
溶解度
31.6 45.8 63.9 85.5 110
回答下列问题:
(1) 时, 的溶解度是 。
(2)要将接近饱和的 溶液变为饱和溶液,可采用的方法是 (填一条)。
(3) 时,向 水中加入 ,充分溶解后,所得溶液的质量是 。
(4) 和 的溶解度受温度影响较大的是 。
(5) 和 具有相同溶解度的温度范围是 。
【答案】(1)
(2)加入 或降低温度或蒸发水
(3)
(4)硝酸钾/
(5)30
【解析】(1)根据表格中的数据可知,20℃时,NH4Cl的溶解度是37.2g。
(2)要将接近饱和的NH4Cl溶液变为饱和溶液,可采用的方法是继续向溶液中加入氯化铵固体;氯化
铵的溶解度随温度降低而减小,降低温度可减小其溶解度,使溶液变为饱和;蒸发掉部分溶剂;
(3)在 40°C 时,硝酸钾的溶解度约为 63.9g;即 100g 水中最多能溶解 63.9g 硝酸钾,向 100g 水中
加入 70g 硝酸钾,只能溶解 63.9g,充分溶解后所得溶液的质量= 100g+63.9g=163.9g;
(4)根据表格中的数据可知,NH Cl和KNO 的溶解度受温度影响较大的是硝酸钾(或KNO);
4 3 3
(5)根据表格中的数据可知,氯化铵在 20°C 时溶解度约为 37.2g,硝酸钾在 20°C 时溶解度约为
31.6g,氯化铵在30°C 时溶解度约为 41.4g,硝酸钾在30°C 时溶解度约为 45.8g;和KNO 具有
3
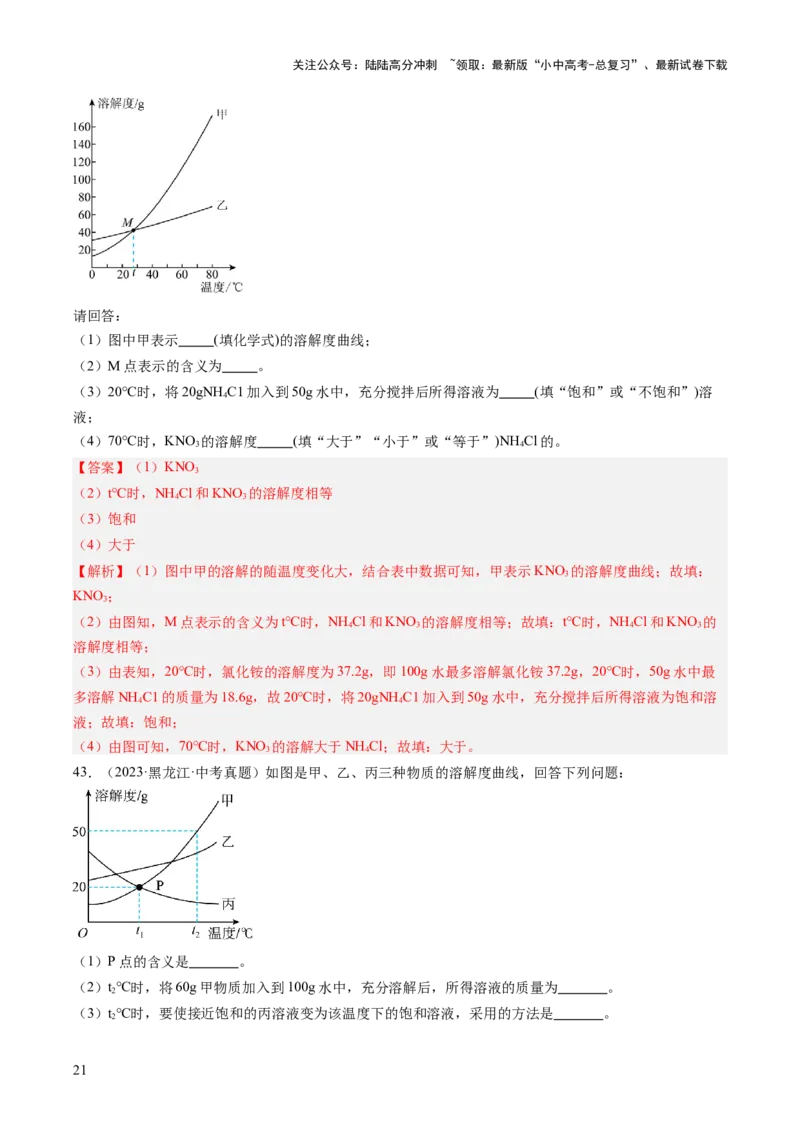
相同溶解度的温度范围是20℃甲>丙
C.析出晶体质量最多的是甲
【答案】(1)t℃,甲、丙的溶解度相等,都为20g
1
(2)150g
(3)加入溶质丙或恒温蒸发溶剂水
(4)降温结晶
(5)BC
【解析】(1)P点是甲、丙溶解度曲线的交点,含义是t℃,甲、丙的溶解度相等,都为20g。
1
(2)t℃时,甲的溶解度为50g,则将60g甲物质加入到100g水中最多溶解50g甲,得到溶液的质量为
2
50g+100g=150g。
(3)变为该温度下的饱和溶液说明不能使用改变温度的方法。将丙的不饱和溶液转化为饱和溶液可以加
入溶质丙或恒温蒸发溶剂水。
(4)甲、乙溶解度都随温度的升高而升高,甲受温度影响较大,乙受温度影响不大。所以甲中含有少量
乙时,最好采用降温结晶的方法提纯甲。
(5)A、甲、乙溶解度随温度的降低而降低,丙的溶解度随温度的降低而升高。所以降温后得到甲、乙的
饱和溶液,丙的不饱和溶液。错误;
B、t℃时溶解度乙>甲=丙,则该温度饱和溶液的溶质质量分数乙>甲=丙,而降温后得到甲、乙饱和溶
1
液,丙的不饱和溶液,则所得溶液的溶质质量分数乙>甲>丙,正确;
C、只有甲、乙有晶体析出,降温后甲溶解度变为比乙大,且甲、乙饱和溶液的质量相等,则降温后析出
晶体质量最多的是甲,正确;
故选BC。
44.(2022·四川甘孜·中考真题)硝酸钾和氯化钾的溶解度曲线如图所示,回答下列问题:
(1)10℃时,硝酸钾的溶解度 (填“>”“<”或“=”)氯化钾的溶解度。
(2)40℃时,将45g氯化钾加入100g水中,所得溶液为 (填“饱和”或“不饱和”)溶液。
(3)配制50g质量分数为15%的氯化钾溶液,实验步骤为:
①计算:需要氯化钾 g,水 mL(水的密度可近似看做1g/mL)。
②称量:用托盘天平称取所需氯化钾,放入烧杯中。
22关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
③量取:量取水时,最好选择 (填“10”“50”或“100”)mL的量筒。
④溶解:玻璃棒的作用是 。
【答案】(1)<
(2)饱和
(3)7.5 42.5 50 加速溶解
【解析】(1)分析图像,10℃时,硝酸钾的溶解度<氯化钾的溶解度;
(2)40℃时,氯化钾的溶解度是40g,则将45g氯化钾加入100g水中,最多溶解40g,则所得溶液为饱和
溶液;
(3)①根据溶质质量=溶液质量×溶质质量分数,氯化钾固体的质量为50×15%=7.5g,水就是
50g-7.5g=42.5g,体积为42.5mL;
③选用量筒需要就近原则,水的体积是42.5mL,故选50mL的量筒;
④溶解时玻璃棒搅拌,作用是加速溶解。
45.(2022·四川资阳·中考真题)盐是一类重要的化合物,研究其性质有十分重要的意义、如图是KNO、
3
NaCl、NH Cl三种物质的溶解度曲线,回答下列问题:
4
(1)“春播一粒种,秋收万粒粟”,春耕之时,施肥可提高农作物产量,题干中的物质属于复合肥料的
是 。(填名称)
(2)40℃时,KNO 的溶解度是 。
3
(3)40℃时,在盛有45.0g水的烧杯中加入5.0gNHCl,充分搅拌后,所得溶液的溶质质量分数为
4
。
(4)下列说法不正确的是______。
A.KNO 的浓溶液一定是KNO 的饱和溶液
3 3
B.40℃时溶解等质量的三种物质,NaCl消耗的水最多
C.a点表示KNO 和NaCl的溶解度相等
3
【答案】(1)硝酸钾
(2)63.9g
(3)10%
(4)AC
【解析】(1)KNO 中含有氮、磷、钾中的氮元素与钾元素,属于复合肥;NaCl中不含氮、磷、钾,不是
3
化肥;NH Cl中只含氮、磷、钾中的氮元素,属于氮肥;故填:硝酸钾。
4
(2)由溶解度曲线可知,40°C时,KNO 的溶解度是63.9g,故填:63.9g。
3
23关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)由溶解度曲线可知,40°C时,NH Cl的溶解度为45.8g,则40°C时,在盛有45.0g水的烧杯中加入
4
5.0gNHCl,充分搅拌后能完全溶解,所得溶液的溶质质量分数为 ,故填:
4
10%。
(4)A、溶液的浓稀与溶液的饱和和不饱和没有关系,因此KNO 的浓溶液不一定是 KNO 的饱和溶液,
3 3
说法错误;
B、40°C时,氯化钠的溶解度最小,因此该温度下溶解等质量的三种物质,NaCl消耗的水最多,说法正
确;
C、溶解度一定要指明温度,不能说a点表示 KNO 和NaCl的溶解度相等,说法错误。
3
故填:AC。
24