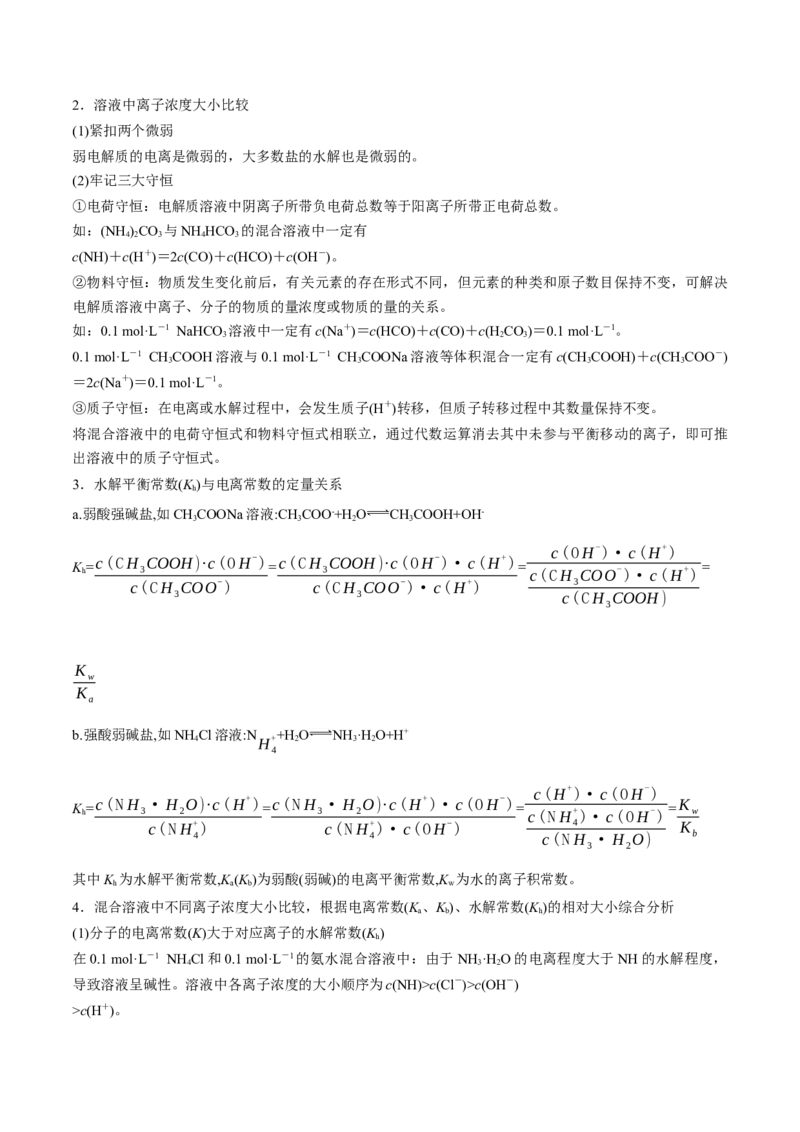文档内容
押江苏卷第 12 题
电解质溶液综合选择题
核心考点 考情统计 考向预测 备考策略
1.三大平衡的影响因素;以电离
平衡常数为载体考查电解质的强弱
2023·江苏卷,12
能利用平衡移动原理分析外界条件 及对应盐的水解强弱和相关计算;
电解质溶液综 2022·江苏卷,12 改变对溶液中电离平衡、水解平 以酸碱中和滴定为载体,考查
合选择题 衡、溶解平衡产生的影响。从解题 “强”滴“弱”过程中微粒浓度的
2021·江苏卷,11 方法的角度讲,物料守恒、电荷守 变化以及其他相关知识;
恒、质子守恒等变形是命题的热点
2021·江苏卷,13
2.以图像为载体,考查微粒浓度
关系和三大守恒定律的运用
1.(2023·江苏,12)室温下,用含少量 的 溶液制备 的过程如题图所示。已知
, 。下列说法正确的是
A. 溶液中:
B.“除镁”得到的上层清液中:C. 溶液中:
D.“沉锰”后的滤液中:
【答案】C
【解析】 溶液中存在电荷守恒: ,A错误;“除镁”得到
的上层清液中为 的饱和溶液,有 ,故 ,B错误;
溶液中存在质子守恒: ,故
,C正确;“沉锰”后的滤液中还存在F-、 等离子,故电荷守
恒中应增加其他离子使等式成立,D错误。
2.(2022·江苏,12)一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收CO,若通
2 2
入CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(H CO)+c( )+c(
2 2 总 2 3
)。HCO 电离常数分别为K =4.4×10-7、K =4.4×10-11。下列说法正确的是
2 3 a1 a2
A.KOH吸收CO 所得到的溶液中:c(H CO)>c( )
2 2 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c( )+c(H CO)
2 3 2 3
C.KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c( )
2 总 2 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降【答案】C
【解析】KOH吸收CO 所得到的溶液,若为NaCO 溶液,则 主要发生第一步水解,溶液中:
2 2 3
c(H CO)<c( ),若为NaHCO 溶液,则 发生水解的程度很小,溶液中:c(H CO)<c( ),A
2 3 3 2 3
不正确;KOH完全转化为KCO 时,依据电荷守恒,溶液中:c(K+)+ c(H+)=c(OH-)+ +c( )+2c(
2 3
),依据物料守恒,溶液中:c(K+)=2[c( )+c( )+c(H CO)],则c(OH-)= c(H+)+c( )
2 3
+2c(H CO),B不正确;KOH溶液吸收CO,c(KOH)=0.1mol∙L-1,c =0.1mol∙L-1,则溶液为KHCO 溶液,
2 3 2 总 3
K = = ≈2.3×10-8>K =4.4×10-11,表明 以水解为主,所以溶液中:c(H CO)>c( ),C
h2 a2 2 3
正确;如图所示的“吸收”“转化”过程中,发生反应为:CO+2KOH=K CO+H O、
2 2 3 2
KCO+CaO+H O=CaCO ↓+2KOH(若生成KHCO 或KCO 与KHCO 的混合物,则原理相同),二式相加得:
2 3 2 3 3 2 3 3
CO+CaO=CaCO ↓,该反应放热,溶液的温度升高,D不正确。
2 3
3.(2021·江苏,11)室温下,通过下列实验探究NaHCO 、NaCO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1mol·L-1NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1mol·L-1NaHCO 溶液与0.1mol·L-1CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:向0.1mol·L-1NaCO 溶液中通入CO,溶液pH从12下降到约为9
2 3 2
实验4:向0.1mol·L-1NaCO 溶液中滴加新制饱和氯水,氯水颜色褪去
2 3
下列说法正确的是
A.由实验1可得出:K (H CO)>
a2 2 3
B.实验2中两溶液混合时有:c(Ca2+)·c(CO ) ×104
4 3
C.过滤后所得清液中一定存在:c(Ca2+)= 且c(Ca2+)≤
D.滤渣中加入醋酸发生反应的离子方程式:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
【答案】C
【解析】0.5mol·L-1NaCO 溶液中存在质子守恒:c(OH-)=c(H+)+c(HCO )+2c(H CO),A错误;该反应的平
2 3 2 3衡常数K= = = = = ×104,当浓度商 <K时,反应正向进行,B
错误;上层清液为碳酸钙的保护溶液,所以清液中满足c(Ca2+)= ,由于硫酸钙沉淀转化为碳酸
钙沉淀,所以清液为硫酸钙的不饱和溶液,则c(Ca2+)≤ ,C正确;醋酸为弱酸,不能拆成离子
形式,D错误。
1.三大平衡及影响因素
水解平衡CHCOO-+ 沉淀溶解平衡AgCl(s)
3
电离平CHCOOH
3
平衡类型 HO CHCOOH+
2 3
CHCOO-+H+
3
OH- Ag+(aq)+Cl-(aq)
研究对象 弱电解质溶液 能水解的盐溶液 难溶电解质
若难溶物
若难溶物的
的溶解度
溶解度与温
与温度成
K 度成正比,
a
升温 促进电离 促进水解 K 增大 正比,促
h
增大 K 增大;
sp
进溶解;
反之,则
反之,则
K 减小
sp
抑制溶解
影
K
a
响 加水 促进电离 促进水解 K h 不变 促进溶解 K sp 不变
不变
因
加入 加入 加入
素
加入相 CHCOONa K CHCOOH或 AgNO 或
3 a 3 3
K 不变 K 不变
h sp
应离子 或盐酸,抑 不变 NaOH,抑制 NaCl,抑
制电离 水解 制溶解
加入反
加入氨
应离子 加入OH-, K 不 加入H+,促
a
K 不变 水,促进 K 不变
h sp
(或物 促进电离 变 进水解
溶解
质)2.溶液中离子浓度大小比较
(1)紧扣两个微弱
弱电解质的电离是微弱的,大多数盐的水解也是微弱的。
(2)牢记三大守恒
①电荷守恒:电解质溶液中阴离子所带负电荷总数等于阳离子所带正电荷总数。
如:(NH )CO 与NH HCO 的混合溶液中一定有
4 2 3 4 3
c(NH)+c(H+)=2c(CO)+c(HCO)+c(OH-)。
②物料守恒:物质发生变化前后,有关元素的存在形式不同,但元素的种类和原子数目保持不变,可解决
电解质溶液中离子、分子的物质的量浓度或物质的量的关系。
如:0.1 mol·L-1 NaHCO 溶液中一定有c(Na+)=c(HCO)+c(CO)+c(H CO)=0.1 mol·L-1。
3 2 3
0.1 mol·L-1 CHCOOH溶液与0.1 mol·L-1 CHCOONa溶液等体积混合一定有c(CHCOOH)+c(CHCOO-)
3 3 3 3
=2c(Na+)=0.1 mol·L-1。
③质子守恒:在电离或水解过程中,会发生质子(H+)转移,但质子转移过程中其数量保持不变。
将混合溶液中的电荷守恒式和物料守恒式相联立,通过代数运算消去其中未参与平衡移动的离子,即可推
出溶液中的质子守恒式。
3.水解平衡常数(K )与电离常数的定量关系
h
a.弱酸强碱盐,如CHCOONa溶液:CH COO-+H O CHCOOH+OH-
3 3 2 3
c(OH-)·c(H+)
K h =
c(CH
3
COOH)·c(OH-)
=
c(CH
3
COOH)·c(OH-)·c(H+)
= c(CH COO-)·c(H+) =
c(CH COO-) c(CH COO-)·c(H+) 3
3 3 c(CH COOH)
3
K
w
K
a
b.强酸弱碱盐,如NH Cl溶液:N +H O NH ·H O+H+
4 H+ 2 3 2
4
c(H+)·c(OH-)
K h =
c(NH
3
·H
2
O)·c(H+)
=
c(NH
3
·H
2
O)·c(H+)·c(OH-)
= c(NH+)·c(OH-) =
K
w
c(NH+) c(NH+)·c(OH-) 4 K
4 4 c(NH ·H O) b
3 2
其中K 为水解平衡常数,K(K )为弱酸(弱碱)的电离平衡常数,K 为水的离子积常数。
h a b w
4.混合溶液中不同离子浓度大小比较,根据电离常数(K、K )、水解常数(K )的相对大小综合分析
a b h
(1)分子的电离常数(K)大于对应离子的水解常数(K )
h
在0.1 mol·L-1 NH Cl和0.1 mol·L-1的氨水混合溶液中:由于NH ·H O的电离程度大于NH的水解程度,
4 3 2
导致溶液呈碱性。溶液中各离子浓度的大小顺序为c(NH)>c(Cl-)>c(OH-)
>c(H+)。(2)分子的电离常数(K)小于对应离子的水解常数(K )
h
在0.1 mol·L-1的HCN和0.1 mol·L-1的NaCN混合溶液中:由于HCN的电离程度小于CN-的水解程度,
导致溶液呈碱性。溶液中各离子浓度的大小顺序为c(Na+)>c(CN-)>c(OH-)>
c(H+),且c(HCN)>c(Na+)=0.1 mol·L-1。
考点 电解质溶液综合选择题
1.(2024·江苏南京六校联合体8月调研,12)硫代硫酸钠( )的制备和应用相关流程如图所示。
已知:25℃时, 的 , ; 的 ,
下列说法正确的是
A.步骤1所得的溶液中:
B.步骤1过程中pH=8时,
C.步骤3所得的清液中:
D.步骤3的离子方程式为:
【答案】D
【解析】步骤1中是向NaCO 溶液中加入NaHSO 溶液得到NaSO 溶液,碳酸的一级电离常数大于亚硫酸
2 3 3 2 3
的二级电离常数,产物为亚硫酸钠和碳酸氢钠,根据物料守恒式可知钠离子浓度大于二倍的含硫微粒浓度
和,A错误;假设等式成立,对其进行变形 ,即 ,此时溶液pH=8即 ,代入数据计算 ,因此该等式不成立,B错误;
步骤3所得是清液,说明没有沉淀生成,则 ,故C错误;步骤3中生成配合物
使沉淀溶解,反应的离子方程式为: ,D正确。
2.(2024·江苏百师联盟高三开学考试,12)已知常温下水溶液中 的分布分数
[如 、 ]随 变化曲线如图所示。将
溶液滴入 溶液中,过程中溶液变浑浊。
已知: ; 。下列说法正确的是
A.曲线 表示
B.水解平衡常数
C.反应过程溶液中始终存在:
D.恰好完全反应后溶液 ,则
【答案】B
【解析】由题中信息可知, 为二元弱酸,电离平衡为 ,用溶液滴定 溶液,发生反应: ,则
酸性强弱: ,所以曲线 表示 的各微粒分布曲线,曲线 代表 ,曲线 代表
,曲线 代表 ,曲线 为 ,曲线 为 。根据分析可知,曲线 表示 ,A
错误; 的水解平衡常数 ,曲线 和 相交时 ,此时
,则 ,B正确;随着 溶液的滴入,
产生 沉淀而析出,溶液中 ,根据电荷守恒:
,则 ,
C错误;恰好完全反应后溶液中 ,由
可知当 时, ,则
,D错误。
3.(2024·江苏扬州期末检测,12)从炼钢粉尘(主要含ZnO、ZnFe O )中回收锌的过程如题12图所示。
2 4
“浸取”过程ZnO转化为[Zn(NH )]2+,并有少量铁元素浸出。已知:25 ℃ K (NH ·HO) = 2×10−5,K
3 4 b 3 2 sp
(ZnS) = 1×10−23。下列说法正确的是
A.25 ℃,pH = 9的NH ·HO /NHCl溶液中:
3 2 4= 2×104
B.0.1 mol·L−1 (NH )S溶液中:c(H+)+c(HS-)+2c(H S) = c(NH ·H O)+c(OH-)
4 2 2 3 2
C.“沉锌”过程中,溶液的pH减小
D.“沉锌”后的溶液中:c(Zn2+)·c(S2−)<1×10−23
【答案】B
【解析】K (NH ·HO) =, =,由于该溶液pH=9,则c(OH-)=10-5mol·L-1, = =2,A项错误;根据质子守
b 3 2
恒可知,B项正确;[Zn(NH )]2+与(NH )S的离子方程式为[Zn(NH )]2++S2-+4H O=ZnS↓+4NH ·H O,则反
3 4 4 2 3 4 2 3 2
应后溶液碱性增强,C项错误;沉锌”后的溶液为ZnS的饱和溶液,c(Zn2+)·c(S2−)= K (ZnS) = 1×10−23,D
sp
项错误。
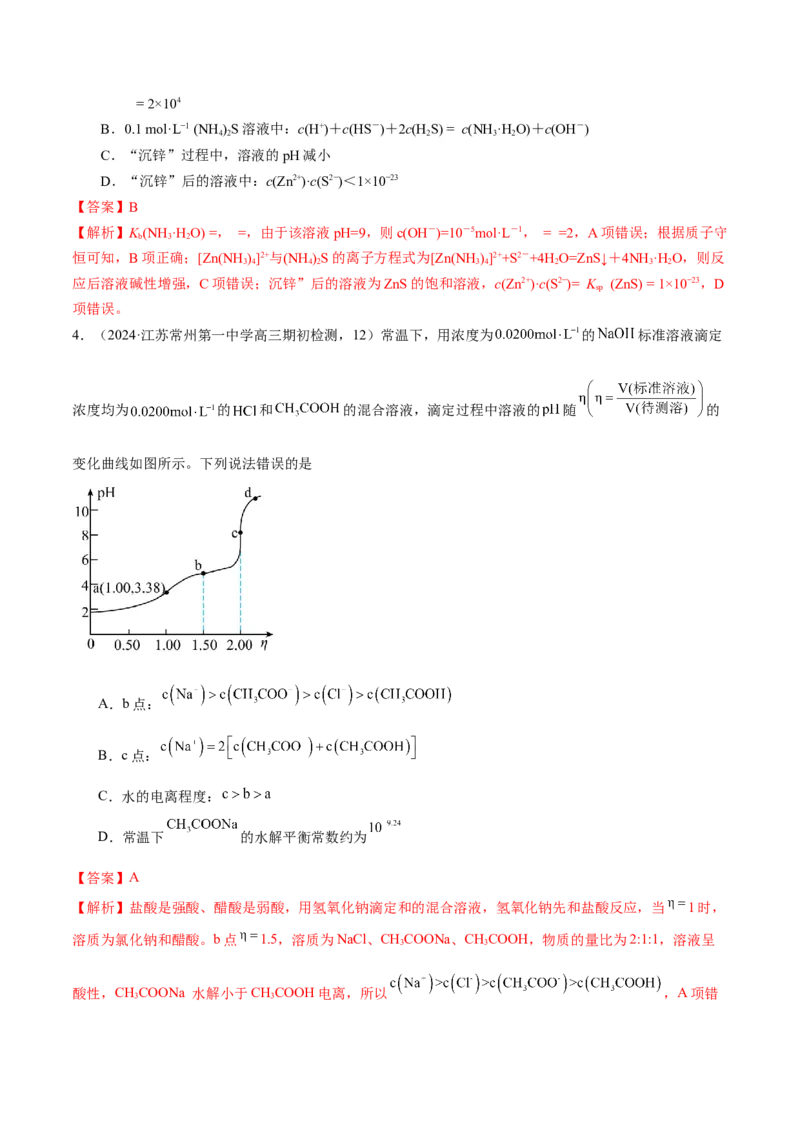
4.(2024·江苏常州第一中学高三期初检测,12)常温下,用浓度为 的 标准溶液滴定
浓度均为 的 和 的混合溶液,滴定过程中溶液的 随 的
变化曲线如图所示。下列说法错误的是
A.b点:
B.c点:
C.水的电离程度:
D.常温下 的水解平衡常数约为
【答案】A
【解析】盐酸是强酸、醋酸是弱酸,用氢氧化钠滴定和的混合溶液,氢氧化钠先和盐酸反应,当 1时,
溶质为氯化钠和醋酸。b点 1.5,溶质为NaCl、CHCOONa、CHCOOH,物质的量比为2:1:1,溶液呈
3 3
酸性,CHCOONa 水解小于CHCOOH电离,所以 ,A项错
3 3误;c点 2,溶质为等物质的量的NaCl、CHCOONa,根据物料守恒
3
,B项正确; c点溶质为NaCl、CHCOONa,CHCOONa水解
3 3
促进水电离,c点之前越小,剩余的酸越多,对电离的抑制作用越大,所以水的电离程度: ,C项
正确;a点 1,溶质是浓度均为0.01mol/L的NaCl、CHCOOH,醋酸电离使溶液呈酸性,pH=3.38,则
3
,常温下的水解平衡常数约为 ,D
项正确。
5.(2024·江苏苏州高三期末,12)用含少量Ca2+、Mg2+的CoCl 溶液制备CoO的过程如图所示。已知:
2
室温下,K (MgF )=5×10-11,K (CaF )=5×10-9,K(HF)=6.3×10-4,K (NH ·H O)=1.8×10-5。下列说法
sp 2 sp 2 a b 3 2
正确的是( )
A. 0.1 mol·L-1 NH F溶液呈酸性,且c(NH)2c(C O)+2c(HC O)+2c(H C O)
4 2 2 4 2 2 2 2 4
D. 若将流程中(NH )C O 换成NaC O,则制得的CoO纯度更高
4 2 2 4 2 2 4
【答案】A
【解析】CoCl 溶液中含有少量 Ca2+和Mg2+,加入NH F沉淀Ca2+和Mg2+,在使用(NH )C O 沉钴得到
2 4 3 2 2 4
CoC O ,最后灼烧得到CoO。NH F溶液呈酸性,说明NH水解程度大,所以c(NH)1,即c(HC O)> c(H C O),A项正确;根据电荷守恒:c(NH)+
a1 2 2 4 2 2 2 4
2c(Fe2+)+c(H+)=2c(SO)+c(OH-),溶液显酸性,则c(H+)> c(OH-),则c(NH)+2c(Fe2+)<2c(SO),B项正确;
上层清液中存在Fe2+和C O,C O也能够被酸性KMnO 溶液氧化,对Fe2+的检验有干扰,C项错误;乙醇
2 2 4
易挥发,容易干燥晶体,D项正确。
8.(2024·江苏南通海安高三开学考试,13) 是一种重要的催化剂。以 为原料制备
的反应方程式为: 。已知室温下: 、
。下列说法正确的是
A.为确认 已完全沉淀,将反应后的混合物静置,向上层清液中加 溶液,观察是否有沉淀
产生
B.为获得纯度较高的 ,可向 溶液中滴加 溶液
C.0.1mol/L 溶液中存在
D.加水稀释一定浓度的 溶液,溶液中的 值逐渐变小
【答案】B
【解析】若加 CaCl 溶液,则会引入新的杂质 NaCl,应向上层清液中继续滴加 CuSO 溶液,A错误;
2 4
NaC O 与CuSO 发生反应NaC O +CuSO =CuC O↓+NaSO ,过滤得到CuC O 固体,B正确;NaC O
2 2 4 4 2 2 4 4 2 4 2 4 2 4 2 2 4
溶液中存在质子守恒有 c(OH-)=c(H+)+2c(HC O)+c(HC O),C 错误;HC O的水解平衡常数为 K=
2 2 4 2 2 h,HC O的电离大于水解,NaHC O 溶液呈酸性,酸性溶液稀释时,c(H+)减小,由于
2 2 4
不变,则溶液中的 值逐渐增大,D错误。
9.(2024·江苏前黄高级中学期中适应性考试,12)室温下,通过下列实验探究NaHCO 、NaCO 溶液的
3 2 3
性质。
实验1:用pH试纸测量0.1mol•L-1NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1mol•L-1NaHCO 溶液与0.1mol•L-1CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:饱和NaCO 溶液中通入CO 产生白色沉淀,溶液pH从12下降到约为9
2 3 2
实验4:0.1mol•L-1NaHCO 溶液中滴加新制饱和氯水,氯水颜色褪去并有气泡
3
下列说法正确的是
A.由实验1可得出:K (H CO)∙K (H CO)<10-16
a1 2 3 a2 2 3
B.实验2中两溶液混合时有:K (CaCO)>2.5×10-3
sp 3
C.实验3中发生反应的离子方程式为 +H O+CO=2
2 2
D.实验4所得溶液中c(Na+)=c( )+c( )+c(H CO)
2 3
【答案】A
【解析】实验1中,K (H CO)∙K (H CO)= ∙ = ,NaHCO
a1 2 3 a2 2 3 3
溶液的pH约为8,表明溶液中HCO水解是主要,电离是次要,c(CO)<c(H CO),所以 <
2 3
c2(H+)=10-16,A项正确;实验2中两溶液混合时,c(Ca2+)=0.05 mol•L-1,c(HCO)<0.05 mol•L-1,则有:
K (CaCO)=c(Ca2+)∙c(HCO)<2.5×10-3,B项错误;NaHCO 以晶体形式产生,不能拆成离子,则反应的离子
sp 3 3
方程式为2Na++ CO+H O+CO=2NaHCO↓,C项错误;滴加氯水,HCO与H+反应生成HCO,有气泡产
2 2 3 2 3
生,说明有一部分HCO 分解生成CO,根据元素质量守恒,溶液中c(Na+)=c(HCO)+c(CO)+c(H CO)+
2 3 2 2 3
c(CO),则c(Na+)>c(HCO)+c(CO)+c(H CO),D项错误。
2 2 3
10.(2024·江苏灌南中学月考,12)室温下用0.1 mol∙L-1 NaSO 溶液吸收SO 的一种脱硫工艺流程如下图
2 3 2所示。已知HSO 电离平衡常数分别为K =1.54×10-2,K =1.02×10-7,HCO 电离平衡常数分别为
2 3 a1 a2 2 3
K =4.30×10-7、K =5.61×10-11,忽略通入SO 所引起的溶液体积变化和HO挥发。
a1 a2 2 2
下列说法正确的是
A.0.1 mol∙L-1 NaSO 溶液中:
2 3
B.NaHSO 溶液中:
3
C.“沉淀”时发生主要反应的离子方程式:
D.“沉淀”分离后的滤液中:
【答案】C
【解析】NaSO 溶液吸收烟气中的SO ,生成NaHSO;由于K (H SO )=1.02×10-7<K (H CO)=4.30×10-
2 3 2 3 a2 2 3 a1 2 3
7,所以NaHSO 与CaCO 反应只能生成NaHCO 和CaSO;CaSO 被通入的O 氧化,生成CaSO,从而获
3 3 3 3 3 2 4
得石膏。0.1 mol∙L-1 NaSO 溶液中,存在电荷守恒c(Na+)+ c(H+)=c( )+2c( )+c(OH-),物料守恒
2 3
c(Na+)=2c( )+2c( )+2c(H SO ),则c(OH-)=c(H+)+c( )+2c(H SO ),A不正确;NaHSO 溶液中,
2 3 2 3 3
K =1.02×10-7,K = ≈6.49×10-13,则以 的电离为主,溶液呈酸性,所以 ,
a2 h2
B不正确;由分析可知,由于K (H SO )=1.02×10-7<K (H CO)=4.30×10-7,所以NaHSO 与CaCO 反应只
a2 2 3 a1 2 3 3 3
能生成NaHCO 和CaSO,“沉淀”时发生主要反应的离子方程式: ,C正
3 3
确;“沉淀”分离后的滤液,仍是CaSO 的饱和溶液,则 ,D不正确。
3
11.(2024·江苏徐州高三期中,12)燃煤烟气脱硫的方法有多种,方法之一是常温下用氨水将 转化为,再氧化成 。已知 的电离常数 , , 的电
离常数 。下列说法正确的是
A. 溶液中:
B. 溶液中:
C.若溶液中 时,溶液的
D.向 溶液中通入空气发生反应的离子方程式:
【答案】C
【解析】 ,由于HSO电离常数 , 的水解常数
<1.0 10-7,则可知HSO电离程度大于NH水解程度,且HSO还存在水解,则
,A项错误;NH HSO 溶液,根据电荷守恒,有
4 3
,B项错误; ,
,则 ,当 ,
,即pH=4,C项正确;向NH HSO 溶液中通入空气,HSO被氧化为SO,离子方程式为:
4 3
2HSO+O=2SO+2H+,HSO是弱酸的酸式根,不能拆,D项错误。
2
12.(2024·江苏常州高三11月期中,12)室温下,通过下列实验探究 溶液的性质。实验Ⅰ:向 溶液中滴加 溶液。
实验Ⅱ:向 溶液中滴加 溶液。
已知: 的电离常数 , , ,溶液混合后体积变
化忽略不计。下列说法正确的是
A.实验Ⅰ滴定达终点读数时,应双手一上一下持滴定管保证其竖直
B.实验Ⅰ滴定至溶液中 时, 至少大于10mL
C.实验Ⅱ初始阶段发生反应的离子方程式为
D.实验Ⅱ最后阶段发生反应(最简整数比)的化学平衡常数表达式为
【答案】D
【解析】达到滴定终点读数时,应将滴定管取下,用手握住滴定管未装有液体的部位进行读数,眼睛与凹
液面最低点水平进行读数,A错误;当 =10mL时,溶质是 、 且两者物质的量
浓度相等,草酸氢根的电离常数为 ,草酸根的水解常数为 ,则草酸
氢根的电离程度大于草酸根的水解程度,因此存在 ,B错误;实验Ⅱ中,由于开始滴
加的氯化钙量较少而过量,因此该反应在初始阶段生成草酸,由于草酸为弱酸,不能拆,因此发生反应的
离子方程式为 ,C错误;由C可知,起始时实验Ⅱ中发生反应
,该反应的平衡常数为
,说明反应完全进行,当 完全消耗后, 再与 反应,发生
,此时平衡常数 =
,D正确。
13.(2024·江苏常州高级中学高三开学考试,12)室温下,通过下列实验探究NaCO 的性质。已知:
2 3
25℃时,HSO 的K =1.4×10-2、K =1.0×10-7,HCO 的K =4.3×10-7、K =5.6×10-11。
2 3 a1 a2 2 3 a1 a2
实验1:配制50mL0.1mol·L-1NaCO 溶液,测得溶液pH约为12;
2 3
实验2:取10mL0.1mol·L-1NaCO 溶液,向其中加入一定量CaSO 固体充分搅拌,一段时间后过滤,向滤
2 3 4
渣中加入足量稀盐酸,固体部分溶解;
实验3:取10mL0.1mol·L-1NaCO 溶液,向其中缓慢滴入等体积0.1mol·L-1稀盐酸。
2 3
下列说法正确的是
A.实验1所得溶液中,c(Na+)<c(CO )+c(HCO )
B.实验2,加入稀盐酸后的上层清液中c(Ca2+)=c(SO )
C.实验3反应后溶液中存在:c(Na+)=c(CO )+c(HCO )+c(H CO)
2 3
D.25℃时,反应CO +H
2
SO 3⇌HCO +HSO 的平衡常数K=2.5×108
【答案】D
【解析】NaCO 溶液呈碱性,c(OH-)>c(H+),电荷守恒关系为c(Na+)+c(H+)=c(HCO )+2c(CO )+c(OH-),
2 3
则c(Na+)>c(HCO )+2c(CO )>c(CO )+c(HCO ),A项错误;向滤渣中加入足量稀盐酸,固体部分溶解,
则滤渣为CaCO 和CaSO 的混合物,CaCO 溶于盐酸生成CaCl ,CaSO 存在溶解平衡,则实验2加入稀盐
3 4 3 2 4
酸后的上层清液中c(Ca2+)>c(SO ),B项错误;NaCO 溶液中滴入等体积0.1mol•L稀盐酸后生成NaHCO
2 3 3和NaCl,存在元素质量守恒:c(Na+)=c(CO )+c(HCO )+c(H CO)+c(Cl-),则c(Na+)>c(CO )+c(HCO )
2 3
+c(H
2
CO
3
),C项错误;反应CO +H
2
SO 3⇌HCO +HSO 的平衡常数K= =
= =2.5×108,D项正确。
14.(2024·江苏扬州高邮高三开学考试,12)燃煤烟气中的 捕集可通过如图所示的物质转化实现。已
知: 。下列说法正确的是
A. 吸收 所得到的溶液中:
B. 完全转化为 时,溶液中存在:
C.“吸收”后所得溶液中:
D.“转化”后得到的上层清液中:
【答案】B
【解析】KOH吸收CO 所得到的溶液,若为KCO 溶液,则主要发生第一步水解,溶液中:c(HCO)<
2 2 3 2 3
c(HCO),若为KHCO 溶液,则发生水解的程度很小,溶液中:c(HCO)<c(HCO),A项错误;KOH完全
3 2 3
转化为KHCO 时,将K 和K 数值带入不等式计算,K ·K c(HCO)+2c(CO),C项
错误;转化后的上层清液为碳酸钙的饱和溶液, ,D项错误。
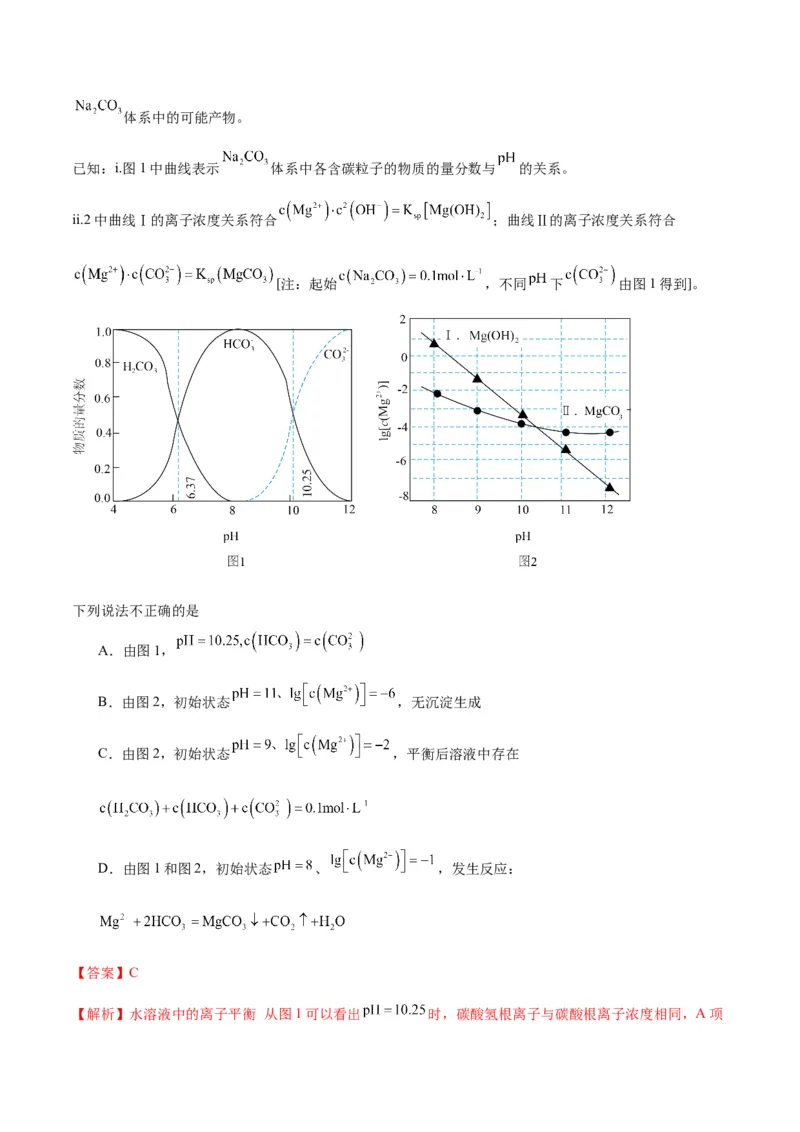
15.(2024·江苏常州联盟校10月学情调研,14)利用平衡移动原理,分析一定温度下 在不同 的体系中的可能产物。
已知:i.图1中曲线表示 体系中各含碳粒子的物质的量分数与 的关系。
ii.2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同 下 由图1得到]。
下列说法不正确的是
A.由图1,
B.由图2,初始状态 ,无沉淀生成
C.由图2,初始状态 ,平衡后溶液中存在
D.由图1和图2,初始状态 、 ,发生反应:
【答案】C
【解析】水溶液中的离子平衡 从图1可以看出 时,碳酸氢根离子与碳酸根离子浓度相同,A项正确;从图2可以看出 、 时,该点位于曲线Ⅰ和曲线Ⅱ的下方,不会产生碳酸镁
沉淀或氢氧化镁沉淀,B项正确;从图2可以看出 、 时,该点位于曲线Ⅱ的上方,
会生成碳酸镁沉淀,根据物料守恒,溶液中 ,C项错误;
时,溶液中主要含碳微粒是 , , 时,该点位于曲线Ⅱ的上方,会生成
碳酸镁沉淀,因此反应的离子方程式为 ,D项正确。
16.(2024·江苏泰州中学高三期初调研,12) 为二元弱碱。室温下,配制一组
的 与 的混合溶液,溶液中相关组分的物质的量
分数随溶液pH变化的曲线如下图所示,下列说法正确的是
A.由图可知 的
B. 的溶液中:
C.等物质的量的 和 混合溶液中
D.在 的水溶液中,
【答案】C
【解析】随着pH的升高,X2+第一步反应变为X(OH)+,X(OH)+第二步反应变为X(OH) ,pH=6.2时,
2;pH=9.2时, 。根据图像左侧的交叉点,pH=6.2时,
, 的 =10-6.2,A项错误; 的溶液中:
,但是加入盐酸,溶液的体积增加,故 <0.05mol/L,B项错误;
X2+的水解程度大于X(OH)+的水解程度,则等物质的量的 和 混合溶液
,C项正确; 的水溶液显酸性, ,D项错误。
17.(2024·江苏常熟高三抽测,12)室温下,通过下列实验探究 、 溶液的性质。
实验1:用 试纸测量 溶液的 ,测得 约为8
实验2:将 溶液与 溶液等体积混合,产生白色沉淀
实验3:饱和 溶液中通入 产生白色沉淀,溶液 从12下降到约为9
实验4:向 溶液中滴加几滴酚酞,加水稀释,溶液红色变浅
下列说法正确的是
A.由实验1可得出:
B.由实验2可推测:
C.实验3中发生反应的离子方程式为
D.实验4中加水稀释后,溶液中 的值增大
【答案】D【解析】由实验1可得出碳酸氢钠溶液中碳酸氢根水解程度大于电离程度即 ,
则 ,A错误;实验2是等体积混合,碳酸氢根少量电离产生碳酸根,
则 >Q(CaCO )>Ksp(CaCO ),B错误;实验3中发生反应的离子方程式为
3 3
↓,C错误;实验4中加水稀释后,水解程度增大,由于溶液体积增大,
溶液碱性减弱,氢离子浓度增大,因此溶液中 的值增大,D正确。
18.(2024·江苏南京、盐城高三期末,12)室温下,用含少量 的粗 溶液制备
晶体的流程如下图所示。
已知 。下列说法项正确的是
A.粗 溶液中:
B.“沉铁”反应为:
C. 溶液中:
D.“沉镁”后的滤液中:
【答案】C【解析】粗 溶液中加入硫酸钠溶液,生成黄钠铁钒,除去铁元素;再向溶液中加入 溶液,生成
沉淀 ,除去镁元素,经过后续操作得到 。粗 溶液的电荷守恒中缺少氢离子和氢氧
根离子浓度,A项错误;溶液呈弱酸性,“沉铁”反应为:3Fe3++Na++2
+6H O=NaFe (SO )(OH) ↓+6H+,B项错误;氟化氢为弱酸, 溶液中根据质子守恒:
2 3 4 2 6
,C项正确;沉镁过程形成 沉淀,根据沉淀溶解平衡,
,
,此时 ,该溶液中,
镁离子浓度相同,形成的是 沉淀,没有形成 沉淀,则溶液中 ,故
得出沉镁后 ,D项错误。
19.(2024·江苏盐城东台中学高三3月月考,9)室温下,通过下列实验探究 溶液的性质(假
设实验前后溶液体积不变)。
实验I:用 试纸测定 溶液的 ,测得 约为6。
实验II:往 溶液中加入少量 溶液,产生白色沉淀。
实验III:往 溶液中通入一定量的 至沉淀完全。
实验IV:往 溶液中加入 产生沉淀和气体
下列说法正确的是A. 溶液中由水电离出的 约为
B.实验II中沉淀成分仅为
C.实验III得到的溶液中有
D.实验IV过滤后所得的溶液中一定存在:
【答案】C
【解析】 水解促进水电离, 的 约为6,溶液中由水电离出的
约为 ,A错误;实验II中沉淀成分为 、Al(OH) ,B错误;实验III得到0.2mol/L
3
的(NH )SO 溶液中, ,C正确;实验IV,铝离子和碳酸根离
4 2 4
子发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,过滤后所得的溶液中不一定含碳酸铝沉淀,所以不
一定存在 ,D错误。