文档内容
专项训练 无机物制备、性质的实验题
1.(2023·全国·统考高考真题)钴配合物 溶于热水,在冷水中微溶,
可通过如下反应制备:
。
具体步骤如下:
Ⅰ.称取 ,用 水溶解。
Ⅱ.分批加入 后,将溶液温度降至 以下,加入 活性炭、
浓氨水,搅拌下逐滴加入 的双氧水。
Ⅲ.加热至 反应 。冷却,过滤。
Ⅳ.将滤得的固体转入含有少量盐酸的 沸水中,趁热过滤。
Ⅴ.滤液转入烧杯,加入 浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
回答下列问题:
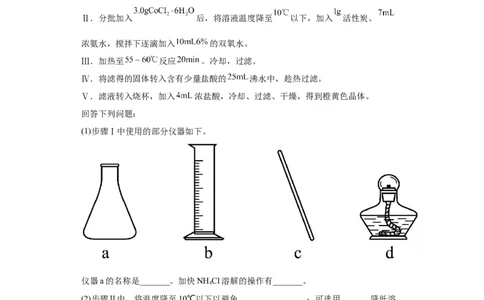
(1)步骤Ⅰ中使用的部分仪器如下。
仪器a的名称是_______。加快NH Cl溶解的操作有_______。
4
(2)步骤Ⅱ中,将温度降至10℃以下以避免_______、_______;可选用_______降低溶
液温度。
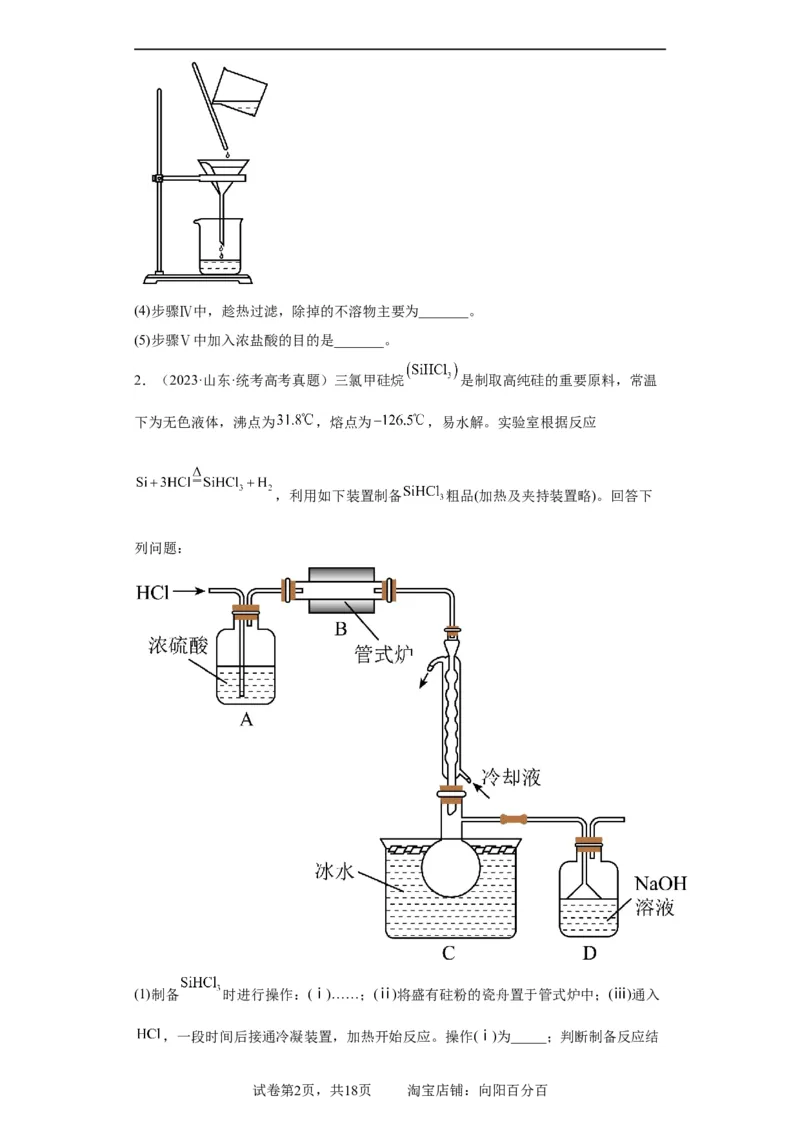
(3)指出下列过滤操作中不规范之处:_______。
试卷第1页,共18页
学科网(北京)股份有限公司(4)步骤Ⅳ中,趁热过滤,除掉的不溶物主要为_______。
(5)步骤Ⅴ中加入浓盐酸的目的是_______。
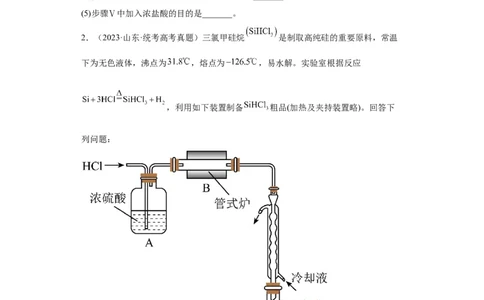
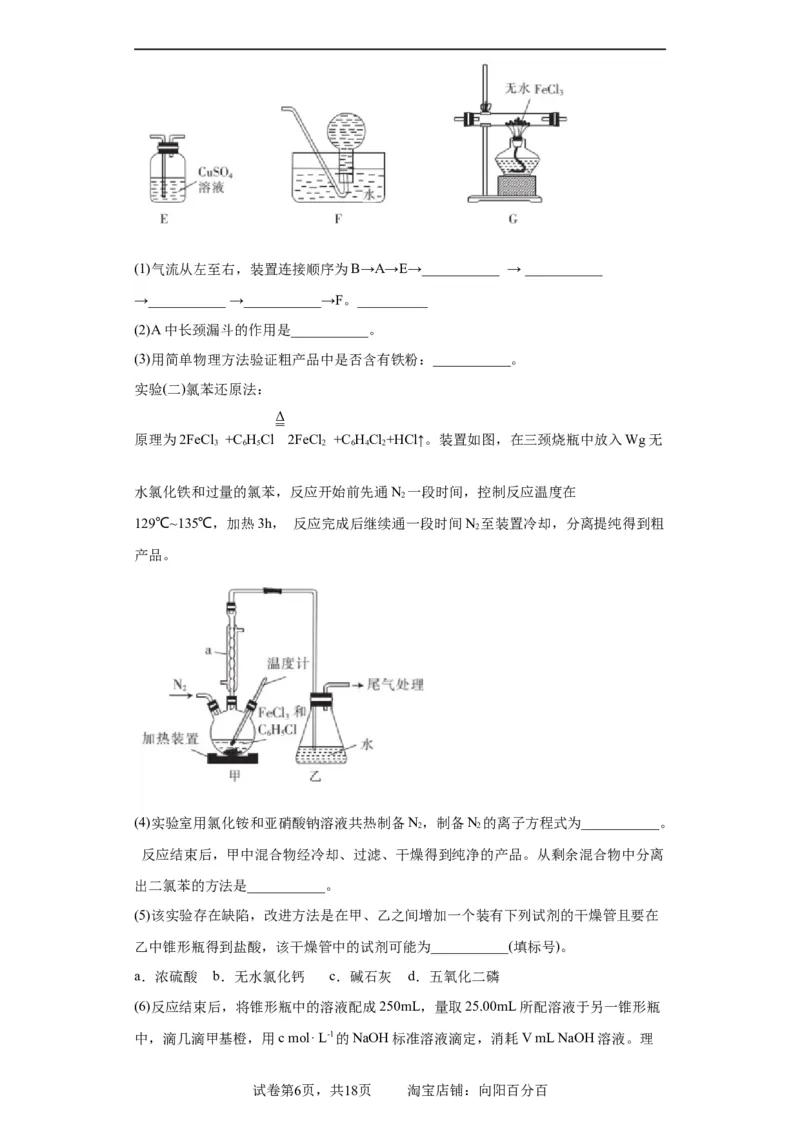
2.(2023·山东·统考高考真题)三氯甲硅烷 是制取高纯硅的重要原料,常温
下为无色液体,沸点为 ,熔点为 ,易水解。实验室根据反应
,利用如下装置制备 粗品(加热及夹持装置略)。回答下
列问题:
(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有砫粉的瓷舟置于管式炉中;(ⅲ)通入
,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为_____;判断制备反应结
试卷第2页,共18页 淘宝店铺:向阳百分百束的实验现象是_____。图示装置存在的两处缺陷是_____。
(2)已知电负性 在浓 溶液中发生反应的化学方程式为_____。
(3)采用如下方法测定溶有少量 的 纯度。
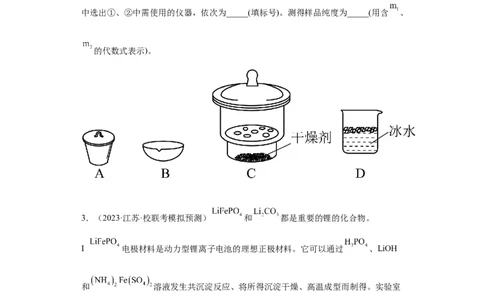
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①_____,
②_____(填操作名称),③称量等操作,测得所得固体氧化物质量为 ,从下列仪器
中选出①、②中需使用的仪器,依次为_____(填标号)。测得样品纯度为_____(用含 、
的代数式表示)。
3.(2023·江苏·校联考模拟预测) 和 都是重要的锂的化合物。
I 电极材料是动力型锂离子电池的理想正极材料。它可以通过 、LiOH
和 溶液发生共沉淀反应、将所得沉淀干燥、高温成型而制得。实验室
制备 的方法如下:
步骤1 将LiOH置于题图所示实验装置的三颈烧瓶中,加入煮沸过的蒸馏水,搅拌使
其溶解。从分液漏斗中滴加 溶液,并持续通入氮气。
试卷第3页,共18页
学科网(北京)股份有限公司步骤2 将 固体溶于蒸馏水中,迅速倒入三颈烧瓶中,快速搅拌,充
分反应后,过滤、洗涤滤渣得 固体。
(1)共沉淀反应投料时,不将 和LiOH溶液直接混合的原因是____________。
(2)写出共沉淀反应的化学方程式:____________。
(3)工业制取 在高温成型前,常向 中加入少量活性炭黑,其作用除了
可以改善成型后 的导电性能外,还能______。
Ⅱ 磷酸锂渣(主要成分为 )和废旧电极材料(含铝、炭、 和 )均可
用于制取 。
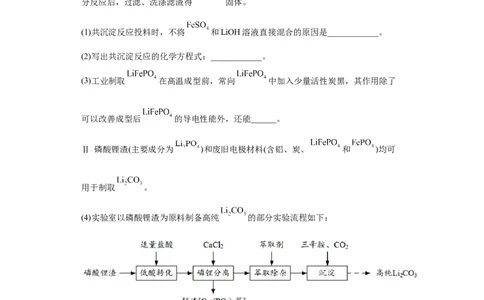
(4)实验室以磷酸锂渣为原料制备高纯 的部分实验流程如下:
①“低酸转化”使 转化为 。写出“磷锂分离”的化学方程式:
____________。
②已知:三辛胺 是一种有机碱,难溶于水。向“萃取”后的溶液中加入
三辛胺再通入 得到 沉淀,加入三辛胺的目的是____________。
试卷第4页,共18页 淘宝店铺:向阳百分百(5)已知: 微溶于水; 、 难溶于水和碱,可溶于盐酸生成LiCl、
、 和 ;pH>3.2时, 沉淀完全。完善由某废旧电极材料制取
的实验方案:边搅拌边向废旧电极材料中加入NaOH溶液至不再产生气泡,过
滤,______,过滤、洗涤,低温干燥得 固体。(实验中须使用的试剂有:双氧水、
盐酸、NaOH溶液、 溶液)
4.(2023·云南楚雄·统考模拟预测)FeCl 是一种净水剂。有关物质的部分性质如下:
2
C HCl(氯 C HCl(二氯
6 5 6 4 2 FeCl FeCl
苯) 苯) 3 2
溶解 不溶于C HCl 、C HCl、苯,易溶于乙
不溶于水,易溶于苯、乙醇 6 5 6 4 2
性 醇,易吸水
熔
-45 53 304 670
点/℃
沸
132 173 316,易升华 700
点/℃
某小组用两种方法制备无水FeCl
2。
实验(一)氢气还原法:
原理为H +2FeCl 2FeCl +2HCl。 已知: 焦性没食子酸溶液用于吸收O。实验室用
2 3 2 2
粗锌和盐酸反应制备氢气,装置如下(装置可以重复使用):
试卷第5页,共18页
学科网(北京)股份有限公司(1)气流从左至右,装置连接顺序为B→A→E→___________ → ___________
→___________ →___________→F。__________
(2)A中长颈漏斗的作用是___________。
(3)用简单物理方法验证粗产品中是否含有铁粉:___________。
实验(二)氯苯还原法:
原理为2FeCl +C HCl 2FeCl +C HCl+HCl↑。装置如图,在三颈烧瓶中放入Wg无
3 6 5 2 6 4 2
水氯化铁和过量的氯苯,反应开始前先通N 一段时间,控制反应温度在
2
129℃~135℃,加热3h, 反应完成后继续通一段时间N 至装置冷却,分离提纯得到粗
2
产品。
(4)实验室用氯化铵和亚硝酸钠溶液共热制备N,制备N 的离子方程式为___________。
2 2
反应结束后,甲中混合物经冷却、过滤、干燥得到纯净的产品。从剩余混合物中分离
出二氯苯的方法是___________。
(5)该实验存在缺陷,改进方法是在甲、乙之间增加一个装有下列试剂的干燥管且要在
乙中锥形瓶得到盐酸,该干燥管中的试剂可能为___________(填标号)。
a.浓硫酸 b.无水氯化钙 c.碱石灰 d.五氧化二磷
(6)反应结束后,将锥形瓶中的溶液配成250mL,量取25.00mL所配溶液于另一锥形瓶
中,滴几滴甲基橙,用c mol· L-1的NaOH标准溶液滴定,消耗V mL NaOH溶液。理
试卷第6页,共18页 淘宝店铺:向阳百分百论上FeCl 的转化率为___________ %。
3
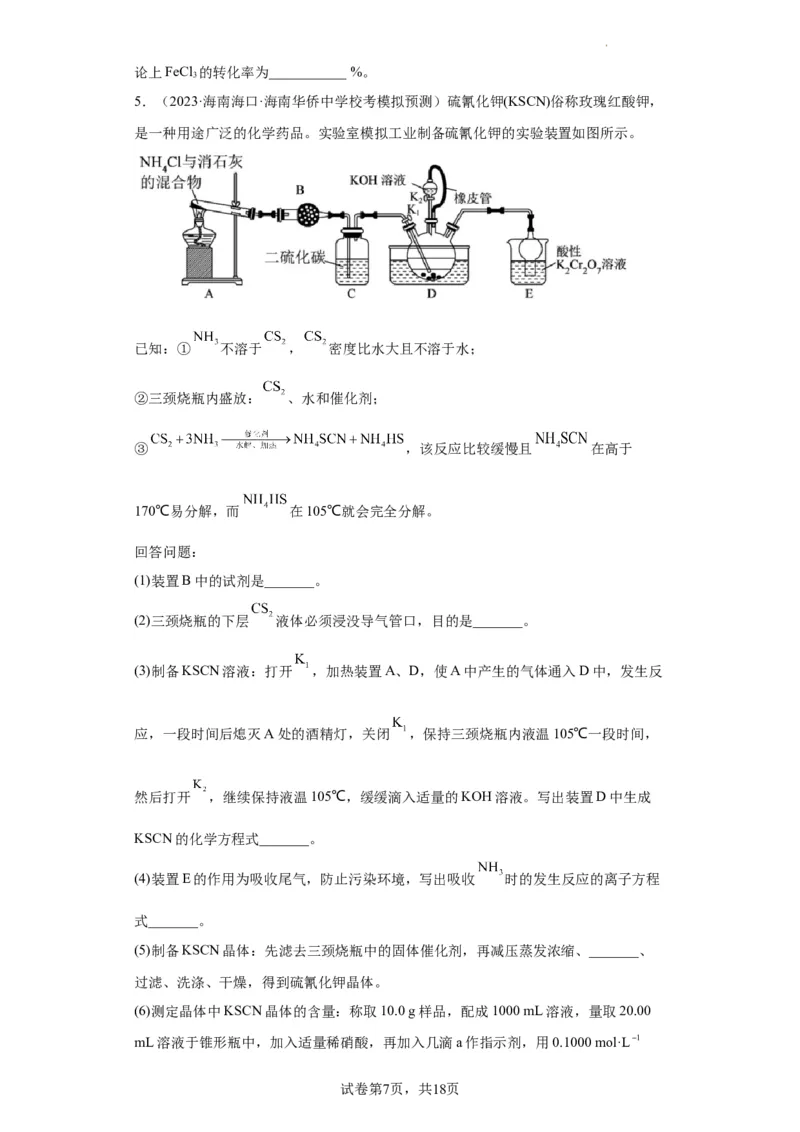
5.(2023·海南海口·海南华侨中学校考模拟预测)硫氰化钾(KSCN)俗称玫瑰红酸钾,
是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如图所示。
已知:① 不溶于 , 密度比水大且不溶于水;
②三颈烧瓶内盛放: 、水和催化剂;
③ ,该反应比较缓慢且 在高于
170℃易分解,而 在105℃就会完全分解。
回答问题:
(1)装置B中的试剂是_______。
(2)三颈烧瓶的下层 液体必须浸没导气管口,目的是_______。
(3)制备KSCN溶液:打开 ,加热装置A、D,使A中产生的气体通入D中,发生反
应,一段时间后熄灭A处的酒精灯,关闭 ,保持三颈烧瓶内液温105℃一段时间,
然后打开 ,继续保持液温105℃,缓缓滴入适量的KOH溶液。写出装置D中生成
KSCN的化学方程式_______。
(4)装置E的作用为吸收尾气,防止污染环境,写出吸收 时的发生反应的离子方程
式_______。
(5)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、_______、
过滤、洗涤、干燥,得到硫氰化钾晶体。
(6)测定晶体中KSCN晶体的含量:称取10.0 g样品,配成1000 mL溶液,量取20.00
mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用0.1000 mol·L
试卷第7页,共18页
学科网(北京)股份有限公司标准溶液滴定,达到滴定终点时消耗 标准溶液18.00 mL。
已知:滴定时发生的反应: (白色)。
①滴定过程的指示剂a为_______。
②晶体中KSCN的质量分数为_______。
6.(2023·辽宁鞍山·鞍山一中校考模拟预测)硫代硫酸钠( )可用作分析试剂及
还原剂,受热、遇酸均易分解。学习小组用如图装置,利用绿矾受热分解生成的
气体制备硫代硫酸钠。
已知:
①绿矾受热分解反应为: ;
② 的沸点为44.8℃。
回答下列问题:
(1)完成实验操作过程:
连接装置,___________,加入药品( 和 混合溶液用煮沸过的蒸馏水配制),
使所有活塞处于关闭状态。开始制备,打开某些活塞,通入一段时间 ;关闭活塞
___________,打开活塞___________,加热绿矾;使用pH传感器始终观测C处溶液
的pH,在pH7~8之间时停止加热,同时关闭活塞 ;……将锥形瓶用热水浴浓缩至
水层表面出现结晶为止,经过___________、过滤、洗涤、干燥得到 晶体。
(2)写出锥形瓶中发生反应的离子方程式___________。
(3)装置B的作用为___________。
(4)将锥形瓶中的反应停止在pH传感器的读数为7~8时的原因是___________。
试卷第8页,共18页 淘宝店铺:向阳百分百(5)该装置存在一个明显的缺点,请提出改进方法___________。
7.(2023·辽宁大连·大连二十四中校考模拟预测)二氯化硝基·五氨合钴(
,摩尔质量:261g/mol)是一种难溶于乙醇的棕黄色针状晶体经常
用于研究配位化合物内界的键合方式。某实验小组对其进行合成与表征,实验原理及
合成步骤如下:
【实验仪器及用品】
小烧杯、锥形瓶、量筒、表面皿、玻璃棉、胶头滴管、镊子、布氏漏斗、抽滤瓶、pH
试纸。无水乙醇、常温和冷的蒸馏水
【实验步骤】
I.量取15.0mL2mol/L的氨水,倒入小烧杯中,向其中加入2.50g (摩
尔质量:250.5g/mol),搅拌使其充分溶解,滤去不溶物;
II.室温时,将滤液置于锥形瓶内,向其中逐滴加入4mol/L盐酸,调整滤液pH至3~4
后,升温至65℃,搅拌状态下加入1.0g ,加热,稳定保持此温度反应30min;
III.将反应后所得溶液冷却至室温,小心加入15.0mL浓盐酸后,降温使其结晶完全:
IV。将得到的固液混合物倒入布氏漏斗中进行抽滤后,经过一系列实验操作,干燥后
得到棕黄色晶体1.9g。
请回答下列问题:
(1) 中Co的配位数为___________。
(2)反应的化学方程式为___________。
(3)步骤II中,对锥形瓶中滤液采取的最佳控温方式为___________。
(4)步骤III中若盐酸加入过多,会导致所得晶体内界中配体 的数量___________(填
“增多”或“减少”),产生这种现象的原因是___________。
(5)请补充最后一步抽滤后获得产品的一系列实验操作为___________。
(6)此实验的产率为___________%(列出计算式即可)。
(7)有文献表明:进行此实验时,若温度不能稳定控制在65℃左右,可能会产生二氯化
亚硝酸根·五氨合钴( );
试卷第9页,共18页
学科网(北京)股份有限公司①上述两种配位化合物的关系是___________(填字母,下同)。
a.同素异形体 b.同系物 c.同分异构体 d.同位素
②上述两种配位化合物的结构中, 的配位方式不同,若想对二者进行鉴别,可采
用的仪器分析方法是___________。
a.原子光谱法 b.红外光谱法 c.核磁共振氢谱法 d.X-射线衍射法
8.(2023·山东·沂水县第一中学校联考模拟预测)亚硝酰硫酸( )在重氮化反
应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,
并测定产品纯度。
已知:i.亚硝酰硫酸遇水分解为硫酸、硝酸和NO,溶于浓硫酸而不分解;
.实验室制备亚硝酰硫酸的原理为 ,
。
(1)仪器Ⅰ的名称为___________,按照气流从左到右的顺序,上述仪器的连接顺序为
___________(填仪器接口的字母,字母之间用“→”连接,部分仪器可以重复使用),
C装置的作用为___________。
(2)反应需控制温度在25~40℃,采用的加热措施为___________,开始时反应缓慢,
但某时刻反应速率明显加快,其原因可能是___________。
(3)测定亚硝酰硫酸的纯度:
步骤①:准确称取 产品,在特定条件下配制成 溶液。
步骤②:取 溶液于锥形瓶中,加入 未知浓度 溶液(过量)和
试卷第10页,共18页 淘宝店铺:向阳百分百的 溶液,摇匀,发生反应
步骤③:向该溶液中滴加 标准溶液进行滴定,消耗 溶
液的体积为 。
步骤④:把亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗 溶
液的体积为 。
滴定终点时的现象为___________,亚硝酰硫酸的纯度为___________(精确到 )。
9.(2023·黑龙江哈尔滨·哈尔滨三中校考模拟预测)锰的化合物在工业、医疗等领域
有重要应用。某兴趣小组设计实验模拟制备KMnO 及探究Mn2+能否氧化为 。
4
Ⅰ. 的制备:
步骤一:
步骤二:
实验操作:
步骤一:将一定比例的 和 固体混合加热,得到墨绿色的固体,冷
却后加水溶解得到碱性 溶液放入烧杯C中。
步骤二:连接装置,检查气密性后装入药品。打开分液漏斗活塞,当C中溶液完全变
为紫红色时,关闭活塞停止反应,分离、提纯获取 晶体。
装置图如下:
(1)B中试剂的作用_______。
试卷第11页,共18页
学科网(北京)股份有限公司(2)反应结束后,未及时分离 晶体,发现C中紫红色溶液变浅。出现这一现象
可能的原因是_______。
Ⅱ.该小组继续探究 能否氧化为 ,进行了下列实验:
装置图 试剂X 实验现象
生成浅棕色沉淀,一段时间后变为
① 溶液
棕黑色
② 和
立即生成棕黑色沉淀
混合液
③ 溶液 无明显现象
滴加 无明显现象,加入
④ 溶液
立即变为紫红色,稍后紫红色很快
和少量
消失,生成棕黑色沉淀
已知:ⅰ. 为棕黑色固体,难溶于水;
ⅱ. 在酸性环境下缓慢分解产生 。
(3)实验①中生成棕黑色沉淀可能的原因_______。
(4)实验②中迅速生成棕黑色沉淀的离子方程式_______。
(5)实验③说明_______。
(6)甲同学猜测实验④中紫红色消失的原因:酸性条件下 不稳定,分解产生了
,乙同学认为不成立,理由是_______;乙同学认为是溶液中剩余的 将
还原,并设计了实验方案证明此推测成立,其方案为_______。
探究结果:在酸性条件下,某些强氧化剂可以将 氧化为 。
10.(2023·海南海口·统考模拟预测)兴趣实验小组在实验室模拟接触法制硫酸的关键
环节。在查资料后开展了以下制备实验。完成其实验过程中的问题。
Ⅰ.催化剂的准备取 的偏钒酸铵加入到 水中,加热到70℃溶解。放入石棉
绒浸透,取出石棉绒灼烧得到黄色固体。(资料:
试卷第12页,共18页 淘宝店铺:向阳百分百)
(1)该步骤中使用到的仪器不包括______(填序号)。
a.玻棒 b.温度计 c.烧杯 d.量筒 e.镊子 f.坩埚 g.天平 h.蒸发皿
(2)检验 的方法是__________。
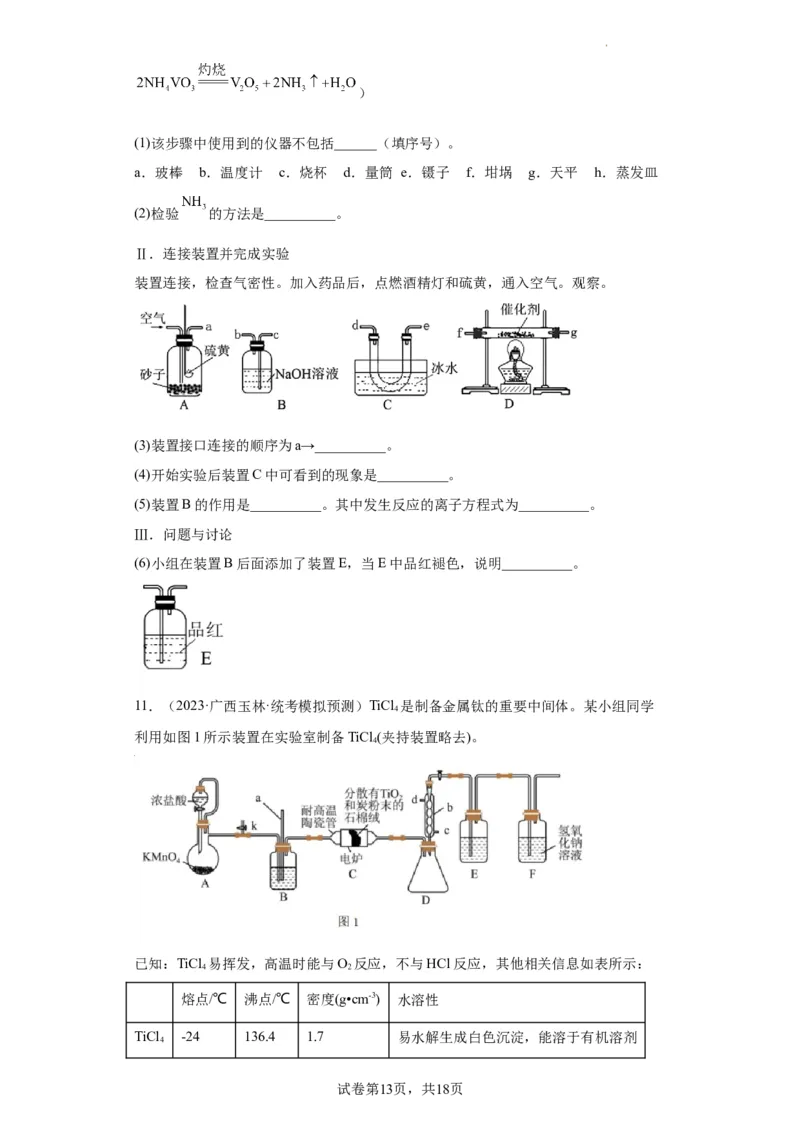
Ⅱ.连接装置并完成实验
装置连接,检查气密性。加入药品后,点燃酒精灯和硫黄,通入空气。观察。
(3)装置接口连接的顺序为a→__________。
(4)开始实验后装置C中可看到的现象是__________。
(5)装置B的作用是__________。其中发生反应的离子方程式为__________。
Ⅲ.问题与讨论
(6)小组在装置B后面添加了装置E,当E中品红褪色,说明__________。
11.(2023·广西玉林·统考模拟预测)TiCl 是制备金属钛的重要中间体。某小组同学
4
利用如图1所示装置在实验室制备TiCl (夹持装置略去)。
4
已知:TiCl 易挥发,高温时能与O 反应,不与HCl反应,其他相关信息如表所示:
4 2
熔点/℃ 沸点/℃ 密度(g•cm-3) 水溶性
TiCl -24 136.4 1.7 易水解生成白色沉淀,能溶于有机溶剂
4
试卷第13页,共18页
学科网(北京)股份有限公司CC1 -23 76.8 1.6 难溶于水
4
回答下列问题:
(1)装置D中仪器b的名称是_____,装置E中的试剂是_____(填试剂名)。
(2)装置B中长导管a的作用是_____。
(3)装置A中发生反应的离子方程式为_____。
(4)装置C中除生成TiCl 外,还生成一种气态不成盐氧化物,该反应的化学方程式为
4
_____。
(5)制得的TiCl 中常含有少量CCl ,从混合液中分离出TiCl 操作的名称是_____。
4 4 4
(6)利用如图2装置测定所得TiCl 的纯度:取mg产品加入烧瓶,向安全漏斗中加入适
4
量蒸馏水,待TiCl 充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴
4
0.1mol•L-1KCrO 溶液作指示剂,用nmol•L-1AgNO 标准溶液滴定至终点,消耗标准溶
2 4 3
液VmL。
已知:常温下,K (AgCl)=1.8×10-10、K (Ag CrO)=1.1×10-12,Ag CrO 呈砖红色,
sp sp 2 4 2 4
TiCl +(2+n)H O=TiO•nH O↓+4HCl。
4 2 2 2
①安全漏斗在本实验中的作用除加水外,还有_____。
②滴定终点的判断方法是_____。
③产品的纯度为_____(用含m、n和V的代数式表示)。
12.(2023·山东·校联考模拟预测)亚硝酰氯 主要用于合成洗涤剂、触媒,也
可用作有机合成中间体。沸点为 ℃,是黄色气体或红褐色液体,遇水极易反应:
,伴随着热量的释放。某化学兴趣小组设计如图装置用
和NO制备亚硝酰氯。
试卷第14页,共18页 淘宝店铺:向阳百分百已知:① , , ;
② 。
回答下列问题:
I.制备亚硝酰氯
(1)装置甲中,盛有铜屑的仪器名称为___________,用上述装置,按气流方向组装,用
字母表示接口的连接顺序为a→___________→h(i→m)j←___________←k(填写接口字
母;仪器可重复使用),装置乙的作用是___________。
(2)实验开始时,先打开装置甲的分液漏斗活塞滴入适量稀硝酸,当观察到装置丁中
___________时,再向三颈瓶中通入 制备 ,当观察到___________说明三颈瓶
中反应结束。
(3)装置丁中冰盐水的作用是___________。
II.产品纯度的测定
实验步骤如下:
①取mg市售亚硝酰氯溶于水,配制成 溶液,取出 于锥形瓶中;
②调pH为6,再加入稍过量的 溶液(杂质不参与反应);
③充分反应后,加入少量硝基苯,振荡、静置,使沉淀表面被有机物覆盖。
④滴入几滴 溶液,再用 标准溶液滴定,滴定至终点时,
共消耗 溶液。
(4)步骤④中滴定终点的现象是___________,市售亚硝酰氯纯度为___________(用m、
、 表示)。
(5)下列操作导致测得市售亚硝酰氯纯度偏小的是___________。
A.步骤①中,将 溶解后立即转移至 容量瓶中
试卷第15页,共18页
学科网(北京)股份有限公司B.步骤②中,有几滴 溶液滴落在锥形瓶外
C.步骤③中,有少量白色沉淀表面没有覆盖有机物
D.步骤④中,滴定终点时,有半滴液体悬挂尖嘴处
13.(2023·浙江·统考高考真题)某研究小组用铝土矿为原料制备絮凝剂聚合氯化铝(
)按如下流程开展实验。
已知:①铝土矿主要成分为 ,含少量 和 。用 溶液溶解铝土矿过
程中 转变为难溶性的铝硅酸盐。
② 的絮凝效果可用盐基度衡量,盐基度
当盐基度为0.60~0.85时,絮凝效果较好。
请回答:
(1)步骤1所得滤液中主要溶质的化学式是___________。
(2)下列说法不正确的是___________。
A.步骤I,反应须在密闭耐高压容器中进行,以实现所需反应温度
B.步骤Ⅱ,滤液浓度较大时通入过量 有利于减少 沉淀中的杂质
C.步骤Ⅲ,为减少 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌
D.步骤中控制 和 的投料比可控制产品盐基度
(3)步骤V采用如图所示的蒸汽浴加热,仪器A的名称是___________;步骤V不宜用
酒精灯直接加热的原因是___________。
试卷第16页,共18页 淘宝店铺:向阳百分百(4)测定产品的盐基度。
的定量测定:称取一定量样品,配成溶液,移取 。溶液于锥形瓶中,调
,滴加指示剂 溶液。在不断摇动下,用 标
准溶液滴定至浅红色(有 沉淀),30秒内不褪色。平行测试3次,平均消耗
标准溶液 。另测得上述样品溶液中 。
①产品的盐基度为___________。
②测定 过程中溶液 过低或过高均会影响测定结果,原因是___________。
14.(2023·湖南长沙·长沙市明德中学校考模拟预测)过硼酸钠是一种用途广泛的无机
过氧化物,可用作织物的漂白、染色,医药上可作为消毒剂和杀菌剂。一种由硼镁矿
(Mg B O•H O)制取过硼酸钠(NaBO •4H O)的工艺流程图如下所示。
2 2 5 2 3 2
已知:① ,若pH>10时,以
形式存在;若pH<9.6时,以 形式存在。
②过硼酸钠为白色晶体,微溶于水,其水溶液不稳定,存在于冷的溶液中,难溶于乙
醇。
③硼砂(Na B O•10H O)为白色晶体,溶于水吸热,在水中溶解度如图1所示。
2 4 7 2
试卷第17页,共18页
学科网(北京)股份有限公司回答下列问题:
(1)步骤Ⅰ中为充分快速使硼镁矿浸出,可采取的措施___________。(填两项操作即可)
(2)根据题中信息,写出步骤Ⅱ中的化学方程式___________。
(3)下列说法正确的是___________。
A.步骤Ⅱ中通入的CO 目的是降低溶液pH值使 转为
2
B.步骤Ⅰ、Ⅱ中操作①为过滤,操作②为蒸发浓缩、趁热抽滤
C.步骤Ⅲ发生化学反应生成过硼酸钠(其阴离子结构如图所示),其中硼元素的化合价
升高
D.步骤Ⅳ中宜选用的洗涤剂和干燥方式分别为蒸馏水和减压干燥
(4)步骤Ⅲ的回流反应过程需要控制恒温水浴(0℃左右)的方法是___________。
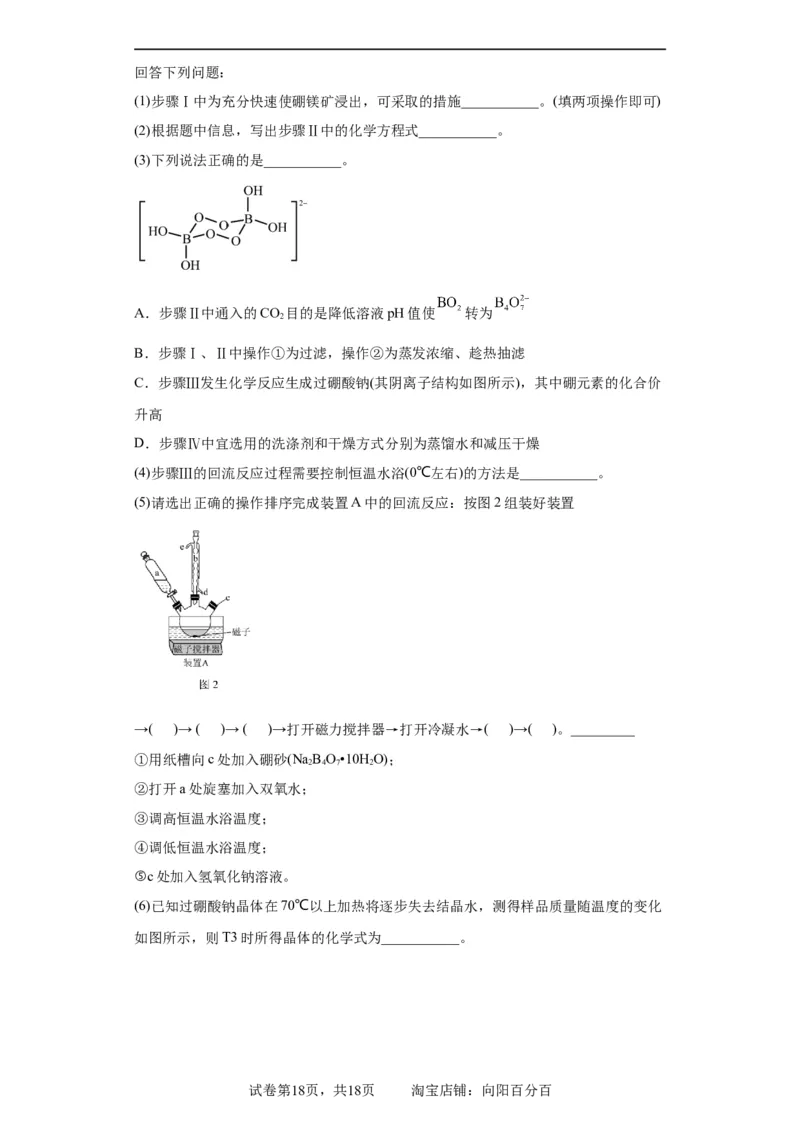
(5)请选出正确的操作排序完成装置A中的回流反应:按图2组装好装置
→( )→ ( )→ ( )→打开磁力搅拌器→打开冷凝水→( )→( )。_________
①用纸槽向c处加入硼砂(Na B O•10H O);
2 4 7 2
②打开a处旋塞加入双氧水;
③调高恒温水浴温度;
④调低恒温水浴温度;
⑤c处加入氢氧化钠溶液。
(6)已知过硼酸钠晶体在70℃以上加热将逐步失去结晶水,测得样品质量随温度的变化
如图所示,则T3时所得晶体的化学式为___________。
试卷第18页,共18页 淘宝店铺:向阳百分百(7)若反应温度控制不当,所得的过硼酸钠晶体中将混有NaBO ,则产品中钠的质量分
2
数___________(填“升高”、“降低”或“不变”)。
15.(2023·广东·校联考模拟预测)碳酸镧[ ,相对分子质量为458]能抑制
人体内磷酸盐的吸收,降低体内血清磷酸盐和磷酸钙的水平,常用于慢性肾衰患者高
磷血症的治疗。某课外小组成员进行实验探究 的制备方法。
已知:
① 难溶于水,易溶于盐酸,溶液pH较高时易生成碱式碳酸镧[ ,
相对分子质量为216]。
②氯化镧( )与易溶的碳酸盐或碳酸氢盐反应可制备 。
Ⅰ.利用氯化镧溶液与碳酸氢铵溶液制备碳酸镧(装置如图1,其中夹持装置已略去)。
实验步骤如下:
ⅰ.连接好实验装置,检查装置的气密性,关闭 、 、 和 。
ⅱ.实验时应先打开活塞______(填“ ”或“ ”)和 ,持续通入一段时间气体。
ⅲ.______,继续通入一段时间另一种气体。
ⅳ.……,最终制得碳酸镧沉淀。
(1)试剂b的名称是______,试剂a的作用是______。装置中硬质玻璃管的作用是
____________。
试卷第19页,共18页
学科网(北京)股份有限公司(2)将操作ⅱ空白处补充完整:____________,将操作ⅲ空白处补充完整:
____________。
(3)实验时,将三颈烧瓶放入冷水中的主要原因是__________________。
(4)氯化镧溶液与碳酸氢铵溶液反应的化学方程式为__________________。
Ⅱ.利用碳酸氢钠溶液与氯化镧溶液制备碳酸镧。
(5)将一定浓度的 溶液滴入氯化镧溶液中,利用手持技术测得氯化镧溶液的pH
随加入 溶液的体积的变化如图2。试分析bc段发生pH突变的原因:
__________________。
Ⅲ.碳酸镧粗产品[设杂质只有 ]组成的测定。
(6)准确称取6.844 g粗产品,溶于10.00 mL稀盐酸中,加入10.00 mL 缓
冲溶液和0.200 g紫脲酸铵混合指示剂,用0.5 molL EDTA( )标准溶液滴定
⋅
至溶液呈蓝紫色( ),消耗60.00 mL EDTA标准溶液。则产品
中n(碳酸镧)∶n(碱式碳酸镧)=______。
试卷第20页,共18页 淘宝店铺:向阳百分百