文档内容
启用前★绝密
长沙市明达中学 2022 年下学期高三年级12月月考
化学试卷
(时间:75 分钟 满分:100 分)
注意事项:
1.答题前,考生务必将自己的学校、姓名、班级、准考证号填写在答题卡上相应的位置。
2.全部答案在答题卡上完成,答在本试卷上无效。
3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案用0.5毫米及以上黑色笔迹签字笔写在答题
卡上。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:C—12 N—14 O—16 V—51 Ga—70
一、选择题:本题共10小题,每小题3分,共30分。每小题只有一个选项符合题意。
1.化学与人类生活、社会可持续发展密切相关,下列说法正确的是( )
A.硫酸钡医学上用作钡餐是因为Ba2+无毒
B.合理利用太阳能、风能和氢能等能源有利于实现“低碳经济”
C.高纯硅广泛应用于光导纤维、太阳能电池和计算机芯片,是因为硅具有半导体性能
D.第24届冬奥会,速滑馆“冰丝带”采用CO 跨临界直冷制冰是化学变化
2
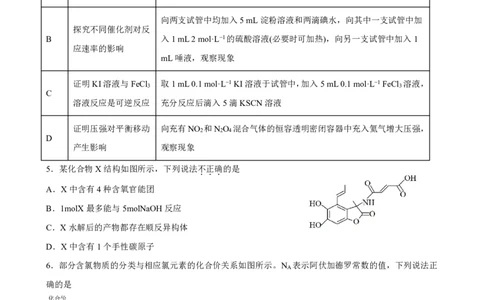
2.化学在生产和日常生活中有着重要的应用,下表中用途与其性质或原理对应关系错误的是
选项 用途 性质或原理
A 硬铝是制造飞机和宇宙飞船的理想材料 硬铝密度小、强度高、具有较强的抗腐蚀能力
B 新制氯水有漂白性 氯气(Cl )具有漂白性
2
C 工业上常用绿矾(FeSO ·7H O) 处理废水中
4 2
Fe2+具有还原性
含有的重铬酸根离子(Cr O 2-)
2 7
D 用小苏打治疗胃酸过多 NaHCO 可中和胃酸
3
3.下列化学用语的表达正确的是
A.原子核内有10个中子的氧原子:16O
8
B.氯原子的结构示意图:
试卷第1页,共8页C.Cr3+的最外层电子排布式:3s23p63d3
D.基态铜原子的价层电子排布图:
4.下列实验的实验目的与实验操作或现象均正确的是
选项 实验目的 实验操作或现象
试管中盛有0.1mol·L−1K Cr O 溶液,溶液中存在平衡Cr O 2-+
2 2 7 2 7
探究浓度对化学平衡
A H O 2CrO 2-+2H+,向其中滴加10滴6mol·L−1NaOH溶液,观察到
2 4
的影响
溶液橙色加深
向两支试管中均加入5mL淀粉溶液和两滴碘水,向其中一支试管中加
探究不同催化剂对反
B 入1mL2mol·L−1的硫酸溶液(必要时可加热),向另一支试管中加入1
应速率的影响
mL唾液,观察现象
证明KI溶液与FeCl 取1mL0.1mol·L−1KI溶液于试管中,加入5mL0.1mol·L−1FeCl 溶液,
3 3
C
溶液反应是可逆反应 充分反应后滴入5滴KSCN溶液
证明压强对平衡移动 向充有NO 和N O 混合气体的恒容透明密闭容器中充入氦气增大压强,
2 2 4
D
产生影响 观察现象
5.某化合物X结构如图所示,下列说法不
.
正
.
确
.
的是
A.X中含有4种含氧官能团
B.1molX最多能与5molNaOH反应
C.X水解后的产物都存在顺反异构体
D.X中含有1个手性碳原子
6.部分含氯物质的分类与相应氯元素的化合价关系如图所示。N 表示阿伏加德罗常数的值,下列说法正
A
确的是
A.1L0.1mol·L1的a的水溶液中氢原子的数目为0.1N
A
B.11.2LCH 和22.4Lb(均为标准状况)在光照下充分反应后的分子总数一定为1.5N
4 A
试卷第2页,共8页C.0.2mol·L-1的d溶液中含有H+数为0.2N
A
D.用a的浓溶液分别和MnO 、KClO 反应制备1molb,转移的电子数均为2N
2 3 A
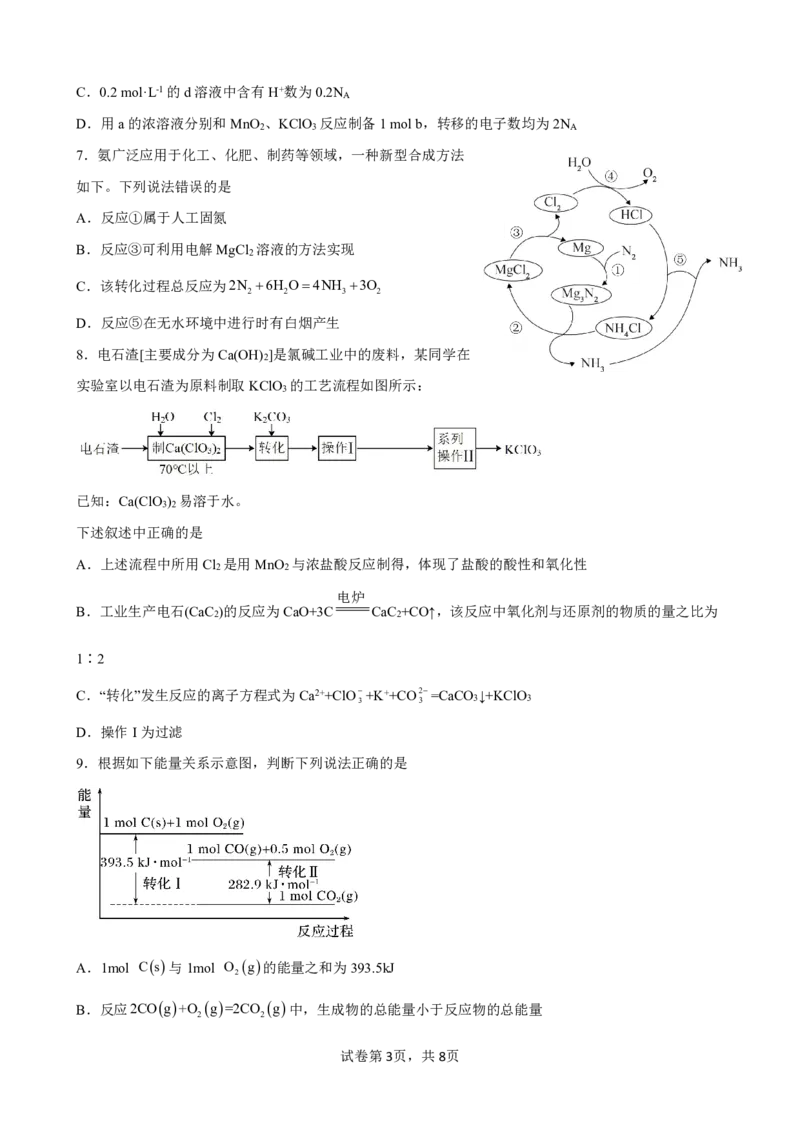
7.氨广泛应用于化工、化肥、制药等领域,一种新型合成方法
如下。下列说法错误的是
A.反应①属于人工固氮
B.反应③可利用电解MgCl 溶液的方法实现
2
C.该转化过程总反应为2N 6H O4NH 3O
2 2 3 2
D.反应⑤在无水环境中进行时有白烟产生
8.电石渣[主要成分为Ca(OH) ]是氯碱工业中的废料,某同学在
2
实验室以电石渣为原料制取KClO 的工艺流程如图所示:
3
已知:Ca(ClO ) 易溶于水。
3 2
下述叙述中正确的是
A.上述流程中所用Cl 是用MnO 与浓盐酸反应制得,体现了盐酸的酸性和氧化性
2 2
电炉
B.工业生产电石(CaC )的反应为CaO+3C CaC +CO↑,该反应中氧化剂与还原剂的物质的量之比为
2 2
1∶2
C.“转化”发生反应的离子方程式为Ca2++ClO+K++CO2=CaCO ↓+KClO
3 3 3 3
D.操作I为过滤
9.根据如下能量关系示意图,判断下列说法正确的是
A.1mol Cs与1mol O g的能量之和为393.5kJ
2
B.反应2COg+O g=2CO g中,生成物的总能量小于反应物的总能量
2 2
试卷第3页,共8页C.由CsCOg的热化学方程式为2Cs+O g=2COg ΔH=110.6kJmol1
2
D.已知热值指一定条件下单位质量的物质完全燃烧所放出的热量,则CO的热值为10.1kJmol1
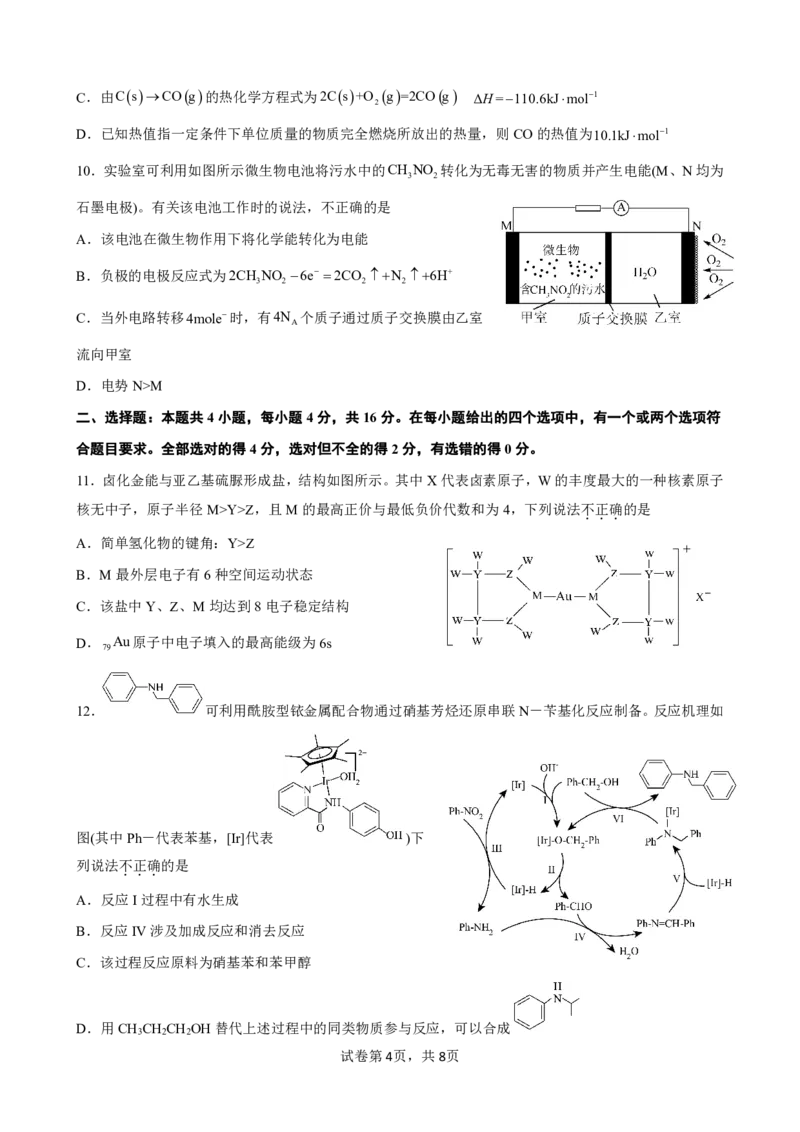
10.实验室可利用如图所示微生物电池将污水中的CH NO 转化为无毒无害的物质并产生电能(M、N均为
3 2
石墨电极)。有关该电池工作时的说法,不正确的是
A.该电池在微生物作用下将化学能转化为电能
B.负极的电极反应式为2CH NO 6e 2CO N 6H
3 2 2 2
C.当外电路转移4mole时,有4N 个质子通过质子交换膜由乙室
A
流向甲室
D.电势N>M
二、选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一个或两个选项符
合题目要求。全部选对的得4分,选对但不全的得2分,有选错的得0分。
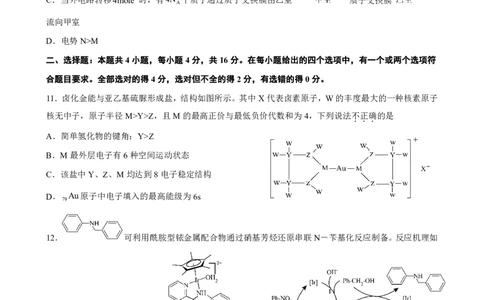
11.卤化金能与亚乙基硫脲形成盐,结构如图所示。其中X代表卤素原子,W的丰度最大的一种核素原子
核无中子,原子半径M>Y>Z,且M的最高正价与最低负价代数和为4,下列说法不
.
正
.
确
.
的是
A.简单氢化物的键角:Y>Z
B.M最外层电子有6种空间运动状态
C.该盐中Y、Z、M均达到8电子稳定结构
D. Au原子中电子填入的最高能级为6s
79
12. 可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如
图(其中Ph-代表苯基,[Ir]代表 )下
列说法不正确的是
...
A.反应I过程中有水生成
B.反应IV涉及加成反应和消去反应
C.该过程反应原料为硝基苯和苯甲醇
D.用CH CH CH OH替代上述过程中的同类物质参与反应,可以合成
3 2 2
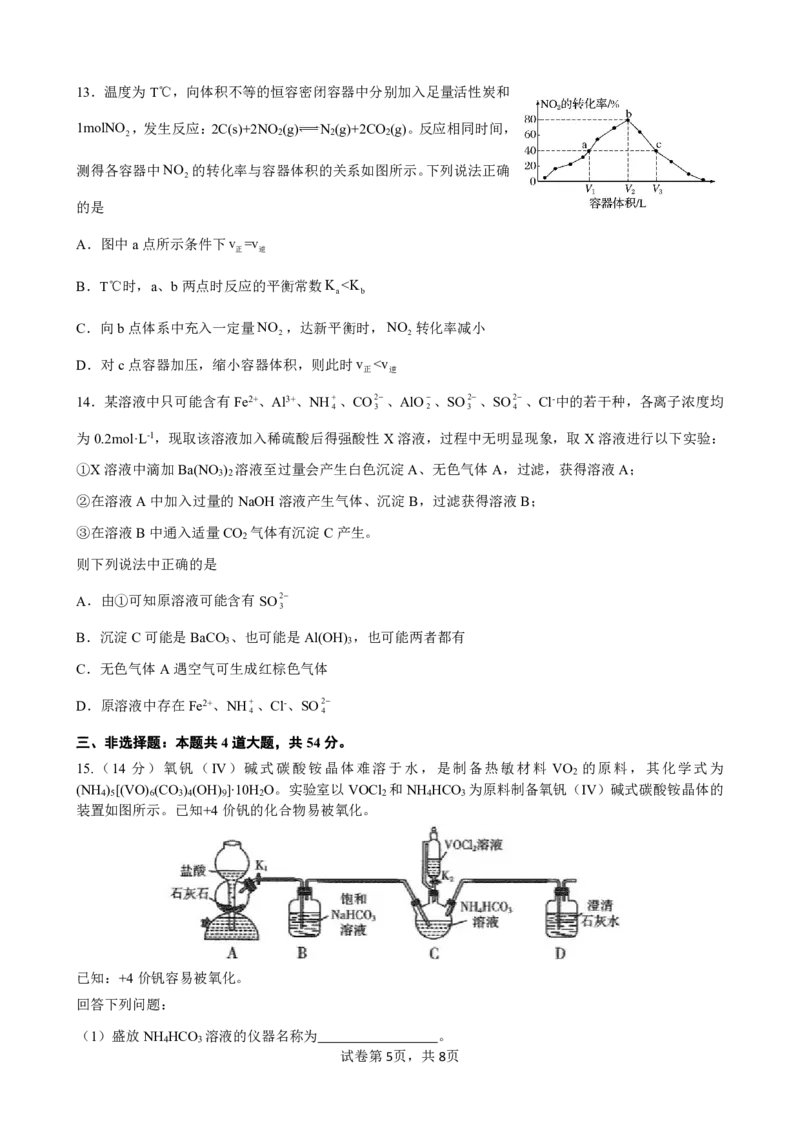
试卷第4页,共8页13.温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和
1molNO ,发生反应:2C(s)+2NO (g) N (g)+2CO (g)。反应相同时间,
2 2 2 2
测得各容器中NO 的转化率与容器体积的关系如图所示。下列说法正确
2
的是
A.图中a点所示条件下v =v
正 逆
B.T℃时,a、b两点时反应的平衡常数K C>Si(1分) (3) 平面三角形(1分) sp2(1分)
844
(4) 6
N
4.41083 (5) -90.3kJ/mol AC 2
A
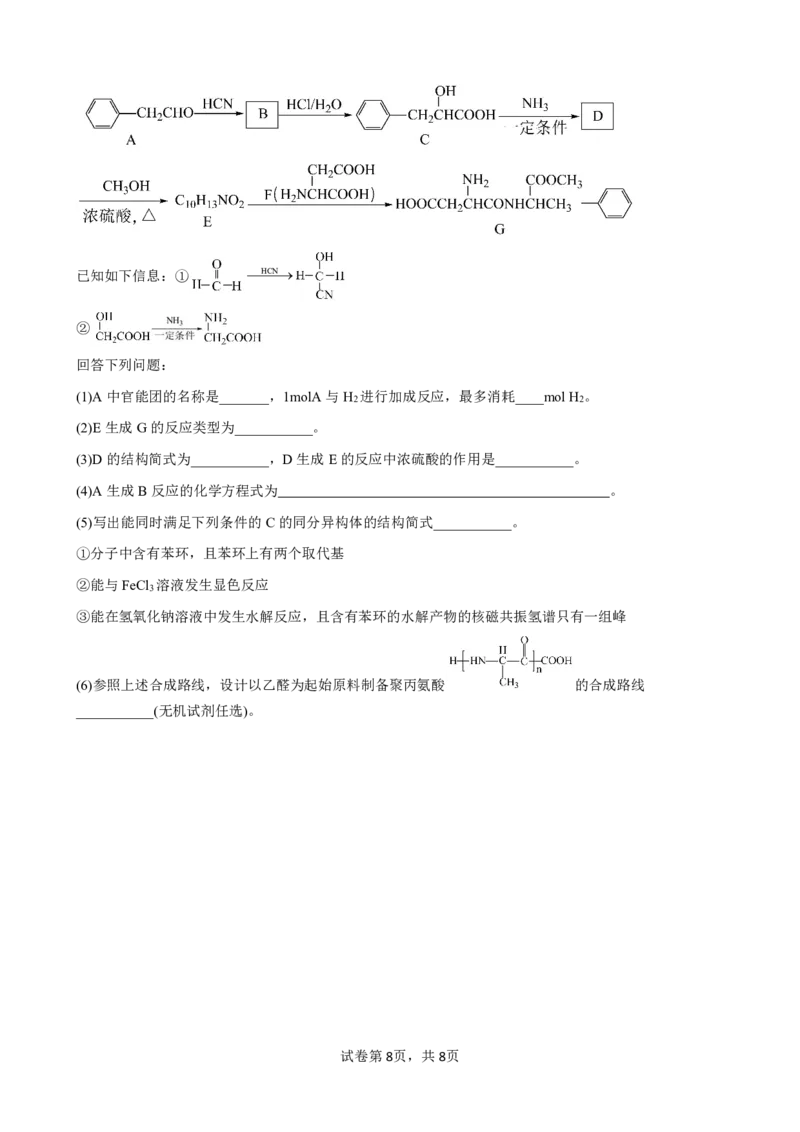
18.(12分)(1) 醛基(1分) 4(1分) (2)取代反应 (1分)
(3) (1分) 催化作用和吸水作用 (1分)
(4) +HCN ;(2分)(5) (2分)
(6)CH CHOHCNCH CH(OH)CNHCl/H2OCH CH(OH)COOHNH3
3 3 3 一定条件
CH CH(NH )COOH (3分)
3 2
答案第1页,共1页