文档内容
热点 06 化学反应机理(反应历程)图像分析
►命题趋势►解题策略►真题回眸►限时检测
考向一 相对能量变化图
考向二 催化剂过渡态能量变化图
化学反应机理(反应历程)图像分析
考向三 无机反应机理图分析
考向四 有机反应机理图分析
新高考强调素养为本的情境化命题,高考通过真实情境的创设,考查学生的信息获取能力和创新思维。
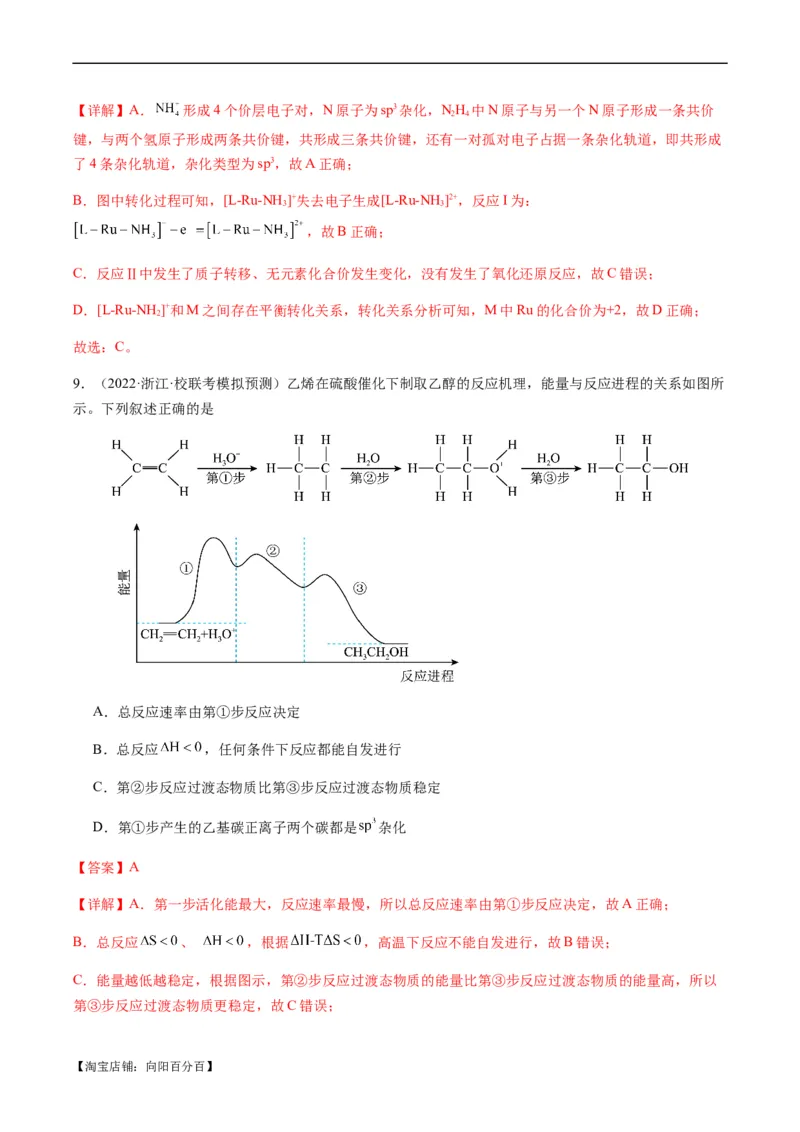
近几年高考中,化学反应机理(反应历程)试题频繁出现,题目主要以图示的形式来描述某一化学变化所
经由的全部反应,就是把一个复杂反应分解成若干个反应,然后按照一定规律组合起来,从而达到阐述复
杂反应的内在联系的目的。
预计在2024年高考中,会以选择题的形式出现,以及在化学反应原理大题中有所涉及,其中以催化剂
的催化反应机理和能垒图像为情境载体进行命题的可能性很大。由于陌生度高,思维转化大,且命题视角
在不断地创新和发展,成为大多数考生的失分点。所以,很有必要对这两类题型的解题模型进行掌握。
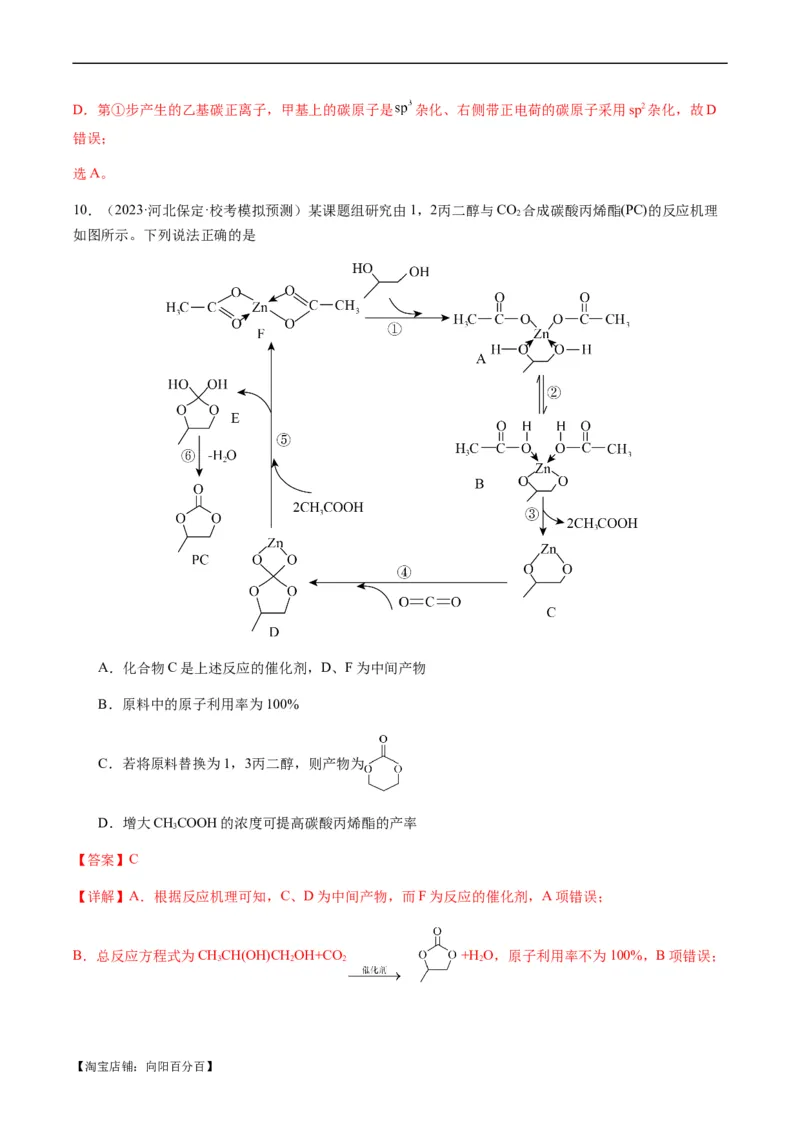
【策略1】理解基元反应、过渡态理论相关知识点
1.基元反应
大多数化学反应都是分几步完成的,其中的每一步反应都称为基元反应。
2.对于基元反应aA+bB===gG+hH,其速率方程可写为v=k·ca(A)·cb(B)(其中k称为速率常数,恒温下,
k不因反应物浓度的改变而变化),这种关系可以表述为基元反应的化学反应速率与反应物浓度以其化学计
量数为指数的幂的乘积成正比。有时称其为质量作用定律。
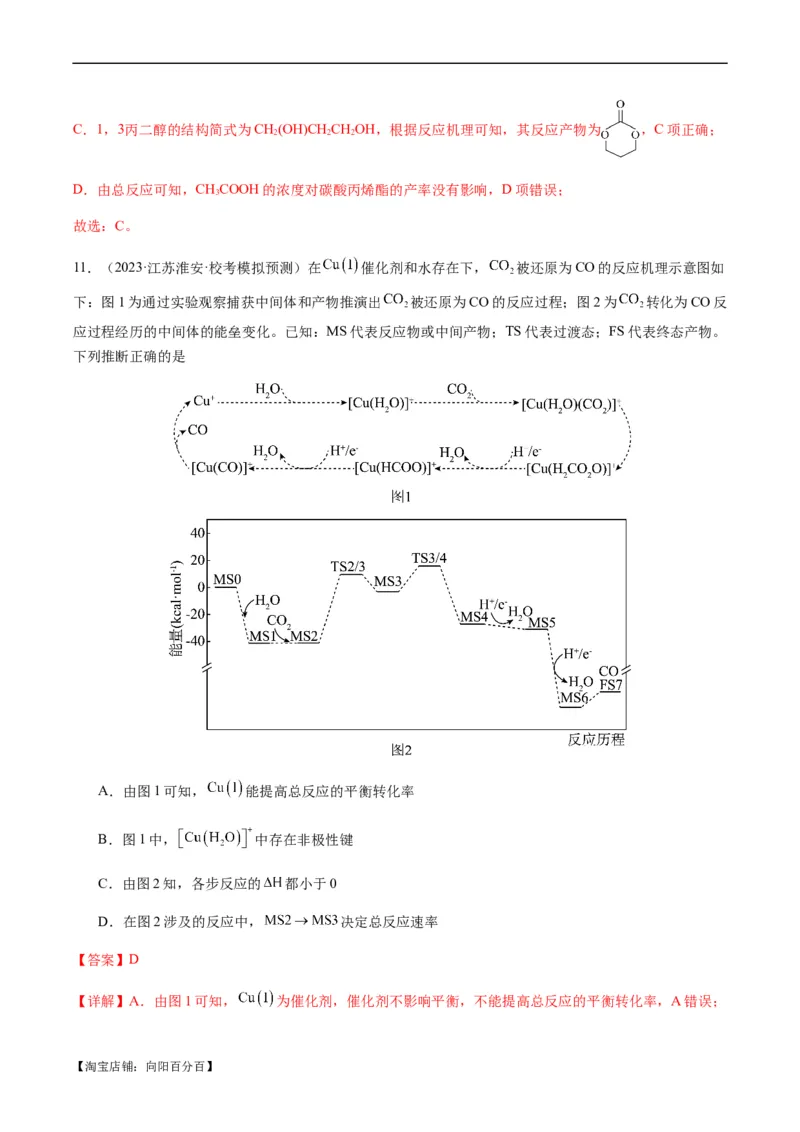
3.许多化学反应,尽管其反应方程式很简单,却不是基元反应,而是经由两个或多个步骤完成的复杂反
应。例如H(g)+I(g)===2HI(g),它的反应历程有如下两步基元反应:
2 2
①I I+I(快)
2
②H +2I === 2HI(慢)
2
其中慢反应为整个反应的决速步骤。
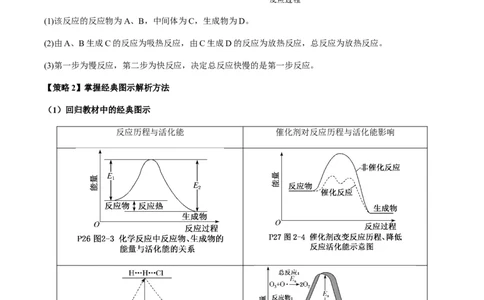
【淘宝店铺:向阳百分百】4.过渡态理论
如图所示是两步完成的化学反应,分析并回答下列问题。
(1)该反应的反应物为A、B,中间体为C,生成物为D。
(2)由A、B生成C的反应为吸热反应,由C生成D的反应为放热反应,总反应为放热反应。
(3)第一步为慢反应,第二步为快反应,决定总反应快慢的是第一步反应。
【策略2】掌握经典图示解析方法
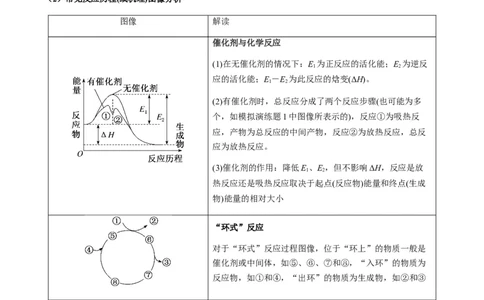
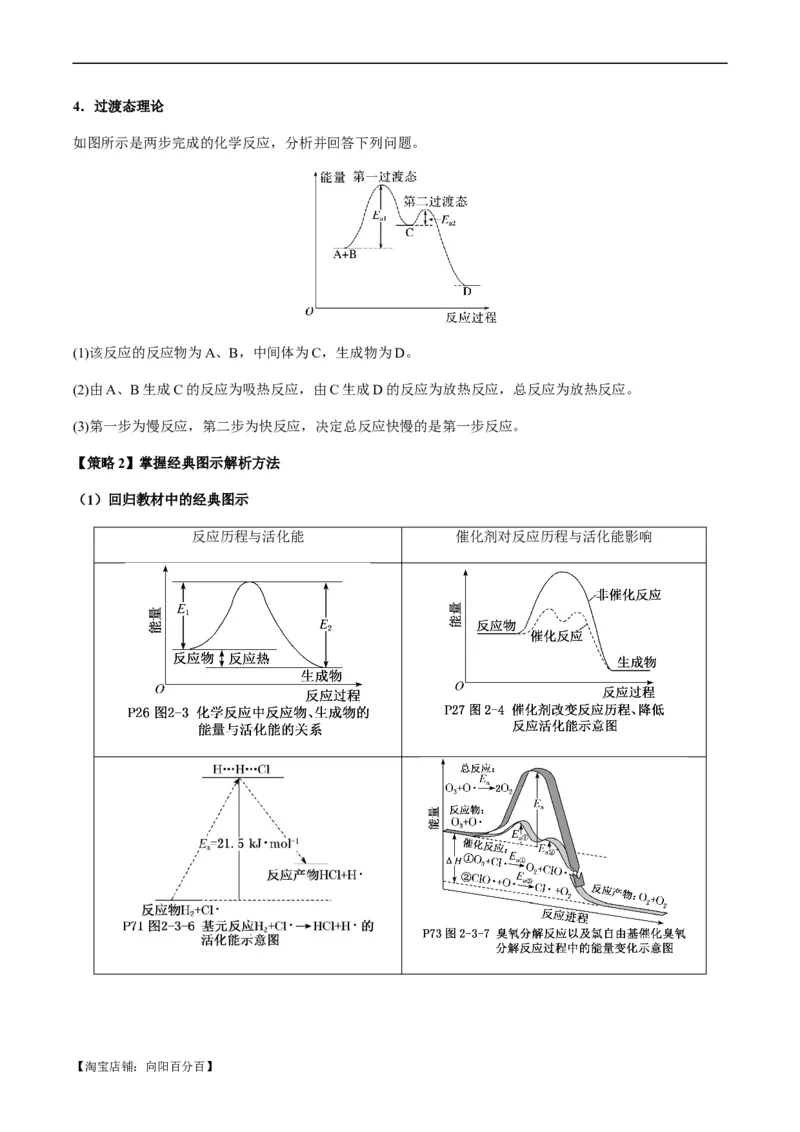
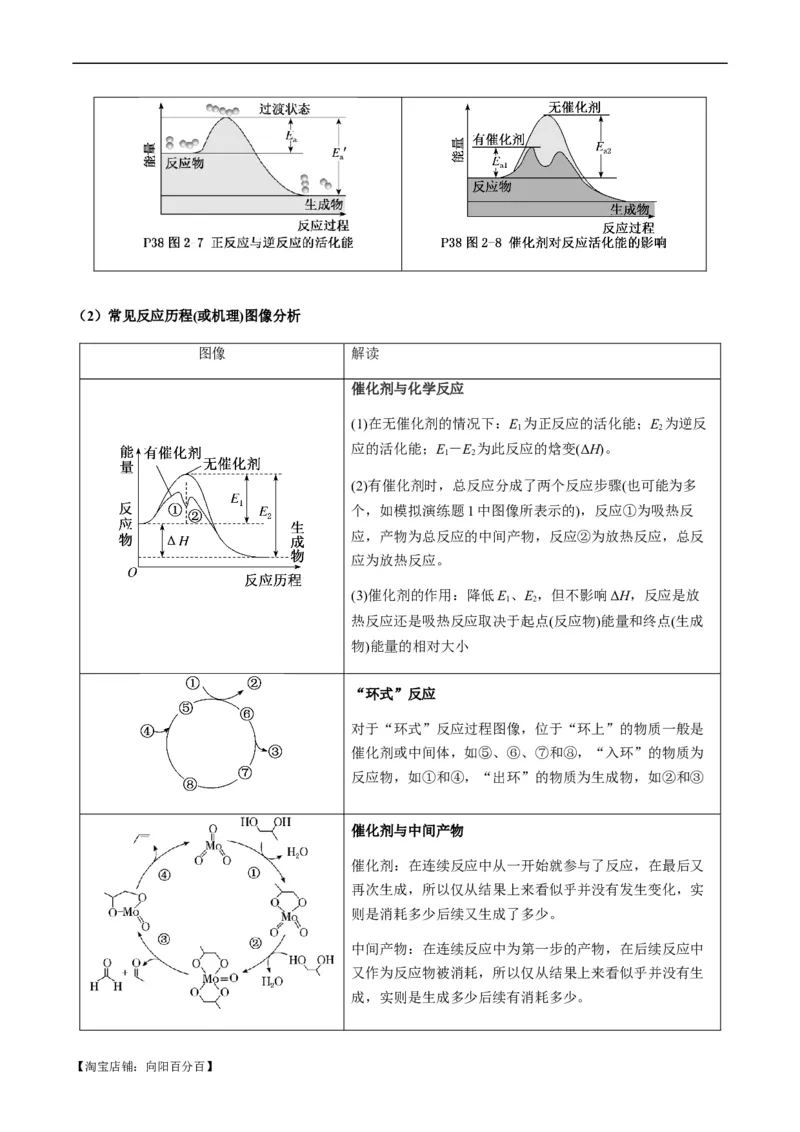
(1)回归教材中的经典图示
反应历程与活化能 催化剂对反应历程与活化能影响
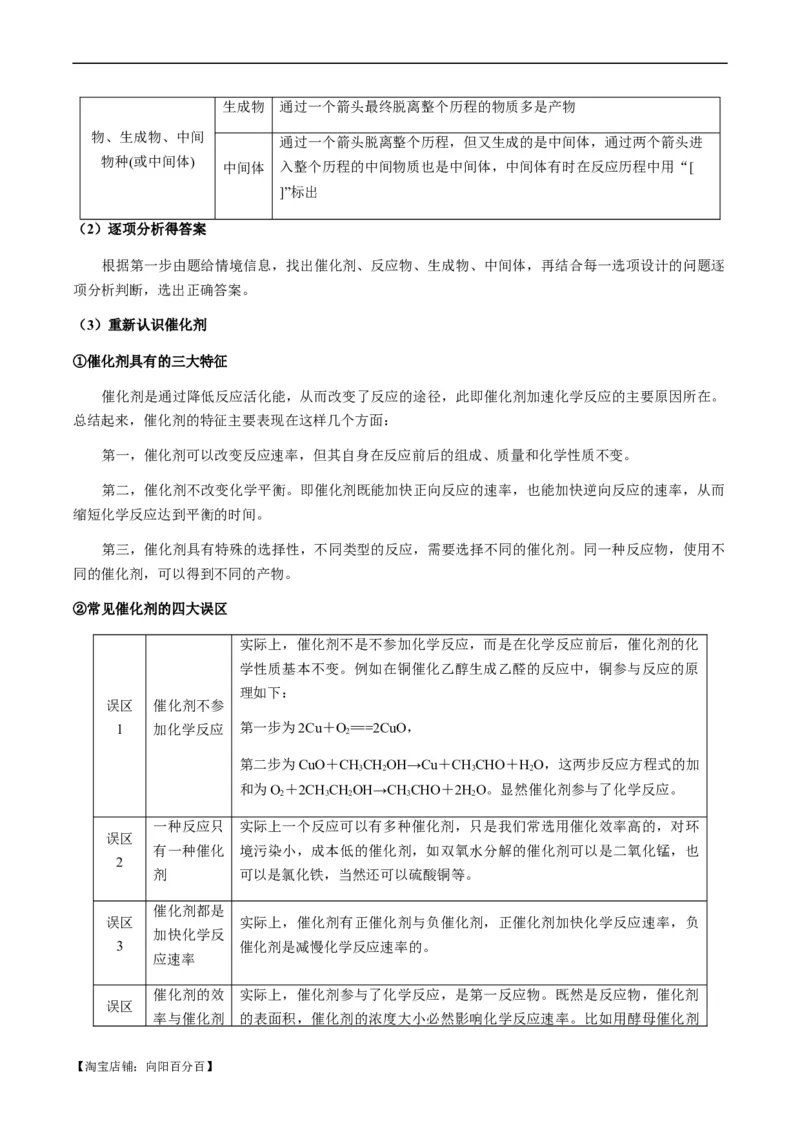
【淘宝店铺:向阳百分百】(2)常见反应历程(或机理)图像分析
图像 解读
催化剂与化学反应
(1)在无催化剂的情况下:E 为正反应的活化能;E 为逆反
1 2
应的活化能;E-E 为此反应的焓变(ΔH)。
1 2
(2)有催化剂时,总反应分成了两个反应步骤(也可能为多
个,如模拟演练题1中图像所表示的),反应①为吸热反
应,产物为总反应的中间产物,反应②为放热反应,总反
应为放热反应。
(3)催化剂的作用:降低E、E,但不影响ΔH,反应是放
1 2
热反应还是吸热反应取决于起点(反应物)能量和终点(生成
物)能量的相对大小
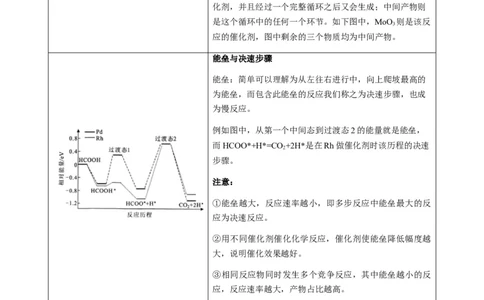
“环式”反应
对于“环式”反应过程图像,位于“环上”的物质一般是
催化剂或中间体,如⑤、⑥、⑦和⑧,“入环”的物质为
反应物,如①和④,“出环”的物质为生成物,如②和③
催化剂与中间产物
催化剂:在连续反应中从一开始就参与了反应,在最后又
再次生成,所以仅从结果上来看似乎并没有发生变化,实
则是消耗多少后续又生成了多少。
中间产物:在连续反应中为第一步的产物,在后续反应中
又作为反应物被消耗,所以仅从结果上来看似乎并没有生
成,实则是生成多少后续有消耗多少。
【淘宝店铺:向阳百分百】例1:在含少量 I-的溶液中,HO 分解的机理为:
2 2
HO + I- → H O + IO- 慢
2 2 2
HO + IO-→ O + I- +H O 快
2 2 2 2
在该反应中I-为催化剂, IO-为中间产物。
1,2-丙二醇脱氧脱水反应的催化循环机理
例2:而在机理图中,先找到确定的反应物,反应物一般
是通过一个箭头进入整个历程的物质,(产物一般多是通过
一个箭头最终脱离这个历程的物质)与之同时反应的就是催
化剂,并且经过一个完整循环之后又会生成;中间产物则
是这个循环中的任何一个环节。如下图中,MoO 则是该反
3
应的催化剂,图中剩余的三个物质均为中间产物。
能垒与决速步骤
能垒:简单可以理解为从左往右进行中,向上爬坡最高的
为能垒,而包含此能垒的反应我们称之为决速步骤,也成
为慢反应。
例如图中,从第一个中间态到过渡态2的能量就是能垒,
而HCOO*+H*=CO +2H*是在Rh做催化剂时该历程的决速
2
步骤。
注意:
①能垒越大,反应速率越小,即多步反应中能垒最大的反
应为决速反应。
②用不同催化剂催化化学反应,催化剂使能垒降低幅度越
大,说明催化效果越好。
③相同反应物同时发生多个竞争反应,其中能垒越小的反
应,反应速率越大,产物占比越高。
【策略3】掌握催化反应机理题的解题思路
(1)通览全图,找准一“剂”三“物”
催化剂在机理图中多数是以完整的循环出现的,以催化剂粒子为主题的多个物
一“剂”指催化剂
种一定在机理图中的主线上
反应物 通过一个箭头进入整个历程的物质一般是反应物
三“物”指反应
【淘宝店铺:向阳百分百】生成物 通过一个箭头最终脱离整个历程的物质多是产物
物、生成物、中间
通过一个箭头脱离整个历程,但又生成的是中间体,通过两个箭头进
物种(或中间体)
中间体 入整个历程的中间物质也是中间体,中间体有时在反应历程中用“[
]”标出
(2)逐项分析得答案
根据第一步由题给情境信息,找出催化剂、反应物、生成物、中间体,再结合每一选项设计的问题逐
项分析判断,选出正确答案。
(3)重新认识催化剂
①催化剂具有的三大特征
催化剂是通过降低反应活化能,从而改变了反应的途径,此即催化剂加速化学反应的主要原因所在。
总结起来,催化剂的特征主要表现在这样几个方面:
第一,催化剂可以改变反应速率,但其自身在反应前后的组成、质量和化学性质不变。
第二,催化剂不改变化学平衡。即催化剂既能加快正向反应的速率,也能加快逆向反应的速率,从而
缩短化学反应达到平衡的时间。
第三,催化剂具有特殊的选择性,不同类型的反应,需要选择不同的催化剂。同一种反应物,使用不
同的催化剂,可以得到不同的产物。
②常见催化剂的四大误区
实际上,催化剂不是不参加化学反应,而是在化学反应前后,催化剂的化
学性质基本不变。例如在铜催化乙醇生成乙醛的反应中,铜参与反应的原
理如下:
误区 催化剂不参
1 加化学反应 第一步为2Cu+O===2CuO,
2
第二步为CuO+CHCHOH→Cu+CHCHO+HO,这两步反应方程式的加
3 2 3 2
和为O+2CHCHOH→CH CHO+2HO。显然催化剂参与了化学反应。
2 3 2 3 2
一种反应只 实际上一个反应可以有多种催化剂,只是我们常选用催化效率高的,对环
误区
有一种催化 境污染小,成本低的催化剂,如双氧水分解的催化剂可以是二氧化锰,也
2
剂 可以是氯化铁,当然还可以硫酸铜等。
催化剂都是
误区 实际上,催化剂有正催化剂与负催化剂,正催化剂加快化学反应速率,负
加快化学反
3 催化剂是减慢化学反应速率的。
应速率
催化剂的效 实际上,催化剂参与了化学反应,是第一反应物。既然是反应物,催化剂
误区
率与催化剂 的表面积,催化剂的浓度大小必然影响化学反应速率。比如用酵母催化剂
【淘宝店铺:向阳百分百】4 的量无关 做食品,酵母量大自然面就膨大快。催化剂的用量是会改变催化效率的。
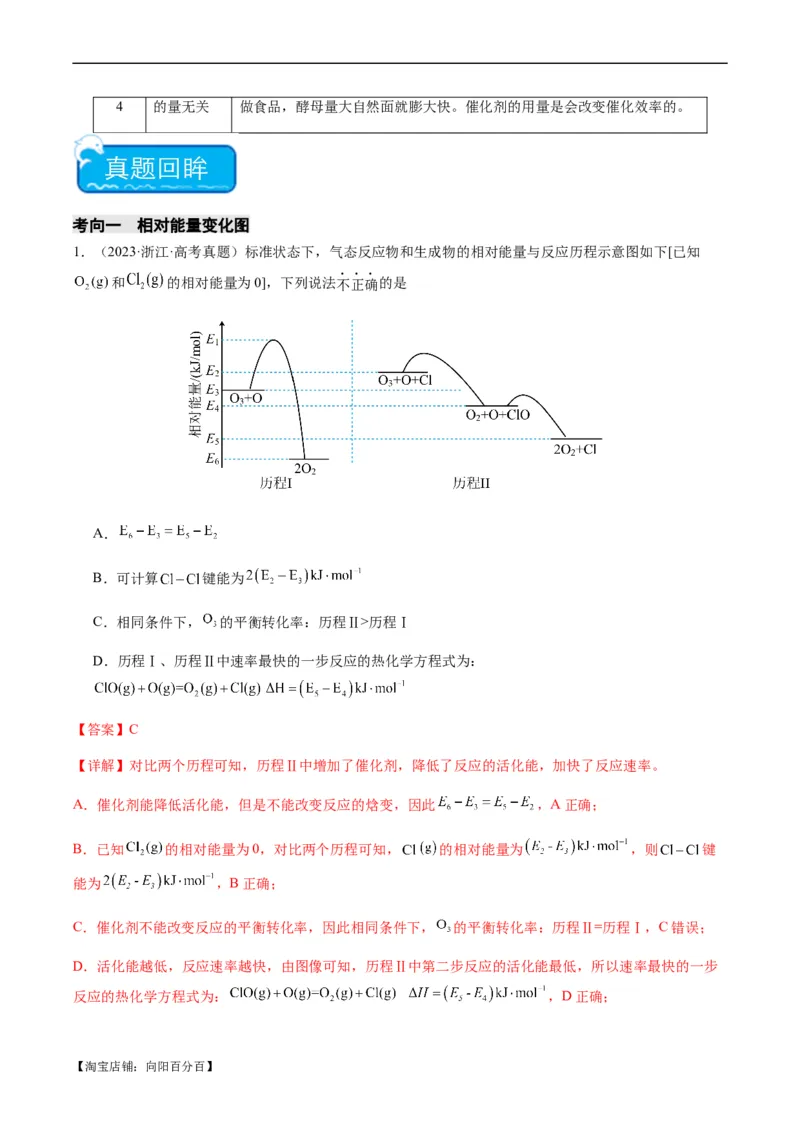
考向一 相对能量变化图
1.(2023·浙江·高考真题)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知
和 的相对能量为0],下列说法不正确的是
A.
B.可计算 键能为
C.相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
【答案】C
【详解】对比两个历程可知,历程Ⅱ中增加了催化剂,降低了反应的活化能,加快了反应速率。
A.催化剂能降低活化能,但是不能改变反应的焓变,因此 ,A正确;
B.已知 的相对能量为0,对比两个历程可知, 的相对能量为 ,则 键
能为 ,B正确;
C.催化剂不能改变反应的平衡转化率,因此相同条件下, 的平衡转化率:历程Ⅱ=历程Ⅰ,C错误;
D.活化能越低,反应速率越快,由图像可知,历程Ⅱ中第二步反应的活化能最低,所以速率最快的一步
反应的热化学方程式为: ,D正确;
【淘宝店铺:向阳百分百】故答案为:C。
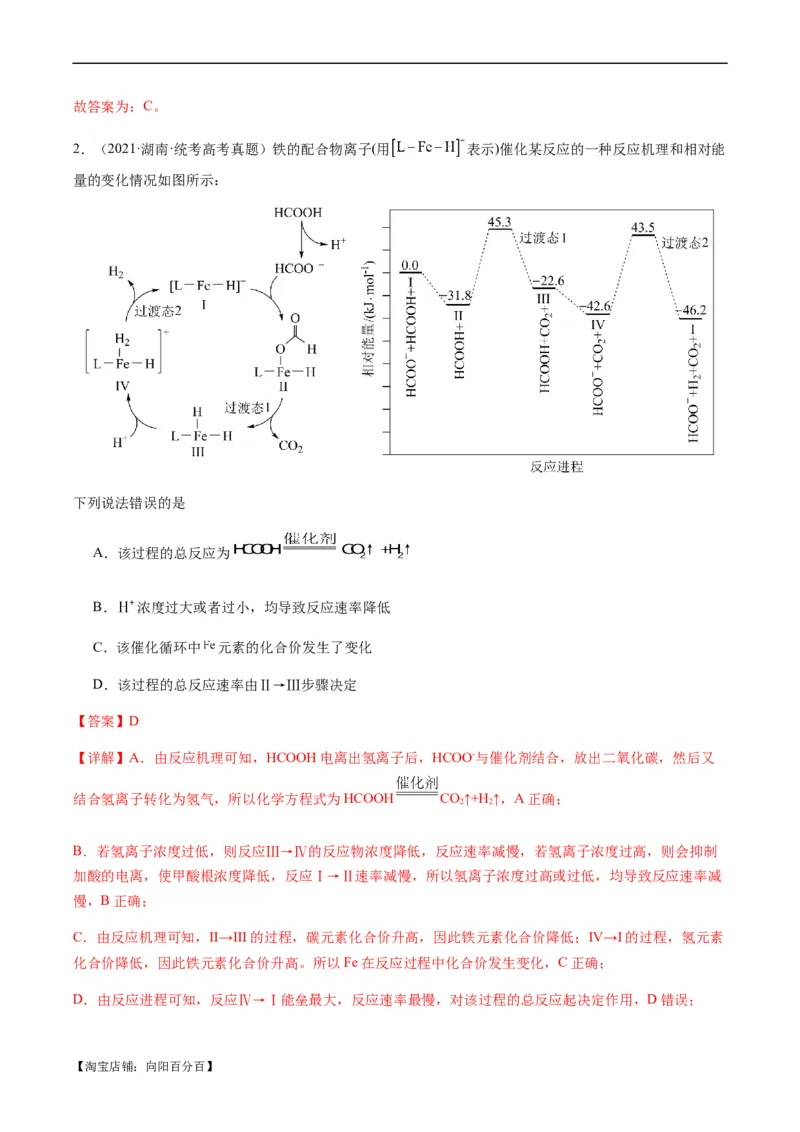
2.(2021·湖南·统考高考真题)铁的配合物离子(用 表示)催化某反应的一种反应机理和相对能
量的变化情况如图所示:
下列说法错误的是
A.该过程的总反应为
B. 浓度过大或者过小,均导致反应速率降低
C.该催化循环中 元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
【答案】D
【详解】A.由反应机理可知,HCOOH电离出氢离子后,HCOO-与催化剂结合,放出二氧化碳,然后又
结合氢离子转化为氢气,所以化学方程式为HCOOH CO↑+H ↑,A正确;
2 2
B.若氢离子浓度过低,则反应Ⅲ→Ⅳ的反应物浓度降低,反应速率减慢,若氢离子浓度过高,则会抑制
加酸的电离,使甲酸根浓度降低,反应Ⅰ→Ⅱ速率减慢,所以氢离子浓度过高或过低,均导致反应速率减
慢,B正确;
C.由反应机理可知,II→III的过程,碳元素化合价升高,因此铁元素化合价降低;IV→I的过程,氢元素
化合价降低,因此铁元素化合价升高。所以Fe在反应过程中化合价发生变化,C正确;
D.由反应进程可知,反应Ⅳ→Ⅰ能垒最大,反应速率最慢,对该过程的总反应起决定作用,D错误;
【淘宝店铺:向阳百分百】故选D。
3.(2023·重庆·统考高考真题·节选)银及其化合物在催化与电化学等领域中具有重要应用。
(1)在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图所示,回答下列问题:
①中间体 生成吸附态 的活化能为 。
②由 生成 的热化学方程式为 。
【答案】(1)83
【详解】
(1)①过渡态物质的总能量与反应物总能量的差值为活化能,中间体 生成吸附态 的活化能为
。
②由图可知, 生成 放出热量 ,放热焓变为负值,
故热化学方程式为 ;
考向二 催化剂过渡态能量变化图
4.(2023·湖南·统考高考真题) 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我
国科学家合成的某 (Ⅱ)催化剂(用 表示)能高效电催化氧化 合成 ,其反应机理如
图所示。
【淘宝店铺:向阳百分百】下列说法错误的是
A. (Ⅱ)被氧化至 (Ⅲ)后,配体 失去质子能力增强
B.M中 的化合价为
C.该过程有非极性键的形成
D.该过程的总反应式:
【答案】B
【详解】A. (Ⅱ)被氧化至 (Ⅲ)后, 中的 带有更多的正电荷,其与N原子成键后,
吸引电子的能力比 (Ⅱ)强,这种作用使得配体 中的 键极性变强且更易断裂,因此其失去
质子( )的能力增强,A说法正确;
B. (Ⅱ)中 的化合价为+2,当其变为 (Ⅲ)后, 的化合价变为+3, (Ⅲ)失去2个质子后,N原
子产生了1个孤电子对, 的化合价不变;M为 ,当 变为M时,N原子
的孤电子对拆为2个电子并转移给 1个电子,其中 的化合价变为 ,因此,B说法不正确;
C.该过程M变为 时,有 键形成, 是非极性键,C说法正确;
D.从整个过程来看, 4个 失去了2个电子后生成了1个 和2个 , (Ⅱ)是催化剂,因此,
该过程的总反应式为 ,D说法正确;
综上所述,本题选B。
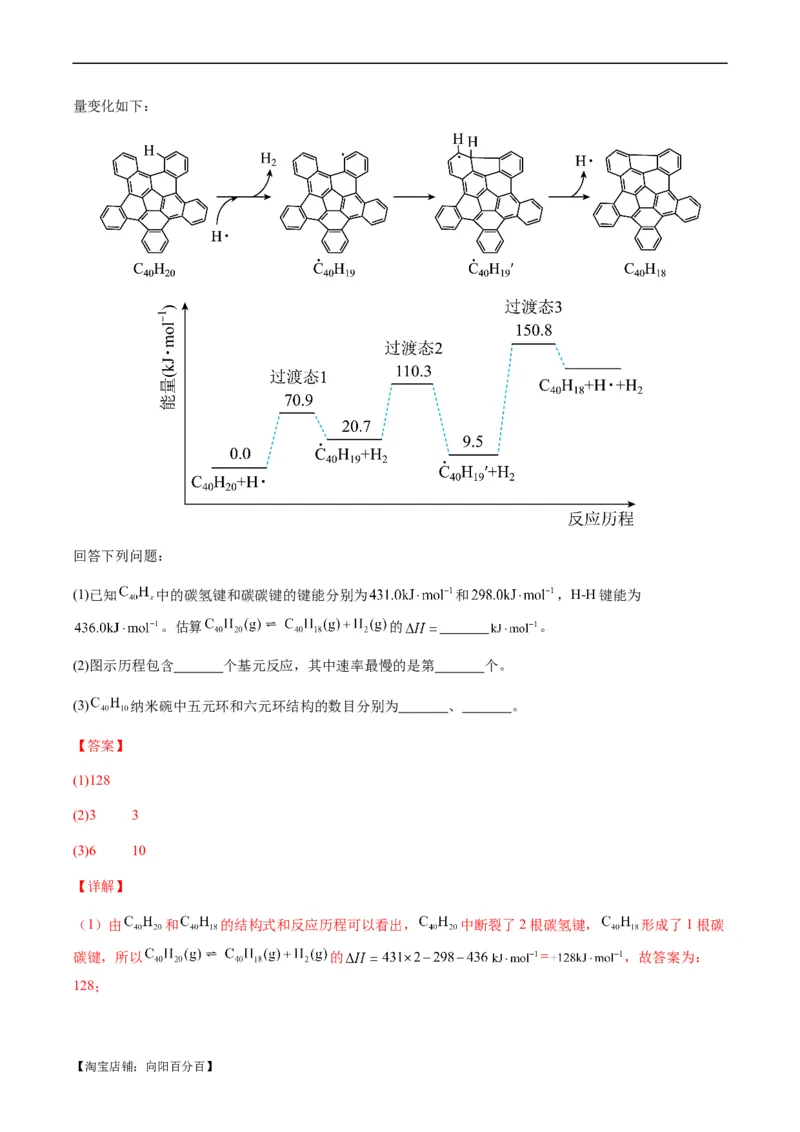
5.(2023·湖北·统考高考真题·节选)纳米碗 是一种奇特的碗状共轭体系。高温条件下, 可以
由 分子经过连续5步氢抽提和闭环脱氢反应生成。 的反应机理和能
【淘宝店铺:向阳百分百】量变化如下:
回答下列问题:
(1)已知 中的碳氢键和碳碳键的键能分别为 和 ,H-H键能为
。估算 的 。
(2)图示历程包含 个基元反应,其中速率最慢的是第 个。
(3) 纳米碗中五元环和六元环结构的数目分别为 、 。
【答案】
(1)128
(2)3 3
(3)6 10
【详解】
(1)由 和 的结构式和反应历程可以看出, 中断裂了2根碳氢键, 形成了1根碳
碳键,所以 的 = ,故答案为:
128;
【淘宝店铺:向阳百分百】(2)由反应历程可知,包含3个基元反应,分别为: ,
, ,其中第三个的活化能最大,反应速率最慢,故
答案为:3;3;
(3)由 的结构分析,可知其中含有1个五元环,10个六元环,每脱两个氢形成一个五元环,则
总共含有6个五元环,10个六元环,故答案为:6;10;
考向三 无机反应机理图分析
6.(2023·重庆·统考高考真题) 和 均可发生水解反应,其中 的水解机理示意图如下:
下列说法正确的是
A. 和 均为极性分子 B. 和 中的 均为 杂化
C. 和 的水解反应机理相同 D. 和 均能与 形成氢键
【答案】D
【详解】A. 中中心原子N周围的价层电子对数为:3+ =4,故空间构型为三角锥形,其分子
中正、负电荷中心不重合,为极性分子,而 中中心原子周围的价层电子对数为:4+ =4,是
正四面体形结构,为非极性分子,A错误;
B. 和 中中心原子N周围的价层电子对数均为:3+ =4,故二者 均为 杂化,B错误;
C.由题干NCl 反应历程图可知,NCl 水解时首先HO中的H原子与NCl 上的孤电子对结合,O与Cl结
3 3 2 3
合形成HClO,而SiCl 上无孤电子对,故SiCl 的水解反应机理与之不相同,C错误;
4 4
D. 和 分子中均存在N-H键和孤电子对,故均能与 形成氢键,D正确;
故答案为:D。
7.(2020·全国·统考高考真题)据文献报道:Fe(CO) 催化某反应的一种反应机理如下图所示。下列叙述
5
错误的是
【淘宝店铺:向阳百分百】A.OH-参与了该催化循环 B.该反应可产生清洁燃料H
2
C.该反应可消耗温室气体CO D.该催化循环中Fe的成键数目发生变化
2
【答案】C
【详解】题干中明确指出,铁配合物Fe(CO) 充当催化剂的作用。机理图中,凡是出现在历程中,进去的
5
箭头表示反应物,出来的箭头表示生成物,既有进去又有出来的箭头表示为催化剂或反应条件,其余可以
看成为中间物种。由题干中提供的反应机理图可知,铁配合物Fe(CO) 在整个反应历程中成键数目,配体
5
种类等均发生了变化;并且也可以观察出,反应过程中所需的反应物除CO外还需要HO,最终产物是
2
CO 和H,同时参与反应的还有OH-,故OH-也可以看成是另一个催化剂或反应条件。
2 2
A.从反应机理图中可知,OH-有进入的箭头也有出去的箭头,说明OH-参与了该催化循环,故A项正确;
B.从反应机理图中可知,该反应的反应物为CO和HO,产物为H 和CO,Fe(CO) 作为整个反应的催化
2 2 2 5
剂,而OH-仅仅在个别步骤中辅助催化剂完成反应,说明该反应方程式为 ,故有
清洁燃料H 生成,故 B项正确;
2
C.由B项分析可知,该反应不是消耗温室气体CO,反而是生成了温室气体CO,故 C项不正确;
2 2
D.从反应机理图中可知,Fe的成键数目和成键微粒在该循环过程中均发生了变化,故 D项正确;
答案选C。
考向四 有机反应机理图分析
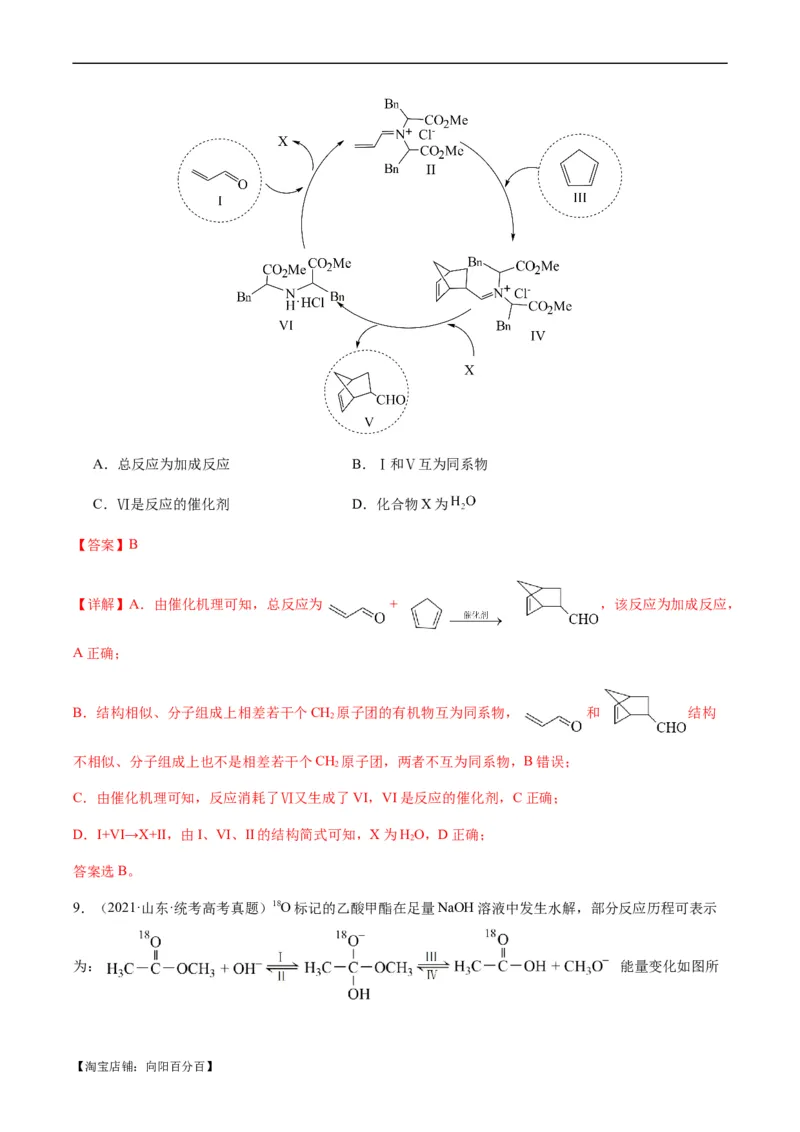
8.(2022·辽宁·统考高考真题)利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得重要进展,
荣获2021年诺贝尔化学奖。某Diels-Alder反应催化机理如下,下列说法错误的是
【淘宝店铺:向阳百分百】A.总反应为加成反应 B.Ⅰ和Ⅴ互为同系物
C.Ⅵ是反应的催化剂 D.化合物X为
【答案】B
【详解】A.由催化机理可知,总反应为 + ,该反应为加成反应,
A正确;
B.结构相似、分子组成上相差若干个CH 原子团的有机物互为同系物, 和 结构
2
不相似、分子组成上也不是相差若干个CH 原子团,两者不互为同系物,B错误;
2
C.由催化机理可知,反应消耗了Ⅵ又生成了VI,VI是反应的催化剂,C正确;
D.I+VI→X+II,由I、VI、II的结构简式可知,X为HO,D正确;
2
答案选B。
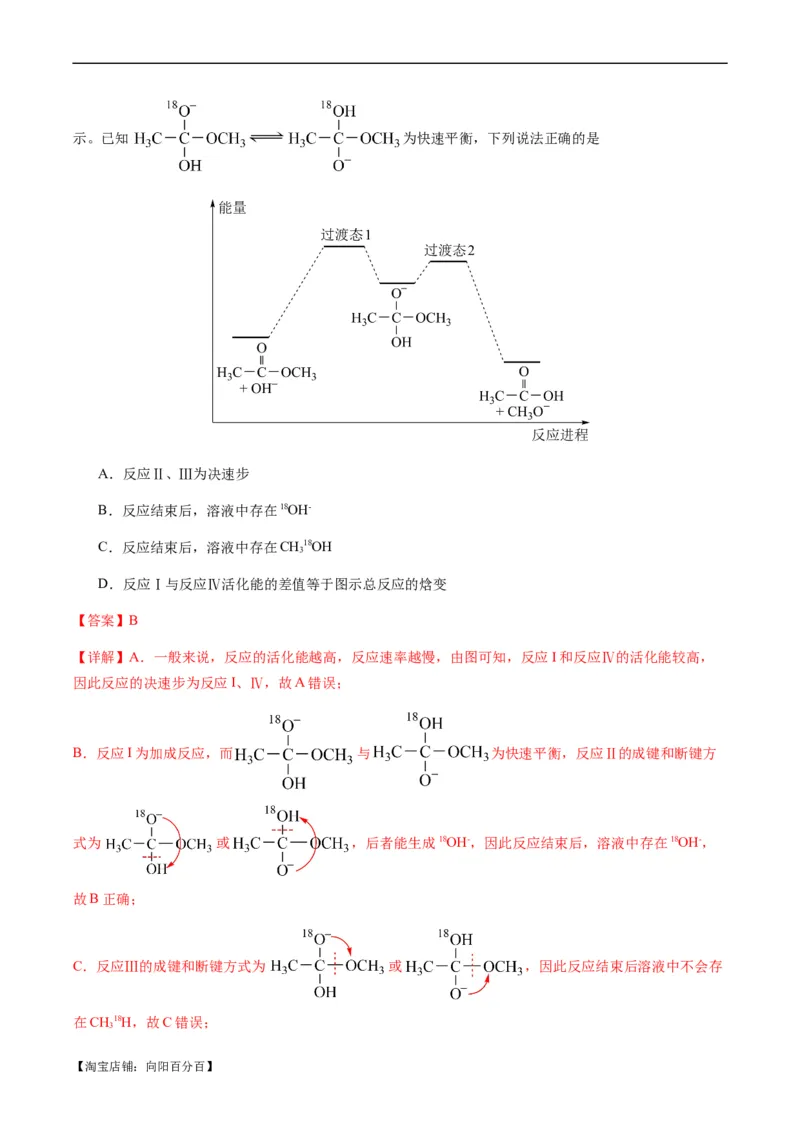
9.(2021·山东·统考高考真题)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示
为: 能量变化如图所
【淘宝店铺:向阳百分百】示。已知 为快速平衡,下列说法正确的是
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
【答案】B
【详解】A.一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应Ⅳ的活化能较高,
因此反应的决速步为反应I、Ⅳ,故A错误;
B.反应I为加成反应,而 与 为快速平衡,反应Ⅱ的成键和断键方
式为 或 ,后者能生成18OH-,因此反应结束后,溶液中存在18OH-,
故B正确;
C.反应Ⅲ的成键和断键方式为 或 ,因此反应结束后溶液中不会存
在CH18H,故C错误;
3
【淘宝店铺:向阳百分百】D.该总反应对应反应物的总能量高于生成物总能量,总反应为放热反应,因此 和CHO-的
3
总能量与 和OH-的总能量之差等于图示总反应的焓变,故D错误;
综上所述,正确的是B项,故答案为B。
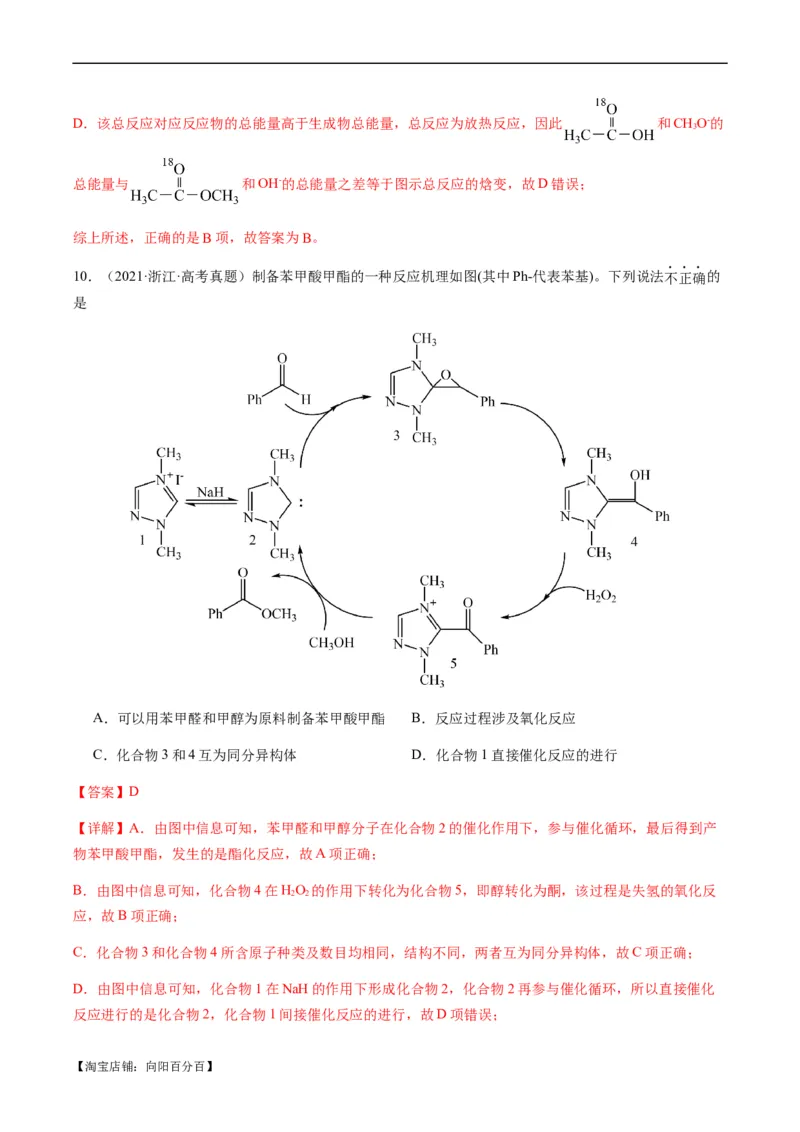
10.(2021·浙江·高考真题)制备苯甲酸甲酯的一种反应机理如图(其中Ph-代表苯基)。下列说法不正确的
是
A.可以用苯甲醛和甲醇为原料制备苯甲酸甲酯 B.反应过程涉及氧化反应
C.化合物3和4互为同分异构体 D.化合物1直接催化反应的进行
【答案】D
【详解】A.由图中信息可知,苯甲醛和甲醇分子在化合物2的催化作用下,参与催化循环,最后得到产
物苯甲酸甲酯,发生的是酯化反应,故A项正确;
B.由图中信息可知,化合物4在HO 的作用下转化为化合物5,即醇转化为酮,该过程是失氢的氧化反
2 2
应,故B项正确;
C.化合物3和化合物4所含原子种类及数目均相同,结构不同,两者互为同分异构体,故C项正确;
D.由图中信息可知,化合物1在NaH的作用下形成化合物2,化合物2再参与催化循环,所以直接催化
反应进行的是化合物2,化合物1间接催化反应的进行,故D项错误;
【淘宝店铺:向阳百分百】综上所述,说法不正确的是D项,故答案为D。
(建议用时:40分钟)
1.(2023·广东广州·校考模拟预测)我国科研人员使用催化剂CoGa 实现了H 还原肉桂醛生成肉桂醇,反
3 2
应机理的示意如下图,下列说法不正确的
A.肉桂醛分子中不存在顺反异构现象
B.苯丙醛分子中有6种不同化学环境的氢原子
C.还原反应过程发生了极性键和非极性键的断裂
D.该催化剂实现了选择性还原肉桂醛中的醛基
【答案】A
【详解】A.肉桂醛中的碳碳双键的位置处有顺反异构现象,故A错误;
B.苯丙醛分子中的等效氢有6种,苯环根据对称性由3种等效氢,在苯环的支链上有3种等效氢,共6种,
故B正确;
C.该反应发生过程中,醛基变为羟基是极性键断裂,H 参加反应时断非极性键,故C正确;
2
D.肉桂醛有碳碳双键和醛基官能团,与H 加入催化剂反应时,碳碳双键容易发生加成反应,但碳碳双键
2
没有反应,醛基变为羟基,该催化剂选择性还原醛基,故D正确;
故本题选A。
2.(2023·吉林长春·统考一模)羟醛缩合反应是一种常用的增长碳链的方法。一种合成目标产物
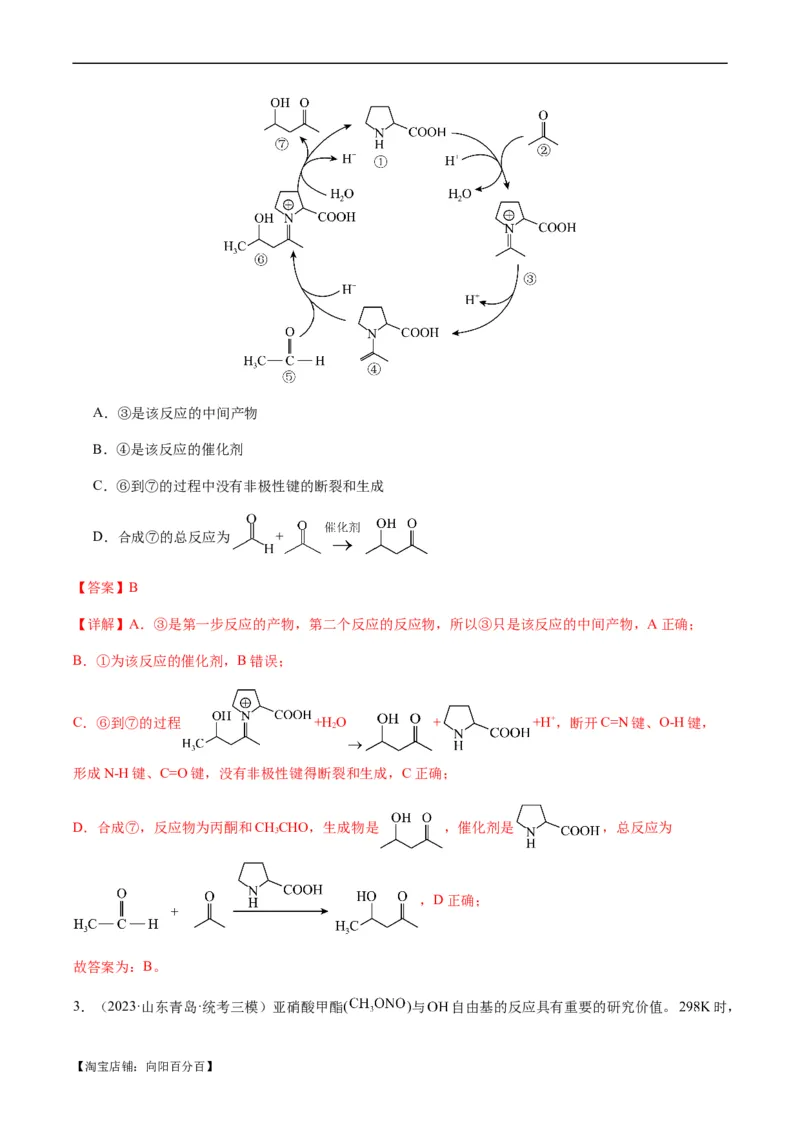
(图中⑦)的反应机理如图所示。下列说法错误的是
【淘宝店铺:向阳百分百】A.③是该反应的中间产物
B.④是该反应的催化剂
C.⑥到⑦的过程中没有非极性键的断裂和生成
D.合成⑦的总反应为 +
【答案】B
【详解】A.③是第一步反应的产物,第二个反应的反应物,所以③只是该反应的中间产物,A正确;
B.①为该反应的催化剂,B错误;
C.⑥到⑦的过程 +H O + +H+,断开C=N键、O-H键,
2
形成N-H键、C=O键,没有非极性键得断裂和生成,C正确;
D.合成⑦,反应物为丙酮和CHCHO,生成物是 ,催化剂是 ,总反应为
3
,D正确;
故答案为:B。
3.(2023·山东青岛·统考三模)亚硝酸甲酯( )与 自由基的反应具有重要的研究价值。 时,
【淘宝店铺:向阳百分百】该反应在空气中存在“氢提取”和“ 加成两种反应路径,反应机理如图2( 表示过渡态, 、
表示中间产物)。下列说法错误的是
A.图1中 的两种构象a更稳定
B.“氢提取”路径中的总反应为放热反应
C.“ 加成”路径中决速步为
D. 时, 与 自由基的反应主要产物为
【答案】C
【详解】A.构象指有机分子中不改变共价键结构,仅单键周围的原子旋转所产生的原子的空间排布、一
种构象改变为另一种构象时,不涉及共价键的断裂和重新形成。根据分子结构理论,由于基团的相互作用
的缘故,椅式构象比船式构象稳定得多,A正确;
B.由图像可知“氢提取”路径中反应物总能量大于生成物总能量,故其总反应为放热反应,B正确;
C.“ 加成”路径总反应的几步基元反应中活化能最大的是 ,故决速步为 ,C
错误;
D. 时,该反应在空气中存在“氢提取”和“ 加成两种反应路径,从反应历程能量图像中分析发
现氢提取路径的活化能小于OH加成路径,且氢提取产物能量更低更稳定,故反应主要产物为氢提取的产
物 ,D正确;
故选C。
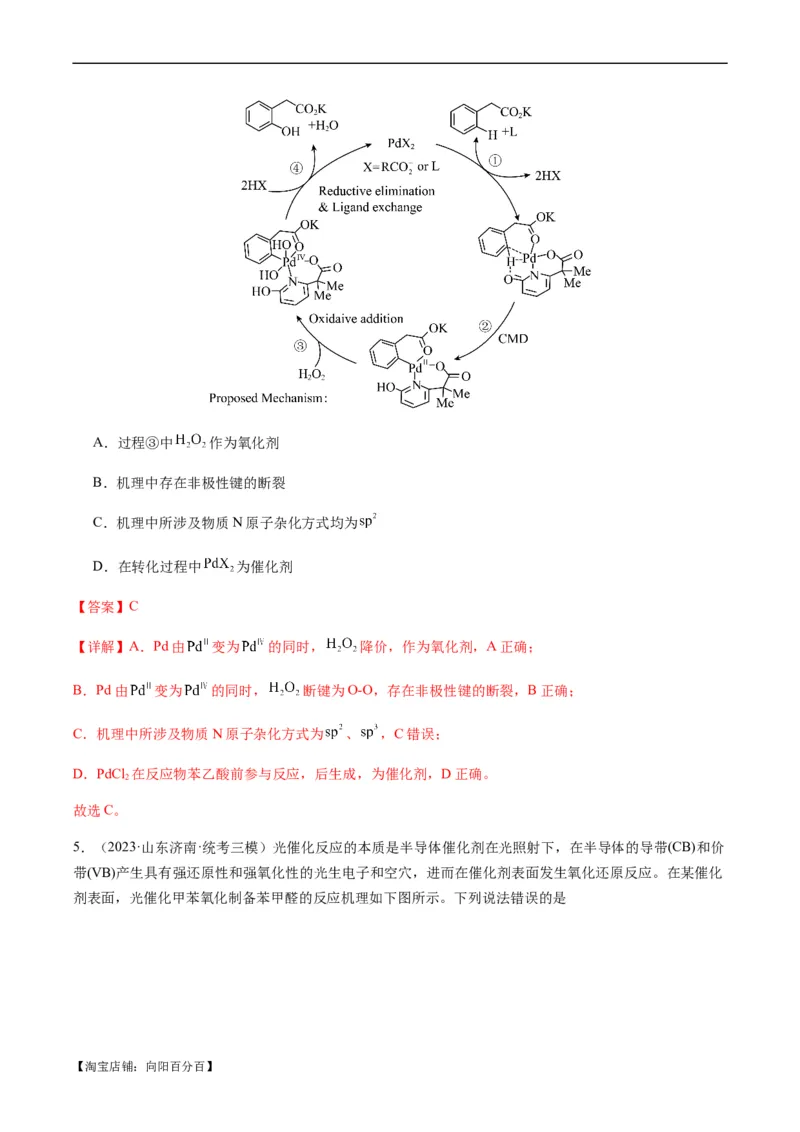
4.(2023·湖北武汉·校考模拟预测)Scripps研究所近期在温和条件下实现了苯乙酸的邻位羟基化反应,如
图为其反应机理,下列说法错误的是
【淘宝店铺:向阳百分百】A.过程③中 作为氧化剂
B.机理中存在非极性键的断裂
C.机理中所涉及物质N原子杂化方式均为
D.在转化过程中 为催化剂
【答案】C
【详解】A.Pd由 变为 的同时, 降价,作为氧化剂,A正确;
B.Pd由 变为 的同时, 断键为O-O,存在非极性键的断裂,B正确;
C.机理中所涉及物质N原子杂化方式为 、 ,C错误;
D.PdCl 在反应物苯乙酸前参与反应,后生成,为催化剂,D正确。
2
故选C。
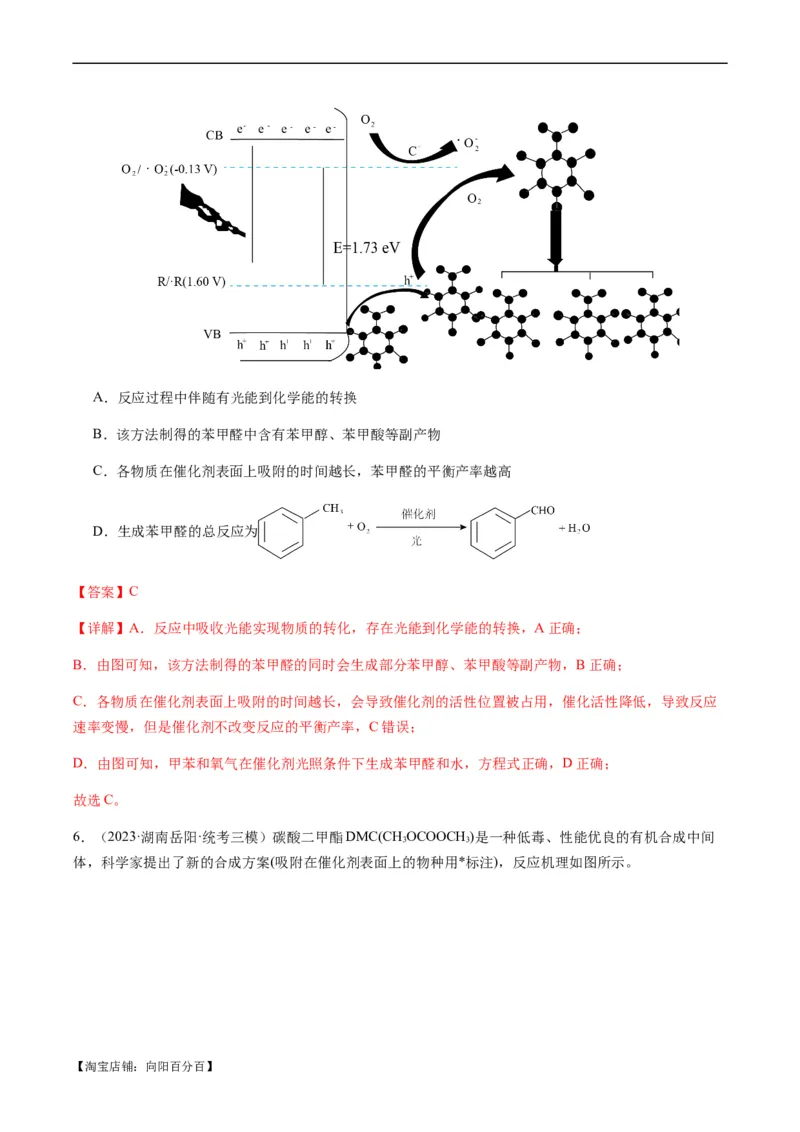
5.(2023·山东济南·统考三模)光催化反应的本质是半导体催化剂在光照射下,在半导体的导带(CB)和价
带(VB)产生具有强还原性和强氧化性的光生电子和空穴,进而在催化剂表面发生氧化还原反应。在某催化
剂表面,光催化甲苯氧化制备苯甲醛的反应机理如下图所示。下列说法错误的是
【淘宝店铺:向阳百分百】A.反应过程中伴随有光能到化学能的转换
B.该方法制得的苯甲醛中含有苯甲醇、苯甲酸等副产物
C.各物质在催化剂表面上吸附的时间越长,苯甲醛的平衡产率越高
D.生成苯甲醛的总反应为
【答案】C
【详解】A.反应中吸收光能实现物质的转化,存在光能到化学能的转换,A正确;
B.由图可知,该方法制得的苯甲醛的同时会生成部分苯甲醇、苯甲酸等副产物,B正确;
C.各物质在催化剂表面上吸附的时间越长,会导致催化剂的活性位置被占用,催化活性降低,导致反应
速率变慢,但是催化剂不改变反应的平衡产率,C错误;
D.由图可知,甲苯和氧气在催化剂光照条件下生成苯甲醛和水,方程式正确,D正确;
故选C。
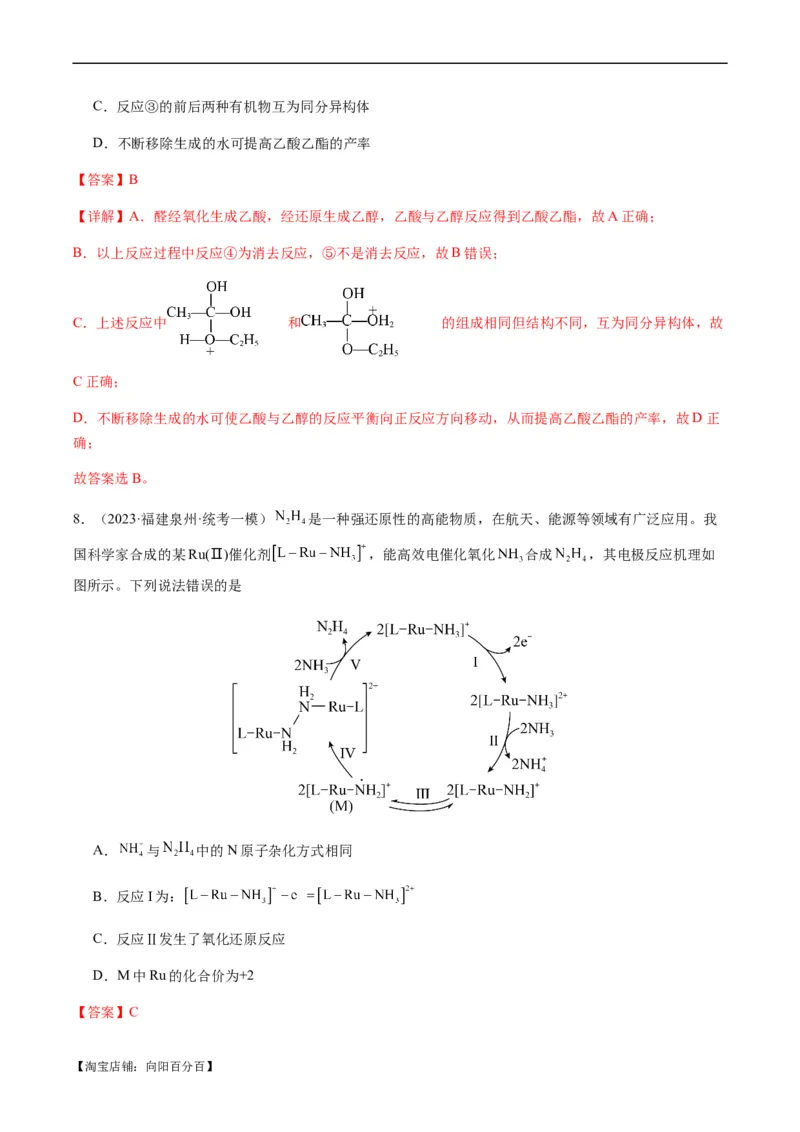
6.(2023·湖南岳阳·统考三模)碳酸二甲酯DMC(CH OCOOCH )是一种低毒、性能优良的有机合成中间
3 3
体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
【淘宝店铺:向阳百分百】下列说法错误的是
A.第2步的基元反应方程式为:CHO·*+CO*→CHOCOO·*
3 2 3
B.反应进程中最大能垒为1.257×104 eV
C.升高温度,可以对于第1步反应的正反应速率增加,对于第3步反应的正反应速率减小
D.适当的提高温度,可以增加碳酸二甲酯的产率
【答案】C
【详解】A.第2步的基元反应方程式为:CHOH·*+CO * → CHOCOO·*,A正确;
3 2 3
B.最大能垒为第1步基元反应:CHOH*+HO·* → CH O·*+HO*,其差值为1.257×104 eV,B正确;
3 3 2
C.升高温度,对于反应速率均增加,C错误;
D.总反应为2CHOH+CO ⥫⥬ CH OCOOCH +H O ΔH>0,为吸热反应;因此适当的提高温度,可以增加
3 2 3 3 2
碳酸二甲酯的产率,D正确;
故选C。
7.(2023·湖北荆州·沙市中学校考模拟预测)制备乙酸乙酯的反应机理如图所示:
下列说法不正确的是
A.一定条件下可以用乙醛为原料直接制备乙酸乙酯
B.以上反应过程中的④、⑤两步均为消去反应
【淘宝店铺:向阳百分百】C.反应③的前后两种有机物互为同分异构体
D.不断移除生成的水可提高乙酸乙酯的产率
【答案】B
【详解】A.醛经氧化生成乙酸,经还原生成乙醇,乙酸与乙醇反应得到乙酸乙酯,故A正确;
B.以上反应过程中反应④为消去反应,⑤不是消去反应,故B错误;
C.上述反应中 和 的组成相同但结构不同,互为同分异构体,故
C正确;
D.不断移除生成的水可使乙酸与乙醇的反应平衡向正反应方向移动,从而提高乙酸乙酯的产率,故D正
确;
故答案选B。
8.(2023·福建泉州·统考一模) 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我
国科学家合成的某Ru(Ⅱ)催化剂 ,能高效电催化氧化 合成 ,其电极反应机理如
图所示。下列说法错误的是
A. 与 中的N原子杂化方式相同
B.反应I为:
C.反应Ⅱ发生了氧化还原反应
D.M中Ru的化合价为+2
【答案】C
【淘宝店铺:向阳百分百】【详解】A. 形成4个价层电子对,N原子为sp3杂化,NH 中N原子与另一个N原子形成一条共价
2 4
键,与两个氢原子形成两条共价键,共形成三条共价键,还有一对孤对电子占据一条杂化轨道,即共形成
了4条杂化轨道,杂化类型为sp3,故A正确;
B.图中转化过程可知,[L-Ru-NH ]+失去电子生成[L-Ru-NH ]2+,反应I为:
3 3
,故B正确;
C.反应Ⅱ中发生了质子转移、无元素化合价发生变化,没有发生了氧化还原反应,故C错误;
D.[L-Ru-NH ]+和M之间存在平衡转化关系,转化关系分析可知,M中Ru的化合价为+2,故D正确;
2
故选:C。
9.(2022·浙江·校联考模拟预测)乙烯在硫酸催化下制取乙醇的反应机理,能量与反应进程的关系如图所
示。下列叙述正确的是
A.总反应速率由第①步反应决定
B.总反应 ,任何条件下反应都能自发进行
C.第②步反应过渡态物质比第③步反应过渡态物质稳定
D.第①步产生的乙基碳正离子两个碳都是 杂化
【答案】A
【详解】A.第一步活化能最大,反应速率最慢,所以总反应速率由第①步反应决定,故A正确;
B.总反应 、 ,根据 ,高温下反应不能自发进行,故B错误;
C.能量越低越稳定,根据图示,第②步反应过渡态物质的能量比第③步反应过渡态物质的能量高,所以
第③步反应过渡态物质更稳定,故C错误;
【淘宝店铺:向阳百分百】D.第①步产生的乙基碳正离子,甲基上的碳原子是 杂化、右侧带正电荷的碳原子采用sp2杂化,故D
错误;
选A。
10.(2023·河北保定·校考模拟预测)某课题组研究由1,2丙二醇与CO 合成碳酸丙烯酯(PC)的反应机理
2
如图所示。下列说法正确的是
A.化合物C是上述反应的催化剂,D、F为中间产物
B.原料中的原子利用率为100%
C.若将原料替换为1,3丙二醇,则产物为
D.增大CHCOOH的浓度可提高碳酸丙烯酯的产率
3
【答案】C
【详解】A.根据反应机理可知,C、D为中间产物,而F为反应的催化剂,A项错误;
B.总反应方程式为CHCH(OH)CH OH+CO +H O,原子利用率不为100%,B项错误;
3 2 2 2
【淘宝店铺:向阳百分百】C.1,3丙二醇的结构简式为CH(OH)CHCHOH,根据反应机理可知,其反应产物为 ,C项正确;
2 2 2
D.由总反应可知,CHCOOH的浓度对碳酸丙烯酯的产率没有影响,D项错误;
3
故选:C。
11.(2023·江苏淮安·校考模拟预测)在 催化剂和水存在下, 被还原为CO的反应机理示意图如
下:图1为通过实验观察捕获中间体和产物推演出 被还原为CO的反应过程;图2为 转化为CO反
应过程经历的中间体的能垒变化。已知:MS代表反应物或中间产物;TS代表过渡态;FS代表终态产物。
下列推断正确的是
A.由图1可知, 能提高总反应的平衡转化率
B.图1中, 中存在非极性键
C.由图2知,各步反应的 都小于0
D.在图2涉及的反应中, 决定总反应速率
【答案】D
【详解】A.由图1可知, 为催化剂,催化剂不影响平衡,不能提高总反应的平衡转化率,A错误;
【淘宝店铺:向阳百分百】B. 中存在配位键和极性共价键,不含非极性键,B错误;
C.由图2知,MS →MS 为吸热反应,ΔH>0,C错误;
2 3
D.在多步反应体系中,反应速率最慢的反应决定了反应的总速率,活化能越高,反应速率越慢,由图2
知,MS →MS 活化能最大,反应速率最慢,决定了总反应速率,D正确;
2 3
故选D。
12.(2023·山东日照·统考三模)甲苯与乙酰氯( )在无水 催化下发生反应,其反应机理如
图所示。乙酰氯经过步骤I得到的中间体可能存在P、O两种形式,且其缺电子的结构与甲苯的π电子云作
用生成过渡态π-络合物N,经过步骤Ⅱ得到σ-络合物M。下列说法错误的是
A.中间体P、Q中不饱和碳原子的杂化方式相同
B.该反应的决速步是步骤Ⅱ
C.甲苯与乙酰氯反应过程中有反应 发生
D.虚线L可表示 与 反应过程中的能量变化
【答案】D
【详解】A.中间体P、Q中不饱和碳原子的杂化方式均为sp、故相同,A正确;
B.根据能量轮廓图,Ⅱ此步活化能最大,故为决速步,B正确;
C.甲苯与乙酰氯反应过程中 做催化剂,参与反应后又重新生成,Ⅰ中生成四氯合铝离子后,又会发
生反应 ,C正确;
【淘宝店铺:向阳百分百】D.图像是针对甲苯与乙酰氯在无水 催化下发生反应的能量变化,当甲基氢被氟原子替代后,C-F比
C-H更牢固,则反应更困难,D错误;
选D。
13.(2023·四川·校联考模拟预测)NH 还原技术是当今有效且成熟的去除NO 的技术之一。使用钒催化
3 x
剂、采用NH 还原技术能有效脱除电厂烟气中的氮氧化物,消除NO的可能反应机理如图所示(“ …”表示催
3
化剂吸附)。
下列说法不正确的是
A.步骤②可表述为 在催化剂的氧化还原位被还原为 ,而催化剂的氧化还原位被氧化为
B.反应过程中消耗1molO ,理论上可处理NO的物质的量为4mol
2
C.钒催化剂能加快反应,但不能提高氮氧化物的平衡转化率
D.该过程中原子利用率未达到100%
【答案】A
【详解】A. 变为 ,N的化合价由-3价升高到-2价,化合价升高被氧化,故A错误;
B.根据关系图和电子守恒,1molO 可以得到4mol电子,同时可以氧化4mol催化剂,最终理论上可以处
2
理4molNO,故B正确;
C.催化剂能加快反应速率,不能提高平衡转化率,故C正确;
D.总反应方程式中生成物为N 和HO,原子利用率未达到100%,化合反应的原子利用率是100%,故D
2 2
正确;
答案选A。
14.(2023·浙江·校联考一模)反应 在加入Fe3+后反应进程中的能量
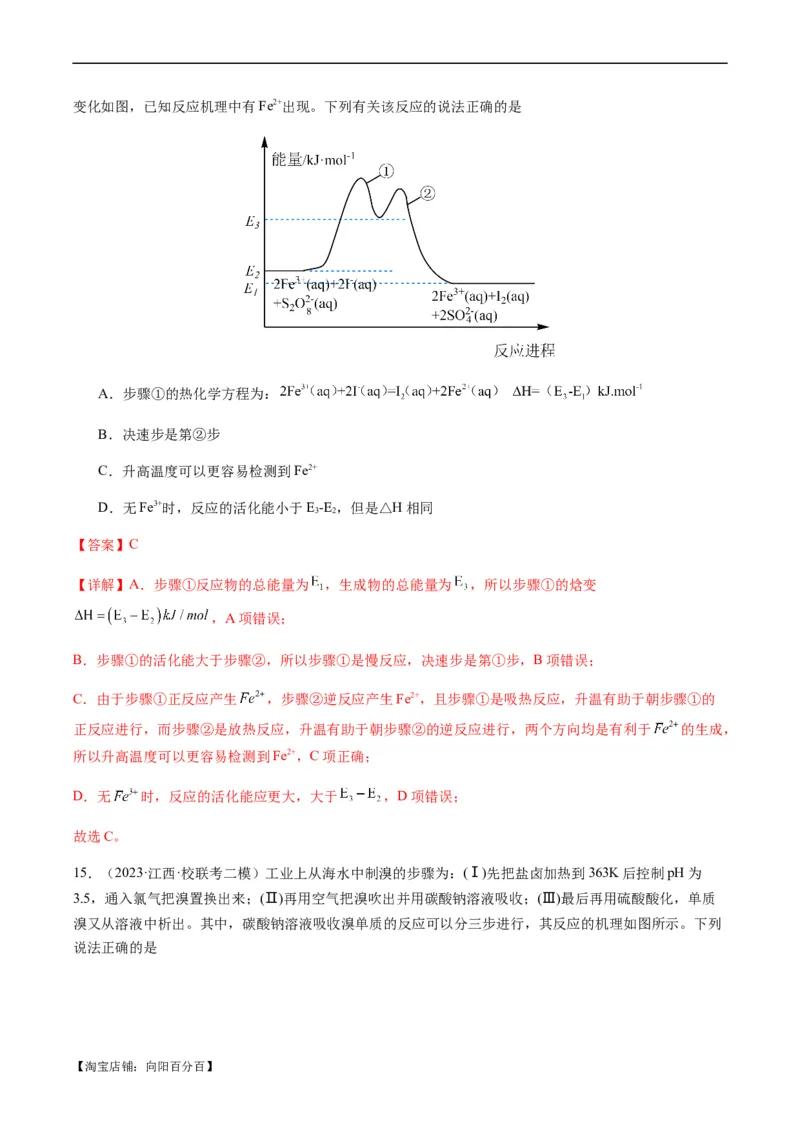
【淘宝店铺:向阳百分百】变化如图,已知反应机理中有Fe2+出现。下列有关该反应的说法正确的是
A.步骤①的热化学方程为:
B.决速步是第②步
C.升高温度可以更容易检测到Fe2+
D.无Fe3+时,反应的活化能小于E-E ,但是△H相同
3 2
【答案】C
【详解】A.步骤①反应物的总能量为 ,生成物的总能量为 ,所以步骤①的焓变
,A项错误;
B.步骤①的活化能大于步骤②,所以步骤①是慢反应,决速步是第①步,B项错误;
C.由于步骤①正反应产生 ,步骤②逆反应产生Fe2+,且步骤①是吸热反应,升温有助于朝步骤①的
正反应进行,而步骤②是放热反应,升温有助于朝步骤②的逆反应进行,两个方向均是有利于 的生成,
所以升高温度可以更容易检测到Fe2+,C项正确;
D.无 时,反应的活化能应更大,大于 ,D项错误;
故选C。
15.(2023·江西·校联考二模)工业上从海水中制溴的步骤为:(Ⅰ)先把盐卤加热到363K后控制pH为
3.5,通入氯气把溴置换出来;(Ⅱ)再用空气把溴吹出并用碳酸钠溶液吸收;(Ⅲ)最后再用硫酸酸化,单质
溴又从溶液中析出。其中,碳酸钠溶液吸收溴单质的反应可以分三步进行,其反应的机理如图所示。下列
说法正确的是
【淘宝店铺:向阳百分百】第一步:
第二步:
第三步:
A.由反应机理可知整个反应过程只涉及极性键的断裂和形成
B.反应产生的CO 主要是由Br 在水溶液中产生的HBr与溶液中CO 反应生成的
2 2
C.对比氯气与NaCO 溶液的反应,常温下在碱性溶液的稳定性:ClO- > BrO-
2 3
D.当1mol Br 完全参与上述反应后,产生的Br-与BrO 的个数之比为3:1
2
【答案】C
【详解】A.Br 中存在非极性键,存在非极性键的断裂和生成,A错误;
2
B.第二步反应主要是溴在碱性溶液发生歧化反应生成Br-、BrO-,从而促使CO 向水解方向移动,生成
CO 气体,B错误;
2
C.BrO-在第三步可以继续发生歧化反应,而ClO- 可以再碱性溶液稳定存在,稳定性:ClO- > BrO-,C正
确;
D.结合得失电子守恒,当1mol Br 完全参与上述反应后,产生的Br-与BrO 的个数之比为5:1,D错误;
2
故选C。
16.(2022·海南海口·校联考模拟预测·节选)我国力争于2030年前实现碳达峰,2060年前实现碳中和,
在这种背景下,CO 的利用和转化成为研究重点。回答下列问题:
2
(1)2021年9月,我国科学家在《科学》杂志发表了二氧化碳人工合成淀粉的研究成果。合成淀粉的重要反
应包括二氧化碳制备甲醇的反应: ,该反应在有催化剂和无催化
剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态):
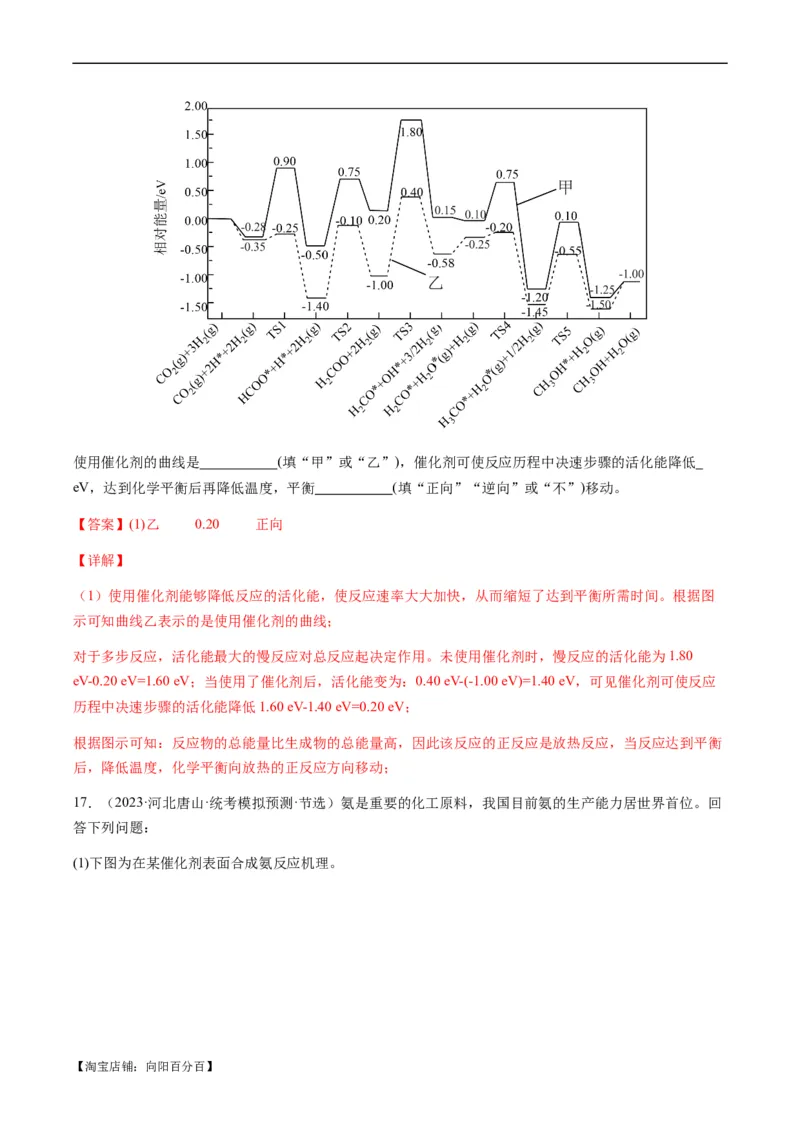
【淘宝店铺:向阳百分百】使用催化剂的曲线是 (填“甲”或“乙”),催化剂可使反应历程中决速步骤的活化能降低
eV,达到化学平衡后再降低温度,平衡 (填“正向”“逆向”或“不”)移动。
【答案】(1)乙 0.20 正向
【详解】
(1)使用催化剂能够降低反应的活化能,使反应速率大大加快,从而缩短了达到平衡所需时间。根据图
示可知曲线乙表示的是使用催化剂的曲线;
对于多步反应,活化能最大的慢反应对总反应起决定作用。未使用催化剂时,慢反应的活化能为1.80
eV-0.20 eV=1.60 eV;当使用了催化剂后,活化能变为:0.40 eV-(-1.00 eV)=1.40 eV,可见催化剂可使反应
历程中决速步骤的活化能降低1.60 eV-1.40 eV=0.20 eV;
根据图示可知:反应物的总能量比生成物的总能量高,因此该反应的正反应是放热反应,当反应达到平衡
后,降低温度,化学平衡向放热的正反应方向移动;
17.(2023·河北唐山·统考模拟预测·节选)氨是重要的化工原料,我国目前氨的生产能力居世界首位。回
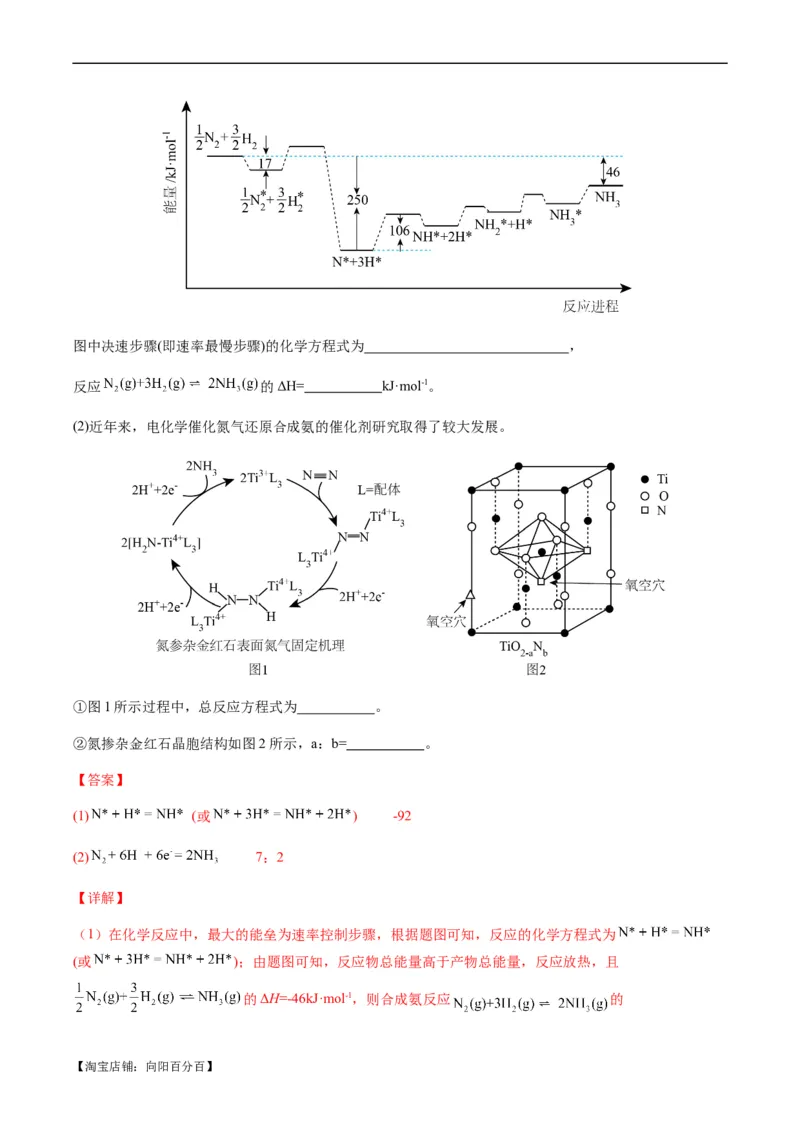
答下列问题:
(1)下图为在某催化剂表面合成氨反应机理。
【淘宝店铺:向阳百分百】图中决速步骤(即速率最慢步骤)的化学方程式为 ,
反应 的ΔH= kJ·mol-1。
(2)近年来,电化学催化氮气还原合成氨的催化剂研究取得了较大发展。
①图1所示过程中,总反应方程式为 。
②氮掺杂金红石晶胞结构如图2所示,a:b= 。
【答案】
(1) (或 ) -92
(2) 7:2
【详解】
(1)在化学反应中,最大的能垒为速率控制步骤,根据题图可知,反应的化学方程式为
(或 );由题图可知,反应物总能量高于产物总能量,反应放热,且
的ΔH=-46kJ·mol-1,则合成氨反应 的
【淘宝店铺:向阳百分百】ΔH=-92kJ·mol-1,故答案为: (或 );-92;
(2)①依据氮掺杂金红石表面氮气固定机理可知,反应物为氮气和氢离子,生成物为氨气,金红石为催
化剂,总反应方程式为 ;
②由晶胞结构示意图可知, 晶胞中N原子数为 ,O原子数为 ,Ti原子
数为4,故 ; ,解得 , ;
18.(2022·浙江·校联考模拟预测·节选)我国力争于2030年前完成碳达峰。2060年前实现碳中和,含碳
化合物的合成与转化具有重要的研究价值和现实意义。
Ⅰ. 甲烷化反应是碳循环利用的重要路径之一。
甲烷化主反应: 。
副反应:a. ;
b. ;
c. 。
(1)副反应b所生成的CO也能发生甲烷化反应,则化学方程式为 。
(2)催化剂的选择是 甲烷化技术的核心。在两种不同催化剂条件下,反应时间相同测得 转化率和生
成 选择性随温度变化的影响如下图所示。
提示:甲烷的选择性是指转化为甲烷的 在全部 反应物中所占的比例。
高于320℃后,以 为催化剂 转化率略有下降,而以Ni为催化剂 转化率仍在上升,其原
因是 。
(3)二氧化碳甲烷化反应在某催化剂催化下的反应机理如图所示。下列叙述不正确的是________。
【淘宝店铺:向阳百分百】A.氢气在Pd表面被吸附解离成氢原子 B.MgO是反应的中间体
C.图中碳元素的价态有多种 D. 浊液加热生成
【答案】
(1)
(2)相同时间内, 为催化剂,催化效果高效,320℃时,反应已达平衡,升高温度平衡左移;Ni为
催化剂,催化效率低,未达平衡,随温度升高,反应速率加快,转化率增大
(3)B
【详解】
(1)CO和H 发生甲烷化反应,生成 和 ,反应方程式为
2
;故答案为 。
(2)有图像可知,低温时 的催化效率高,但是该反应为放热反应,高于320℃后,平衡逆向移
动, 转化率略有下降;而以Ni为催化剂,低温时反应速率慢,升高温度反应速度加快,反应相同时间
转化率增加;故答案为相同时间内, 为催化剂,催化效果高效,320℃时,反应已达平衡,
升高温度平衡左移;Ni为催化剂,催化效率低,未达平衡,随温度升高,反应速率加快,转化率增大。
(3)A.如图可知,氢气再Pb催化剂表面解离成氢原子;故A正确;
B.MgO为MgOCH 和H生成CH 和MgO,MgO再和CO 反应生成MgOCO 继续反应,所以MgO不是中
3 4 2 2
间体;故B错误;
C.如图所示,C存在的形式有CH,CO 和MgOCO等,碳元素的价态有多种;故C正确;
4 2
【淘宝店铺:向阳百分百】D. 浊液加热, 和HO生成 和CO;故D正确;
2 2
故答案选B。
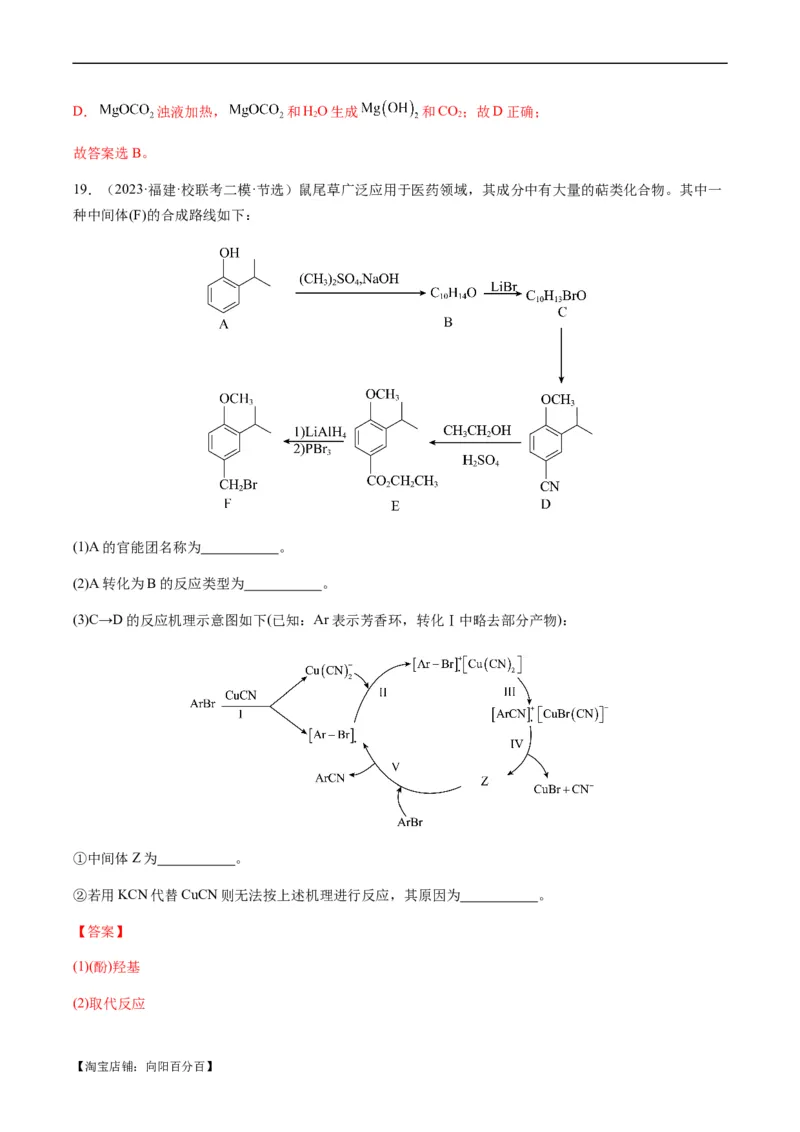
19.(2023·福建·校联考二模·节选)鼠尾草广泛应用于医药领域,其成分中有大量的萜类化合物。其中一
种中间体(F)的合成路线如下:
(1)A的官能团名称为 。
(2)A转化为B的反应类型为 。
(3)C→D的反应机理示意图如下(已知:Ar表示芳香环,转化Ⅰ中略去部分产物):
①中间体Z为 。
②若用KCN代替CuCN则无法按上述机理进行反应,其原因为 。
【答案】
(1)(酚)羟基
(2)取代反应
【淘宝店铺:向阳百分百】(3)[ArCN] 氧化性太弱无法实现转化Ⅰ,也无法形成后续的配离子中间体
【详解】
(1)根据A的结构简式,含有的官能团为(酚)羟基;
(2)根据分析,A为 ,转化为B ,发生取代反应;
(3)①根据图示信息,中间体Z为[ArCN];
② 氧化性太弱无法实现转化Ⅰ,也无法形成后续的配离子中间体,所以用KCN代替CuCN则无法按上
述机理进行反应;
20.(2023·江苏南通·校考模拟预测) 与 的干法重整(DRM)反应可同时转化温室气体并生成CO
和 ,对实现“碳中和”具有重要意义。
(1) 、 、CO的燃烧热分别为 、 、 ,则
的 。
(2)研究表明 、 、 三种双金属合金团簇可用于催化DRM反应,在催化剂表面涉及多个
基元反应,其反应机理如图,过程1-甲烷逐步脱氢;过程2- 的活化(包括直接活化和氢诱导活化);过
程3- 和 的氧化;过程4-扩散吸附反应(吸附在催化剂表面上的物种用*标注)。
① 的氢诱导活化反应方程式为 。
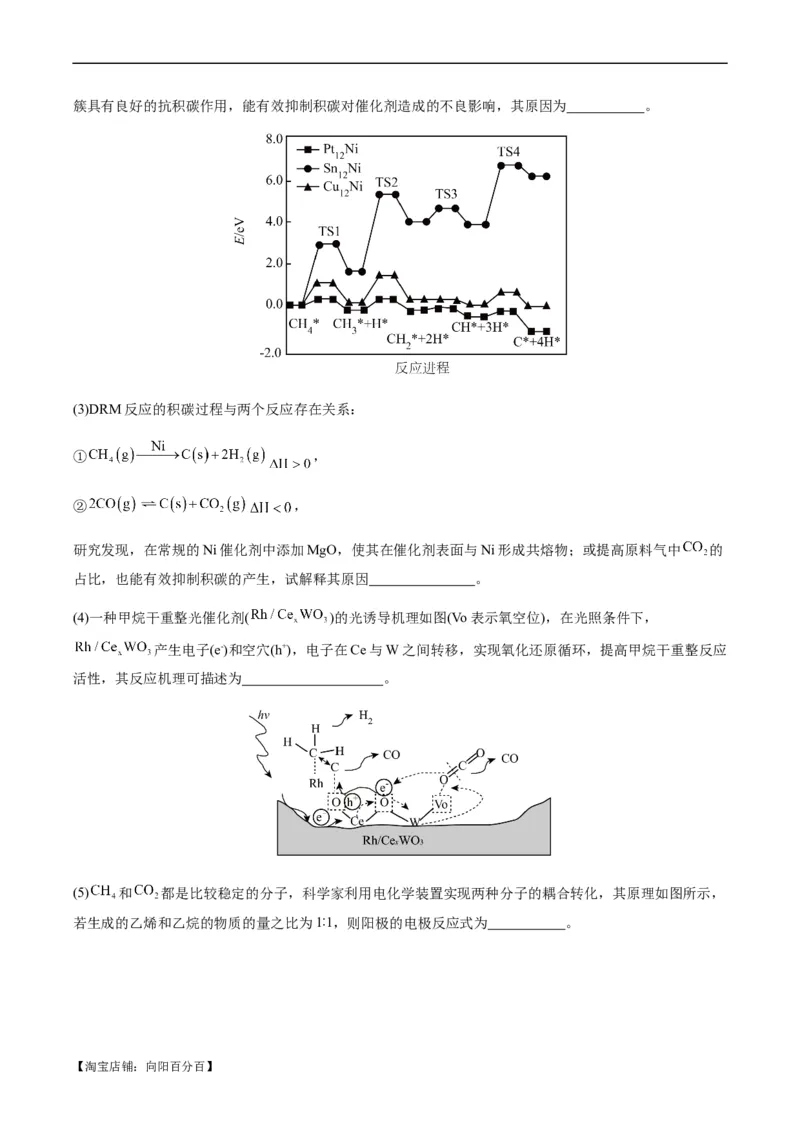
②过程1-甲烷逐步脱氢过程的能量变化如图(TS1、TS2、TS3、TS4均表示过渡态)。 双金属合金团
【淘宝店铺:向阳百分百】簇具有良好的抗积碳作用,能有效抑制积碳对催化剂造成的不良影响,其原因为 。
(3)DRM反应的积碳过程与两个反应存在关系:
① ,
② ,
研究发现,在常规的Ni催化剂中添加MgO,使其在催化剂表面与Ni形成共熔物;或提高原料气中 的
占比,也能有效抑制积碳的产生,试解释其原因 。
(4)一种甲烷干重整光催化剂( )的光诱导机理如图(Vo表示氧空位),在光照条件下,
产生电子(e-)和空穴(h+),电子在Ce与W之间转移,实现氧化还原循环,提高甲烷干重整反应
活性,其反应机理可描述为 。
(5) 和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示,
若生成的乙烯和乙烷的物质的量之比为1∶1,则阳极的电极反应式为 。
【淘宝店铺:向阳百分百】【答案】
(1)+247.3kJ/mol
(2) 积炭反应为最后一步,三种催化剂中 所需活化能最大,反应不易发
生,故产生积炭较少
(3)MgO在Ni催化剂表面形成共熔物,减小了Ni催化剂的表面积,减慢了反应①的速率;增大 浓度可
以促使反应②平衡左移
(4)光照时,光催化剂产生电子(e-)和空穴(h+),空穴(h+)和Rh附近的氧原子与吸附在Rh上的 生成CO
和 ,e-从 原子转移到W,进而转移到吸附在氧空位的 分子上, 获得电子后生成CO并在氧
空位留下O原子,O原子再迁移到新的氧空位上,从而形成氧化还原循环
(5)
【详解】
(1)由CH、H、CO的燃烧热分别为-890.3 kJ/mol、-285.8kJ/mol,-283kJ/mol可得如下热化学方程式①
4 2
△H=-890.3 kJ/mol、② △H=-285.8kJ/mol、③
1 2
△H=-283kJ/mol,由盖斯定律可知,反应①-2 ②-2 ③得CH(g)+CO (g)=2CO(g)
3 4 2
+2H (g),则反应△H=△H-2△H-2△H=+247.3 kJ/mol,故答案为:+247.3 kJ/mol;
2 1 2 3
(2)①由图可知,在氢诱导活化中,CO★和H★反应转化为COOH★,COOH★转化为CO★和OH★,则二氧
2
化碳的氢诱导活化反应方程式为CO★+H★=CO★+OH★,故答案为CO★+H★=CO★+OH★;
2 2
②由图可知,脱氢反应第4步为CH★=C★+H★,发生该步反应,三种催化剂中Sn Ni需要克服的活化能最
12
大,反应不易发生,故产生的积碳较少,故答案为:积炭反应为最后一步,三种催化剂中Sn Ni所需活化
12
能最大,反应不易发生,故产生积炭较少;
(3)在常规的镍催化剂中添加氧化镁,氧化镁在镍催化剂表面形成共熔物,减小了镍催化剂的表面积,
【淘宝店铺:向阳百分百】减慢了反应①的速率,所以能有效抑制积碳的产生;提高原料气中提高原料气中二氧化碳的比例,二氧化
碳浓度增大,反应②平衡向逆反应方向移动,碳的物质的量减小,所以能有效抑制积碳的产生,故答案为:
MgO在Ni催化剂表面形成共熔物,减小了Ni催化剂的表面积,减慢了反应①的速率;增大 浓度可以
促使反应②平衡左移;
(4)由图可知,光诱导机理为光照时,光催化剂产生电子(e-)和空穴(h+),空穴(h+)和Rh附近的氧原子与吸
附在Rh上的 生成CO和 ,e-从 原子转移到W,进而转移到吸附在氧空位的 分子上,
获得电子后生成CO并在氧空位留下O原子,O原子再迁移到新的氧空位上,从而形成氧化还原循环,故
答案为:光照时,光催化剂产生电子(e-)和空穴(h+),空穴(h+)和Rh附近的氧原子与吸附在Rh上的 生
成CO和 ,e-从 原子转移到W,进而转移到吸附在氧空位的 分子上, 获得电子后生成CO并
在氧空位留下O原子,O原子再迁移到新的氧空位上,从而形成氧化还原循环;
(5)由图可知,电极B为电解池的阳极,氧离子作用下甲烷在阳极失去电子发生氧化反应生成乙烯、乙
烷和水,电极反应式为 ,故答案为:
。
【淘宝店铺:向阳百分百】【淘宝店铺:向阳百分百】