文档内容
章末重要化学方程式书写强化练
1.钠及其重要化合物
(1)知识网络构建
(2)重要反应必练
写出下列反应的化学方程式,是离子反应的写出离子方程式。
①Na和H O的反应
2
2Na + 2H O == =2Na + + 2OH - + H ↑;
2 2
②Na在空气中燃烧
2Na + O ==== = N a O ;
2 2 2
③Na O 和H O的反应
2 2 2
2Na O + 2H O == =4Na + + 4OH - + O ↑;
2 2 2 2
④Na O 和CO 的反应
2 2 2
2Na O + 2CO == =2Na CO + O ;
2 2 2 2 3 2
⑤向NaOH溶液中通入过量CO
2
OH - + CO == =HCO ;
2
⑥将Na CO 溶液与石灰乳混合
2 3
CO + Ca(OH) == =CaCO + 2OH - ;
2 3
⑦向Na CO 稀溶液中通入过量CO
2 3 2
CO + CO + H O == =2HCO ;
2 2
⑧将NaHCO 溶液和NaOH溶液等物质的量混合
3
HCO + OH - == =CO + H O;
2
⑨将NaHCO 溶液与澄清石灰水等物质的量混合
3
HCO + Ca 2 + + OH - == =CaCO ↓ + H O;
3 2
⑩将NaHCO 溶液与少量澄清石灰水混合
3
2HCO + Ca 2 + + 2OH - == =CaCO ↓ + CO + 2H O。
3 2
2.铝及其重要化合物
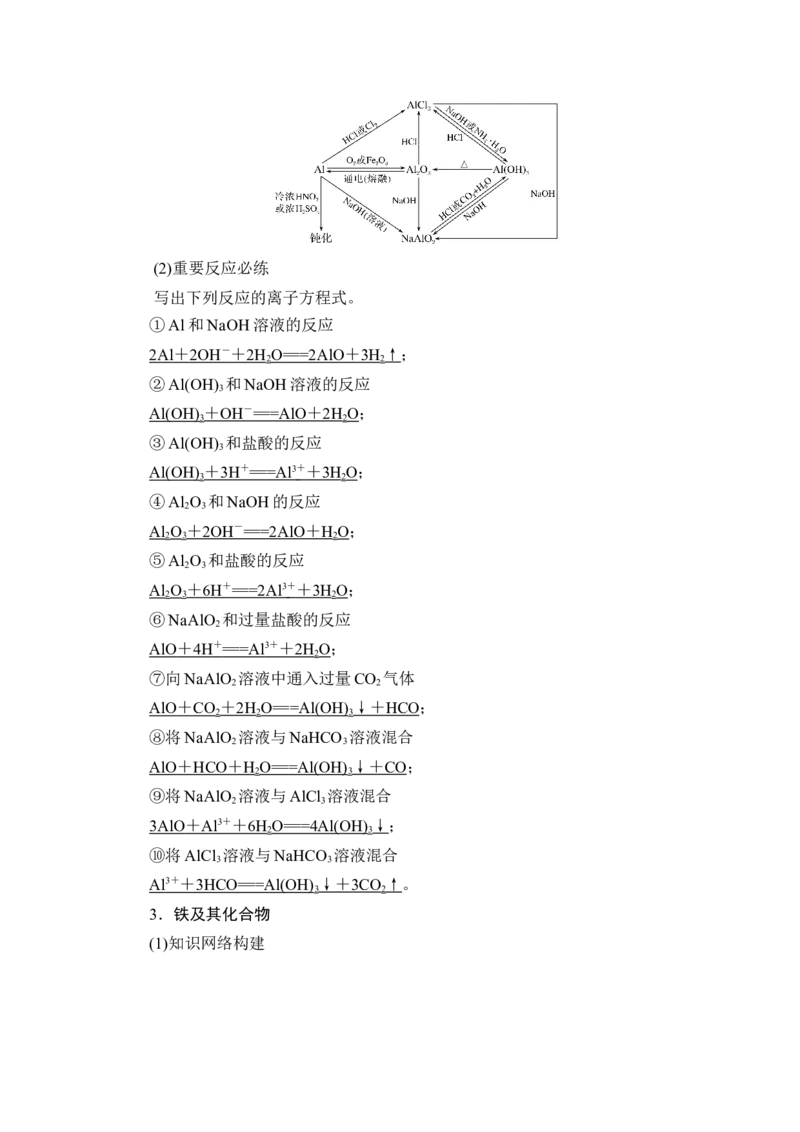
(1)知识网络构建(2)重要反应必练
写出下列反应的离子方程式。
①Al和NaOH溶液的反应
2Al + 2OH - + 2H O == =2AlO + 3H ↑;
2 2
②Al(OH) 和NaOH溶液的反应
3
Al(OH) + OH - == =AlO + 2H O;
3 2
③Al(OH) 和盐酸的反应
3
Al(OH) + 3H + == =A l 3 + + 3H O;
3 2
④Al O 和NaOH的反应
2 3
Al O + 2OH - == =2AlO + H O;
2 3 2
⑤Al O 和盐酸的反应
2 3
Al O + 6H + == =2A l 3 + + 3H O;
2 3 2
⑥NaAlO 和过量盐酸的反应
2
AlO + 4H + == =Al 3 + + 2H O;
2
⑦向NaAlO 溶液中通入过量CO 气体
2 2
AlO + CO + 2H O == =Al(OH) ↓ + HCO ;
2 2 3
⑧将NaAlO 溶液与NaHCO 溶液混合
2 3
AlO + HCO + H O == =Al(OH) ↓ + CO ;
2 3
⑨将NaAlO 溶液与AlCl 溶液混合
2 3
3AlO + Al 3 + + 6H O == =4Al(OH) ↓;
2 3
⑩将AlCl 溶液与NaHCO 溶液混合
3 3
Al 3 + + 3HCO == =Al(OH) ↓ + 3CO ↑。
3 2
3.铁及其化合物
(1)知识网络构建(2)重要反应必练
写出下列反应的化学方程式,是离子反应的写离子方程式。
①Fe和过量稀HNO 的反应
3
Fe + 4H + + NO == =Fe 3 + + NO ↑ + 2H O;
2
②Fe高温下和水蒸气的反应
3Fe + 4H O(g) ===== Fe O + 4H ;
2 3 4 2
③铝与氧化铁的铝热反应
Fe O + 2A l ==== = 2F e + A l O ;
2 3 2 3
④用赤铁矿冶炼铁的原理
Fe O + 3CO ==== = 2F e + 3CO ;
2 3 2
⑤Fe(OH) 长时间露置于空气中
2
4Fe(OH) + O + 2H O == =4Fe(OH) ;
2 2 2 3
⑥FeO和稀HNO 的反应
3
3FeO + 10H + + NO == =3Fe 3 + + NO ↑ + 5H O;
2
⑦Fe(OH) 和HI的反应
3
2Fe(OH) + 6H + + 2 I - == =2F e 2 + + I + 6H O;
3 2 2
⑧FeBr 溶液和少量Cl 的反应
2 2
2Fe 2 + + Cl == =2Fe 3 + + 2Cl - ;
2
⑨FeBr 溶液和等物质的量的Cl 反应
2 2
2Fe 2 + + 2Br - + 2Cl == =2Fe 3 + + Br + 4C l - ;
2 2
⑩FeBr 溶液和过量Cl 的反应
2 2
2Fe 2 + + 4Br - + 3Cl == =2Fe 3 + + 2Br + 6C l - 。
2 2
4.铜及其化合物
(1)知识网络构建(2)重要反应必练
①在潮湿的空气里形成铜锈
2Cu + O + CO + H O == =Cu (OH) CO ;
2 2 2 2 2 3
②铜与氯化铁溶液反应
Cu + 2Fe 3 + == =Cu 2 + + 2Fe 2 + ;
③碱式碳酸铜受热分解
Cu (OH) CO ==== = 2CuO + CO ↑ + H O;
2 2 3 2 2
④碱式碳酸铜与强酸反应
Cu (OH) CO + 4H + == =2C u 2 + + CO ↑ + 3H O。
2 2 3 2 2