文档内容
第 02 讲 物质的量浓度
目录
01考情透视·目标导航..........................................................................................................2
02知识导图·思维引航..........................................................................................................3
03考点突破·考法探究..........................................................................................................3
考点一 物质的量浓度及相关计算....................................................................................................................3
知识点1 物质的量浓度..............................................................3
知识点2 物质的量浓度和溶质质量分数的比较..........................................4
考向1 理解物质的量浓度概念........................................................4
考向2 物质的量浓度及相关计算......................................................5
考点二 溶液浓度的计算与换算........................................................................................................................5
知识点1 理解公式..................................................................5
知识点2 掌握规律.................................................................6
考向1 有关气体溶于水的浓度计算....................................................7
考向2 混合规律的应用..............................................................7
考点三 一定物质的量浓度溶液的配制............................................................................................................8
知识点1 容量瓶的构造及使用........................................................8
知识点2 配制一定物质的量浓度溶液操作..............................................8
考向1 配制一定物质的量浓度的溶液..................................................9
考向2 配制一定物质的量浓度的溶液的误差分析.......................................11
04真题练习·命题洞见........................................................................................................12考点要求 考题统计 考情分析
物质的量浓
度的计算
从近三年高考试题来看,有关物质的量浓度的概
2022•海南卷7题,2分 念主要体现在N 、水溶液中的离子平衡及化学计
A
算中;一定物质的量浓度溶液的配制是重要的化
学定量实验之一,融合于选择题的化学实验基本
操作,填空题主要以穿插在生活、生产中的化学
分析计算(如食品污染物空气污染物的测定、食品
中的营养物质的测定、化工生产中的产品是否合
2023•全国甲卷9题,6分;
格等等)为主,中需关注滴定实验中有关物质的量
一定物质的 2022山东卷6题,2分; 浓度的计算。
量浓度溶液
2022•全国乙卷27(1)题,2分;
的配制及误
差分析 2022•广东卷7题(1)(2),4分;
2021广东卷7题,2分
复习目标:
1.掌握物质的量浓度的含义和应用,能运用物质的量浓度进行简单计算。
2.建立n、M、V 、c之间相互转化关系及进行简单计算的思维模型。
m
3.掌握一定物质的量浓度的溶液的配制方法。
4.学会一定物质的量浓度的溶液的配制的过程中的误差分析。考点一 物质的量浓度及相关计算
知识点1 物质的量浓度
1.概念
物质的量浓度表示___________________里所含溶质B的物质的量,也称为_____________,符号为
c 。
B
2.常用单位:___________或___________。
3.公式:n=c V⇒
B【名师提醒】
1.V是溶液的体积,不是溶剂的体积,也不是溶质与溶剂的体积之和。
2.n必须是溶质B的物质的量。
知识点2 物质的量浓度和溶质质量分数的比较
物质的量浓度c 溶质质量分数w
以单位体积溶液中所含溶质的物 以溶质的质量与溶液的质量比
概念
质的量来表示溶液组成的物理量 值来表示溶液的组成的物理量
溶质的单位 ___________ g
溶液的单位 ___________ g
表达式 c= w=×100%
两者关系 w=(M:摩尔质量;单位:g·mol-1;ρ:密度,单位:g·cm-3)
考向1 理解物质的量浓度概念
【例1】某试剂瓶上贴有标签:“100 mL 1.0 mol·L-1MgCl 溶液”。下列对该试剂理解正确的是( )
2
A.该溶液中含有的微粒主要有MgCl 、Mg2+、Cl-、HO
2 2
B.若取50 mL溶液,其中的c(Cl-)=1.0 mol·L-1
C.取该溶液5.0 mL恰好与100 mL 0.1 mol·L-1AgNO 溶液完全反应
3
D.该溶液与100 mL 1.0 mol·L-1NaCl溶液中的c(Cl-)相等
【易错警示】
1 . 注 意 物 质 溶 于 水 后 溶 质 是 否 改 变 , 如 : NaO 、 NaO―→NaOH , SO ―→HSO ,
2 2 2 3 2 4
CuSO ·5H O―→CuSO 。
4 2 4
2.不能用水的体积代替溶液的体积,尤其是固体、气体溶于水,一般根据溶液的密度进行计算。
【变式训练】设N 为阿伏加德罗常数的值,下列对0.3 mol·L-1KSO 溶液的叙述正确的是( )。
A 2 4
A.1 L该溶液中含有0.3N 个K+
A
B.1 L该溶液中含有K+和SO 2-的总数为0.9N
4 A
C.2 L该溶液中K+的浓度为1.2 mol·L-1
D.将0.3 mol硫酸钾溶于1 L水中,所得硫酸钾溶液的浓度为0.3 mol·L-1考向2 物质的量浓度及相关计算
【例2】(2024•安徽省芜湖市期中)下列溶液的物质的量浓度的相关计算正确的是( )
A.同浓度的三种物质的溶液:NaSO 、MgSO 、Al (SO ) 溶液体积之比为3∶2∶1,则SO 2-浓度之
2 4 4 2 4 3 4
比为3∶2∶3
B.将100mL 5 的盐酸加水稀释至1L,再取出5mL,这5mL溶液的物质的量浓度为0.5mol/L
C.将1mol•L-1的NaCl溶液和0.5mol•L-1的BaCl 溶液等体积混合后,忽略溶液体积变化,
2
c(Cl-)=0.75mol•L-1
D.标准状况下,22.4L HCl溶于1L水,盐酸的物质的量浓度为1mol•L-1
【变式训练】某同学购买了一瓶“84”消毒液,包装说明如图:
净含量:1000 mL
主要成分: 25%NaClO
密度:1.19 g·cm-3
使用方法:稀释100倍(体积比)后使用
注意事项:密封保存,易吸收空气中的CO 而变质
2
根据以上信息和相关知识判断,下列分析不正确的是( )。
A.该“84”消毒液的物质的量浓度约为4.0 mol·L-1
B.一瓶该“84”消毒液最多能吸收空气中CO 约为89.6 L(标准状况)
2
C.取100 mL该“84”消毒液稀释100倍后用于消毒,稀释后的溶液中c(Na+)约为0.04 mol·L-1
D.参阅该“84”消毒液的配方,欲用 NaClO固体配制480 mL含25%NaClO的消毒液,需要称量
NaClO固体的质量约为143 g
考点二 溶液浓度的计算与换算知识点1 理解公式
1.物质的量浓度与溶质质量分数之间的换算
c====,w= 。(ρ:g·cm-3)
2.物质的量浓度与溶解度(S)的换算(饱和溶液)
c===,S=。(ρ:g·cm-3)
3.气体溶质溶于水中制得溶液,其物质的量浓度和质量分数的计算
在标准状况下,1 L水中溶解某气体V L,所得溶液密度为ρ,则:c===(ρ:g·cm-3),w=×100%=
=×100%。
【易错提醒】
1.溶液的体积不能用溶剂水的体积和溶质的体积之和来代替,应该用溶液的质量除以溶液的密度;
2.两溶液混合,由于其密度可不相等,所以体积不等于两混合溶液体积之和。
3.物质溶于水后注意看溶质是否发生了变化。如 Na、NaO 、NO 、SO 等溶于水,由于它们与水反
2 2 2 3
应,所以溶质发生了变化。
知识点2 掌握规律
1.稀释定律
(1)如用V、V、c、c 分别表示稀释前后溶液的体积和溶质的物质的量浓度,有___________。
1 2 1 2
(2)如用m、m、w 、w 分别表示稀释前后溶液的质量和质量分数,有___________。
1 2 1 2
2.混合规律
同一溶质不同浓度的溶液混合后溶质质量分数的判断方法:设溶质质量分数分别为 w 和w 的两溶液
1 2
混合后所得溶液溶质的质量分数为w。
(1)两溶液等质量混合:w=(w +w )。
1 2
(2)两溶液等体积混合:
a.若溶液中溶质的密度大于溶剂的密度,则w≥(w +w ),如HSO 溶液。
1 2 2 4
b.若溶液中溶质的密度小于溶剂的密度,则w≤(w +w ),如氨水、酒精溶液。
1 2
考向1 有关气体溶于水的浓度计算
【例1】标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,则下列关系中不正确的是( )
A.ρ=(17V+22 400)/(22.4+22.4V)
B.w=17c/(1 000ρ)
C.w=17V/(17V+22 400)
D.c=1 000Vρ/(17V+22 400)
【思维建模】
计算气体溶于水后物质的量浓度的一般思路
【变式训练】在T ℃时,将a g NH 完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,
3
溶质的质量分数为w,其中含NH的物质的量为b mol。下列叙述中正确的是 ( )
A.溶质的质量分数为w=×100%
B.溶质的物质的量浓度c= mol·L-1
C.溶液中c(OH-)= mol·L-1
D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
考向2 混合规律的应用
【例2】若以w 和w 分别表示浓度为a mol·L-1和 b mol·L-1的氨水的质量分数,且知2a=b,则下
1 2
列判断正确的是 ( )
A.2w =w B.2w =w C.w >2w D.w <w <2w
1 2 2 1 2 1 1 2 1
【思维建模】
1.溶液稀释
(1)溶质的质量在稀释前后保持不变,即mw =mw 。
1 1 2 2
(2)溶质的物质的量在稀释前后保持不变,即cV=c V。
1 1 2 2
(3)溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。
2.溶液混合,混合前后:cV+c V=c V ,其中V =m /ρ ,据此可进行相关计算。
1 1 2 2 混 混 混 混 混
【变式训练】浓度不等的两种硫酸溶液等质量混合后,溶液中溶质的质量分数为 a%,而等体积混合
后,溶质的质量分数为b%;浓度不等的两种氨水等质量混合时,其溶质的质量分数为 a%,而等体积混合后,溶质的质量分数为c%,那么a、b、c数值的关系是( )
A.a>b>c B.b>a>c C.c>b>a D.c>a>b
考点三 一定物质的量浓度溶液的配制
知识点1 容量瓶的构造及使用
1.容量瓶上标有___________、___________和___________。常用规格有 100 mL、250 mL、500
mL、1 000 mL等。
2.
容量瓶在使用前要___________,其操作顺序为装水盖塞→倒立→正立→玻璃塞旋转180°→倒立。
【名师提醒】
1.选用容量瓶的原则——“大而近”,如需90 mL溶液,则选用100 mL容量瓶。
2.选用容量瓶时,应指明其规格。
3.往容量瓶中转移液体时,用玻璃棒引流,玻璃棒末端应在容量瓶刻度线以下。
知识点2 配制一定物质的量浓度溶液操作
以配制500 mL 1.0 mol·L-1 NaCl溶液为例:【易错提醒】
1.做需要补充仪器的实验题时,要学会“有序思考”——按照实验的先后顺序、步骤,思考每一步
所需仪器,然后与已知仪器对比,就一定不会漏写某种仪器。
2.容量瓶的规格,常见的有100 mL、250 mL、500 mL、1 000 mL。
3.所用定量仪器量筒、托盘天平的精确度。
考向1 配制一定物质的量浓度的溶液
【例 1】(2024•宁夏石嘴山市期末)用溶质质量分数为 的浓硫酸(ρ=1.84g· cm-3)配制稀硫酸,下列操作正确的是( )
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.必须用到的定量仪器有200mL容量瓶和托盘天平
C.量取浓硫酸的体积为20.0mL
D.量取浓硫酸时仰视,定容时俯视,都会使所配硫酸溶液浓度偏大
【思维建模】
溶液配制过程中的“四个数据”
数据 要求或解释
药吕的质量 实验室中一般用托盘天平称量药品,而托盘天平只能精确到 0.1 g,所以记录数据时
只能保留小数点后一位数字。如所需NaCl的质量为14.6 g,不能写为14.60 g
容量瓶的规格 (1)选择容量瓶的规格时应该与所配溶液体积相等或稍大,如需配制480 mL某溶液,
则应该选择500 mL容量瓶; (2)回答补充仪器的问题时应该注明容量瓶的规格,如
回答“500 mL容量瓶”时,不能只回答“容量瓶”
洗涤烧杯和玻 移液时洗涤烧杯和玻璃棒2~3次是为了确保溶质全部转入容量瓶中,否则会导致溶
璃棒2~3次 液浓度偏低
液面距容量瓶 定容时,当液面距容量瓶刻度线1~2 cm时,应该改用胶头滴管滴加,否则容易导致
刻度线1~2 cm 液体体积超过刻度线,使溶液浓度偏低
【变式训练】(2024•辽宁省本溪市开学考试)某种天然碱的化学式为aNaHCO ·bNaHCO ·cHO,某实验
3 3 2
小组欲测定该天然碱中NaCO 与NaHCO 的比例,进行了如下实验。回答下列问题
2 3 3
(1)配制一定物质的量浓度的稀盐酸溶液。
①若要配制250mL0.10mol·L-1稀盐酸,需量取120.1mol·L-1的浓盐酸 (计算结果保留1位
小数)。
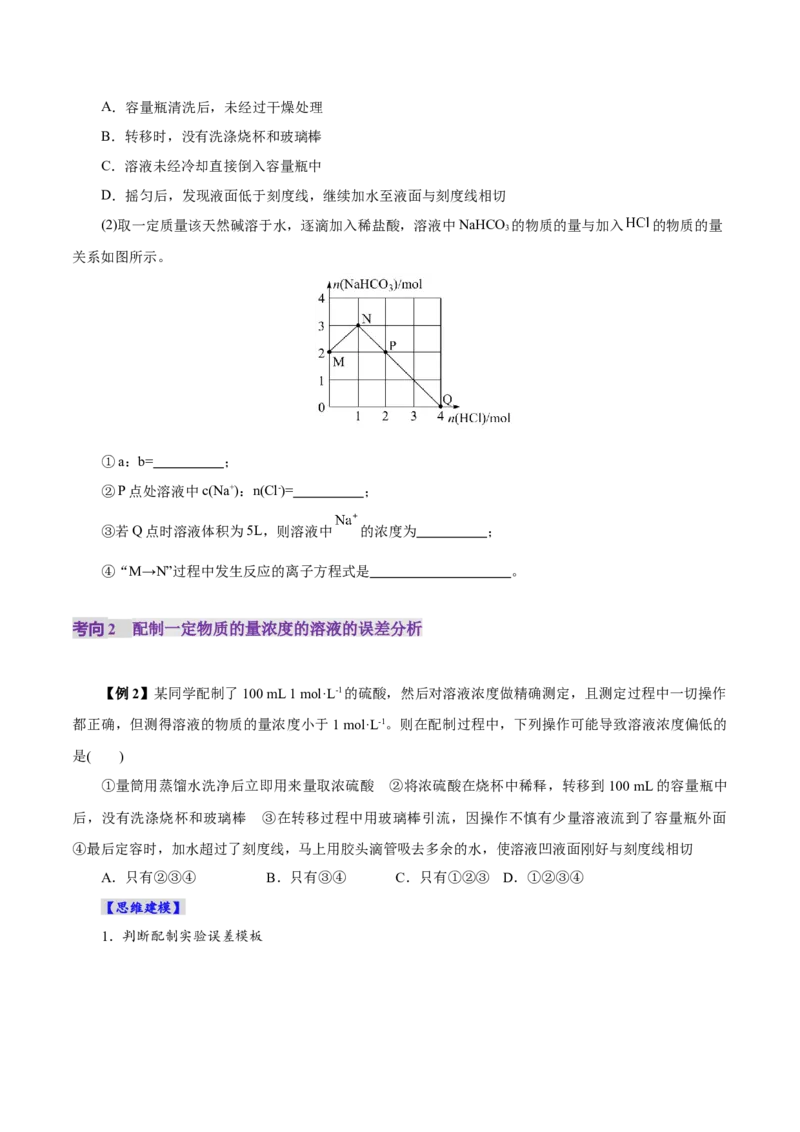
②配制溶液过程中,下列关于容量瓶的操作,正确的是 (填字母,下同)。
A.检验容量瓶是否漏水 B.定容
C.转移 D.摇匀
③下列情况会使所配溶液浓度偏低的是 。A.容量瓶清洗后,未经过干燥处理
B.转移时,没有洗涤烧杯和玻璃棒
C.溶液未经冷却直接倒入容量瓶中
D.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
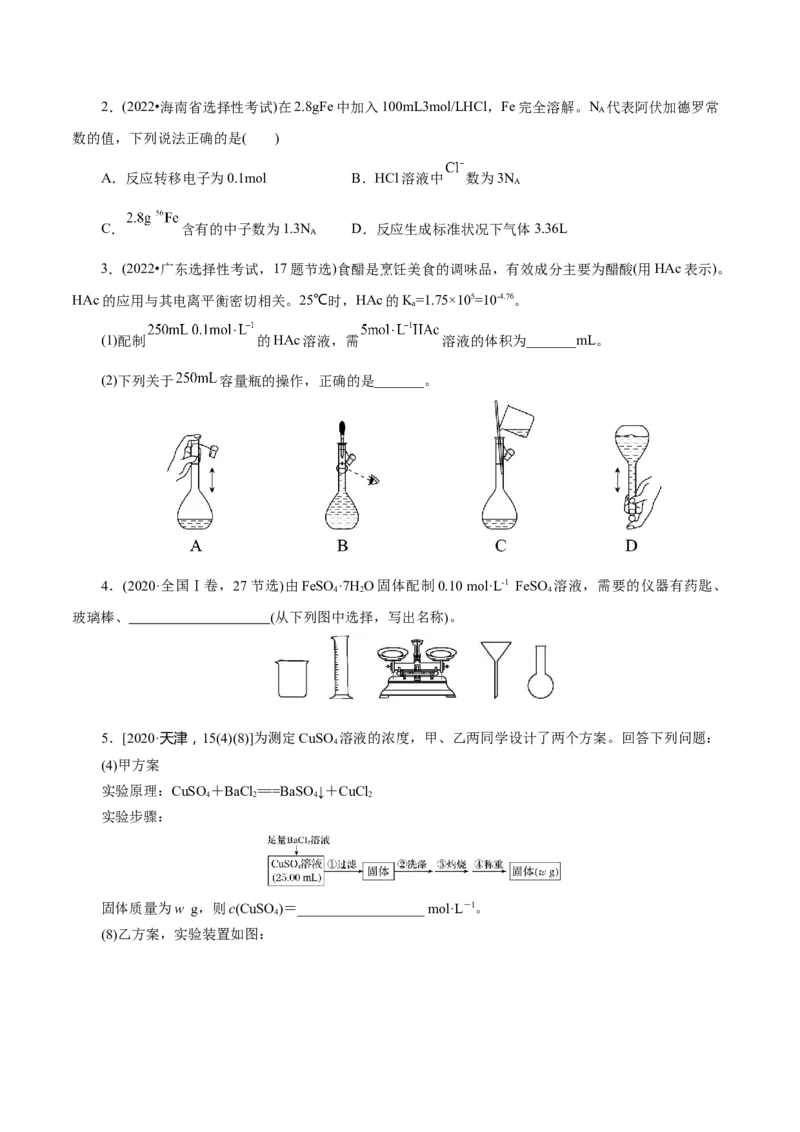
(2)取一定质量该天然碱溶于水,逐滴加入稀盐酸,溶液中NaHCO 的物质的量与加入 的物质的量
3
关系如图所示。
①a:b= ;
②P点处溶液中c(Na+):n(Cl-)= ;
③若Q点时溶液体积为5L,则溶液中 的浓度为 ;
④“M→N”过程中发生反应的离子方程式是 。
考向2 配制一定物质的量浓度的溶液的误差分析
【例2】某同学配制了100 mL 1 mol·L-1的硫酸,然后对溶液浓度做精确测定,且测定过程中一切操作
都正确,但测得溶液的物质的量浓度小于1 mol·L-1。则在配制过程中,下列操作可能导致溶液浓度偏低的
是( )
①量筒用蒸馏水洗净后立即用来量取浓硫酸 ②将浓硫酸在烧杯中稀释,转移到100 mL的容量瓶中
后,没有洗涤烧杯和玻璃棒 ③在转移过程中用玻璃棒引流,因操作不慎有少量溶液流到了容量瓶外面
④最后定容时,加水超过了刻度线,马上用胶头滴管吸去多余的水,使溶液凹液面刚好与刻度线相切
A.只有②③④ B.只有③④ C.只有①②③ D.①②③④
【思维建模】
1.判断配制实验误差模板2.误差分析的思维流程
3.对于定容时俯视、仰视对结果的影响,要学会画线分析(如图)
【变式训练】某消毒小组人员用18.4mol•L-1的浓硫酸配制500mL0.1mol•L-1的稀硫酸用于84消毒液消
毒能力的实验探究,在配制过程中,下列操作中能使所配溶液的浓度偏低的有__________________(填代
号)。
①用量筒量取98%的硫酸时俯视
②未等稀释后的HSO 溶液冷却至室温就转移到容量瓶中
2 4
③转移前,容量瓶中含有少量蒸馏水
④转移过程中,有少量液体溅出
⑤定容时,加蒸馏水超过标线,又用胶头滴管吸出
1.(2023•全国甲卷,9)实验室将粗盐提纯并配制 的NaCl溶液。下列仪器中,本实验必
须用到的有( )
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥ B.①④⑤⑥ C.②③⑦⑧ D.①⑤⑥⑧2.(2022•海南省选择性考试)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常
A
数的值,下列说法正确的是( )
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
3.(2022•广东选择性考试,17题节选)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。
HAc的应用与其电离平衡密切相关。25℃时,HAc的K=1.75×105=10-4.76。
a
(1)配制 的HAc溶液,需 溶液的体积为_______mL。
(2)下列关于 容量瓶的操作,正确的是_______。
4.(2020·全国Ⅰ卷,27节选)由FeSO ·7H O固体配制0.10 mol·L-1 FeSO 溶液,需要的仪器有药匙、
4 2 4
玻璃棒、 (从下列图中选择,写出名称)。
5.[2020·天津,15(4)(8)]为测定CuSO 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
4
(4)甲方案
实验原理:CuSO +BaCl ===BaSO ↓+CuCl
4 2 4 2
实验步骤:
固体质量为w g,则c(CuSO )=__________________ mol·L-1。
4
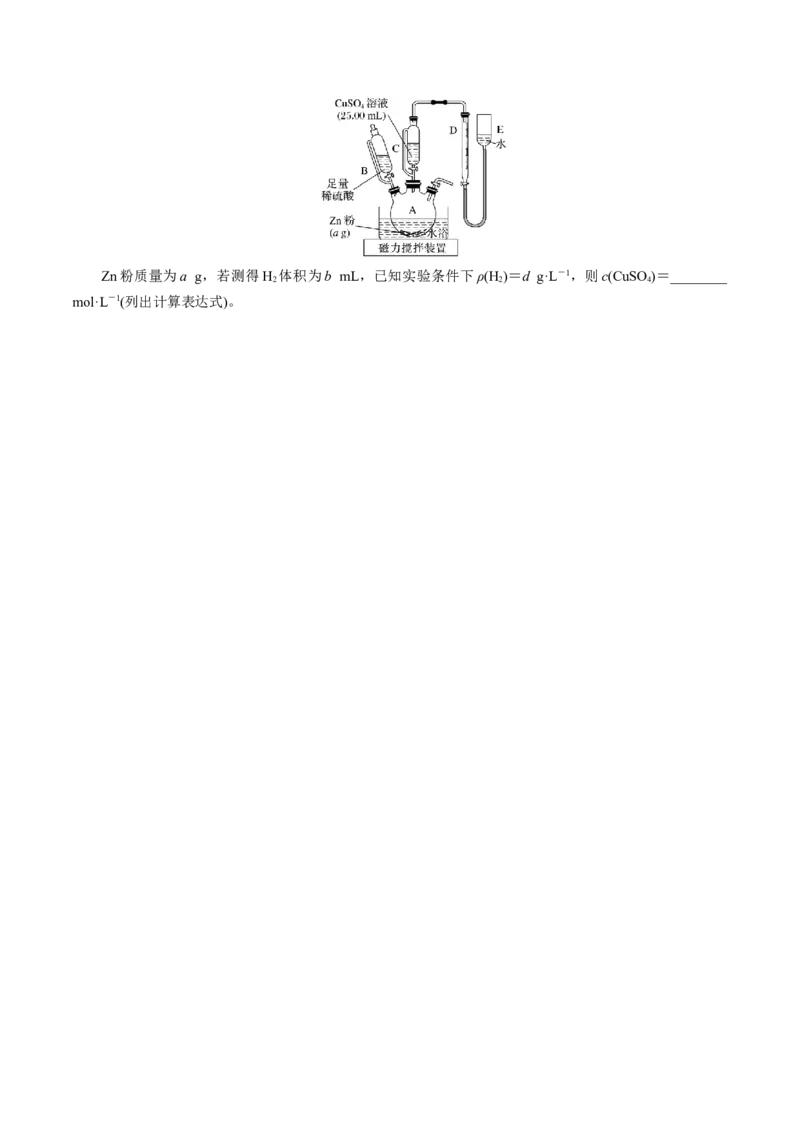
(8)乙方案,实验装置如图:Zn粉质量为a g,若测得H 体积为b mL,已知实验条件下ρ(H )=d g·L-1,则c(CuSO )=________
2 2 4
mol·L-1(列出计算表达式)。