文档内容
第 05 讲 物质的量浓度及溶液配制
1.能从宏观和微观的角度理解物质的量浓度的含义及其微观粒子间的关系。
2.了解容量瓶的特点、用途及使用注意事项,掌握配制一定物质的量浓度溶液的方法及操作,建立实
验误差分析思维模型,并能应用模型解决实际问题。
【核心素养分析】
1.宏观辨识与微观探析:能从不同层次认识物质的多样性,能根据溶液的体积和溶质的物质的量浓度
计算溶质的物质的量、溶质的微粒数目。
2. 科学探究与创新意识:能从问题和实际出发,确定探究目的,设计配制一定物质的量浓度溶液的实
验方案,进行实验探究;在探究中学会合作与交流,能够正确分析实验过程中可能存在的误差问题。
知识点一、物质的量浓度与溶质的质量分数
1.物质的量浓度
(1)概念:表示单位体积溶液中所含溶质B的物质的量。
(2)表达式:c =。
B
(3)单位:mol·L-1(或mol/L)。
2.溶质的质量分数
(1)概念:以溶液里溶质质量与溶液质量的比值表示溶液组成的物理量,一般用百分数表示。
(2)表达式:w(B)=×100%。
3.物质的量浓度与溶质的质量分数
物理量 物质的量浓度 溶质的质量分数
表示单位体积溶液里所含溶质 B 以溶液里溶质质量与溶液质量的比
定义
的物质的量的物理量 值表示溶液组成的物理量
表达式 c = ω(B)= ×100%
B
单位 mol·L-1
【易错警示】
(1)溶液中溶质的判断
Na、NaO、NaO――→NaOH
2 2 2
CO、SO 、SO ――→HCO、HSO 、HSO
2 2 3 2 3 2 3 2 4NH ――→NH ·H O(但仍按NH 进行计算)
3 3 2 3
CuSO ·5H O――→CuSO ,NaCO·10H O――→NaCO
4 2 4 2 3 2 2 3
(2)混淆溶液的体积和溶剂的体积
①不能用水的体积代替溶液的体积,尤其是固体、气体溶于水,一般根据溶液的密度和总质量进行计
算:
V==。
②两溶液混合,溶液的体积并不是两液体体积的加和,应依据混合溶液的密度进行计算。(若题目说忽
略体积变化,则总体积可由混合前体积直接相加)
知识点二 一定物质的量浓度溶液的配制
1.容量瓶的构造及使用方法
在使用前首先要检查是否漏水,检查合格后,用蒸馏水洗涤干净。具体操作如下:
【特别提醒】容量瓶使用的四个“不能”
①不能将固体或浓溶液直接在容量瓶中溶解或稀释;
②不能作为反应容器或用来长期贮存溶液;
③不能将过冷或过热的溶液转移到容量瓶中,(因为容量瓶的容积是在瓶身所标温度下确定的);
④不能配制任意体积的溶液,只能配制容量瓶上规定容积的溶液。
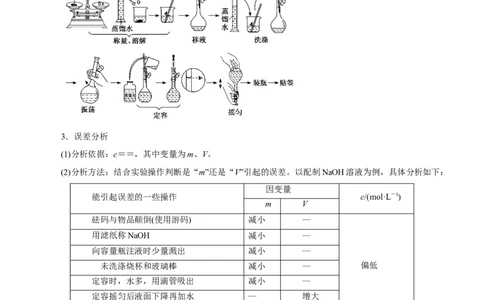
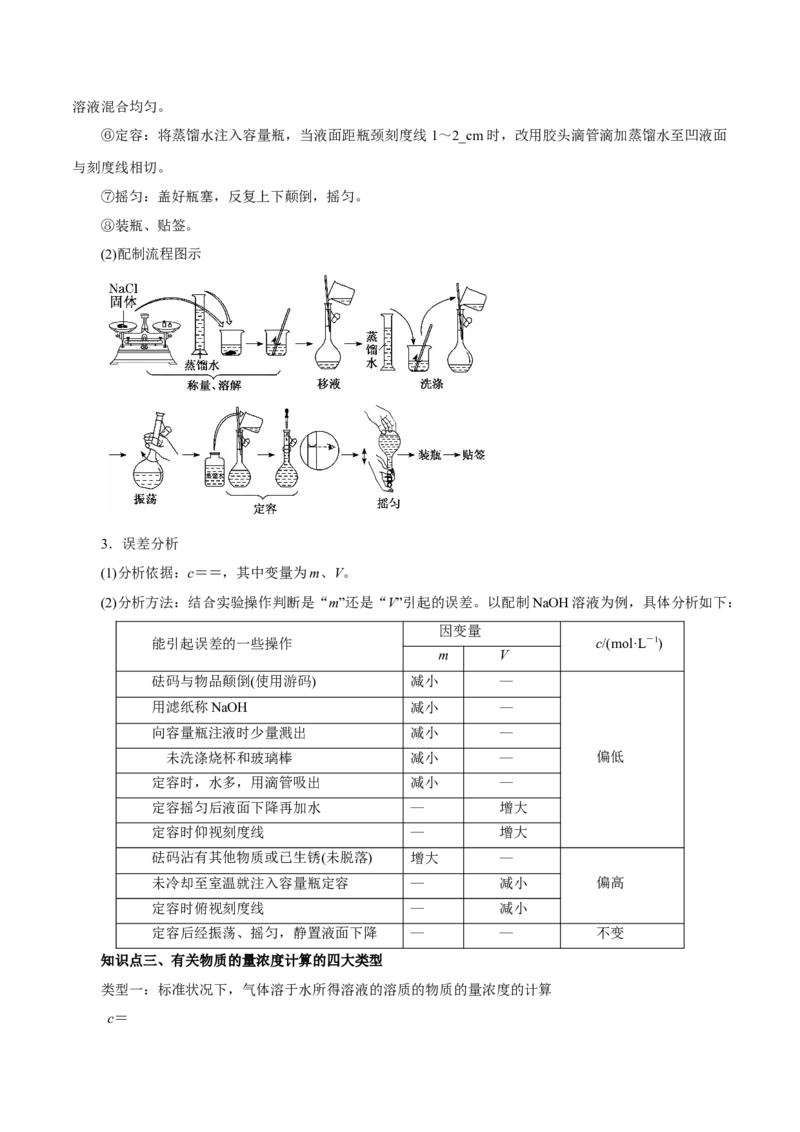
2.配制过程示意图
(1)配制过程(以配制100 mL 1.00 mol·L-1 NaCl溶液为例)
①计算:需NaCl固体的质量为5.9 g。
②称量:根据计算结果,用托盘天平称量NaCl固体。
③溶解:将称好的NaCl固体放入烧杯中,加适量蒸馏水溶解,并用玻璃棒搅拌。
④移液:待烧杯中的溶液冷却至室温后,用玻璃棒引流将溶液注入 100 mL容量瓶中。
⑤洗涤:用适量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液全部注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀。
⑥定容:将蒸馏水注入容量瓶,当液面距瓶颈刻度线1~2_cm时,改用胶头滴管滴加蒸馏水至凹液面
与刻度线相切。
⑦摇匀:盖好瓶塞,反复上下颠倒,摇匀。
⑧装瓶、贴签。
(2)配制流程图示
3.误差分析
(1)分析依据:c==,其中变量为m、V。
(2)分析方法:结合实验操作判断是“m”还是“V”引起的误差。以配制NaOH溶液为例,具体分析如下:
因变量
能引起误差的一些操作 c/(mol·L-1)
m V
砝码与物品颠倒(使用游码) 减小 —
用滤纸称NaOH 减小 —
向容量瓶注液时少量溅出 减小 —
未洗涤烧杯和玻璃棒 减小 — 偏低
定容时,水多,用滴管吸出 减小 —
定容摇匀后液面下降再加水 — 增大
定容时仰视刻度线 — 增大
砝码沾有其他物质或已生锈(未脱落) 增大 —
未冷却至室温就注入容量瓶定容 — 减小 偏高
定容时俯视刻度线 — 减小
定容后经振荡、摇匀,静置液面下降 — — 不变
知识点三、有关物质的量浓度计算的四大类型
类型一:标准状况下,气体溶于水所得溶液的溶质的物质的量浓度的计算
c=类型二:溶液中溶质的质量分数与溶质的物质的量浓度的换算
(1)计算公式:c=(c为溶质的物质的量浓度,单位为mol·L-1;ρ为溶液的密度,单位为g·cm-3;w为
溶质的质量分数;M为溶质的摩尔质量,单位为g·mol-1)。
当溶液为饱和溶液时,因为w=,可得c=。
(2)公式的推导(按溶液体积为V L推导)
c===或w===。
类型三:溶液稀释和同种溶质的溶液混合的计算
(1)溶液稀释
①溶质的质量在稀释前后保持不变,即mw =mw 。
1 1 2 2
②溶质的物质的量在稀释前后保持不变,即cV=cV。
1 1 2 2
③溶液质量守恒,即m(稀)=m(浓)+m(水)(体积一般不守恒)。
(2)同种溶质不同物质的量浓度的溶液混合
①混合前后溶质的质量保持不变,即mw +mw =m w 。
1 1 2 2 混 混
②混合前后溶质的物质的量保持不变,即cV+cV=c V 。
1 1 2 2 混 混
类型四:应用电荷守恒式求算未知离子的浓度
溶液中所有阳离子所带正电荷总数与所有阴离子所带负电荷总数相等。
例如:CHCOONa和CHCOOH的混合溶液中存在
3 3
c(CHCOO-)+c(OH-)=c(Na+)+c(H+)。
3
【易错警示】
1.正确判断溶液的溶质并计算其物质的量
(1)与水发生反应生成新的物质,如Na、NaO、NaO――→NaOH;SO ――→HSO ;
2 2 2 3 2 4
NO ――→HNO。
2 3
(2)特殊物质,如NH 溶于水后溶质为NH ·H O,但计算浓度时仍以NH 作为溶质。
3 3 2 3
(3)含结晶水的物质:CuSO ·5H O―→CuSO ;NaCO·10H O―→NaCO。
4 2 4 2 3 2 2 3
2.准确计算溶液的体积
不能用水的体积代替溶液的体积,尤其是固体、气体溶于水,一般根据溶液的密度进行计算:
V=×10-3 L。
注意:溶液稀释或混合时,若题中注明“忽略混合后溶液体积变化”,则溶液的总体积一般按相加计
算。
3.注意溶质的浓度与溶液中某离子浓度的关系
溶质的浓度和离子浓度可能不同,要注意根据化学式具体分析。如1 mol·L-1Al (SO ) 溶液中c(SO)=3
2 4 3mol·L-1,c(Al3+)=2 mol·L-1(当考虑Al3+水解时,则其浓度小于2 mol·L-1)。
高频考点一 考查物质的量浓度的计算
例1.V L Fe (SO ) 溶液中含有a g SO,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的
2 4 3
物质的量浓度为( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
【答案】A
【解析】依题意知,c(SO)= mol·L-1,c(Fe3+)= mol·L-1×= mol·L-1,故有 mol·L-1×0.5V L=2V
L×c ,c = mol·L-1。
B B
【方法技巧】
1.气体溶于水时物质的量浓度的计算
气体溶于水,求溶液中溶质的物质的量浓度的一般思维:(设气体体积为V,溶液体积为V)
1 2
2.溶液稀释定律(守恒观点)
(1)溶质的质量在稀释前后保持不变,即mw =mw 。
1 1 2 2
(2)溶质的物质的量在稀释前后保持不变,即cV=cV。
1 1 2 2
(3)溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。
3.同溶质不同物质的量浓度溶液的混合计算
(1)混合后溶液体积保持不变时,cV+cV=c ·(V+V)。
1 1 2 2 混 1 2
(2)混合后溶液体积发生改变时,cV+cV=c V ,其中V =。
1 1 2 2 混 混 混
4.溶质相同、质量分数不同的两溶液混合规律
同一溶质、质量分数分别为a%、b%的两溶液混合。
①当溶液密度大于1 g·cm-3时,必然是溶液浓度越大,密度越大,等体
积混合后,质量分数w>(a%+b%)(如HSO 、HNO、HCl、NaOH等多数溶
2 4 3
等体积混合
液)。
②当溶液密度小于1 g·cm-3时,必然是溶液越浓,密度越小,等体积混
合后,质量分数w<(a%+b%)(如酒精、氨水溶液)两溶液等质量混合时(无论ρ>1 g·cm-3还是ρ<1 g·cm-3),则混合后溶液
等质量混合
中溶质的质量分数w=(a%+b%)
5.物质的量浓度与溶质质量分数的换算
体积为V mL,密度为ρ g·cm-3的溶液,含有摩尔质量为M g·mol-1的溶质m g,溶质的质量分数为
w,则溶质的物质的量浓度c与溶质的质量分数w的关系是:
c====,反之,w=。
6.物质的量浓度(c)与溶解度(S)的换算
若某饱和溶液的密度为ρ g/cm3,溶质的摩尔质量为M g·mol-1,溶解度为S g,则溶解度与物质的量
浓度的表达式分别为:S=,c===。
【变式探究】将标准状况下的某气体(摩尔质量为M g·mol-1)溶于a g水中,所得溶液的密度为b
g·cm-3,溶质的物质的量浓度为c mol·L-1,则该气体溶入水中的体积是( )
A. L B. L
C. L D. L
【答案】C
【解析】设溶入水中气体的体积为V L,则÷[(+a)÷b]×103=c,化简整理得:V=。
高频考点二 溶液的稀释与混合
例2.(2021·浙江1月选考)玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
3S+6KOH=====2KS+KSO +3HO
2 2 3 2
(x-1)S+KS=====KS(x=2~6)
2 2 x
S+KSO =====KSO
2 3 2 2 3
请计算:
(1)0.480 g硫单质与体积为V的1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS和KSO ,则V=
2 2 3
______ mL。
(2)3.840 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS 和KSO ,则x=
2 x 2 2 3
________。
【解析】(1)硫与KOH溶液反应只生成KS和KSO ,则
2 2 3
3S + 6KOH=====2KS+KSO +3HO
2 2 3 2
96 g 6 mol
0.480 g 1.00 mol·L-1×V×10-3 L
=
解得V=30.0 mL。
(2)由已知化学方程式可得只生成KS 和KSO 的化学方程式为2(x+1)S+6KOH===2K S+KSO +
2 x 2 2 3 2 x 2 2 33HO,3.840 g 硫单质为 0.12 mol,n(KOH)=1.00 mol·L-1×60.0×10-3 L=0.06 mol,则 2(x+1)∶6=
2
0.12∶0.06
解得x=5。
【答案】(1)30.0 (2)5
【方法技巧】
1.溶液稀释定律(守恒观点)
(1)溶质的质量在稀释前后保持不变,即mw =mw 。
1 1 2 2
(2)溶质的物质的量在稀释前后保持不变,即cV=cV。
1 1 2 2
(3)溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。
2.同溶质不同物质的量浓度溶液的混合计算
(1)混合后溶液体积保持不变时,cV+cV=c ×(V+V)。
1 1 2 2 混 1 2
(2)混合后溶液体积发生改变时,cV+cV=c V ,其中V =。
1 1 2 2 混 混 混
3.不同溶质溶液混合反应,有关物质浓度的计算
(1)明确各反应物、产物之间的物质的量之比。
(2)巧用电荷守恒思想:电解质溶液中阳离子所带正电荷总数等于阴离子所带负电荷总数。
4.溶质相同、质量分数不同的两溶液混合定律(教师用书独具)
同一溶质、质量分数分别为a%、b%的两溶液混合。
(1)等质量混合
两溶液等质量混合时(无论ρ>1 g·cm-3还是ρ<1 g·cm-3),则混合后溶液中溶质的质量分数w=(a%+
b%)。
以上规律概括为“计算推理有技巧,有大必有小,均值均在中间找,谁多向谁靠”。
(2)等体积混合
①当溶液密度大于1 g·cm-3时,必然是溶液浓度越大,密度越大(如HSO 、HNO、HCl、NaOH等多
2 4 3
数溶液),等体积混合后,质量分数w>(a%+b%)。
②当溶液密度小于1 g·cm-3时,必然是溶液浓度越大,密度越小(如酒精、氨水溶液),等体积混合后,
质量分数w<(a%+b%)。
【变式探究】(1)将3p%的硫酸与等体积的p%的硫酸混合得到q%的稀硫酸,则p、q的关系正确的是
________。
①q=2p ②q>2p
③q<2p ④无法确定
(2)若上题中的溶质是乙醇而非硫酸,则p、q的关系是________。①q=2p ②q>2p
③q<2p ④无法确定
【答案】(1)② (2)③
【解析】当两者等体积混合时,设浓溶液的密度为ρ,稀溶液的密度为ρ,体积各为1 L,则混合后
1 2
w==()×p%=(1+)p%,当ρ>ρ 时,如HSO 溶液、HNO 溶液,w>2p%;当ρ<ρ 时,如氨水、酒精
1 2 2 4 3 1 2
溶液,w <2p%。
高频考点三 一定物质的量浓度溶液配制
例3.(2021·山东卷)为完成下列各组实验,所选玻璃仪器和试剂是否准确、完整(不考虑存放试剂的容
器)?
实验目的 玻璃仪器 试剂 判断
配制100 mL一定物质的量 100 mL容量瓶、胶头滴 蒸馏水、
浓度的NaCl溶液 管、烧杯、量筒、玻璃棒 NaCl固体
【解析】配制100 mL一定物质的量浓度的NaCl溶液的步骤为:计算、称量、溶解、转移、洗涤、定
容、摇匀等,需要的仪器有:托盘天平、药匙、烧杯、量筒、玻璃棒、100 mL容量瓶、胶头滴管等。
【答案】是
【方法技巧】 溶液配制过程中的“四个数据”准确应用
数据 要求或解释
实验室中一般用托盘天平称量固体药品,而托盘天平只能精确到
药品的质量(保
0.1 g,所以记录数据时只能保留小数点后一位数字。如所需NaCl的
留小数点后一位)
质量为14.6 g,不能写为14.60 g
(1)选择容量瓶的规格时应该与所配溶液体积相等或稍大,如需
用480 mL某溶液,则应该选择500 mL容量瓶,计算所用溶质的量
容量瓶的规格
时,一定要以容量瓶总体积500 mL为依据。
(2)回答补充仪器的问题时应该注明容量瓶的规格,如回答“500
mL容量瓶”时,不能只回答“容量瓶”
洗涤烧杯 移液时洗涤烧杯2~3次是为了确保溶质全部转移到容量瓶中,
(2~3次) 否则会导致溶液浓度偏低
液面离容量瓶 定容时,当液面离容量瓶颈刻度线1~2 cm时,改用胶头滴管加
颈刻度线(1~2 cm) 蒸馏水,否则容易导致液体体积超过刻度线,溶液浓度偏低
【举一反三】(2020·全国Ⅰ卷·节选)由FeSO ·7H O固体配制0.10 mol·L-1 FeSO 溶液,需要的仪器有
4 2 4
药匙、玻璃棒、________________(从下列图中选择,写出名称)。
【解析】利用固体配制一定物质的量浓度的溶液时需要用托盘天平称量固体,用烧杯溶解固体,用量筒量取蒸馏水。
【答案】烧杯、量筒、托盘天平
【变式探究】用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸,下列操作
正确的是( )
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.必需的定量仪器有50 mL量筒、250 mL容量瓶和托盘天平
C.量取浓硫酸的体积为25.0 mL
D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
【答案】C
【解析】稀释浓硫酸时,应将浓硫酸缓慢注入水中并不断搅拌,A项错误;该实验不需要托盘天平,
B项错误;根据溶质质量不变知,配制该稀硫酸需要浓硫酸的体积为V==25.0 mL,C项正确;不能在容
量瓶里稀释浓硫酸,应在烧杯里稀释并冷却后,再转移到容量瓶中,最后加水定容,D项错误。
高频考点四 配制溶液的误差分析技巧
例4.抗击新冠病毒疫情期间,需要配制0.01 mol·L-1的KMnO 消毒液,下列操作会导致所配溶液浓度
4
偏高的是( )
A.取KMnO 样品时不慎在表面沾了点蒸馏水
4
B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶刻度线
D.摇匀后见液面下降,再加水至刻度线
【答案】C
【解析】选项A中的操作使取得样品的质量偏小,溶液浓度偏低;选项B中液体溅出,溶质减少,溶
液浓度偏低;选项D中加水量偏多,溶液浓度偏低。
【方法技巧】配制溶液的误差分析技巧
(1)误差分析的思维流程
(2)定容时视线引起误差的分析方法
①仰视刻度线[图(a)],导致溶液体积偏大,结果偏低。
②俯视刻度线[图(b)],导致溶液体积偏小,结果偏高。【变式探究】利用碳酸钠晶体(Na CO·10H O)来配制0.5 mol·L-1的碳酸钠溶液1 000 mL,假如其他操
2 3 2
作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
A.称取碳酸钠晶体100.0 g
B.定容时俯视刻度线
C.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗
D.移液前,容量瓶中有少量蒸馏水
【答案】B
【解析】0.5 mol·L-1的碳酸钠溶液1 000 mL需称取NaCO·10H O 143.0 g,结果偏低,A不符合题意;
2 3 2
定容时俯视刻度线,会造成所配溶液的体积偏小,结果偏高,B符合题意;未冲洗溶解碳酸钠晶体的烧杯,
会造成碳酸钠损失,结果偏低,C不符合题意;容量瓶中有少量蒸馏水对所配溶液的浓度无影响,D不符
合题意。