文档内容
第 05 讲 离子反应 离子方程式
(模拟精练+真题演练)
1.(2023·上海静安·统考二模)能与硫酸铁溶液发生氧化还原反应的电解质是
A.氯化钡 B.铁 C.氢氧化钠 D.碘化氢
【答案】D
【解析】A.氯化钡与硫酸铁反应生成硫酸钡和氯化铁,是非氧化还原反应,故A不符合
题意;B.铁与硫酸铁反应生成硫酸亚铁,是氧化还原反应,但铁是单质,不是电解质,
故B不符合题意;C.氢氧化钠与硫酸铁反应生成氢氧化铁和硫酸钠,是非氧化还原反应,
故C不符合题意;D.碘化氢与硫酸铁反应生成硫酸亚铁、硫酸和单质碘,是氧化还原反
应,且碘化氢是电解质,故D符合题意。综上所述,答案为D。
2.(2023·上海崇明·统考二模)下列属于弱电解质的是
A.CaCO B.SO C.NH ·H O D.Ba(OH)
3 2 3 2 2
【答案】C
【解析】A.CaCO 属于盐,属于强电解质,故A不符合题意;B.SO 是非金属性氧化物,
3 2
属于非电解质,故B不符合题意;C.NH ·H O属于弱碱,属于弱电解质,故C符合题意;
3 2
D.Ba(OH) 属于强碱,属于强电解质,故D不符合题意。综上所述,答案为C。
2
3.(2023·福建厦门·统考二模)下列食品添加剂不属于电解质的是
A.二氧化硫 B.亚硝酸钠 C.葡萄糖酸 D.山梨酸钾
【答案】A
【分析】电解质是溶于水或在熔融状态下能够导电的化合物;非电解质是溶于水或在熔融
状态下不能够导电的化合物;酸、碱、盐、金属氧化物等均属于电解质;
【解析】A.二氧化硫为非电解质,故A符合题意;B.亚硝酸钠属于盐,为电解质,故B
不符合题意;C.葡萄糖酸属于有机酸,为电解质,故C不符合题意;D.山梨酸钾属于盐,
为电解质,故D不符合题意;故选A。
4.(2023·上海青浦·统考二模)向 溶液中加入几滴酚酞溶液,然后向
混合液中匀速、逐滴加入 溶液,滴加过程中测得溶液电导率的变化如图所
示。下列说法不正确的是A.烧杯中红色逐渐变浅直至完全褪去
B.由于水存在微弱电离、 存在微弱溶解,理论上电导率不会为0
C.电导率减小的过程中,发生反应:
D.若用同浓度的 溶液代替稀硫酸重复上述实验,电导率变化与原实验相同
【答案】D
【解析】A. 浓度减小直至反应完全,烧杯中红色逐渐变浅直至完全褪去,A正确;
B.由于水存在微弱电离、 存在微弱溶解,溶液中存在少量离子,理论上电导率不
会为0,B正确;C.电导率减小的过程中,离子浓度减小,发生反应:
,C正确;D.若用同浓度的 溶液代替
稀硫酸重复上述实验,反应生成硫酸钡沉淀,溶液中存在钠离子和氢氧根,电导率不会减
少到几乎为0,电导率变化与原实验不相同,D错误;故选D。
5.(2022·辽宁抚顺·抚顺一中校考模拟预测)下列化学方程式中,不能用离子方程式H+
+OH-= HO表示的是
2
A.Cu(OH) +2HNO =Cu(NO)+2H O B.Ba(OH) +2 HCl = BaCl +2H O
2 3 3 2 2 2 2 2
C.2NaOH + H SO = Na SO +2H O D.HCl+KOH=KCl+ H O
2 4 2 4 2 2
【答案】A
【解析】A.Cu(OH) 是沉淀,不能拆,则不能用离子方程式 H++ OH- = H O表示,A符合
2 2
题意;B.Ba(OH) 、HCl、BaCl 均为可溶性强电解质,在离子反应中均可拆写为离子形式,
2 2
可用离子方程式 H++ OH- = H O表示,B不符合题意;C.NaOH、HSO 、NaSO 均为可
2 2 4 2 4
溶性强电解质,在离子反应中均可拆写为离子形式,可用离子方程式 H++ OH- = H O表示,
2
C不符合题意;D.HCl、KOH、KCl均可溶性强电解质,在离子反应中均可拆写为离子形
式,可用离子方程式 H++ OH- = H O表示,D不符合题意;综上所述答案为A。
2
6.(2022·北京延庆·统考一模)用如图所示装置(搅拌装置已略去)探究溶液中离子浓度的
变化,灯光变化不可能出现“亮→暗(或灭)→亮”现象的是A B C D
试剂a NaOH Ca(OH) Ba(OH) HSO
2 2 2 3
试剂b CHCOOH Ca(HCO ) HSO HS
3 3 2 2 4 2
【答案】A
【解析】A.醋酸为弱电解质,加入NaOH反应生成强电解质醋酸钠,所以不会出现变暗
的过程,A符合题意;B.Ca(HCO ) 为强电解质,所以开始灯亮,加入氢氧化钙后二者反
3 2
应生成碳酸钙沉淀和水,溶液中的离子浓度逐渐降低,直至接近于零,此时灯灭,之后又
随着氢氧化钙的加入,溶液中的离子浓度增大,灯泡变亮,B不符合题意;C.硫酸为强电
解质,开始灯亮,加入氢氧化钡后二者反应生成硫酸钡和水,溶液中溶液中的离子浓度逐
渐降低,直至接近于零,此时灯灭,之后又随着氢氧化钡的加入,溶液中的离子浓度增大,
灯泡变亮,C不符合题意;D.HS为弱电解质,开始灯亮,加入亚硫酸后二者反应生成硫
2
单质和水,硫难溶于水,所以的离子浓度逐渐降低,直至接近于零,此时灯灭,之后随着
亚硫酸的加入,溶液中的离子浓度增大,灯泡变亮,D不符合题意;综上所述答案为A。
7.(2023·江苏·统考二模)下列化学反应表示正确的是
A.用水吸收二氧化氮制硝酸:
B.用烧碱溶液吸收硝酸工业尾气:
C.雷雨天气空气中的氮气和氧气反应:
D.铜粉和稀硝酸反应:
【答案】B
【解析】A.水吸收二氧化氮制硝酸同时生成NO: ,A错误;
B.用烧碱溶液吸收硝酸工业尾气生成亚硝酸钠和水,: ,
B正确;C.雷雨天气空气中的氮气和氧气反应生成NO: ,C错误;D.
铜粉和稀硝酸反应生成硝酸铜和NO: ,D错误;故
选B。
8.(2023·广东惠州·统考一模)下列解释实验事实的离子方程式书写正确的是A.钠投入氯化铜溶液中:
B.氯气通入水中:
C.二氧化硫与酸性高锰酸钾溶液反应:
D.硫酸溶液中加入氢氧化钡溶液:
【答案】C
【解析】A.钠投入氯化铜溶液中,先和水反应生成氢氧化钠和氢气,氢氧化钠再和氯化
铜反应生成氢氧化铜沉淀和氯化钠,A错误;B.氯气和水反应生成盐酸和次氯酸,盐酸
能拆成离子形式,但次氯酸不能拆,B错误;C.二氧化硫和高锰酸钾反应生成硫酸钾和硫
酸锰和硫酸,反应的离子方程式为 ,C正确;
D.硫酸溶液中加入氢氧化钡溶液: ,D错误;故
选C。
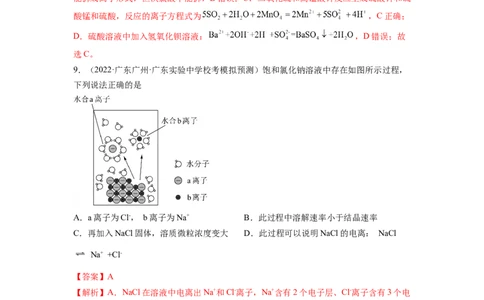
9.(2022·广东广州·广东实验中学校考模拟预测)饱和氯化钠溶液中存在如图所示过程,
下列说法正确的是
A.a离子为Cl-, b离子为Na+ B.此过程中溶解速率小于结晶速率
C.再加入NaCl固体,溶质微粒浓度变大 D.此过程可以说明NaCl的电离: NaCl
Na+ +Cl-
【答案】A
【解析】A.NaCl在溶液中电离出Na+和Cl-离子,Na+含有2个电子层、Cl-离子含有3个电
子层,则离子半径Cl->Na+,Na+带正电易吸引水分子中的氧原子、Cl-离子带负电易吸引水
分子中的氢原子,根据图示可知,a为Cl-、b为Na+,故A正确;B.饱和溶液中始终存在
溶解与结晶过程,溶解速率等于结晶速率,故B错误;C.饱和氯化钠溶液中加入NaCl固
体不能继续溶解,则溶质质量不变,溶质微粒浓度不变,故C错误;D.NaCl是强电解质,
在水中完全电离,电离方程式为NaCl=Na++Cl-,故D错误;故选:A。
10.(2022·山东德州·统考三模)用1 mol/L氨水(控制1滴/s逐滴加入,下同)滴定60
mL0.02 mol/L硫酸铜溶液;氨水稍过量后,再用1 mol/L的硫酸反滴定铜氨配合物溶液。
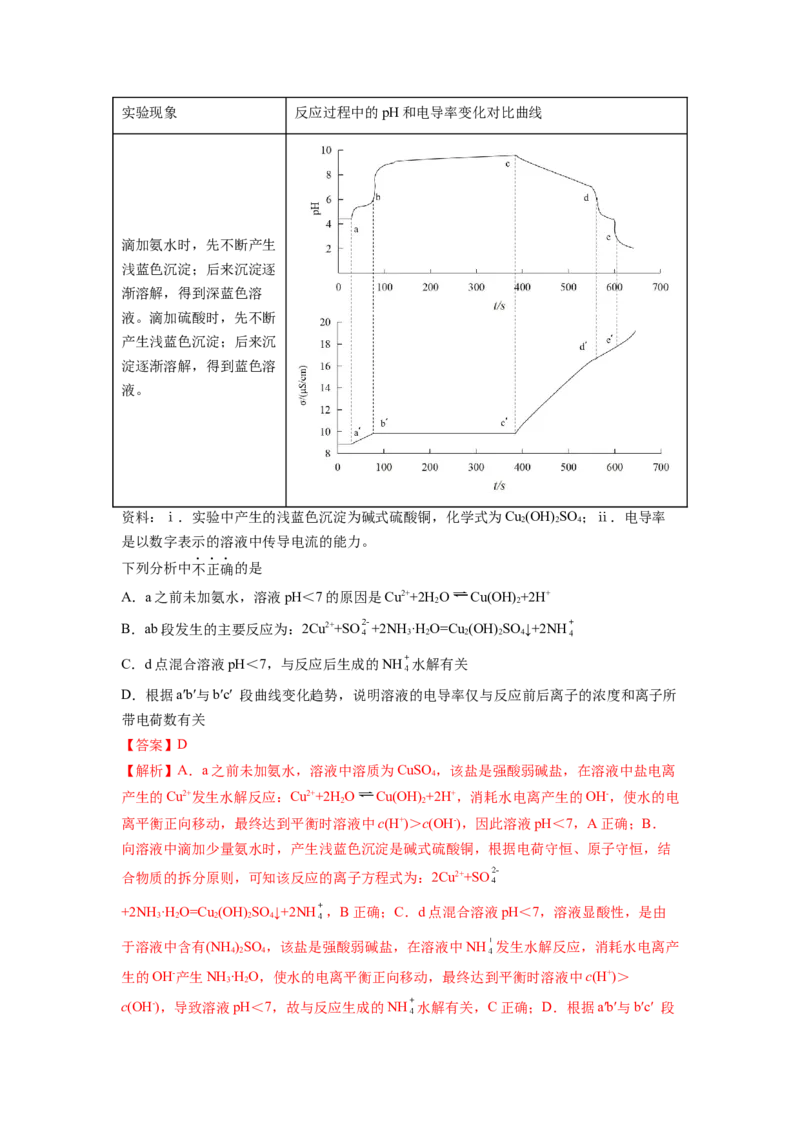
实验记录如下:实验现象 反应过程中的pH和电导率变化对比曲线
滴加氨水时,先不断产生
浅蓝色沉淀;后来沉淀逐
渐溶解,得到深蓝色溶
液。滴加硫酸时,先不断
产生浅蓝色沉淀;后来沉
淀逐渐溶解,得到蓝色溶
液。
资料:ⅰ.实验中产生的浅蓝色沉淀为碱式硫酸铜,化学式为Cu (OH) SO ;ⅱ.电导率
2 2 4
是以数字表示的溶液中传导电流的能力。
下列分析中不正确的是
A.a之前未加氨水,溶液pH<7的原因是Cu2++2H O Cu(OH) +2H+
2 2
B.ab段发生的主要反应为:2Cu2++SO +2NH·H O=Cu (OH) SO ↓+2NH
3 2 2 2 4
C.d点混合溶液pH<7,与反应后生成的NH 水解有关
D.根据a′b′与b′c′ 段曲线变化趋势,说明溶液的电导率仅与反应前后离子的浓度和离子所
带电荷数有关
【答案】D
【解析】A.a之前未加氨水,溶液中溶质为CuSO ,该盐是强酸弱碱盐,在溶液中盐电离
4
产生的Cu2+发生水解反应:Cu2++2H O Cu(OH) +2H+,消耗水电离产生的OH-,使水的电
2 2
离平衡正向移动,最终达到平衡时溶液中c(H+)>c(OH-),因此溶液pH<7,A正确;B.
向溶液中滴加少量氨水时,产生浅蓝色沉淀是碱式硫酸铜,根据电荷守恒、原子守恒,结
合物质的拆分原则,可知该反应的离子方程式为:2Cu2++SO
+2NH·H O=Cu (OH) SO ↓+2NH ,B正确;C.d点混合溶液pH<7,溶液显酸性,是由
3 2 2 2 4
于溶液中含有(NH )SO ,该盐是强酸弱碱盐,在溶液中NH 发生水解反应,消耗水电离产
4 2 4
生的OH-产生NH ∙H O,使水的电离平衡正向移动,最终达到平衡时溶液中c(H+)>
3 2
c(OH-),导致溶液pH<7,故与反应生成的NH 水解有关,C正确;D.根据a′b′与b′c′ 段曲线变化趋势,说明溶液的电导率不仅与反应前后离子的浓度和离子所带电荷数有关,而
且也与离子的种类有关,D错误;故合理选项是D。
11.(2022·上海闵行·统考一模)某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀
释时pH变化曲线如图所示。
(1)a、b、c三点溶液中水的电离程度大小关系:_______。
(2)①b点溶液中c(H+) =_______+_______ (填微粒浓度)。________
②用等浓度的NaOH溶液和b、c处溶液反应,消耗NaOH溶液的体积。 _______ (填
“>”“<”或“=”)。
(3)阐述a、c两点溶液的导电能力强弱:_______。
【答案】(1)a>b>c
(2)① ②>
(3)a、c两点溶液的离子㳖度cb,综上所
述,a、b、c三点溶液中水的电离程度a>b>c,故答案为:a>b>c;
(2)①b点溶液中,根据质子守恒得出 ,故答案为:
;②用等浓度的NaOH溶液和b、c处溶液反应,b点溶液中铵根和
氢离子均消耗NaOH,而c点溶液只有盐酸消耗NaOH(盐酸完全电离),故消耗NaOH溶
液的体积 > ,故答案为:>;
(3)溶液的导电能力和溶液中自由移动离子浓度的大小有关,当溶液的体积相等时,a、c
两点溶液的离子浓度c