文档内容
第 06 练
元素“位—构—性”的综合推断
一、元素综合推断的具体方法
这类题目往往将元素化合物知识、物质结构理论、化学基本理论等知识串联起来,综
合性较强,解题的关键是正确推断元素。具体方法:
阅读题目(建立印象) → 根据题设特点(短周期元素原子结构特征,元素主要化合
价的特征关系,元素及化合物的特殊性质,元素在周期表中的特殊位置等)→找出突破口
→假设→验证。如:已知X、Y、Z、W四种短周期元素的位置关系如图:
则可以推出X为He,再依次推知Y为F、Z为O、W为P。
二、主要考点
1.原子或离子半径大小,第一电离能、电负性大小比较
2.元素在周期表中的位置
3.气态氢化物的稳定性
4.元素金属性或非金属性
5.元素最高价氧化物对应水化物的酸碱性
6.元素间组成化合物的种类及性质
7.化学键
三、元素金属性、非金属性强弱的比较方法
1.元素金属性强弱的实验比较法。
(1)单质与水或非氧化性酸反应越剧烈,金属性越强。
(2)单质还原性越强或离子氧化性越弱,金属性越强。
(3)最高价氧化物对应水化物的碱性越强,金属性越强。
(4)若Xn++Y―→X+Ym+,则Y金属性比X强。
2.元素非金属性强弱的实验比较法。
(1)与H2化合越容易,气态氢化物越稳定,非金属性越强。
(2)单质氧化性越强,阴离子还原性越弱,非金属性越强。
(3)最高价氧化物对应水化物的酸性越强,非金属性越强。
(4)An-+B―→Bm-+A,则B非金属性比A强。
3.元素性质递变规律
(1)同周期,从左到右,主族元素的金属性减弱,非金属性增强。(2)同主族,从上到下,元素的金属性增强,非金属性减弱。
四、“四看”突破粒子半径大小比较
1.“一看”电子层数:当最外层电子数相同,电子层数不同时,电子层数越多,半径越
大。4.“二看”原子序数:当核外电子数相同时,原子序数越大,离子半径越小。
2.“三看”核电荷数:当电子层数相同时,核电荷数越大,半径越小。
3.“四看”核外电子数:对于同元素,当电子层数和核电荷数均相同时,核外电子数越
多,半径越大。
1.(2023·浙江·校联考三模)前四周期的元素X、Y、Z、Q、W的原子序数依次增大,基
态X原子的半径是所有原子中最小的,Y与X可形成室温下XY、XY 两种无色液体,基
2 2 2
态Z原子的M电子层上p轨道为半充满状态,Y、Q同主族,W原子的价层电子排布式为
,下列说法不正确的是
A.电负性:
B.简单离子半径:
C.同周期中第一电离能比Q大的元素有1种
D. 三种元素形成的某些化合物,可存在于某些使用后的碱性电池中
【答案】C
【分析】五种前四周期的元素X、Y、Z、Q、W的原子序数依次增大,其中基态X原子的
半径是所有原子中最小的,则X为H元素;Y与X可形成室温下XY、XY 两种无色液体,
2 2 2
则Y为O,基态Z原子的M电子层上P轨道为半充满状态,其外围电子排布式为3s23p3,
故Z为P元素;W原子的特征电子构型为3d54s2,则W为Mn元素;Y、Q同主族,由Y
为O元素,故Q为S元素,据此分析解题。
【详解】A.由分析可知,Y、Z、Q分别为O、P、S,根据同一周期从左往右电负性依次
增大,同一主族从上往下电负性依次减小,故电负性O>S>P即 ,A正确;
B.由分析可知,X、Y、Z、Q分别为H、O、P、S,根据电子层数越多半径越大,电子层
数相同,核电荷数越大,半径越小可知,简单离子半径P3->S2->O2->H+即 ,
B正确;
C.由分析可知,Q为S,根据同一周期从左往右元素的第一电离能呈增大趋势,ⅡA与Ⅲ
A、ⅤA与ⅥA反常,故同周期中第一电离能比Q大的元素有P、Cl、Ar等3种,C错误;
D.由分析可知, 分别为H、O、Mn三种元素形成的某些化合物,如MnOOH
可存在于某些使用后的碱性电池中,D正确;
故答案为:C。
2.(2023·山东·校联考模拟预测)某点击化学试剂由原子序数依次增大的X、Y、M、Z四种短周期元素组成,其中基态Y原子的电子总数是其最高能级电子数的2倍,2的原子序
数是Y的两倍, 衰变方程: 。下列说法错误的是
A.简单氢化物的沸点:M>X
B.简单氢化物还原性:Z>X>M
C. 和 互为同位素
D.元素Y的第一电离能小于同周期相邻两种元素的
【答案】C
【分析】根据基态Y原子的电子总数是其最高能级电子数的2倍,可推出Y是O,Z是
S,再分析衰变方程发现M质子数比X大2,原子序数XO>N,则简单氢化物还原性:
Z>X>M,故B正确;
C. 和 在组成上都是氮气,属于同种物质,都是分子,一定不是同位素,故C错
误;
D.同周期元素从左到右第一电离能呈增大趋势,但基态N原子是半充满稳定结构,第一
电离能大于O原子,因此O的第一电离能小于N和F,故D正确;
故选:C。
3.(2023·重庆·统考三模)X、Y、Z、Q、W是原子序数依次增大的前四周期元素,其中
X是宇宙中含量最多的元素;在同周期元素中,第一电离能数值比Y大的元素有2种:Z
元素原子的价层电子排布是 ;Q、W元素原子的最外层均只有1个电子,Q元素的
原子半径是前四周期中最大的,W元素基态原子内层轨道均排满电子。下列说法正确的是
A.电负性: B. 属于酸性氧化物
C.Q与Z可以形成多种化合物 D.W元素位于元素周期表的d区
【答案】C
【分析】X、Y、Z、Q、W是原子序数依次增大的前四周期元素,其中X是宇宙中含量最
多的元素,则X为H元素;Z元素原子的价层电子排布是nsnnp2n,s能级填充满只能容纳2
个电子,即n=2,故Z为O元素;由原子序数可知Y处于第二周期,而在同周期元素中第
一电离能数值比Y大的元素有2种,可知Y为N元素;Q、W元素原子的最外层均只有1
个电子,Q元素的原子半径是前四周期中最大的,可知Q为K元素,由原子序数可知W处
于第四周期,而W元素基态原子内层轨道均排满电子,其核外电子数为2+8+18+1=29,则
W为Cu元素,据此分析解题。
【详解】由分析可知,X为H元素、Y为N元素、Z为O元素、Q为K元素、W为Cu元素;
A.同周期主族元素自左而右电负性增大,N、O在它们的氢化物中都表现负价,说明二者
的电负性都比氢元素大,则电负性:H<N<O,A错误;
B.YZ 是NO,与水反应除生成HNO 外还有NO生成,不是酸性氧化物,B错误;
2 4 2 4 3
C.K元素与氧元素可以形成KO、KO、KO ,C正确;
2 2 2 2
D.Cu处于第四周期第IB族,属于ds区元素,D错误;
故答案为:C。
4.(2023·湖南衡阳·校联考三模)前四周期主族元素W、X、Y、Z、M原子序数依次增大,
其中W为宇宙中含量最多的元素,W与X、X与Y、Y与Z、Z与M原子序数差的数值可
组成一个公比为2的等比数列。下列说法正确的是
A.简单离子半径:
B.X与氧气在加热条件下反应生成
C.W与Y或Z均可形成 化合物
D.单质M的导电性良好
【答案】C
【分析】宙中含量最多的元素为H,因此W为H,W与X、X与Y、Y与Z、Z与M原子
序数差的数值可组成一个公比为2的等比数列,则X为Li、Y为N、Z为P、M为Ga。
【详解】A. Z的简单离子为 、Y的简单离子为 、X的简单离子为 ,则简单离
子半径: ,A项错误;
B.Li与氧气反应不能生成 ,B项错误;
C.W与Y可形成 ,W与Z可形成 ,均为 化合物,C项正确;
D.Ga是半导体,导电性介于金属与非金属之间,D项错误;
故选C。
5.(2023·山东烟台·校联考模拟预测)X、Y、Z、W、P、Q为短周期元素,其中Y的原
子序数最小,它们的最高正价与原子半径关系如图所示。下列说法正确的是
A.Y在元素周期表中位于p区 B.第一电离能:Z>P>Q>X
C.离子半径: D.氧化物对应水化物的酸性:Q>P>Z【答案】C
【分析】由题干图示信息可知,X为+1价,原子半径最大,故X为Na,Y为+2价,原子
序数最小,Y为Be,Z为+4价,原子半径大于Y,故Z为Si,W为+5价,原子半径小于
Y,W为N,P为+6价,则P为S,Q为+7价,则Q为Cl,据此分析解题。
【详解】A.由分析可知,Y为Be,故Y在元素周期表中位于s区,A错误;
B.由分析可知,X为Na、Z为Si、P为S、Q为Cl,为同一周期元素,从左往右第一电离
能呈增大趋势,故第一电离能Cl>S>Si>Na即Q >P> Z>X,B错误;
C.由分析可知,W为N、P为S、Q为Cl,离子半径为S2->Cl->N3-即 ,C
正确;
D.由分析可知,Q为Cl、P为S、Z为Si,其最高价氧化物对应水化物的酸性为HClO>
4
HSO >HSiO 即Q>P>Z,但不是最高价氧化物对应水化物的酸性则无此规律,如HSO >
2 4 2 3 2 4
HClO,D错误;
故答案为:C。
6.(2023·湖北·校联考模拟预测)五种短周期主族元素X、Y、Z、M、Q的原子序数依次
增大,X的2p轨道半充满,Y的s能级电子数和p能级电子数相等, Z是至今发现的电负
性最大的元素,M在元素周期表中处于周期序数等于族序数的位置,Q的单质被广泛用作
半导体材料。下列叙述中不正确的是
A.元素的第一电离能:XX>Y
D.最高价氧化物对应的水化物的酸性:X>Q>M
【答案】A
【分析】五种短周期主族元素X、Y、Z、M、Q的原子序数依次增大,X的2p轨道半充满,
则X为N;Y的s能级电子数和p能级电子数相等,Y原子核外电子排布式为1s22s22p4,则
Y为O;Z是至今发现的电负性最大的元素,则Z是F元素,M在元素周期表中处于周期
序数等于族序数的位置,M为Al,Q的单质被广泛用作半导体材料,Q为Si。
【详解】A.X、Y、Z为N、O、F,同周期元素第一电离能从左往右逐渐增大,N的2p轨
道为半充满,第一电离能大于O元素,则元素的第一电离能:YX>Y,C正确;
D.X、Q、M分别为N、Si、Al,最高价氧化物对应的水化物分别为HNO、HSiO、Al
3 2 3
(OH),酸性:X>Q>M,D正确;
3
故选A。7.(2023·云南曲靖·统考二模)X、Y、Z、W是短周期主族元素,工业上通过液化空气再
分离获得X元素的单质X;Y元素基态原子最外电子层的s、p能级上电子数相等;Z元素
2
的+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。
下列有关这些元素性质的说法一定正确的是
A.X元素的最简单氢化物分子的空间构型为三角锥形
B.Y元素最高价氧化物的晶体类型为共价晶体
C.Z元素的离子半径小于W元素的离子半径
D.Z元素的单质在一定条件下能与X元素的单质反应
【答案】D
【分析】工业上通过分离液态空气获得X 单质,则X是N或O。Y元素原子最外电子层上
2
s、p电子数相等,Y是C或Si。Z元素+2价阳离子的核外电子排布与氖原子相同,Z是
Mg。W元素原子的M层有1个未成对的p电子,W是Al或Cl。
【详解】A.X元素的最简单氢化物可能是NH 或HO,分子空间构型可能是三角锥形或V
3 2
形,A不正确;
B.Y元素最高价氧化物为CO 或SiO,晶体类型可能是分子晶体或共价晶体,B不正确;
2 2
C.若W是氯元素,则氯离子电子层数比镁离子多,所以离子半径大于镁离子半径,C不
正确;
D.镁既能和氮气反应生成氮化镁,也能和氧气反应生成氧化镁,D正确;
答案选D。
8.(2023·安徽·校联考三模)X、Y、Z、W是原子序数依次增大的短周期主族元素,其中
X与Z同族,Y的第一电离能高于同周期的相邻元素,W的原子序数是X原子价电子数的
4倍,下列说法正确的是
A.氢化物的沸点:W>X
B.Y在元素周期表中一定位于p区
C.最高价含氧酸的酸性:W>X>Z
D.X、Z元素形成的单质的晶体类型一定相同
【答案】C
【分析】X、Y、Z、W是原子序数依次增大的短周期主族元素,W的原子序数是X原子价
电子数的4倍,则X为C元素、W为S元素;X与Z同族,则Z为Si元素;Y的第一电离
能高于同周期的相邻元素,则Y可能为N元素或Mg元素。
【详解】A.碳元素形成的氢化物可能为液态烃和固态烃,液态烃和固态烃的沸点都高于
硫化氢,故A错误;
B.镁元素的原子序数为12,基态原子的价电子排布式为3s2,位于元素周期表的s区,故
B错误;
C.元素的非金属性越强,最高价含氧酸的酸性越强,元素非金属性强弱顺序为S>C>Si,
则最高价含氧酸的酸性强弱顺序为W>X>Z,故C正确;D.碳单质的晶体类型可能为共价晶体,如金刚石,也可能为分子晶体,如C ,还可能为
60
混合型晶体,如石墨,而硅单质形成的晶体只能为共价晶体,则碳元素和硅元素形成的单
质的晶体类型不一定相同,故D错误;
故选C。
9.(2023·山东聊城·校联考三模)某平面形分子常用于感光复印纸的生产,其结构如图所
示,其中W、X、Y、Z为原子序数依次增大的短周期主族元素,且仅X、Y位于同一周期;
Z原子的核外电子数是其次外层电子数的2倍。下列说法正确的是
A.原子半径: B.元素 的含氧酸是强酸
C.该分子中 、 原子的杂化类型均为 D. 、 、 形成的化合物不会含有离子
键
【答案】C
【分析】短周期主族元素Z原子的核外电子数是其次外层电子数的2倍,可推知Z是S,
由平面形分子的结构可知X可形成4个共价键,Y可以形成3个共价键,且仅X、Y位于
同一周期,可知X为C,Y为N,又因W、X、Y、Z为原子序数依次增大,且属于另一个
周期,所以W为H。
【详解】A.根据原子在元素周期表中的位置可知,原子半径: ,即 ,故
A错误;
B.元素 是S,它有多种含氧酸,只有最高价含氧酸是强酸,故B错误;
C.由结构图和平面形分子可知 、 原子的杂化类型均为 ,故C正确;
D. 、 、 可形成的化合物可以是硫酸铵或硫酸氢铵,是铵盐,会含有离子键,故D
错误;
故答案为:C。
10.(2023·重庆·重庆南开中学校考三模)白铜是一种延展性好、硬度高、色泽美观、耐
腐蚀的合金材料,其主要成分为Cu、Ni、Zn,还含有少量S、P、As等元素。关于上述涉
及到的元素,下列说法正确的是
A.基态Ni原子的简化电子排布式为:
B.基态As原子最高能级的轨道形状为哑铃形
C.第一电离能:S>P>Cu
D.S、P为p区元素,Cu、Zn为d区元素
【答案】B【详解】A.基态Ni原子的简化电子排布式为:[Ar] ,故A错误;
B.基态As原子最高能级为4p,其轨道为哑铃形,故B正确;
C.第一电离能:P>S>Cu,故C错误;
D.S、P为p区元素,Cu、Zn为ds区元素,故D错误;
故答案选:B。
【点睛】本题考查了原子结构与元素性质,明确基态原子核外电子排布规律、熟悉同周期
元素性质递变规律是解题关键,题目难度不大。
11.(2023·湖北荆州·统考模拟预测)某化合物A除在有机合成中有广泛的应用外,还可
用作聚合引发剂、煤油抗氧化剂、杀菌剂、抗癌药和脑肿瘤的中子俘获疗法,其结构如图
所示,W、X、Y、Z、N均为短周期主族元素,原子半径为Y>Z>N>W,X、Y基态电子排
布中未成对电子数相同,下列说法不正确的是
A.最简单氢化物水溶液的pH:Z>Y>W B.第一电离能W>Y>N
C.该结构中所有原子均满足8电子稳定结构D.X元素的最高价态为+4
【答案】A
【分析】W、X、Y、Z、N均为短周期主族元素,原子半径为Y>Z>N>W,由化合物A的
结构可知,化合物中W、X、Y、Z、N形成的共价键数目分别为4、4、2、1、4,X、Y基
态电子排布中未成对电子数相同,则W为N元素、X为C元素、Y为S元素、Z为Cl元素、
N为B元素。
【详解】A.氨气的水溶液氨水呈碱性,溶液pH大于7,而硫化氢和氯化氢的水溶液均呈
酸性,溶液pH均小于7,则氨水的pH最大,故A错误;
B.同周期元素,从左到右第一电离能呈增大趋势,磷原子的3p轨道为稳定的半充满结构,
元素的第一电离能大于相邻元素,则磷元素的第一电离能大于硫元素,同主族元素,从上
到下第一电离能依次增大,则氮元素的第一电离能大于磷元素,硫元素的第一电离能大于
硼元素,则三种元素的第一电离能大小顺序为N>S>B,故B正确;
C.由化合物A的结构可知,化合物中N、C、S、Cl、B均满足8电子稳定结构,故C正
确;
D.碳元素原子序数为6,最高正化合价为+4价,故D正确;
故选A。12.(2023·辽宁朝阳·朝阳市第一高级中学校联考二模)第二周期主族元素X、Y,基态原
子均有两个未成对电子,可形成化学式为 ,且分子中每个原子均满足8电子稳定结构。
下列叙述错误的是
A. 的结构式为
B.X与Y的氢化物的熔、沸点一定是前者低于后者
C. 分子中所有原子都在一条直线上
D. 分子很活泼,能与 、HCl等发生加成反应
【答案】B
【分析】第二周期主族元素中,基态原子均有两个未成对电子的元素为C元素 ;
O元素 ,根据形成化合物每个原子均满足8电子,其原子的排列为
则X为C、Y为O,以此作答。
【详解】A.根据形成化合物每个原子均满足8电子,其原子的排列为 ,
A正确;
B.X为C元素其氢化物有简单的 ,也有其他的烃,可以有气态、液态和固态,不一
定比Y的氢化物 或 的沸点低,B错误;
C.中心的三个碳原子都是sp杂化,键角都是 ,因此每个原子均在一条直线上,C正
确;
D.结构中含有-C=C=C-,易与 加成反应生成酰胺,D正确;
故选B。
13.(2023·天津河西·天津市新华中学校考模拟预测)一种对中枢神经有抑制作用的药物
结构如图。其中W、X、Y、Z原子序数依次增大,X、Y、Z位于第二周期,Y的气态氢
化物的水溶性显碱性。
下列判断不正确的是
A.第一电离能:XB>O>F,故C
错误;
D.Be最高价氧化物水化物为Be(OH) ,溶液显两性,B最高价氧化物的水化物为HBO,
2 3 3
溶液显酸性,故D错误;
故选:A。
19.(2022·河北·高考真题)两种化合物的结构如图,其中X、Y、Z、R、Q是原子序数依
次增大的五种短周期主族元素,下列说法错误的是A.在两种化合物中,X、Y、Z、R、Q均满足最外层8电子稳定结构
B.X、Y、Z、R、Q中,R的非金属性及简单氢化物的稳定性均最强
C.将装有YZ 气体的透明密闭容器浸入冰水中,气体颜色变浅
2
D.Z的某种同素异形体在大气中的含量与环境污染密切相关
【答案】A
【分析】X、Y、Z、R、Q是原子序数依次增大的五种短周期主族元素,由两种化合物的
结构示意图可知,X、Y、Z、R、Q形成共价键的数目分别为4、3、2、1、5,则五种元素
分别为C元素、N元素、O元素、F元素、P元素。
【详解】A.由两种化合物的结构示意图可知,化合物中磷原子的最外层电子数为10,不
满足最外层8电子稳定结构,故A错误;
B.C元素、N元素、O元素、F元素、P元素中位于元素周期表右上角的氟元素的非金属
性最强,元素的非金属性越强,简单氢化物的稳定性最强,故B正确;
C.红棕色二氧化氮转化为无色四氧化二氮的反应为放热反应,降低温度,平衡向正反应
方向移动,气体的颜色变浅,则将装有二氧化氮气体的透明密闭容器浸入冰水中,气体颜
色变浅,故C正确;
D.氧气和臭氧是氧元素形成的不同种单质,互为同素异形体,臭氧层破坏会造成环境污
染,则臭氧在大气中的含量与环境污染密切相关,故D正确;
故选A。
20.(2022·海南·统考高考真题)短周期主族元素X、Y、Z、W的原子序数依次增大,
X、Y同周期并相邻,Y是组成水的元素之一,Z在同周期主族元素中金属性最强,W原子
在同周期主族元素中原子半径最小,下列判断正确的是
A. 是非极性分子
B.简单氢化物沸点:
C.Y与Z形成的化合物是离子化合物
D.X、Y、Z三种元素组成的化合物水溶液呈酸性
【答案】C
【分析】X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y同周期并相邻,且
Y是组成水的元素之一,则Y为O元素,X为N元素,Z在同周期主族元素中金属性最强,
则Z为Na元素,W原子在同周期主族元素中原子半径最小,则W为Cl元素,据此分析解
答。
【详解】A.由分析,X为N元素,W为Cl元素,NCl 分子的空间构型为三角锥形,其正
3
负电荷的中心不重合,属于极性分子,A错误;B.HO和NH 均含有氢键,但HO分子形成的氢键更多,故沸点HO>NH ,B错误;
2 3 2 2 3
C.Y为O元素,Z为Na元素,两者形成的化合物为NaO、NaO 均为离子化合物,C正
2 2 2
确;
D.N、O、Na三种元素组成的化合物NaNO 呈中性、NaNO 呈碱性,D错误;
3 2
答案选C。
21.(2022·浙江·统考高考真题)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增
大。X的核外电子数等于其周期数, 分子呈三角锥形,Z的核外电子数等于X、Y核
外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
A.X与Z形成的10电子微粒有2种
B.Z与Q形成的一种化合物可用于饮用水的消毒
C. 与 的晶体类型不同
D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
【答案】B
【分析】X的核外电子数等于其周期数,X为H,YX 分子呈三角锥形,Y为N,Z的核外
3
电子数等于X、Y核外电子数之和,则Z为O,M与X同主族,则M为Na,Q是同周期中
非金属性最强的元素,则Q为Cl,综合分析,X为H,Y为N,Z为O,M为Na,Q为
Cl,以此解题。
【详解】A.由分析可知X为H,Z为O,则其形成的10电子微粒有HO、OH-、HO+,A
2 3
错误;
B.由分析可知Z为O,Q为Cl,可形成ClO ,有氧化性,可用于自来水消毒,B正确;
2
C.由分析可知Z为O,M为Na,Q为Cl,则MZ为NaO,为离子晶体,MQ为NaCl,
2 2
为离子晶体,晶体类型相同,C错误;
D.由分析可知X为H,Y为N,Z为O,这三种元素可以形成NH₃·H₂O,其溶液显碱性,
D错误;
故选B。
22.(2022·广东·高考真题)甲~戊均为短周期元素,在元素周期表中的相对位置如图所
示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是
甲 乙
丙 丁 戊
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
【答案】C【分析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或
高氯酸,若是高氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊为
S,甲为C、乙为O、丙为Si、丁为P。
【详解】A.根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故
A正确;
B.根据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;
C.甲的氢化物可能为氨气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产
生;若是甲烷、乙烷等,则遇氯化氢不反应,没有白烟生成,故C错误;
D.丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强碱反应,
故D正确。
综上所述,答案为C。
23.(2022·湖南·高考真题)科学家合成了一种新的共价化合物(结构如图所示),X、Y、
Z、W为原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下
列说法错误的是
A.原子半径: B.非金属性:
C.Z的单质具有较强的还原性 D.原子序数为82的元素与W位于同一主族
【答案】C
【分析】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1
个共价键,X、Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y
的原子序数之和,则X为C元素、Y为O元素、Z为F元素、W为Si元素。
【详解】A.同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大小顺序
为C>O>F,故A正确;
B.同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元素的非金
属性依次减弱,则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;
C.位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;
D.原子序数为82的元素为铅元素,与硅元素都位于元素周期表ⅣA族,故D正确;
故选C。
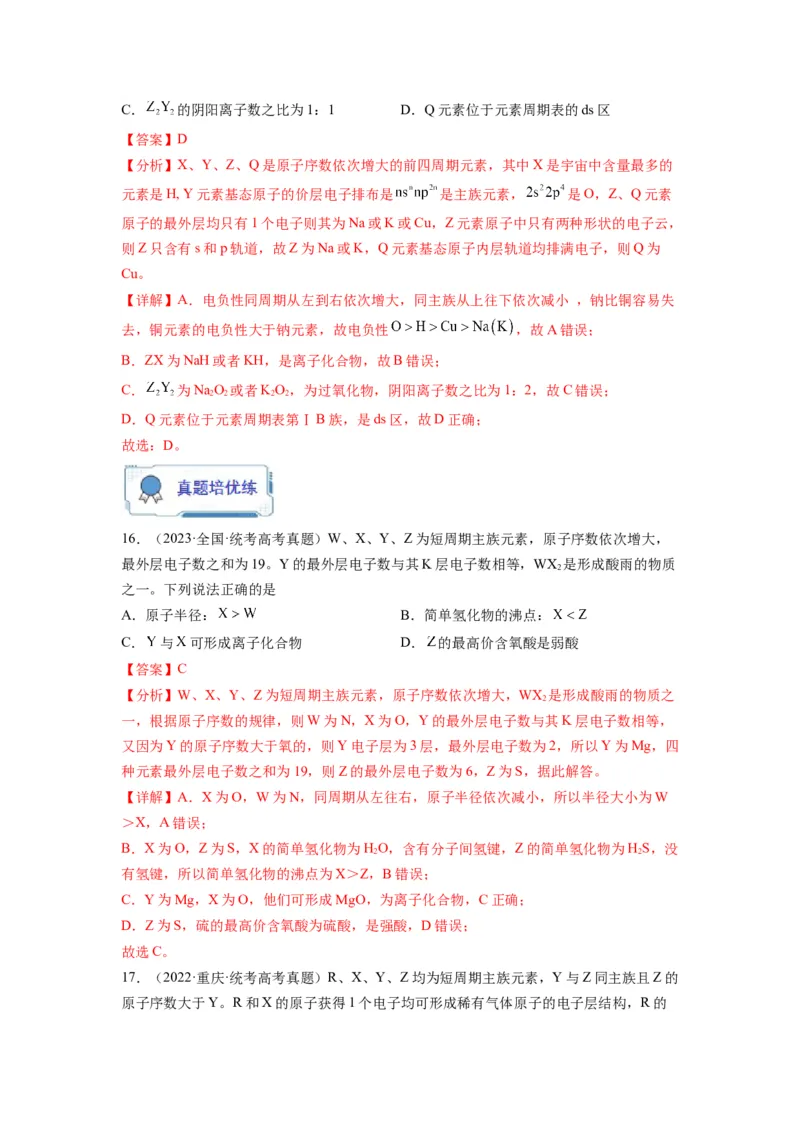
24.(2022·全国·统考高考真题)化合物 可用于电讯器材、高级玻璃的
制造。W、X、Y、Z为短周期元素,原子序数依次增加,且加和为21。 分子的总电子
数为奇数,常温下为气体。该化合物的热重曲线如图所示,在 以下热分解时无刺激
性气体逸出。下列叙述正确的是A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物的酸性:
C. 阶段热分解失去4个
D. 热分解后生成固体化合物
【答案】D
【分析】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周
4 5 8 2
期元素,原子序数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下
热分解时无刺激性气体逸出,则说明失去的是水,即W为H,Z为O,YZ 分子的总电子
2
数为奇数,常温下为气体,则Y为N,原子序数依次增加,且加和为21,则X为B。
【详解】A.X(B)的单质常温下为固体,故A错误;
B.根据非金属性越强,其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸
性:X(H BO)<Y(HNO ),故B错误;
3 3 3
C.根据前面已知200℃以下热分解时无刺激性气体逸出,则说明失去的是水,若100~
200℃阶段热分解失去4个HO,则质量分数 ,
2
则说明不是失去4个HO,故C错误;
2
D.化合物(NH B O·4H O)在500℃热分解后若生成固体化合物XZ(B O),根据硼元素守
4 5 8 2 2 3 2 3
恒,则得到关系式2NH B O·4H O~5B O,则固体化合物B O 质量分数为
4 5 8 2 2 3 2 3
,说明假设正确,故D正确。
综上所述,答案为D。
25.(2023·辽宁·统考高考真题)某种镁盐具有良好的电化学性能,其阴离子结构如下图
所示。W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W、Y原子序数之和等于
Z,Y原子价电子数是Q原子价电子数的2倍。下列说法错误的是A.W与X的化合物为极性分子 B.第一电离能
C.Q的氧化物是两性氧化物 D.该阴离子中含有配位键
【答案】AB
【分析】W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W形成1条单键且核电荷
数最小,W为H,X形成4条键,核电荷数大于H,且小于其他三种元素,X为C,Y形成
2条单键,核电荷数大于C,Y为O,W、Y原子序数之和等于Z,Z为F,Y原子价电子
数为Q原子价电子数的2倍,Q为Al。
【详解】A.W与X的化合物不一定为极性分子,如CH 就是非极性分子,A错误;
4
B.同周期元素从左到右第一电离能呈增大趋势,则第一电离能F>O>C,B错误;
C.Q为Al,Al O 为两性氧化物,C正确;
2 3
D.该阴离子中L与Q之间形成配位键,D正确;
故答案选AB。