文档内容
专题 03 铁 金属材料
第 08 练 金属材料
1.下列物质中,属于纯净物的是 ( )
A.明矾 B.生铁 C.不锈钢 D.赤铁矿
2.某种钢铁材料含碳为2.4%,这种材料是( )
A.生铁 B.特种钢 C.碳素钢 D.高碳钢
3.不能由单质直接化合制得的是( )
A.NaCl B.AlCl C.FeCl D.CuCl
3 2 2
4.常温下,将铝片投入浓HSO 中,下列说法正确的是( )
2 4
A.铝被钝化 B.不发生反应 C.产生大量SO D.产生大量H
2 2
5.金属一般具有的特点是( )
A.有金属光泽,能导电,有延展性 B.熔点和沸点较低
C.能在空气中稳定存在, 不易被氧化 D.在反应中作氧化剂
6.合金在生产和生活中具有广泛的应用,下列用品中所用的材料不属于合金的是( )
A.铁锅 (生铁) B.刀具(不锈钢) C.体温计(水银) D.高压锅(硬铝)
7.下列说法不正确的是( )
A. 不锈钢是含铁、铬、镍的合金 B. 合金中可能含有非金属元素
C. 合金一定只含有两种元素 D. 合金的熔点一般比各组分金属的低
8.下列有关金属冶炼方法的叙述,不正确的是( )
A.湿法炼铜的原理属于置换反应
B.1 000年前中国就能炼锌,现代炼锌主要利用热还原法
C.铝热法应用很普遍,可冶炼Mn、Mg、W等金属
D.钠、镁、铝等活泼金属的冶炼采用电解法
9.在Mg、Al、Cu、Fe四种元素中,每种元素都有某些方面不同于其他三种元素。若从中选出铁元素,
则选择的理由正确的是( )
A.在冷的浓硫酸、浓硝酸中发生钝化
B.在不同化合物中能显示不同的化合价
C.能与盐酸反应产生氢气,不能与氢氧化钠溶液反应产生氢气
D.能被磁铁吸引10.铝是地壳中含量最高的金属元素,下列关于铝及其化合物的说法错误的是( )
A.可用NaOH溶液除去Fe O 粉末中少量的Al O
2 3 2 3
B.纯铝的硬度和强度较小,不适合用于制造机器零件
C.铝制品廉价易得,适用于厨房蒸煮和长期存放碱性食物
D.铝在冷的浓硝酸中发生钝化,因此可用铝槽车运输浓硝酸
11.下列离子方程式书写正确的是( )
A.向FeI 溶液中滴加少量新制氯水:2Fe2++Cl=2Fe3++2Cl-
2 2
B.向CuCl 溶液中加入少量钠:2Na+Cu2+=Cu+2Na+
2
C.向NaOH溶液中加入足量的铝粉:2Al+6OH-=2AlO -+3H ↑
2 2
D.Fe O 溶于稀硫酸中:Fe O+6H+=2Fe3++3H O
2 3 2 3 2
12.合金是一类用途广泛的金属材料,下列关于合金的说法不正确的是( )
A.人类历史上使用最早的合金是青铜
B.目前世界上用途最广泛的合金是钢
C.合金是两种金属熔合而成的具有金属特性的物质
D.合金的熔点比它的各成分金属的熔点都低
13.下列物质的性质与用途具有对应关系的是( )
A.Al O 的两性,铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物
2 3
B.NaHCO 受热易分解,可用NaHCO 治疗胃酸过多
3 3
C.Fe O 是碱性氧化物,Fe O 可作红色油漆和涂料
2 3 2 3
D.抗坏血酸(维生素 )具有氧化性,可用作水果罐头中的抗氧化剂
14.下列说法正确的是
A.Al O 难溶于水,不跟水反应,所以它不是Al(OH) 对应的氧化物
2 3 3
B.因为Al O 是金属氧化物,所以它是碱性氧化物
2 3
C.Al O 能跟所有的酸、碱溶液反应
2 3
D.Al O 和NaO按物质的量之比1:1投入水中可得到澄清溶液
2 3 2
1.1825年丹麦化学家用无水AlCl 与钾作用第一次获得金属铝,当时由于价格非常昂贵,被称为“银
3
色的金子”。直到19世纪后期发明了电解法生产铝,才使铝的价格大大下降,使铝成为当今广泛应用的一
种金属材料。下列关于铝的叙述正确的是( )
A.铝是地壳中含量最多的元素B.常温下,铝不能与浓硫酸反应
C.铝是一种比较活泼的金属,在冶金工业中常作还原剂
D.铝锅不易生锈,所以可以用来蒸煮或长时间存放酸性、碱性食物
2.等量的金属铝与足量的盐酸和氢氧化钠反应,生成的气体( )
A.与酸反应放出的多 B.与碱反应放出的多 C.无法判断 D.一样多
3.铝制品不易被腐蚀,其主要原因是因为铝( )
A.化学性质不活泼 B.熔点高 C.表面有致密氧化膜 D.密度小
4.不锈钢通常不与酸、碱、盐反应,是因为加入了( )
A.Ni和Cr B.Ni和Au C.Cr和Au D.Cr和Pt
5.下列有关铝及其氧化物与强碱溶液反应的说法中,正确的是( )
A.都有氢气生成 B.都生成盐和HO
2
C.反应后铝元素主要以AlO形式存在 D.反应后铝元素主要以Al3+的形式存在
6.下面关于铝合金的说法中,错误的是( )
A.铝合金是一种混合物,它比纯铝的熔点低
B.高温铝液易被氧化,铝合金应在熔剂层覆盖下熔炼
C.镁铝合金耐腐蚀,但能被烧碱腐蚀
D.镁铝合金在冷的浓硫酸中不反应
7.铝是重要的金属材料之一,下列关于铝的叙述中,不正确的是( )
A.铝原子最外层有3个电子 B.铝是地壳中含量最多的金属元素
C.在常温下,铝不能与氧气反应 D.铝易被氧化,而Al3+则很难被还原
8.类推是化学学习和研究常用的重要思维方法,但所得结论要经过实践的检验才能确定其正确与否。
根据你所掌握的知识,判断下列类推结论中正确的是( )
A.Mg燃烧不能用Mg灭火,故 燃烧也不能用CO 灭火
2
B.Al在O 中燃烧生成Al O,故Fe在O 中燃烧生成Fe O
2 2 3 2 2 3
C.CO 与NaO 反应生成NaCO 和O,故SO 与NaO 反应生成NaSO 和O
2 2 2 2 3 2 2 2 2 2 3 2
D.Al与NaOH溶液反应生成H,故Mg与NaOH溶液反应也生成H
2 2
9.下列说法正确的是( )
A.金属钠着火,可以用干粉灭火器灭火
B.铁主要以 价和 价化合物的形态存在于矿石之中,游离态的铁单质存在于陨铁中
C.铝制餐具可以用来长时间存放酸性或碱性食物
D.储氢合金指的是能够用物理吸附的方法吸收氢气的合金,如镧镍合金等
10.下列关于铝单质的叙述中,正确的是( )A.铝制品在空气中有很强的抗腐蚀性是因为铝的化学性质很稳定
B.不能用铝制的器皿来盛放酸梅汤或碱水是因为铝会和酸或碱反应
C.铝和NaOH溶液反应:2Al+OH-+2H O=2AlO-+3H ↑
2 2 2
D.用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝会滴落下来,是
因为金属铝的熔点较低
11.化学与材料、生活和环境密切相关。下列有关说法中正确的是( )
A.日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应
B.水泥厂用高压电作用于气溶胶以除去烟尘,是根据胶体带电这个性质而设计的
C.食品包装袋里面装有硅胶和铁粉,硅胶和铁粉的作用相同,都可以防止食品氧化
D.高速铁路极大地提高了人们出行的方便,高铁车厢大部分是采用铝合金材料制造的
12.下列对金属及其化合物叙述正确的是( )
A.Na与NaO 投入水中都可生成氢气
2 2
B.Al与Al O 都可溶于NaOH溶液,它们都是两性物质
2 3
C.NaO与Al O 都可溶于水,形成对应的碱NaOH和Al(OH)
2 2 3 3
D.Al(OH) 与Fe(OH) 都可以在加热条件下生成对应的氧化物Al O 和Fe O
3 3 2 3 2 3
13.下列有关金属的描述不正确的是( )
A.金属都有金属光泽,能导电、导热,有延展性
B.含金属元素的离子不一定都是阳离子
C.许多金属或它们的化合物都能发生焰色反应,这种化学变化可用于验证金属元素的存在
D.铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物
14.中国航空铝材处于世界领先行列,下列关于铝合金的说法不正确的是( )
A.铝合金是一种混合物,它比纯铝的熔点低
B.镁铝合金耐腐蚀,但能被烧碱溶液腐蚀
C.高温铝液易被氧化,铝合金应在熔剂层覆盖下熔炼
D.镁铝合金在盐酸中无法溶解
15.在FeCl 、CuCl 混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,下列说法中正确的是(
3 2
)
A.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+
B.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,可能含Cu2+和Fe3+
C.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe3+和Fe2+,一定不含Cu2+
D.若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+和Fe3+
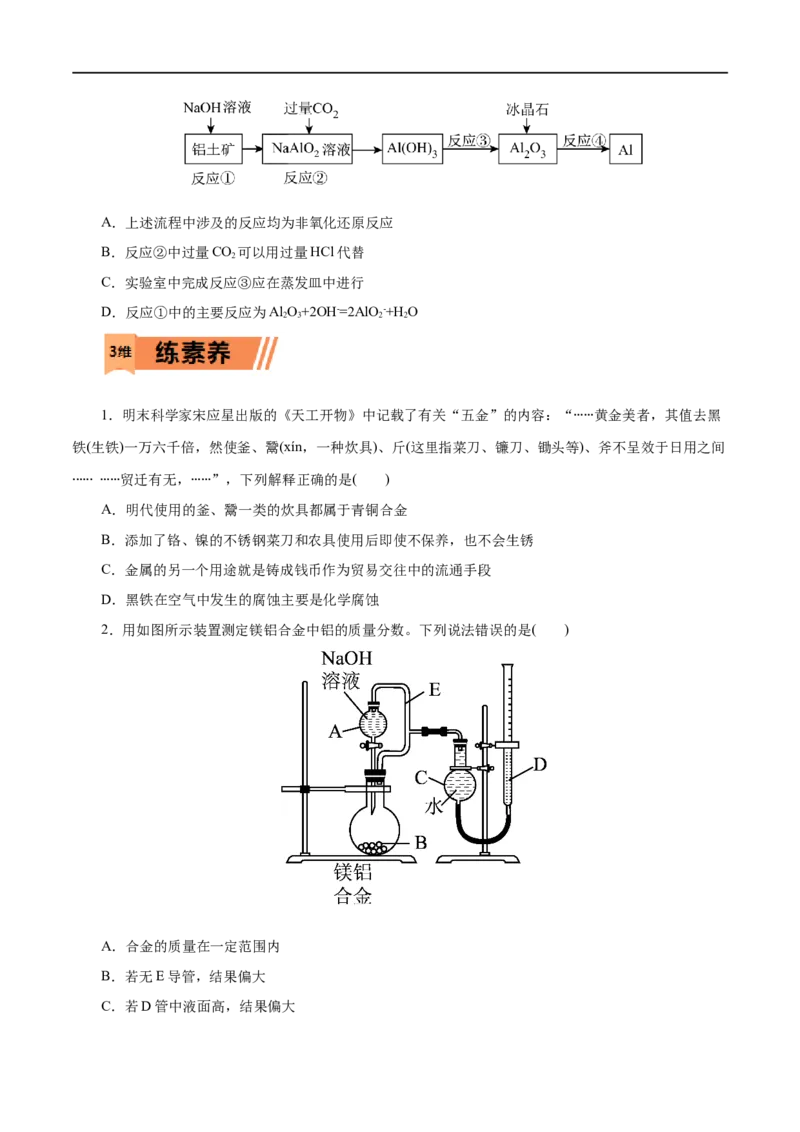
16.从铝土矿中提取铝的工艺流程如图所示,下列说法正确的是( )A.上述流程中涉及的反应均为非氧化还原反应
B.反应②中过量CO 可以用过量HCl代替
2
C.实验室中完成反应③应在蒸发皿中进行
D.反应①中的主要反应为Al O+2OH-=2AlO -+H O
2 3 2 2
1.明末科学家宋应星出版的《天工开物》中记载了有关“五金”的内容:“∙∙∙∙∙∙黄金美者,其值去黑
铁(生铁)一万六千倍,然使釜、鬵(xín,一种炊具)、斤(这里指菜刀、镰刀、锄头等)、斧不呈效于日用之间
∙∙∙∙∙∙ ∙∙∙∙∙∙贸迁有无,∙∙∙∙∙∙”,下列解释正确的是( )
A.明代使用的釜、鬵一类的炊具都属于青铜合金
B.添加了铬、镍的不锈钢菜刀和农具使用后即使不保养,也不会生锈
C.金属的另一个用途就是铸成钱币作为贸易交往中的流通手段
D.黑铁在空气中发生的腐蚀主要是化学腐蚀
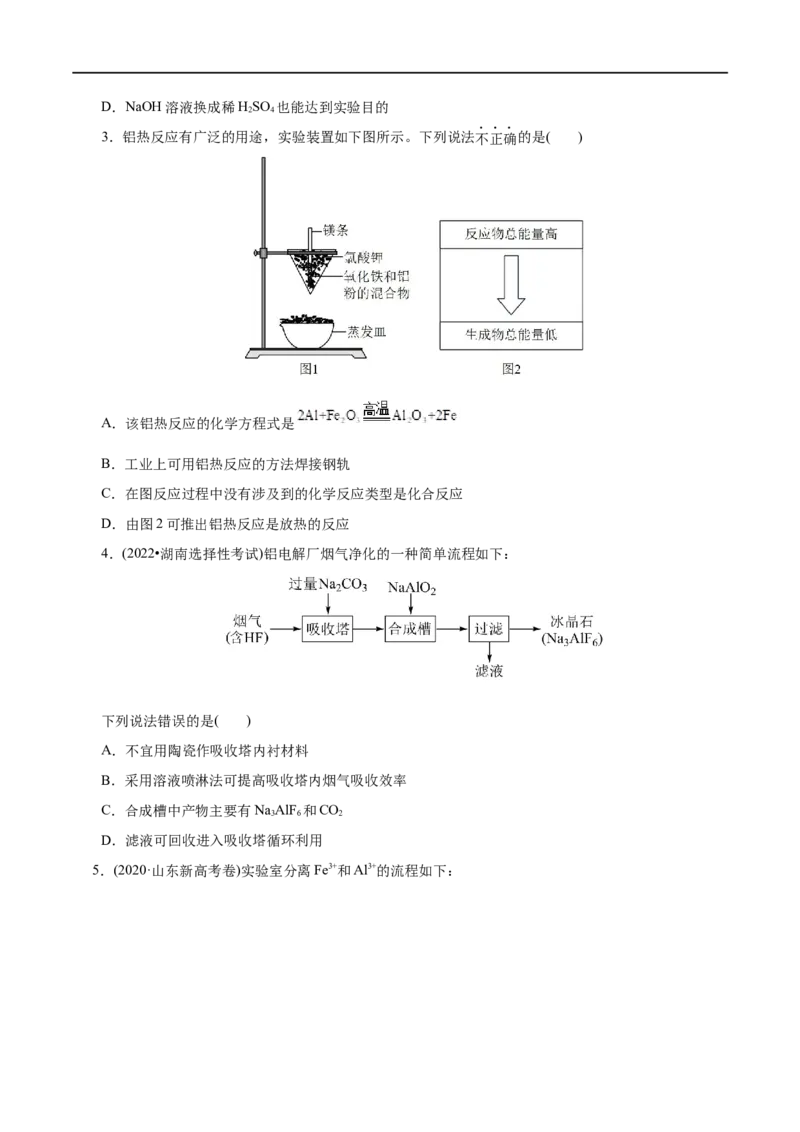
2.用如图所示装置测定镁铝合金中铝的质量分数。下列说法错误的是( )
A.合金的质量在一定范围内
B.若无E导管,结果偏大
C.若D管中液面高,结果偏大D.NaOH溶液换成稀HSO 也能达到实验目的
2 4
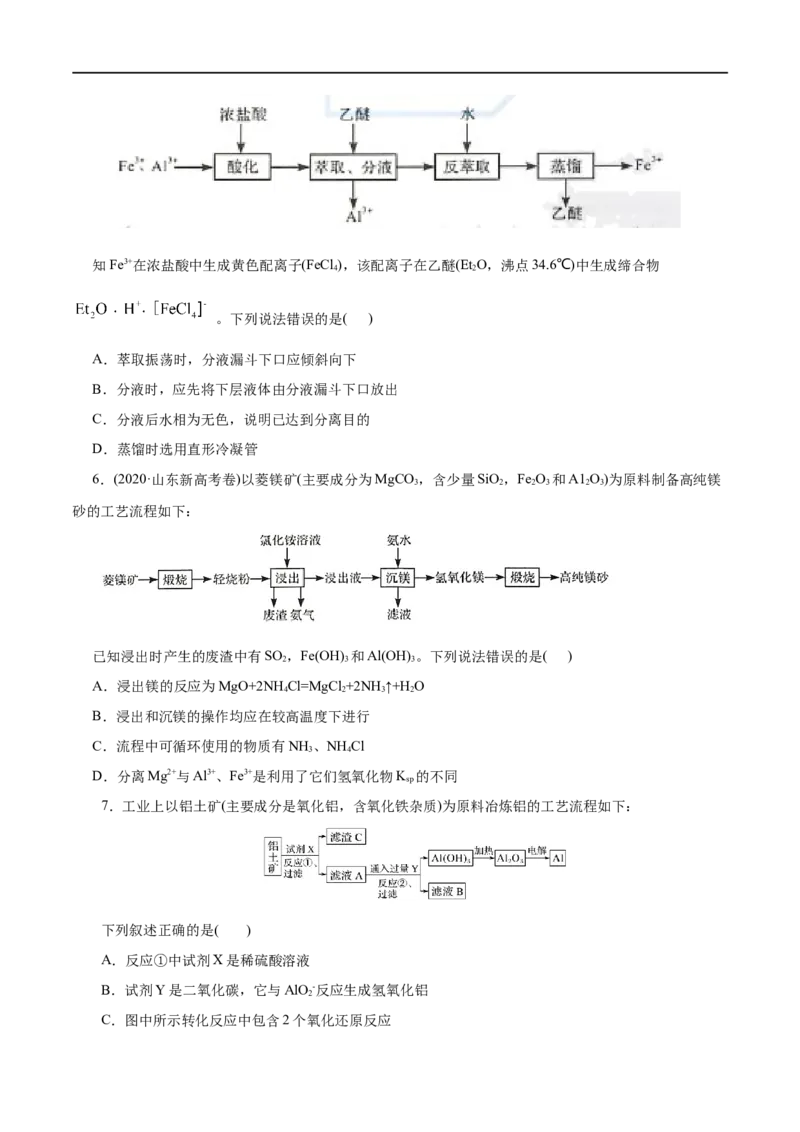
3.铝热反应有广泛的用途,实验装置如下图所示。下列说法不正确的是( )
A.该铝热反应的化学方程式是
B.工业上可用铝热反应的方法焊接钢轨
C.在图反应过程中没有涉及到的化学反应类型是化合反应
D.由图2可推出铝热反应是放热的反应
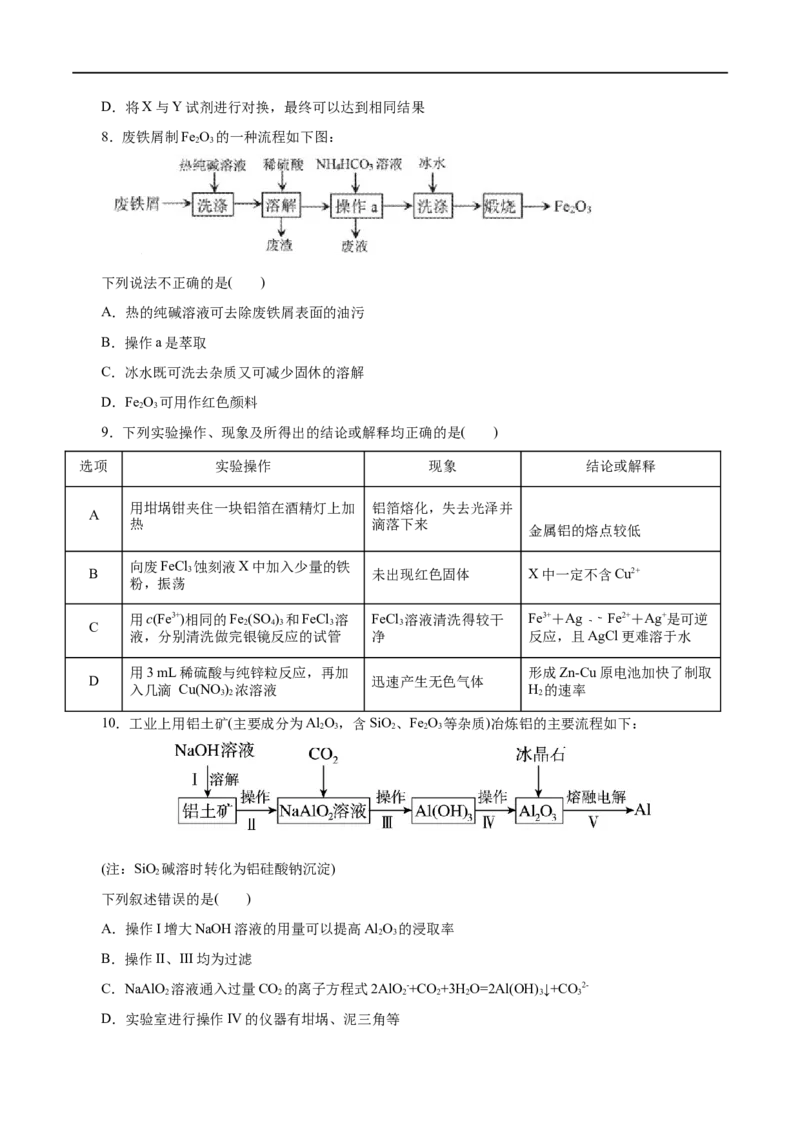
4.(2022•湖南选择性考试)铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是( )
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有NaAlF 和CO
3 6 2
D.滤液可回收进入吸收塔循环利用
5.(2020·山东新高考卷)实验室分离Fe3+和Al3+的流程如下:知Fe3+在浓盐酸中生成黄色配离子(FeCl ),该配离子在乙醚(Et O,沸点34.6℃)中生成缔合物
4 2
。下列说法错误的是( )
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
6.(2020·山东新高考卷)以菱镁矿(主要成分为MgCO ,含少量SiO,Fe O 和A1 O)为原料制备高纯镁
3 2 2 3 2 3
砂的工艺流程如下:
已知浸出时产生的废渣中有SO ,Fe(OH) 和Al(OH) 。下列说法错误的是( )
2 3 3
A.浸出镁的反应为MgO+2NH Cl=MgCl +2NH↑+H O
4 2 3 2
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有NH 、NH Cl
3 4
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
7.工业上以铝土矿(主要成分是氧化铝,含氧化铁杂质)为原料冶炼铝的工艺流程如下:
下列叙述正确的是( )
A.反应①中试剂X是稀硫酸溶液
B.试剂Y是二氧化碳,它与AlO-反应生成氢氧化铝
2
C.图中所示转化反应中包含2个氧化还原反应D.将X与Y试剂进行对换,最终可以达到相同结果
8.废铁屑制Fe O 的一种流程如下图:
2 3
下列说法不正确的是( )
A.热的纯碱溶液可去除废铁屑表面的油污
B.操作a是萃取
C.冰水既可洗去杂质又可减少固休的溶解
D.Fe O 可用作红色颜料
2 3
9.下列实验操作、现象及所得出的结论或解释均正确的是( )
选项 实验操作 现象 结论或解释
用坩埚钳夹住一块铝箔在酒精灯上加 铝箔熔化,失去光泽并
A
热 滴落下来
金属铝的熔点较低
向废FeCl 蚀刻液X中加入少量的铁
B 3 未出现红色固体 X中一定不含Cu2+
粉,振荡
用c(Fe3+)相同的Fe (SO ) 和FeCl 溶 FeCl 溶液清洗得较干 Fe3++Ag Fe2++Ag+是可逆
C 2 4 3 3 3
液,分别清洗做完银镜反应的试管 净 反应,且AgCl更难溶于水
用3 mL稀硫酸与纯锌粒反应,再加 形成Zn-Cu原电池加快了制取
D 迅速产生无色气体
入几滴 Cu(NO ) 浓溶液 H 的速率
3 2 2
10.工业上用铝土矿(主要成分为Al O,含SiO、Fe O 等杂质)冶炼铝的主要流程如下:
2 3 2 2 3
(注:SiO 碱溶时转化为铝硅酸钠沉淀)
2
下列叙述错误的是( )
A.操作I增大NaOH溶液的用量可以提高Al O 的浸取率
2 3
B.操作II、III均为过滤
C.NaAlO 溶液通入过量CO 的离子方程式2AlO-+CO +3H O=2Al(OH) ↓+CO 2-
2 2 2 2 2 3 3
D.实验室进行操作IV的仪器有坩埚、泥三角等