文档内容
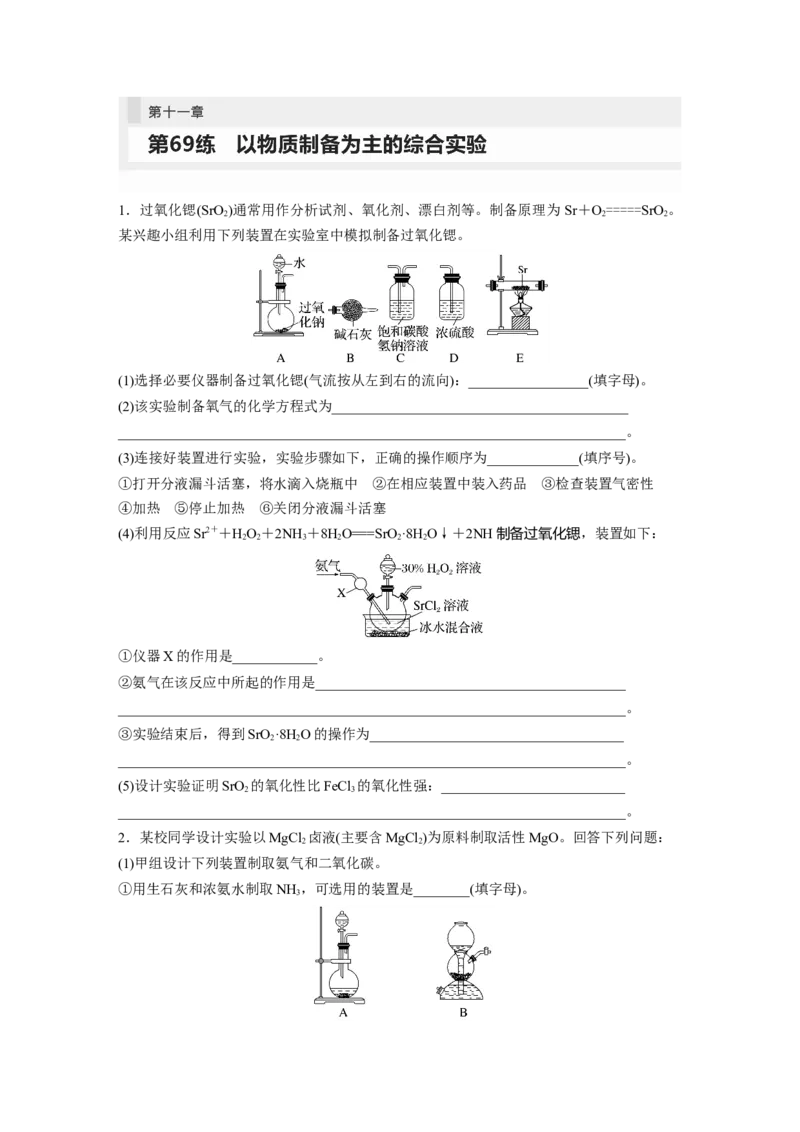
1.过氧化锶(SrO )通常用作分析试剂、氧化剂、漂白剂等。制备原理为 Sr+O=====SrO 。
2 2 2
某兴趣小组利用下列装置在实验室中模拟制备过氧化锶。
(1)选择必要仪器制备过氧化锶(气流按从左到右的流向):_________________(填字母)。
(2)该实验制备氧气的化学方程式为__________________________________________
________________________________________________________________________。
(3)连接好装置进行实验,实验步骤如下,正确的操作顺序为_____________(填序号)。
①打开分液漏斗活塞,将水滴入烧瓶中 ②在相应装置中装入药品 ③检查装置气密性
④加热 ⑤停止加热 ⑥关闭分液漏斗活塞
(4)利用反应Sr2++HO+2NH +8HO===SrO ·8H O↓+2NH制备过氧化锶,装置如下:
2 2 3 2 2 2
①仪器X的作用是____________。
②氨气在该反应中所起的作用是____________________________________________
________________________________________________________________________。
③实验结束后,得到SrO ·8H O的操作为____________________________________
2 2
________________________________________________________________________。
(5)设计实验证明SrO 的氧化性比FeCl 的氧化性强:__________________________
2 3
________________________________________________________________________。
2.某校同学设计实验以MgCl 卤液(主要含MgCl )为原料制取活性MgO。回答下列问题:
2 2
(1)甲组设计下列装置制取氨气和二氧化碳。
①用生石灰和浓氨水制取NH ,可选用的装置是________(填字母)。
3②若用石灰石和稀盐酸制取CO,反应的离子方程式为__________________________。
2
(2)乙组利用甲组制备的NH 和CO 制取3MgCO ·Mg(OH) ·3H O。
3 2 3 2 2
①接口b处通入的气体是________(填化学式)。
②装置D的作用是_______________________________________________________。
③生成3MgCO ·Mg(OH) ·3H O的化学方程式为______________________________
3 2 2
________________________________________________________________________。
(3)丙组灼烧3MgCO ·Mg(OH) ·3H O制活性MgO时,所需的硅酸盐质仪器除酒精灯和坩埚
3 2 2
外,还需要_____________________________________________________________。
3.实验室以2-丁醇(CHCHOHCH CH)为原料制备2-氯丁烷(CHCHClCH CH),实验装置
3 2 3 3 2 3
如图所示(夹持、加热装置已略去):
相关信息如表所示:
物质 熔点/℃ 沸点/℃ 密度/(g·cm-3) 其他
2-丁醇 -114.7 99.5 0.81 与水互溶
2-氯丁烷 -131.3 68.2 0.87 微溶于水,碱性水解
[实验步骤]
步骤1:在甲装置中的圆底烧瓶内加入无水ZnCl 和100 mL 12 mol·L-1浓盐酸,充分溶解、
2
冷却,再加入45.68 mL 2-丁醇,加热一段时间。
步骤2:将反应混合物移至乙装置的蒸馏烧瓶内,蒸馏并收集115 ℃以下的馏分。
步骤3:从馏分中分离出有机相,进行系列操作,放置一段时间后过滤。
步骤4:滤液经进一步精制得产品。
回答下列问题:
(1)Ⅰ中应放的仪器是________(填“A”或“B”,下同), Ⅱ中应放的仪器是____________。
(2)步骤1中加入的无水ZnCl 的作用是______________________________________
2
________________________________________________________________________。
(3)步骤3进行系列操作的顺序是____________(填序号,可重复使用)。
①10%Na CO 溶液洗涤 ②加入CaCl 固体 ③蒸馏水洗涤
2 3 2
用NaCO 溶液洗涤时操作要迅速,其原因是_________________________________。
2 3(4)步骤4进一步精制得产品所采用的操作方法是____________(填名称)。
(5)测定实验中生成2-氯丁烷的产率。将全部产品加入足量NaOH溶液中,加热,冷却后,
滴入硝酸溶液至溶液呈酸性,再滴入足量的硝酸银溶液,得到57.40 g沉淀,则2-氯丁烷的
产率是____________。
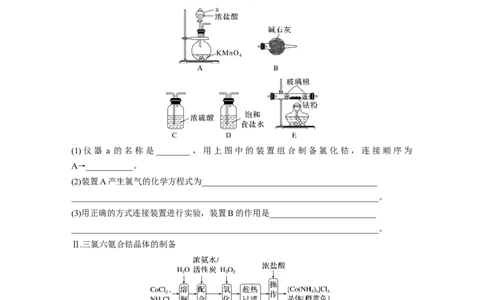
4.(2022·河南洛阳模拟)Cl(三氯六氨合钴)是一种重要的化工产品,常用于合成其他Co(Ⅱ)
3
配合物。以下是一种制备三氯六氨合钴的实验方法,回答下列问题:
Ⅰ.氯化钴的制备
已知氯化钴(CoCl )易潮解,Co(Ⅲ)的氧化性强于Cl ,可用高熔点金属钴与氯气反应制取。
2 2
实验室提供下列装置进行组合(连接用橡胶管省略):
(1)仪器 a 的名称是________,用上图中的装置组合制备氯化钴,连接顺序为
A→___________。
(2)装置A产生氯气的化学方程式为_________________________________________
________________________________________________________________________。
(3)用正确的方式连接装置进行实验,装置B的作用是_________________________
________________________________________________________________________。
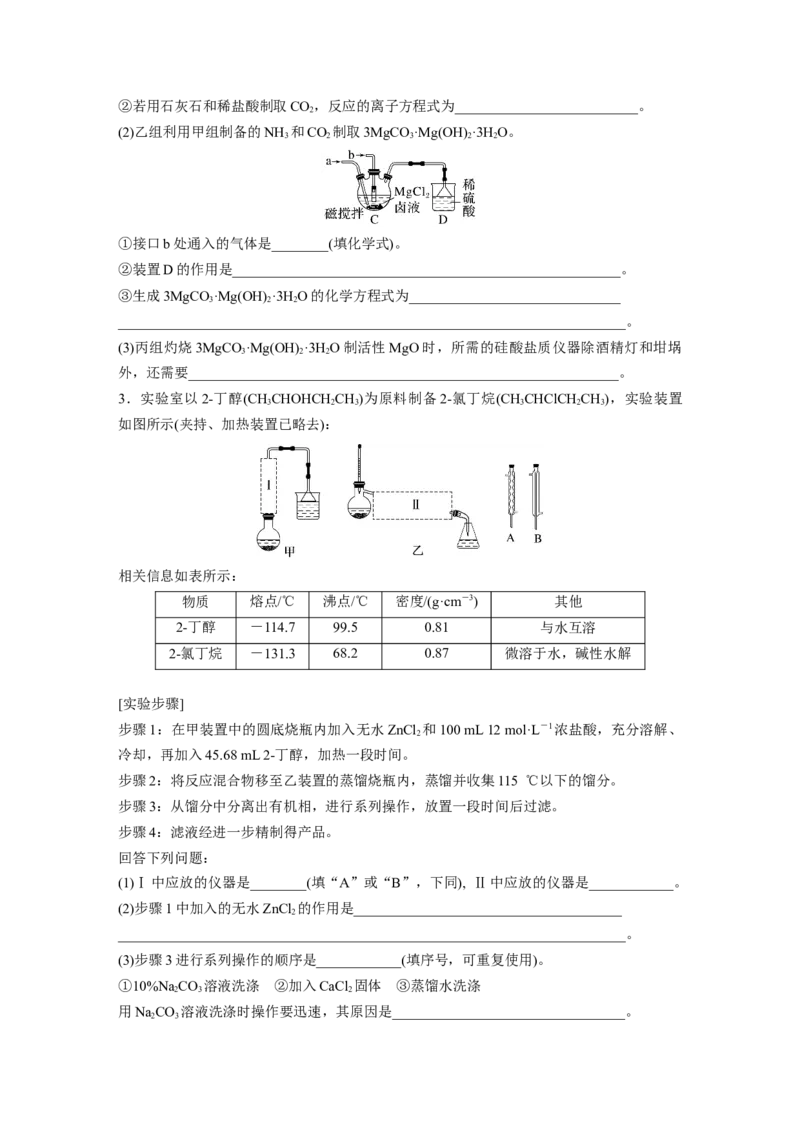
Ⅱ.三氯六氨合钴晶体的制备
(4)“氧化”的目的是______________________________________________________
________________________________________________________________________。
“操作X”包括冷却结晶、过滤,并依次用少量冷的稀盐酸和无水乙醇对晶体进行洗涤,用
无水乙醇洗涤的目的是____________________________________________________
________________________________________________________________________。
(5)制备Cl 总反应的化学方程式为
3________________________________________________________________________。
反应中活性炭的作用是________(填字母)。
a.脱色剂 b.氧化剂
c.还原剂 d.催化剂