文档内容
第 11 讲 硫及其化合物
【练基础】
1.下列有关硫元素及其化合物的说法或描述正确的是( )
A.硫黄矿制备硫酸经历两步:S――→SO ――→HSO
3 2 4
B.酸雨与土壤中的金属氧化物反应后,硫元素以单质的形式进入土壤中
C.在燃煤中加入石灰石可减少SO 排放,发生的反应为2CaCO +2SO +O=====2CO+2CaSO
2 3 2 2 2 4
D.土壤中的闪锌矿(ZnS)遇到硫酸铜溶液转化为铜蓝(CuS),说明CuS很稳定,不具有还原性
2.下列说法错误的是( )
A.残留在试管内壁上的硫可用CS 溶解除去,也可用热的NaOH溶液除去
2
B.硫单质与变价金属反应时一般生成低价态的金属硫化物
C.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理
D.单质硫或含硫物质燃烧时,氧气少量时生成SO ,氧气足量时生成SO
2 3
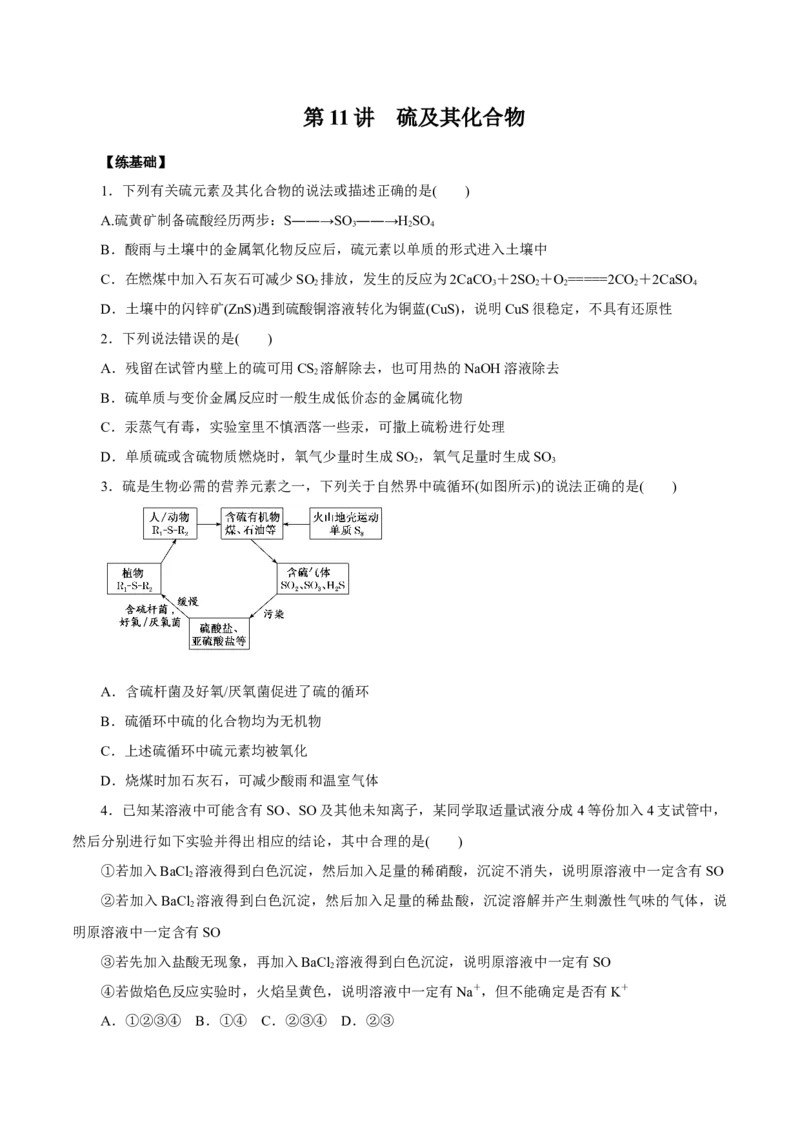
3.硫是生物必需的营养元素之一,下列关于自然界中硫循环(如图所示)的说法正确的是( )
A.含硫杆菌及好氧/厌氧菌促进了硫的循环
B.硫循环中硫的化合物均为无机物
C.上述硫循环中硫元素均被氧化
D.烧煤时加石灰石,可减少酸雨和温室气体
4.已知某溶液中可能含有SO、SO及其他未知离子,某同学取适量试液分成4等份加入4支试管中,
然后分别进行如下实验并得出相应的结论,其中合理的是( )
①若加入BaCl 溶液得到白色沉淀,然后加入足量的稀硝酸,沉淀不消失,说明原溶液中一定含有SO
2
②若加入BaCl 溶液得到白色沉淀,然后加入足量的稀盐酸,沉淀溶解并产生刺激性气味的气体,说
2
明原溶液中一定含有SO
③若先加入盐酸无现象,再加入BaCl 溶液得到白色沉淀,说明原溶液中一定有SO
2
④若做焰色反应实验时,火焰呈黄色,说明溶液中一定有Na+,但不能确定是否有K+
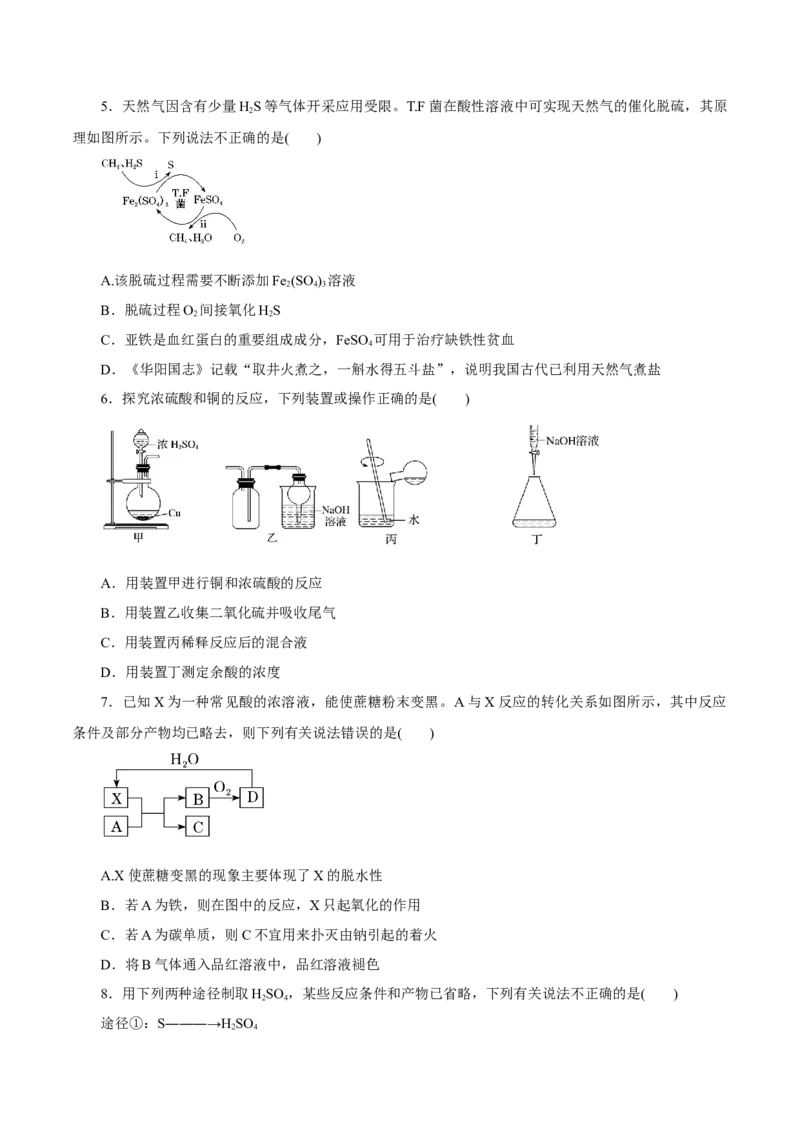
A.①②③④ B.①④ C.②③④ D.②③5.天然气因含有少量HS等气体开采应用受限。T.F菌在酸性溶液中可实现天然气的催化脱硫,其原
2
理如图所示。下列说法不正确的是( )
A.该脱硫过程需要不断添加Fe (SO ) 溶液
2 4 3
B.脱硫过程O 间接氧化HS
2 2
C.亚铁是血红蛋白的重要组成成分,FeSO 可用于治疗缺铁性贫血
4
D.《华阳国志》记载“取井火煮之,一斛水得五斗盐”,说明我国古代已利用天然气煮盐
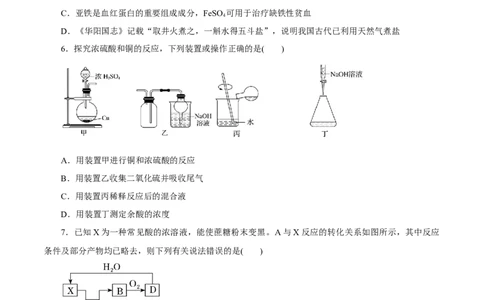
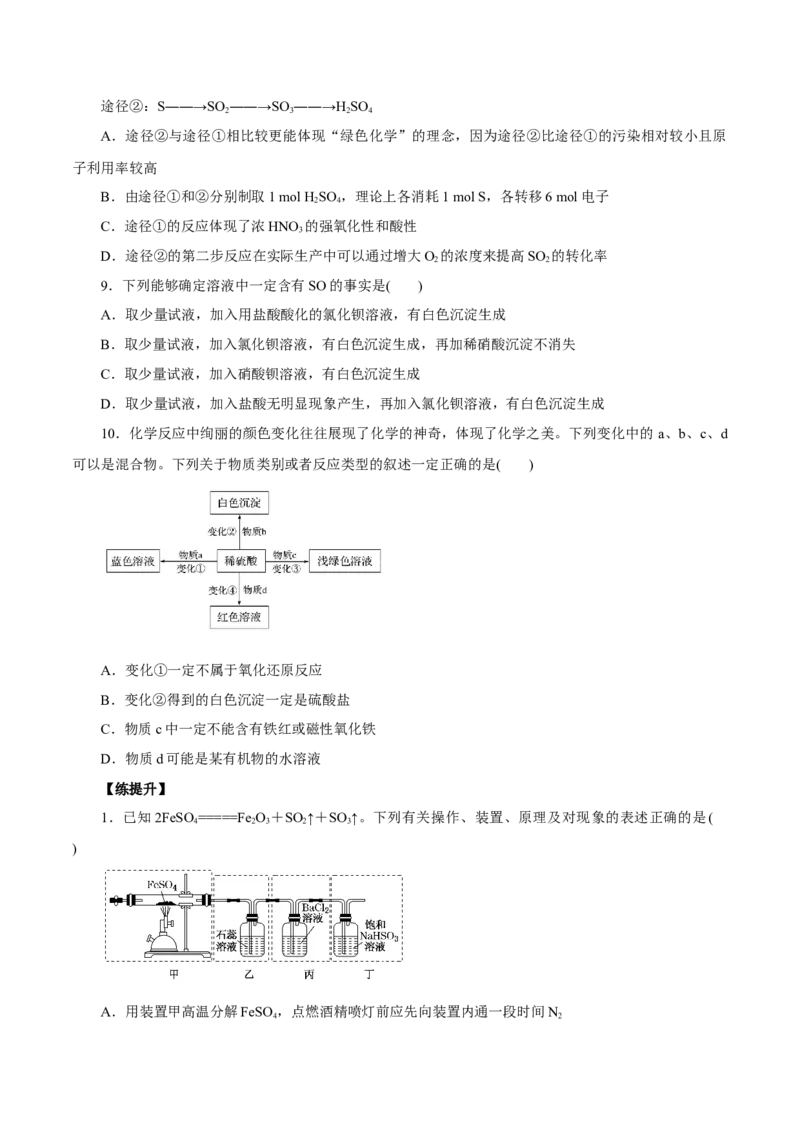
6.探究浓硫酸和铜的反应,下列装置或操作正确的是( )
A.用装置甲进行铜和浓硫酸的反应
B.用装置乙收集二氧化硫并吸收尾气
C.用装置丙稀释反应后的混合液
D.用装置丁测定余酸的浓度
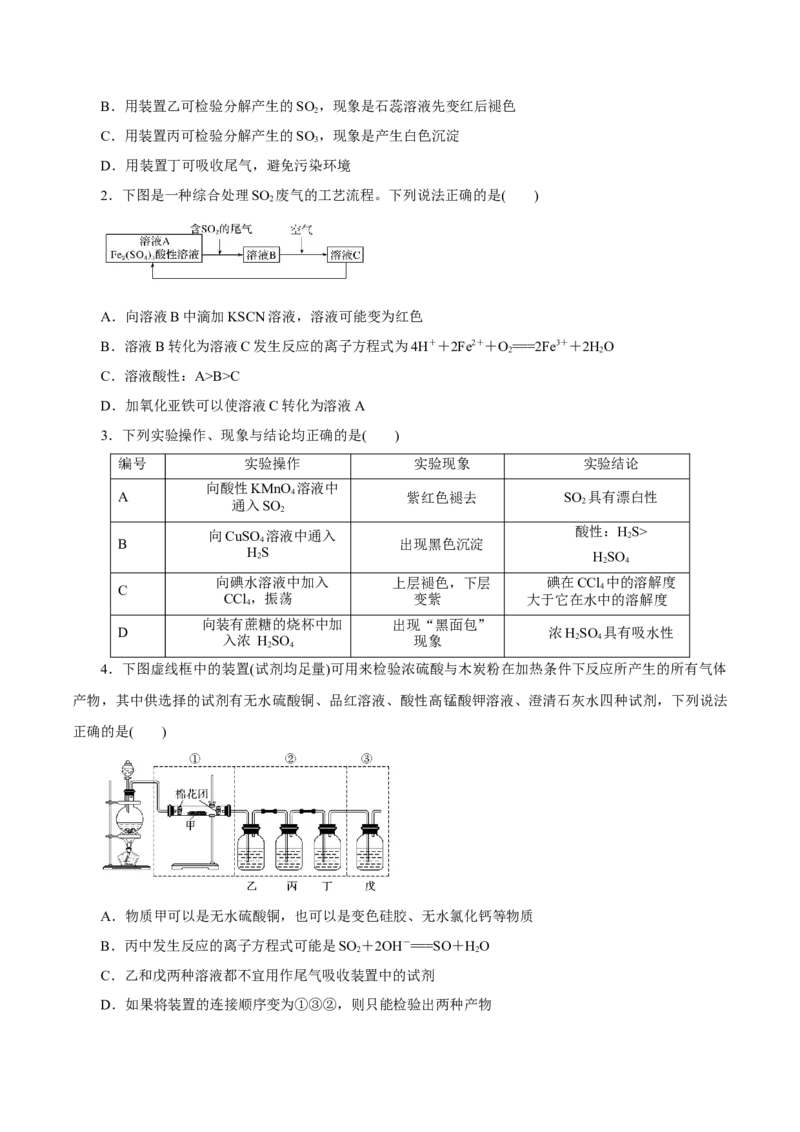
7.已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如图所示,其中反应
条件及部分产物均已略去,则下列有关说法错误的是( )
A.X使蔗糖变黑的现象主要体现了X的脱水性
B.若A为铁,则在图中的反应,X只起氧化的作用
C.若A为碳单质,则C不宜用来扑灭由钠引起的着火
D.将B气体通入品红溶液中,品红溶液褪色
8.用下列两种途径制取HSO ,某些反应条件和产物已省略,下列有关说法不正确的是( )
2 4
途径①:S―――→HSO
2 4途径②:S――→SO ――→SO ――→HSO
2 3 2 4
A.途径②与途径①相比较更能体现“绿色化学”的理念,因为途径②比途径①的污染相对较小且原
子利用率较高
B.由途径①和②分别制取1 mol H SO ,理论上各消耗1 mol S,各转移6 mol电子
2 4
C.途径①的反应体现了浓HNO 的强氧化性和酸性
3
D.途径②的第二步反应在实际生产中可以通过增大O 的浓度来提高SO 的转化率
2 2
9.下列能够确定溶液中一定含有SO的事实是( )
A.取少量试液,加入用盐酸酸化的氯化钡溶液,有白色沉淀生成
B.取少量试液,加入氯化钡溶液,有白色沉淀生成,再加稀硝酸沉淀不消失
C.取少量试液,加入硝酸钡溶液,有白色沉淀生成
D.取少量试液,加入盐酸无明显现象产生,再加入氯化钡溶液,有白色沉淀生成
10.化学反应中绚丽的颜色变化往往展现了化学的神奇,体现了化学之美。下列变化中的 a、b、c、d
可以是混合物。下列关于物质类别或者反应类型的叙述一定正确的是( )
A.变化①一定不属于氧化还原反应
B.变化②得到的白色沉淀一定是硫酸盐
C.物质c中一定不能含有铁红或磁性氧化铁
D.物质d可能是某有机物的水溶液
【练提升】
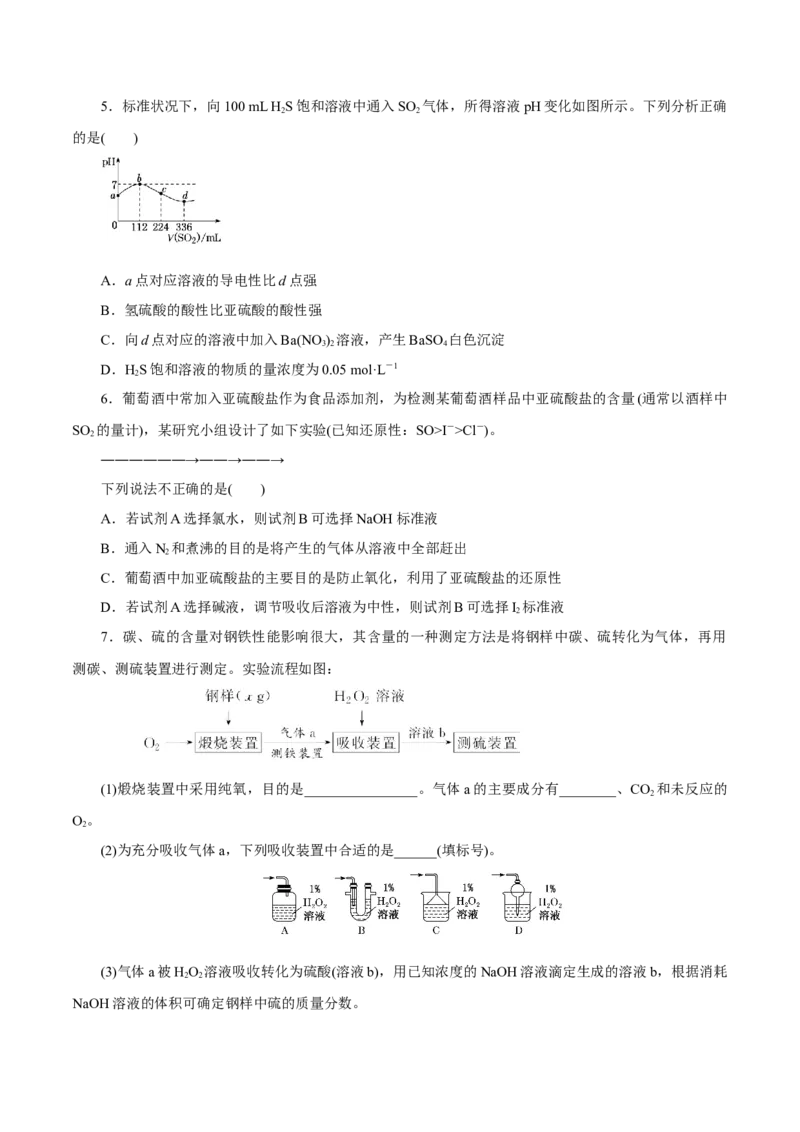
1.已知2FeSO =====Fe O +SO ↑+SO ↑。下列有关操作、装置、原理及对现象的表述正确的是(
4 2 3 2 3
)
A.用装置甲高温分解FeSO ,点燃酒精喷灯前应先向装置内通一段时间N
4 2B.用装置乙可检验分解产生的SO ,现象是石蕊溶液先变红后褪色
2
C.用装置丙可检验分解产生的SO ,现象是产生白色沉淀
3
D.用装置丁可吸收尾气,避免污染环境
2.下图是一种综合处理SO 废气的工艺流程。下列说法正确的是( )
2
A.向溶液B中滴加KSCN溶液,溶液可能变为红色
B.溶液B转化为溶液C发生反应的离子方程式为4H++2Fe2++O===2Fe3++2HO
2 2
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
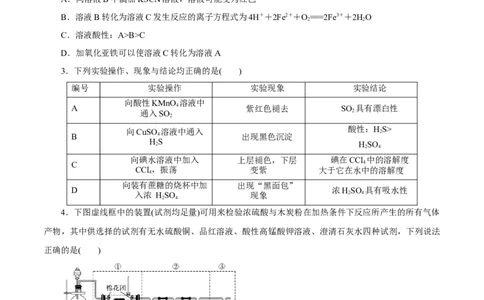
3.下列实验操作、现象与结论均正确的是( )
编号 实验操作 实验现象 实验结论
向酸性KMnO 溶液中
A 4 紫红色褪去 SO 具有漂白性
通入SO 2
2
向CuSO 溶液中通入 酸性:H 2 S>
B 4 出现黑色沉淀
HS
2 HSO
2 4
向碘水溶液中加入 上层褪色,下层 碘在CCl 中的溶解度
C 4
CCl ,振荡 变紫 大于它在水中的溶解度
4
向装有蔗糖的烧杯中加 出现“黑面包”
D 浓HSO 具有吸水性
入浓 HSO 现象 2 4
2 4
4.下图虚线框中的装置(试剂均足量)可用来检验浓硫酸与木炭粉在加热条件下反应所产生的所有气体
产物,其中供选择的试剂有无水硫酸铜、品红溶液、酸性高锰酸钾溶液、澄清石灰水四种试剂,下列说法
正确的是( )
A.物质甲可以是无水硫酸铜,也可以是变色硅胶、无水氯化钙等物质
B.丙中发生反应的离子方程式可能是SO +2OH-===SO+HO
2 2
C.乙和戊两种溶液都不宜用作尾气吸收装置中的试剂
D.如果将装置的连接顺序变为①③②,则只能检验出两种产物5.标准状况下,向100 mL H S饱和溶液中通入SO 气体,所得溶液pH变化如图所示。下列分析正确
2 2
的是( )
A.a点对应溶液的导电性比d点强
B.氢硫酸的酸性比亚硫酸的酸性强
C.向d点对应的溶液中加入Ba(NO ) 溶液,产生BaSO 白色沉淀
3 2 4
D.HS饱和溶液的物质的量浓度为0.05 mol·L-1
2
6.葡萄酒中常加入亚硫酸盐作为食品添加剂,为检测某葡萄酒样品中亚硫酸盐的含量(通常以酒样中
SO 的量计),某研究小组设计了如下实验(已知还原性:SO>I->Cl-)。
2
――――――→――→――→
下列说法不正确的是( )
A.若试剂A选择氯水,则试剂B可选择NaOH标准液
B.通入N 和煮沸的目的是将产生的气体从溶液中全部赶出
2
C.葡萄酒中加亚硫酸盐的主要目的是防止氧化,利用了亚硫酸盐的还原性
D.若试剂A选择碱液,调节吸收后溶液为中性,则试剂B可选择I 标准液
2
7.碳、硫的含量对钢铁性能影响很大,其含量的一种测定方法是将钢样中碳、硫转化为气体,再用
测碳、测硫装置进行测定。实验流程如图:
(1)煅烧装置中采用纯氧,目的是________________。气体a的主要成分有________、CO 和未反应的
2
O。
2
(2)为充分吸收气体a,下列吸收装置中合适的是______(填标号)。
(3)气体a被HO 溶液吸收转化为硫酸(溶液b),用已知浓度的NaOH溶液滴定生成的溶液b,根据消耗
2 2
NaOH溶液的体积可确定钢样中硫的质量分数。①滴定时 NaOH 溶液置于________(填仪器名称)中,若以酚酞为指示剂,终点时的现象为
________________________________________________________________________。
②若称取1 g钢样进行实验,滴定消耗0.01 mol·L-1 NaOH溶液2.0 mL,则该钢样中硫的质量分数为
________。
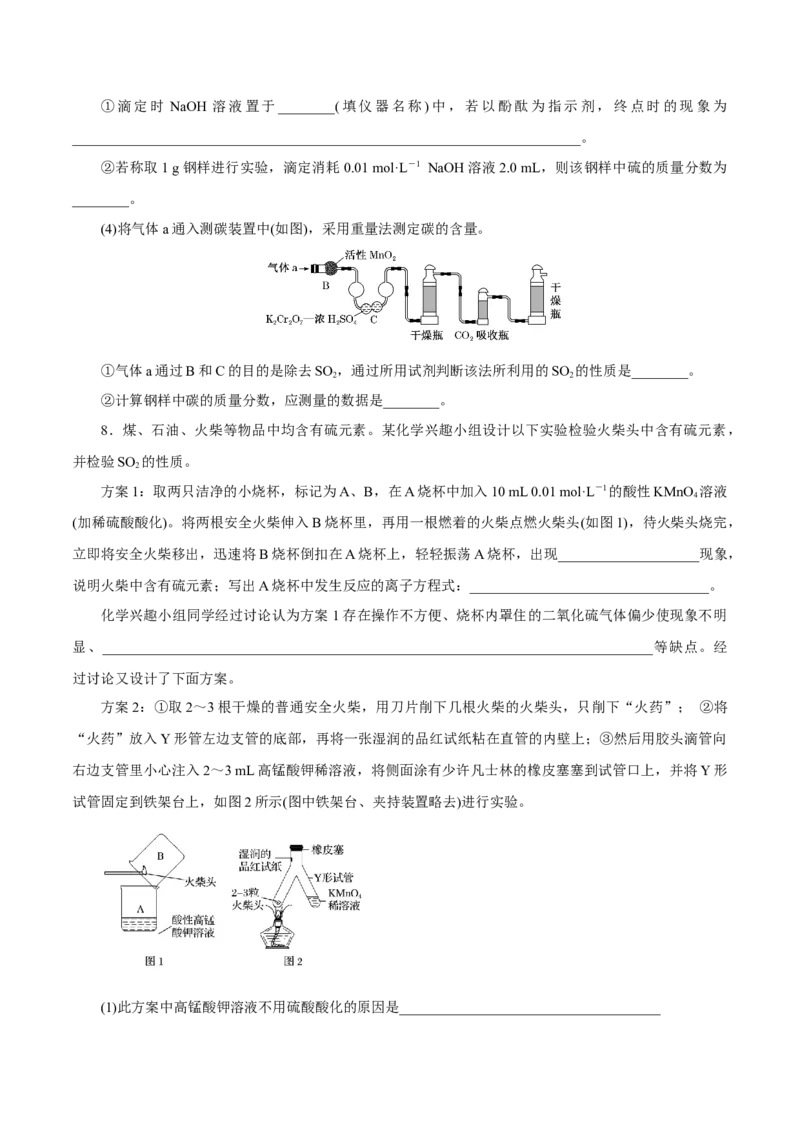
(4)将气体a通入测碳装置中(如图),采用重量法测定碳的含量。
①气体a通过B和C的目的是除去SO ,通过所用试剂判断该法所利用的SO 的性质是________。
2 2
②计算钢样中碳的质量分数,应测量的数据是________。
8.煤、石油、火柴等物品中均含有硫元素。某化学兴趣小组设计以下实验检验火柴头中含有硫元素,
并检验SO 的性质。
2
方案1:取两只洁净的小烧杯,标记为A、B,在A烧杯中加入10 mL 0.01 mol·L-1的酸性KMnO 溶液
4
(加稀硫酸酸化)。将两根安全火柴伸入B烧杯里,再用一根燃着的火柴点燃火柴头(如图1),待火柴头烧完,
立即将安全火柴移出,迅速将B烧杯倒扣在A烧杯上,轻轻振荡A烧杯,出现____________________现象,
说明火柴中含有硫元素;写出A烧杯中发生反应的离子方程式:__________________________________。
化学兴趣小组同学经过讨论认为方案1存在操作不方便、烧杯内罩住的二氧化硫气体偏少使现象不明
显、______________________________________________________________________________等缺点。经
过讨论又设计了下面方案。
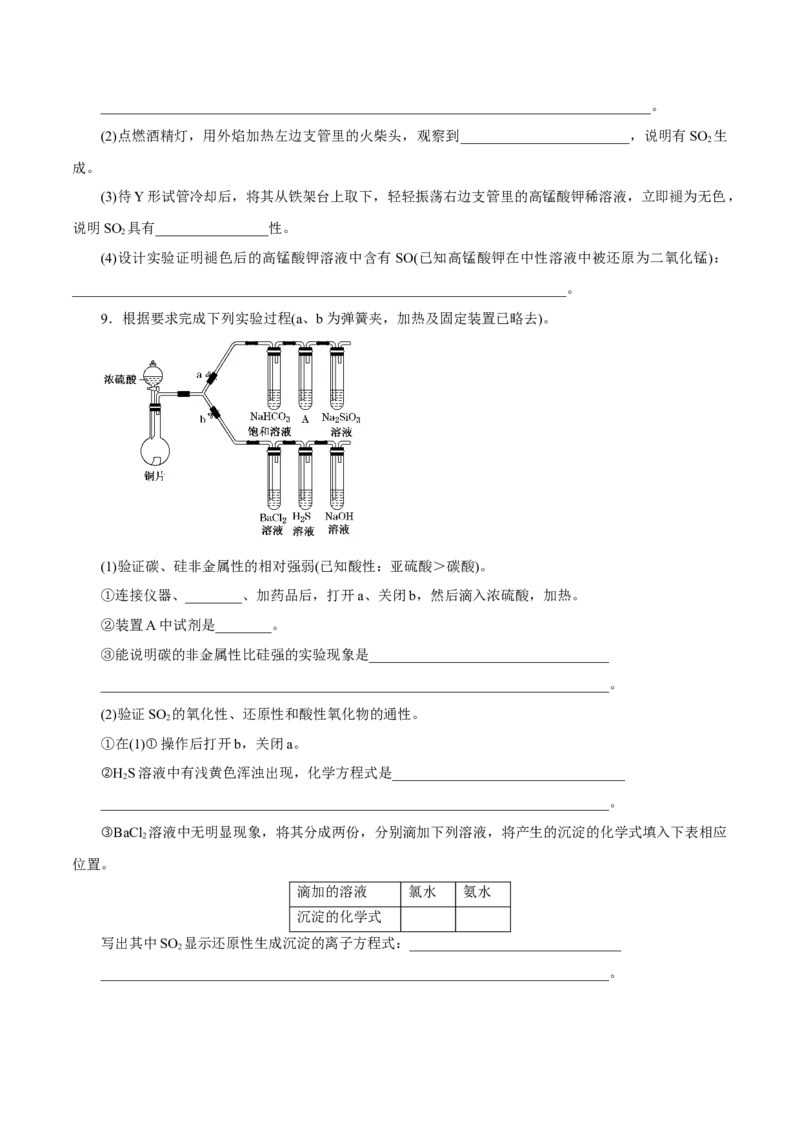
方案2:①取2~3根干燥的普通安全火柴,用刀片削下几根火柴的火柴头,只削下“火药”; ②将
“火药”放入Y形管左边支管的底部,再将一张湿润的品红试纸粘在直管的内壁上;③然后用胶头滴管向
右边支管里小心注入2~3 mL高锰酸钾稀溶液,将侧面涂有少许凡士林的橡皮塞塞到试管口上,并将Y形
试管固定到铁架台上,如图2所示(图中铁架台、夹持装置略去)进行实验。
(1)此方案中高锰酸钾溶液不用硫酸酸化的原因是___________________________________________________________________________________________________________________。
(2)点燃酒精灯,用外焰加热左边支管里的火柴头,观察到________________________,说明有SO 生
2
成。
(3)待Y形试管冷却后,将其从铁架台上取下,轻轻振荡右边支管里的高锰酸钾稀溶液,立即褪为无色,
说明SO 具有________________性。
2
(4)设计实验证明褪色后的高锰酸钾溶液中含有 SO(已知高锰酸钾在中性溶液中被还原为二氧化锰):
______________________________________________________________________。
9.根据要求完成下列实验过程(a、b为弹簧夹,加热及固定装置已略去)。
(1)验证碳、硅非金属性的相对强弱(已知酸性:亚硫酸>碳酸)。
①连接仪器、________、加药品后,打开a、关闭b,然后滴入浓硫酸,加热。
②装置A中试剂是________。
③能说明碳的非金属性比硅强的实验现象是__________________________________
________________________________________________________________________。
(2)验证SO 的氧化性、还原性和酸性氧化物的通性。
2
①在(1)①操作后打开b,关闭a。
②H S溶液中有浅黄色浑浊出现,化学方程式是_________________________________
2
________________________________________________________________________。
③BaCl 溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应
2
位置。
滴加的溶液 氯水 氨水
沉淀的化学式
写出其中SO 显示还原性生成沉淀的离子方程式:______________________________
2
________________________________________________________________________。10.某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO 并完成相关性
2
质探究(不考虑水蒸气)。
(1)有同学认为制得的 SO 中可能混有杂质,其化学式为 ________和________,原因是
2
_____________________________________________________________________________。
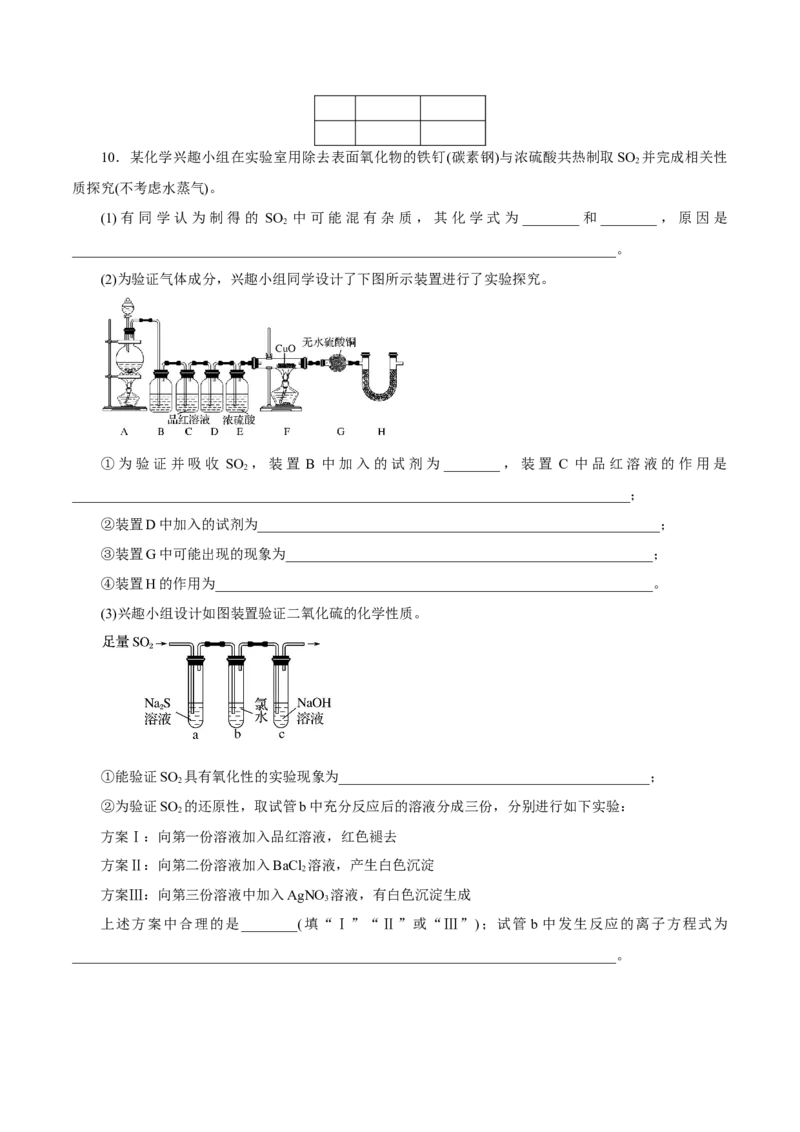
(2)为验证气体成分,兴趣小组同学设计了下图所示装置进行了实验探究。
①为验证并吸收 SO ,装置 B 中加入的试剂为________,装置 C 中品红溶液的作用是
2
_______________________________________________________________________________;
②装置D中加入的试剂为_________________________________________________________;
③装置G中可能出现的现象为____________________________________________________;
④装置H的作用为______________________________________________________________。
(3)兴趣小组设计如图装置验证二氧化硫的化学性质。
①能验证SO 具有氧化性的实验现象为____________________________________________;
2
②为验证SO 的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
2
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去
方案Ⅱ:向第二份溶液加入BaCl 溶液,产生白色沉淀
2
方案Ⅲ:向第三份溶液中加入AgNO 溶液,有白色沉淀生成
3
上述方案中合理的是________(填“Ⅰ”“Ⅱ”或“Ⅲ”);试管 b 中发生反应的离子方程式为
_____________________________________________________________________________。