文档内容
第 17 讲 化学能与热能
第一部分:高考真题感悟
1.(2021·广东·高考真题)“天问一号”着陆火星,“嫦娥五号”采回月壤。腾飞中国离不开化学,长征
系列运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法正确的是
A.煤油是可再生能源
B. 燃烧过程中热能转化为化学能
C.火星陨石中的 质量数为20
D.月壤中的 与地球上的 互为同位素
【答案】C
【解析】A.煤油来源于石油,属于不可再生能源,故A错误;B.氢气的燃烧过程放出热量,将化学能
变为热能,故B错误;C.元素符号左上角数字为质量数,所以火星陨石中的20Ne 质量数为20,故C正确;
D.同位素须为同种元素,3He 和 3H的质子数不同,不可能为同位素关系,故D错误;故选C。
2.(2021·海南·高考真题)元末陶宗仪《辍耕录》中记载:“杭人削松木为小片,其薄为纸,熔硫磺涂木
片顶端分许,名日发烛……,盖以发火及代灯烛用也。”下列有关说法错误的是
A.将松木削薄为纸片状有助于发火和燃烧
B.“发烛”发火和燃烧利用了物质的可燃性
C.“发烛”发火和燃烧伴随不同形式的能量转化
D.硫磺是“发烛”发火和燃烧反应的催化剂
【答案】D
【解析】A.将松木削薄为纸片状可以增大可燃物与氧气接触面积,有助于发火和燃烧,A正确;B.发烛
具有可燃性,“发烛”发火和燃烧利用了物质的可燃性,B正确;C.“发烛”发火和燃烧伴随不同形式
的能量转化,如化学能转化为光能、热能等,C正确;D.硫磺也燃烧,不是催化剂,D错误;选D。
3.(2017·浙江·高考真题)根据能量变化示意图,下列热化学方程式正确的是A.N(g)+3H(g)=2NH (g) ΔH=-(b-a)kJ·mol-1
2 2 3
B.N(g)+3H(g)=2NH (g) ΔH=-(a-b)kJ·mol-1
2 2 3
C.2NH (l)=N (g)+3H(g) ΔH=2(a+b-c)kJ·mol-1
3 2 2
D.2NH (l)=N (g)+3H(g) ΔH=2(b+c-a)kJ·mol-1
3 2 2
【答案】D
【解析】由图中信息可知,0.5N (g)+1.5H (g)=NH (g) ΔH= -(b-a)kJ·mol-1,0.5N (g)+1.5H (g)=NH (l) ΔH= -
2 2 3 2 2 3
(b+c-a)kJ·mol-1。A.由0.5N (g)+1.5H (g)=NH (g) ΔH= -(b-a)kJ·mol-1可得出,N(g)+3H(g)=2NH (g) ΔH=
2 2 3 2 2 3
-2(b-a)kJ·mol-1,A不正确;B.由A选项中的分析可知,N(g)+3H(g)=2NH (g) ΔH= -2(b-a)kJ·mol-1,B不
2 2 3
正确;C.由0.5N (g)+1.5H (g)=NH (l) ΔH= -(b+c-a)kJ·mol-1可知,2NH (l)=N (g)+3H(g) ΔH=2(b+c-
2 2 3 3 2 2
a)kJ·mol-1,C不正确;D.由C选项的分析可知,2NH (l)=N (g)+3H(g) ΔH=2(b+c-a)kJ·mol-1,D正确;故
3 2 2
选D。
4.(2016·浙江·高考真题)已知:CH(g)的燃烧热为-890.31kJ•mol-1,则下列热化学方程式正确的是
4
A.CH(g)+2O(g)=CO (g)+2HO(l) H=+890.31kJ•mol-1
4 2 2 2
B.CH
4
(g)+2O
2
(g)=CO
2
+2H
2
O(g) H△=-890.31kJ•mol-1
C.CH
4
(g)+O
2
(g)=CO(g)+2H
2
O(l) △H=-890.31kJ•mol-1
D.CH 4 (g)+2O 2 (g)=CO 2 (g)+2H 2 O(l) △ H=-890.31kJ•mol-1
【答案】D △
【解析】CH(g)的燃烧热是1mol甲烷完全燃烧生成二氧化碳和液态水放出的能量,CH(g)的燃烧热
4 4
为-890.31kJ•mol-1,表示甲烷燃烧热的热化学方程式是CH(g)+2O(g)=CO (g)+2HO(l)
4 2 2 2
H=-890.31kJ•mol-1,故选D。
△5.(2021·海南·高考真题)2020年9月22日,中国向全世界宣布,努力争取2060年前实现碳中和。下列
措施不利于大气中 减少的是
A.用氨水捕集废气中的 ,将其转化为氮肥B.大力推广使用风能、水能、氢能等清洁能源
C.大力推广使用干冰实现人工增雨,缓解旱情
D.通过植树造林,利用光合作用吸收大气中的
【答案】C
【解析】A.氨水能与酸性氧化物二氧化碳反应生成碳酸铵或碳酸氢铵,则用氨水捕集废气中的二氧化碳,
将其转化为氮肥有利于大气中二氧化碳的减少,故A不符合题意;B.大力推广使用风能、水能、氢能等
清洁能源可以减少化石能源的使用,从而减少二氧化碳气体的排放,有利于大气中二氧化碳的减少,故B
不符合题意;C.大力推广使用干冰实现人工增雨,会增加大气中二氧化碳的量,不利于大气中二氧化碳
的减少,故C符合题意;D.通过植树造林,利用光合作用吸收大气中的二氧化碳有利于大气中二氧化碳
的减少,故D不符合题意;故选C。
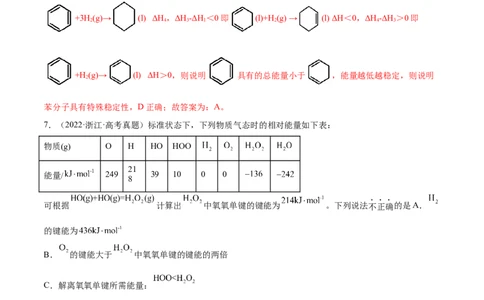
6.(2022·浙江·高考真题)相关有机物分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图
所示:
下列推理不正确的是
A.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
2 3
C.3ΔH<ΔH,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D.ΔH-ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
【答案】A
【解析】A.虽然2ΔH≈ΔH,但ΔH≠ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目、双键的
1 2 2 3
位置有关,不能简单的说碳碳双键加氢放出的热量与分子内碳碳双键数目成正比,A错误;B.ΔH<
2
ΔH,即单双键交替的物质能量低,更稳定,说明单双键交替的两个碳碳双键间存在相互作用,有利于物
3
质稳定,B正确;C.由图示可知,反应I为: (l)+H (g)→ (l) ΔH,反应IV为:
2 1+3H (g)→ (l) ΔH,故反应I是1mol碳碳双键加成,如果苯环上有三个完全独立的碳碳三键,则
2 4
3ΔH=ΔH ,现3ΔH<ΔH,说明苯分子中不存在三个完全独立的碳碳双键,C正确;D.由图示可知,反
1 4 1 4
应I为: (l)+H (g)→ (l) ΔH,反应III为: (l)+2H (g) → (l) ΔH 反应IV为:
2 1 2 3,
+3H (g)→ (l) ΔH,ΔH-ΔH <0即 (l)+H (g) → (l) ΔH<0,ΔH-ΔH >0即
2 4 3 1 2 4 3
+H (g)→ (l) ΔH>0,则说明 具有的总能量小于 ,能量越低越稳定,则说明
2
苯分子具有特殊稳定性,D正确;故答案为:A。
7.(2022·浙江·高考真题)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO
21
能量/ 249 39 10 0 0
8
可根据 计算出 中氧氧单键的键能为 。下列说法不正确的是A.
的键能为
B. 的键能大于 中氧氧单键的键能的两倍
C.解离氧氧单键所需能量:
D.
【答案】C
【解析】A.根据表格中的数据可知, 的键能为218×2=436 ,A正确;B.由表格中的数据可知
的键能为:249×2=498 ,由题中信息可知 中氧氧单键的键能为 ,则 的键能大于 中氧氧单键的键能的两倍,B正确;C.由表格中的数据可知HOO=HO+O,解离其中氧氧单键
需要的能量为249+39-10=278 , 中氧氧单键的键能为 ,C错误;D.由表中的数
据可知 的 ,D正确;故选C。
8.(2021·浙江·高考真题)相同温度和压强下,关于反应的 ,下列判断正确的是
A. B.
C. D.
【答案】C
【解析】一般的烯烃与氢气发生的加成反应为放热反应,但是,由于苯环结构的特殊性决定了苯环结构的
稳定性,苯与氢气发生加成反应生成1,3-环己二烯时,破坏了苯环结构的稳定性,因此该反应为吸热反
应。A.环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放热反应,因此, ,A不
正确;B.苯分子中没有碳碳双键,其中的碳碳键是介于单键和双键之间的特殊的共价键,因此,其与氢
气完全加成的反应热不等于环己烯、1,3-环己二烯分别与氢气发生的加成反应的反应热之和,即
,B不正确;C.环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放反应,
,由于1mol 1,3-环己二烯与氢气完全加成后消耗的氢气是等量环己烯的2倍,故其放出的
热量更多,其 ;苯与氢气发生加成反应生成1,3-环己二烯的反应为吸热反应( ),根据
盖斯定律可知,苯与氢气完全加成的反应热 ,因此 ,C正确;D.根据盖斯定律可知,苯与氢气完全加成的反应热 ,因此 ,D不正确。综上所述,本题选
C。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·湖南衡阳·三模) 常见金属 和卤素单质反应的熔变 (单位: )示意图如图,反
应物和生成物均为常温时的稳定状态。下列说法错误的是
A. 与 反应的
B.由 分解制得 的反应是吸热反应
C.化合物的热稳定性顺序:
D.
【答案】C
【解析】A.根据上述图示可构造热化学方程式如下:①M(s)+Cl (g)=MCl (s) ,② M(s)
2 2
+Br (l)=MBr (s) ,根据盖斯定律可知,①-②可得 ,所以
2 2
对应的反应热 ,A正确;B.生成 的反应为放热反应,所以由 分解制得
的反应是吸热反应,B正确;C.能量越低的物质越稳定,结合卤素的性质变化规律可知,上述化合物
的稳定性顺序为: ,C错误;D.与A项分析原理相同,结合图示信息构造两个
热化学方程式分别为:①M(s)+F (g)=MF(s) ,② M(s)+Br (l)=MBr (s)
2 2 2 2,根据盖斯定律可知,②-①可得 ,所以对应的反应热 ,D
正确;故选C。
2.(2022·上海上海·二模)如图装置进行实验,向小试管中加入稀盐酸。观察到U形管内两边红墨水液面
逐渐变为左低右高,与此现象有关的推论是
A.反应物总能量低于生成物
B.发生了析氢腐蚀,产生较多气体
C.生成物中化学键形成会放出能量
D.锥形瓶内气体分子间平均距离变大
【答案】D
【解析】A.涉及反应为放热过程,反应物总能量高于生成物,A错误;B.小试管与锥形瓶整个体系并不
连通,即使产生气体,也不会造成红黑水液面变化,B错误;C.所有的生成物中化学键形成都会放出能
量,但是最终能否影响实验得看成键释放的能量与断键吸收能量的相对大小,从而确定反应放热与否,C
的说法没错,但是不符合题意;D.小试管内反应放热,导致锥形瓶内温度升高,瓶内气体分子间平均距
离变大,从而导致红墨水液面左低右高,D正确;故合理选项为D。
3.(2022·上海崇明·二模)有关反应热效应的说法正确的是
A.常温下自发进行的反应也可以是吸热反应
B.氧化还原反应都属于放热反应
C.有催化剂参与的反应是放热反应
D.有化学键断裂的反应是吸热反应
【答案】A
【解析】A. 若反应的 ,反应可自发进行,若反应的 ,则常温下自发进行的反应也可以
是吸热反应,故A正确;B. 是氧化还原反应,但属于吸热反应,故B错误;C. 化学反
应的吸放热与是否有催化剂参与无关,故C错误;D. 所有的化学反应均有化学键的断裂和生成,反应物
断键吸收的热量比生成物成键放出的热量多,该反应为吸热反应,反之为放热反应,故D错误;故选A。
4.(2022·上海松江·二模)将溶质物质的量相同的酸溶液与碱溶液相混合,a:盐酸和氢氧化钠,b:醋酸和氢氧化钠,c:醋酸和氨水。其所放出热量比较,正确的是
A.a>b>c B.c>b>a C.b>c>a D.a=b=c
【答案】A
【解析】HCl和氢氧化钠在溶液中完全电离,发生反应 ,反应放热;醋酸不完全电离,醋酸
与氢氧化钠发生反应 ,随着反应的进行,醋酸逐渐电离,电离吸热,故放
出的热量比a少;醋酸和氨水均不完全电离,发生反应 ,反应
过程中醋酸和 。逐渐电离,电离吸收的热量比b要多,故放出的热量比b少,故A正确;故选
A。
5.(2022·河南·模拟预测)2022年冬奥会火炬体现了艺术设计与科技创新的完美融合。火炬选用碳纤维与
树脂的复合材料制成,降低了材料用量,燃料使用氢燃料,使火炬燃烧时的碳排放为“零”,体现出“绿
色”办奥理念和科技冬奥成果。下列有关说法正确的是
A.树脂属于无机非金属材料
B.氢能是清洁的可再生能源
C.碳纤维与金刚石互为同素异形体
D.氢气燃烧时能量变化只有化学能到热能的转化
【答案】B
【解析】A.树脂属于有机高分子材料,故A错误;B. 氢气燃烧生成水,且可通过电解水得到氢气,故
氢能是清洁的可再生能源,故B正确;C. 碳纤维指的是含碳量在90%以上的高强度高模量纤维,还含有
其他成分,属于混合物,故碳纤维与金刚石不互为同素异形体,故C错误;D. 氢气燃烧时能量变化除了
有化学能到热能的转化,还包括化学能到光能的转化,故D错误;故选B。
6.(2022·北京·101中学三模)下图是计算机模拟的在催化剂表面上水煤气变化的反应历程。吸附在催化
剂表面的物种用“*”标注。下列说法正确的是
A.①表示CO和 从催化剂表面脱离的过程
B.②和④中化学键变化相同,因此吸收的能量相同
C.由图可知 为吸热反应
D.相同条件下,反应速率④>②
【答案】B
【解析】A.由题干反应历程图信息可知,①表示CO和 在催化剂表面吸附的过程,A错误;B.由题
干反应历程图信息可知,②和④中化学键变化相同均为HO中的H-O键,因此吸收的能量相同,B正确;
2
C.由题干反应历程图信息可知,反应 中反应物CO和HO的总能量高
2
于生成物CO 和H 的总能量,故为放热反应,C错误;D.由题干反应历程图信息可知,过程②需要的活
2 2
化能(1.59-(-0.32))=1.91eV低于反应④的活化能(1.86-(0.16))=2.02eV,相同条件下,活化能越大,反应速率
越慢,故反应速率④<②,D错误;故答案为:B。
7.(2022·上海上海·模拟预测)N(g)与H(g)化合生成NH (g)的能量变化如图,下列说法正确的是
2 2 3A.N 与H 的键能数值总和为1080
2 2
B.N(g)+3H(g) 2NH (g)+46 kJ
2 2 3
C.1 mol H (g)的能量比2 mol H(g)的能量低
2
D.若使用催化剂会改变反应的热效应
【答案】C
【解析】A.由图中可知, molN≡N与 molH-H的键能总和为1080kJ,则N 与H 的键能数值总和不等
2 2
于1080,A不正确;B.从图中可以看出, molN2+ molH → 1molNH ,放热(314+377+435-
2 3
1080)kJ=46kJ,则N(g)+3H(g) 2NH (g)+92kJ,B不正确;C.H(g)断裂共价键生成2H(g),需要吸
2 2 3 2
收热量,所以1 mol H (g)的能量比2 mol H(g)的能量低,C正确;D.若使用催化剂,可以改变反应的活化
2
能,但不能改变反应的热效应,D不正确;故选C。
8.(2022·上海奉贤·二模)在25℃、 下, 氢气燃烧生成气态水的能量变化如下图所示,
已知:2H(g) + O(g)→2H O(g) ,下列有关说法正确的是
2 2 2
A.O—H键的键能为930kJ·mol-1
B.a= 249
C.物质所具有的总能量大小关系为:甲>乙>丙D.1molH O(l)分解为2molH与1molO时吸收930kJ热量
2
【答案】B
【解析】A.2molH原子和1molO形成2molO-H键,故H-O键的键能为 ,A错误;
B.该反应的反应热等于反应物总键能减去生成物总键能,故 ,
a=249,B正确;C.断键吸热,成键放热,甲到乙为断键过程,乙到丙为成键过程,故乙的能量最高,C
错误;D.1molH O(g)分解为2molH与1molO时吸收930kJ热量,D错误;故选B。
2
9.(2022·湖南·模拟预测)丙烷与氯气反应可得到两种一氯代物,其反应机理为游离基(电中性的原子或
原子团)间的反应,部分反应过程如图所示,下列说法正确的是
A.含碳自由基的形成过程中只断裂了极性键
B.生成自由基CHCHCH 的速率较快
3 2 2
C.主要有机产物是CHCHClCH
3 3
D.生成一氯代物的反应可能是吸热反应
【答案】C
【解析】A.由图中信息知,含碳自由基是丙烷与Cl·作用的结果,原料中的Cl 转化为Cl·时断裂了非极性
2
键,A项错误;B.由图可知,过渡态I活化能较高,相应的反应速率较慢,即生成自由基CH
3
CH 2CH
2
的
速率较慢,B项错误;C.由于生成CH 3CHCH
3
的速率较快且CH 3CHCH
3
的能量更低,故主要有机产物是
CHCHClCH ,C项正确;D.含碳自由基与Cl·结合可得到一氯代物,结合中会形成共价键,释放出能量,
3 3
故产物总能量低于反应物总能量,反应是放热反应,D项错误;故答案选C
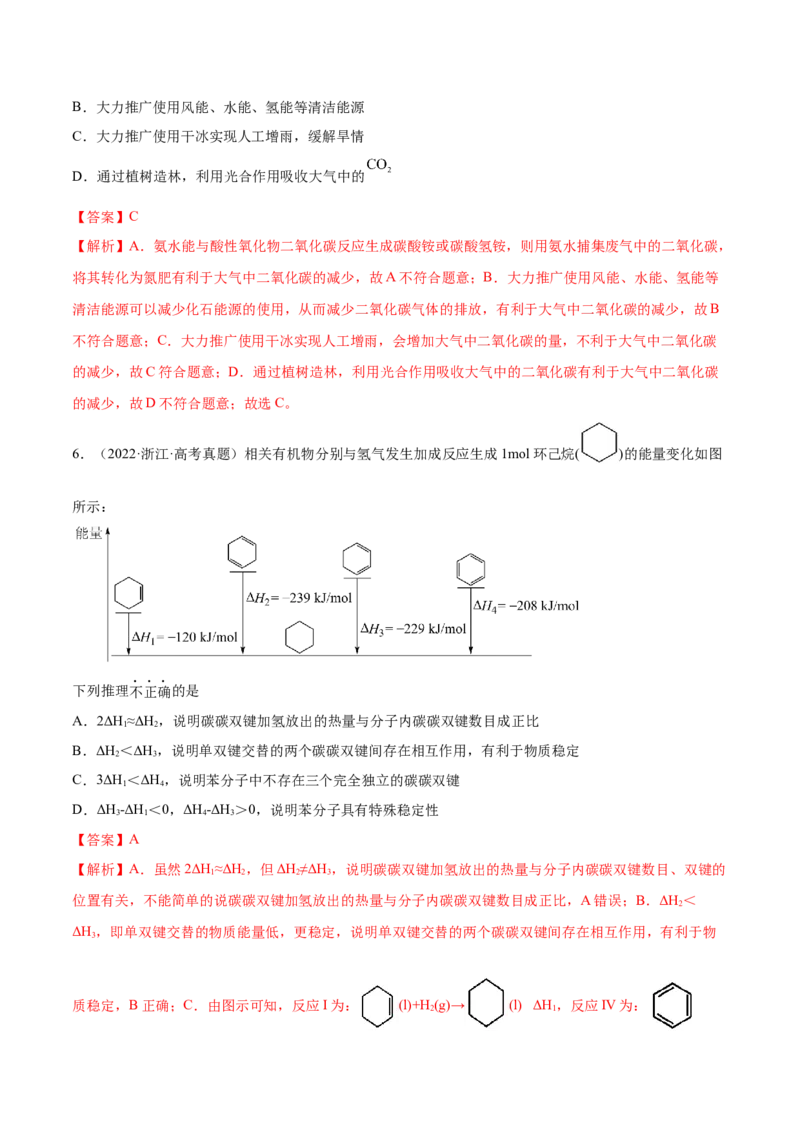
10.(2022·浙江·三模)已知:在标准压强(100kPa)、298K,由最稳定的单质合成1mol物质B的反应焓变,
叫做物质B的标准摩尔生成焓,用△H(kJ/mol)表示。有关物质的△H有如图所示关系。下列有关判断正确
的是A.HO(l)的△H>-241.8kJ·mol-1 B.NH 比NH 稳定
2 3 2 4
C.NH(l)标准燃烧热为534.2kJ·mol-1 D.NO(g)的键能大于N(g)与O(g)的键能之和
2 4 2 2
【答案】B
【解析】A. HO(g)→ HO(l),需要继续放热,放出的热量越多,对应焓变的数值越小,所以
2 2
△H<-241.8kJ·mol-1,A错误;B.物质所具备的能量越低越稳定,标准摩尔生成焓的定义可知,NH 相对
3
能量为-45.9 kJ·mol-1,NH 相对能量为50.6 kJ·mol-1,所以NH 更稳定 ,B正确;C.NH(l)标准燃烧热应
2 4 3 2 4
该生成N 和HO(l),题干中无HO(l)的相对能量,无法计算,C错误;D.△H=生成物总能量-反应物总能
2 2 2
量所以 NO(g) = N (g)+O(g) H= 0+0-91.3= - 91.3 kJ·mol-1<0,△H=反应物总键能-生成物总键能<0,所以
2 2
NO(g)的键能小于N(g)与O(g△)的键能之和,D错误;故选B。
2 2
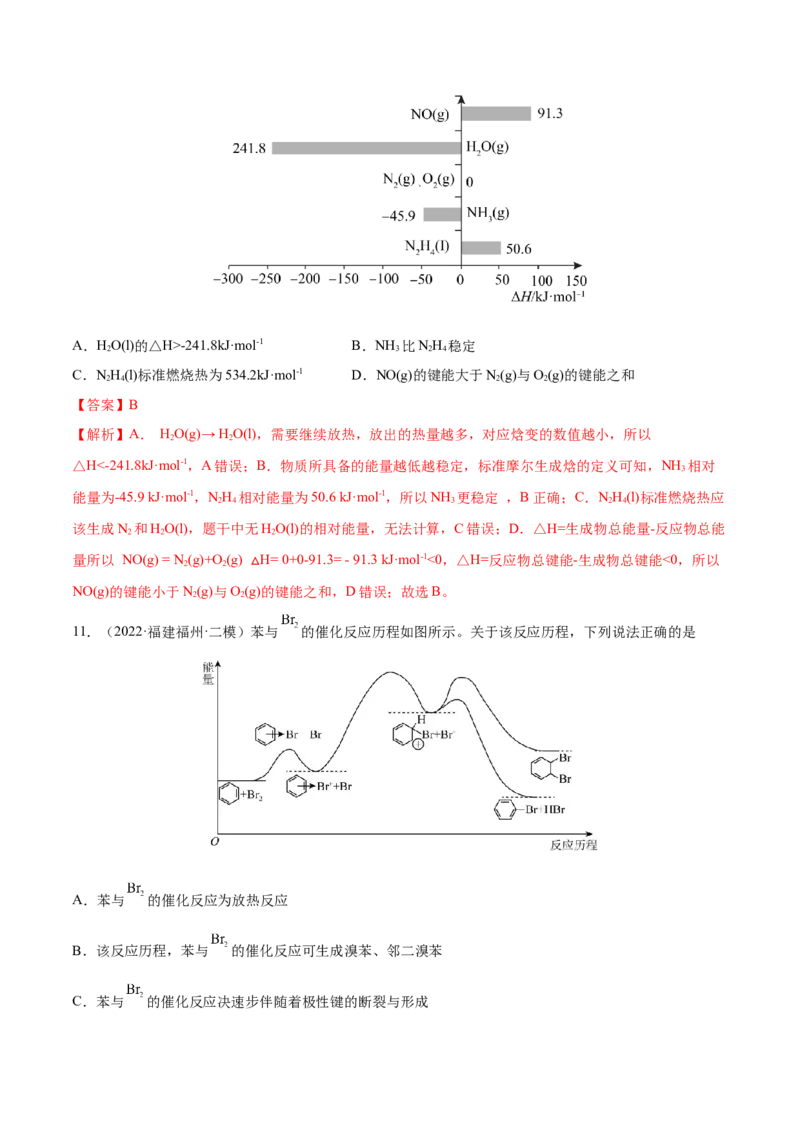
11.(2022·福建福州·二模)苯与 的催化反应历程如图所示。关于该反应历程,下列说法正确的是
A.苯与 的催化反应为放热反应
B.该反应历程,苯与 的催化反应可生成溴苯、邻二溴苯
C.苯与 的催化反应决速步伴随着极性键的断裂与形成D.从反应速率角度,苯与Br ,的催化反应主反应为取代反应,原因是该反应活化能更低
2
【答案】D
【解析】A.由图可知,苯与Br 的加成反应是吸热反应,取代反应是放热反应,故A错误;B.该反应历
2
程,苯与 的催化反应可生成溴苯,但不能生成邻二溴苯,故B错误;C.由于 转化为
的活化能最大,反应速率最慢,故是总反应的决速步骤,但步骤中不存在极性键的断裂,故C错
误;D.第三步中取代反应的活化能低,生成物本身所具有的能量低,更稳定,故苯与Br 的催化反应主反
2
应为取代反应,故D正确;故选D。
12.(2022·湖北·黄冈中学模拟预测)金属插入CH 的C—H键形成高氧化态过渡金属化合物的反应频繁出
4
现在光分解作用、金属有机化学等领域,如图是CH 与Zr形成过渡金属化合物的过程。下列说法不正确的
4
是( )
A.整个反应快慢,由CH—Zr···H→状态2反应决定
2 2
B.Zr+CH →CH—Zr···H活化能为213.67kJ•mol-1
4 3
C.在中间产物中CH—Zr···H状态最稳定
3
D.Zr+CH →CH—Zr···H ΔH=+39.54kJ•mol-1
4 3
【答案】B
【解析】A.整个反应的快慢取决于最慢的反应,反应的活化能越高,反应速率越慢,由图中可知,由
CH— Zr···H →状态2活化能最大,故整个反应的快慢就取决于该反应,A正确;B.由图中可以读出,Zr
2 2
+CH →CH—Zr···H活化能为99.20 kJ • mol -1,B错误;C.物质所具有的能量越低越稳定,由图中可知,
4 3在中间产物中CH—Zr···H的能量为-114.47kJ • mol-1为最低,故中间产物中CH—Zr···H状态最稳定,C正
3 3
确;D.由图中可知,Zr + CH 的总能量为0kJ • mol一1,而CH —Zr···H 的总能量为+ 39. 54 kJ • mol一1,
4 3
故Zr + CH →CH —Zr···H ΔH= + 39. 54 kJ • mol一1,D正确;故答案为:B。
4 3
二、主观题(共3小题,共40分)
13.(2021·全国·高三专题练习)(16分)(Ⅰ)丙烷是一种优良的燃料。试回答下列问题:
(1)已知丙烷完全燃烧生成CO 和1 mol H O(l)放出553.75kJ的热量,写出表示丙烷标准燃烧热的热化学方
2 2
程式:_____________。
(2)二甲醚(CHOCH )是一种新型燃料,应用前景广阔。1 mol 二甲醚完全燃烧生成CO 和液态水放出1 455
3 3 2
kJ的热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO 和液态水共放出1 645 kJ的热量,则混合
2
气体中,丙烷和二甲醚的物质的量之比为________。
(Ⅱ)CH 、H、C都是优质的能源物质,它们燃烧的热化学方程式为:
4 2
①CH(g)+2O(g)=CO (g)+2HO(l) ΔH=-890.3 kJ·mol-1
4 2 2 2
②2H(g)+O(g)=2HO(l) ΔH=-571.6 kJ·mol-1
2 2 2
③C(s)+O(g)=CO (g) ΔH=-393.5 kJ·mol-1
2 2
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O 作用产生的能量存活,甲烷细菌使1 mol甲烷生成
2
CO 气体与液态水,放出的能量____________(填“>”“<”或“=”)890.3 kJ。
2
(2)甲烷与CO 可用于合成合成气(主要成分是一氧化碳和氢气):CH+CO=2CO+2H,1 g CH 完全反应可
2 4 2 2 4
释放15.46 kJ的热量,则:
①能表示该反应过程中能量变化的是____________(填字母)。
②若将物质的量均为1 mol的CH 与CO 充入某恒容密闭容器中,体系放出的热量随着时间的变化如图所
4 2
示,则CH 的转化率为____________(用小数表示,保留2位小数)。
4(3)C(s)与H(g)不反应,所以C(s)+2H(g)=CH (g)的反应热无法直接测量,但通过上述反应可求出C(s)+
2 2 4
2H(g)=CH (g) 的反应热ΔH=____________。
2 4
(4)目前对于上述三种物质的研究是燃料研究的重点,下列关于上述三种物质的研究方向中可行的是
_______________(填字母)。
A.寻找优质催化剂,使CO 与HO反应生成CH 与O,并放出热量
2 2 4 2
B.寻找优质催化剂,在常温常压下使CO 分解生成碳与O
2 2
C.寻找优质催化剂,利用太阳能使大气中的CO 与海底开采的CH 合成合成气(CO、H)
2 4 2
D.将固态碳合成为C ,以C 作为燃料
60 60
【答案】(除标注外,每空2分)(Ⅰ) (1)C H(g)+5O(g)=3CO (g)+4HO(l) =-2215kJ/mol
3 8 2 2 2
(2)1:3(3分)
(Ⅱ)(1)=
(2) ①D ②0.63
(3) -74.8 kJ·mol-1 (3分)
(4)C
【解析】(Ⅰ) (1)燃烧热是指1mol燃料完全燃烧后放出的热量,已知丙烷完全燃烧生成CO 和1 mol H O(l)
2 2
放出553.75kJ的热量,又知1mol丙烷完全燃烧生成4molH O,故表示丙烷标准燃烧热的热化学方程式:
2
C H(g)+5O(g)=3CO (g)+4HO(l) =4×-553.75kJ/mol=-2215kJ/mol,故答案为:C H(g)+5O(g)=3CO (g)
3 8 2 2 2 3 8 2 2
+4H O(l) =-2215kJ/mol;
2
(2)假设1 mol丙烷和二甲醚的混合气体中含有丙烷为xmol,则二甲醚为(1-x)mol,完全燃烧生成CO 和
2
液态水共放出1 645 kJ的热量,则有:2215 kJ/mol +1455 kJ/mol (1-x)=1645kJ,解得:x=0.25mol,故混合
气体中,丙烷和二甲醚的物质的量之比为x:(1-x)=0.25:(1-0.25)=1:3,故答案为:1:3;
(Ⅱ)(1)化学反应的焓变与反应途径无关,只与反应物和生成物的状态有关,故甲烷细菌使1 mol甲烷生成
CO 气体与液态水,放出的能量=890.3 kJ,故答案为:=;
2
(2) 根据1 g CH 完全反应可释放15.46 kJ的热量,故1molCH 完全燃烧释放的能量为:16×15.46
4 4
kJ=247.46kJ,据此解题:
①A.该过程是一个释放能量的过程,故反应物总能量高于生成物总能量,但图中数值不对,A错误;B.
该过程是一个释放能量的过程,故反应物总能量高于生成物总能量,B错误;C. 该过程是一个释放能量的过程,故反应物总能量高于生成物总能量,但图中数值不对,C错误;D.根据上述分析可知,D图中的数
值和能量相对大小均正确,D正确;故答案为:D。
②根据甲烷与CO 反应的热化学方程式可知:
2
,解得:x=0.63mol,故甲烷的转化率=
=0.63,故答案为:0.63;
(3) 根据盖斯定律并结合反应①CH(g)+2O(g)=CO (g)+2HO(l) ΔH=-890.3 kJ·mol-1
4 2 2 2
②2H(g)+O(g)=2HO(l) ΔH=-571.6 kJ·mol-1 ③C(s)+O(g)=CO (g) ΔH=-393.5 kJ·mol-1,可知
2 2 2 2 2
反应C(s)+2H(g)=CH (g)可由②+③-①,故反应C(s)+2H(g)=CH (g) 的反应热ΔH=(-571.6 kJ·mol-1)+(
2 4 2 4
-393.5 kJ·mol-1)-( -890.3 kJ·mol-1)=-74.8 kJ·mol-1,故答案为:-74.8 kJ·mol-1;
(4) A.甲烷与氧气的反应为放热反应,可知CO 与HO反应生成CH 和O 为吸热反应,A错误;B.使
2 2 4 2
CO 分解生成碳与O 的反应为吸热反应,常温下不能发生,B不正确;
2 2
C.大气中的CO 和海底开采的CH 合成合成气(CO、H),具有可行性,利用优质催化剂、太阳能实现
2 4 2
转化,C正确;D.将固态碳合成C ,以C 作燃料,产物相同,研究方向不可行,D错误;故答案为:
60 60
C。
14.(2021·全国·高三专题练习)(10分)化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_________(填字母)。
A.碳与水蒸气反应 B.铝和氧化铁反应 C.CaCO 受热分解 D.氢气还原三氧
3
化钨制取钨 E.锌与盐酸反应
(2)获取能量变化的途径
①通过化学键的键能计算。通常人们把断裂1mol某化学键所吸收的能量或形成1mol某化学键所释放的能
量看作该化学键的键能,键能的大小可用于估算化学反应的反应热ΔH。已知部分化学键的键能数据如表
所示:
化学键 H-H Cl-Cl H-Cl
键能/(kJ·mol-1) 436 243 431
则H(g)+Cl (g)=2HCl(g)的反应热ΔH为__________________________
2 2②通过盖斯定律可计算。发射卫星用 作燃料, 作氧化剂,两者反应生成N 和水蒸气,已知:
2
N(g) +2O(g)= 2NO (g) H =+67.7kJ/mol;N H(g)+O(g)= N(g)+2HO(g) H=-534kJ/mol,写出
2 2 2 1 2 4 2 2 2 2
气体肼和NO 气体反应生成△ N 和水蒸气的热化学方程式 △
2 2
___________________________________________________
③利用实验装置测量利用下图图装置测定中和热的实验步骤如下:
①用量筒量取0.25mol/L的硫酸50mL倒入小烧杯中,测出硫酸溶液
温度;
②用另一量筒量取50mL 0.55mol/L NaOH溶液,并用同一温度计测出
其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液的最
高温度。
回答下列问题:
I.仪器a的名称为______________________________
II.做了四次实验,并将实验数据记录如下:
起始温度t℃
温度 1
终止温度t/℃
2
实验次数
HSO NaOH 平均值
2 4
1 26.2 26.0 26.1 29.5
2 27.0 27.4 27.2 32.3
3 25.9 25.9 25.9 29.2
4 26.4 26.2 26.3 29.8
近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=
4.18 J/(g·℃),通过以上数据计算中和热ΔH=_________________( 结果保留小数点后一位)。
【答案】(每空2分)(1)BE (2)①-183kJ•mol-1 ②2NH(g)+2NO (g)=3N(g)+4HO(g)
2 4 2 2 2
H=−1135.7kJ/mol ③I.环形玻璃搅拌棒 Ⅱ.-56.8kJ/mol
△【解析】(1)常见的吸热反应有:大多数的分解反应、C或氢气作还原剂的氧化还原反应、氯化铵晶体与氢
氧化钡晶体的反应等,大多数化合反应,铝热反应,金属与酸的反应等属于放热反应,所以属于放热反应
的有B、E;
(2)①焓变=反应物键能之和-生成物键能之和,所以H(g)+Cl (g)=2HCl(g)的反应热ΔH=436kJ•mol-1+243
2 2
kJ•mol-1-(2×431)kJ•mol-1=-183 kJ•mol-1;
②已知:i:N(g)+2O(g)=2NO (g) ΔH =+67.7kJ/mol
2 2 2 1ii:NH(g)+O(g)=N(g)+2HO(g) ΔH =−534kJ/mol,
2 4 2 2 2 2
盖斯定律计算得到ii×2−i得到2NH(g)+2NO (g)=3N(g)+4HO(g) 的ΔH =−1135.7kJ/mol,故答案为:
2 4 2 2 2
2NH(g)+2NO (g)=3N(g)+4HO(g) ΔH =−1135.7kJ/mol
2 4 2 2 2
③ I.根据仪器的结构特点可知a为环形玻璃搅拌棒。
Ⅱ.第2次实验的误差较大,舍弃,将另外三次实验的最终温度和起始温度做差,取平均值,得到
△T=3.4℃;氢氧化钠过量,硫酸中氢离子为0.025mol,所以中和生成的水为0.025mol,溶液质量为
100g,升高3.4℃,热量为:100×3.4×4.18=1421.2J,所以每生成1mol水的放热为:
1421.2÷0.025=56848J≈56.8kJ,所以中和热为:ΔH=-56.8kJ/mol。
15.(14分)(1)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键需要的能量分别是436 kJ、391
kJ、946 kJ,则N 与H 反应生成NH 的热化学方程式为_________________。
2 2 3
(2)已知化学反应A(g)+B (g)===2AB(g)的能量变化如图所示,回答下列问题:
2 2
①该反应的ΔH_______0(填 “大于”“小于”或“等于”);
②反应物的总键能为______________;
③写出该反应的热化学方程式________________________________。
(3)联氨(又称肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
2 4
①2O(g)+N(g)=NO(l) ΔH
2 2 2 4 1
②N(g)+2H(g)=NH(l) ΔH
2 2 2 4 2
③O(g)+2H(g)=2HO(g) ΔH
2 2 2 3
④2NH(l) + N O(l)= 3N(g)+ 4H O(g) ΔH =-1048.9kJ/mol
2 4 2 4 2 2 4
写出联氨的结构式_______________,上述反应热效应之间的关系式为ΔH=__________,联氨和NO 可作
4 2 4
为火箭推进剂的主要原因为_______________________________。
【答案】(每空2分)(1)N(g)+3H(g)===2NH (g) ΔH=-92 kJ·mol-1
2 2 3
(2)①大于 ②akJ·mol-1 ③A(g)+B (g)===2AB(g) ΔH=+(a-b)kJ·mol-1
2 2
(3) 2ΔH-2ΔH -ΔH 反应放热量大、产生大量气体、无污染
3 2 1【解析】(1)N 与H 反应生成NH 的化学方程式为N(g)+3H (g)=2NH(g),该反应的ΔH=反应
2 2 3 2 2 3
物的键能总和-生成物的键能总和=E(N≡N)+3E(H—H)-6E(N—H)=946kJ/mol+3×436kJ/
mol-6×391kJ/mol=-92kJ/mol;N 与H 反应生成NH 的热化学方程式为:N(g)+3H (g)=2NH(g)
2 2 3 2 2 3
ΔH=-92kJ/mol。
(2)①1molA (g)和1molB (g)具有的总能量小于2molAB(g)具有的总能量,反应A(g)+B
2 2 2 2
(g)=2AB(g)为吸热反应,ΔH大于0。
②根据图像,反应物的总键能为akJ/mol。
③根据图像,该反应的ΔH=+(a-b)kJ/mol,该反应的热化学方程式为:A(g)+B (g)=2AB(g)
2 2
ΔH=+(a-b)kJ/mol。
(3)N原子最外层有5个电子,H原子最外层有1个电子,根据价键规则,NH 的电子式为 ,
2 4
NH 的结构式为 。应用盖斯定律,消去O(g)、H(g),将③×2-①-②×2得④,则
2 4 2 2
ΔH=2ΔH -ΔH -2ΔH 。根据反应④知,联氨和NO 可作为火箭推进剂的主要原因为:反应放热量大、产生
4 3 1 2 2 4
大量气体、无污染。