文档内容
第 18 讲 化学反应速率
1.等质量的锌与过量盐酸在不同的实验条件下进行反应,实验数据见下表。收集相同条件下相同体积的
氢气,所需时间最短的一组是
组别 A B C D
温度/℃ 50 50 30 30
锌的状
粉末 块状 粉末 块状
态
【答案】A
【解析】影响化学反应速率的因素有反应物浓度、反应温度、压强、催化剂以及接触面积等。A、B两组
温度均为50℃,但A组为粉末接触面积大于B组,所以反应速率A>B;同理可得C>D,A、C均为粉
末,但A组的反应温度高于C,所以反应速率A>C,故A正确;答案选A。
2.已知 的速率方程为 (k为速率常数,只与温度、催化剂有
关)。实验测得, 在催化剂X表面反应的变化数据如下:
t/min 0 10 20 30 40 50 60 70
0.100 0.080 0.040 0.020 0
下列说法正确的是
A. ,
B. min时,
C.相同条件下,增大 的浓度或催化剂X的表面积,都能加快反应速率
D.保持其他条件不变,若 起始浓度为0.200 mol·L ,当浓度减至一半时共耗时50 min
【答案】D
【分析】根据表中数据分析,该反应的速率始终不变, 的消耗是匀速的,说明反应速率与 无
关,故速率方程中n=0;【解析】A.由分析可知,n=0,与 浓度无关,为匀速反应,每10min一氧化二氮浓度减小0.02
,则 ,A错误;
B.由分析可知,n=0,与 浓度无关,为匀速反应,t=10min时瞬时速率等于平均速率 =
= ≠ ,B错误;
C.速率方程中n=0,反应速率与 的浓度无关,C错误;
D.保持其他条件不变,该反应的反应速率不变,即为 ,若起始浓度 ,
减至一半时所耗时间为 =50min,D正确;
答案选D。
3.2SO (g)+O(g) 2SO (g) ∆H=-198kJ•mol-1。在VO 存在时该反应机理为:
2 2 3 2 5
①VO+SO→2VO +SO(快);②4VO +O →2VO(慢)。下列说法不正确的是
2 5 2 2 3 2 2 2 5
A.该反应速率主要由第②步基元反应决定
B.由反应机理可知,VO 和VO 都是该反应的催化剂
2 5 2
C.VO 的存在提高了该反应活化分子百分数,使单位时间内有效碰撞次数增加,反应速率加快
2 5
D.逆反应的活化能比正反应的活化能大198kJ•mol-1
【答案】B
【解析】A.反应①为快反应,反应②为慢反应,总反应速率由最慢的一步决定,该反应速率主要取决于
慢反应,即第②步反应,故A正确;
B.根据反应机理可知,VO 是反应的催化剂,而VO 是中间产物,故B错误;
2 5 2
C.根据反应机理可知,VO 是反应的催化剂,所以提高了该反应活化分子百分数,使有效碰撞次数增
2 5
加,反应速率加快,故C正确;
D.∆H=正反应的活化能﹣逆反应的活化能=-198kJ/mol,所以逆反应的活化能大于198kJ/mol,故D正
确;
故选B。
4.反应2NO(g)+2H (g) N(g)+2HO(g),每生成1molN ,放出664kJ的热量,该反应的速率表达式为
2 2 2 2
⇌(k、m、n待测,k为速率常数,一般只受温度影响),其反应过程包含下列两步:①
(慢);② (快)。T℃时测得有关实验数据如下:
序号 c(NO)/(mol·L-1) c(H)/(mol·L-1) 速率/(mol·L-1·min-1)
2
I 0.0060 0.0010
Ⅱ 0.0060 0.0020
Ⅲ 0.0010 0.0060
Ⅳ 0.0020 0.0060
下列说法正确的是
A.HO 是该反应的催化剂
2 2
B.该反应的快慢主要取决于步骤①
C.该反应速率表达式中m=n=1
D.向容器中充入2molNO和2molH ,充分反应后,放出664kJ的热量
2
【答案】B
【解析】A.两步反应① (慢);② (快),可得出 是该反应的中间
产物,故A错误。
B.反应的快慢主要取决于慢反应,即步骤①,故B正确。
C.根据序号I、Ⅱ得到 ,则n=1,根据序号Ⅲ、Ⅳ得到,
则m=2,故C错误。
D.每生成7gN,放出166kJ的热量,则反应生成1mol氮气(质量28g)时放出664kJ的热量,但此反应为可
2
逆反应,充入2molNO和2molH 转化率小于100%,放出的热量小于664kJ。故D错误。
2,
故选B。
5.下列各组反应刚开始时,放出H 速率最大的是
2
选 物质的 酸的体
金属 酸的浓度 反应温度
项 量 积(粉末状)
A Al 0.1 mol 18.4 mol·Lˉ1 浓HSO 10 mL 60℃
2 4
B Zn 0.1 mol 3 mol·Lˉ1 HCl 10 mL 30℃
C Fe 0.1 mol 18.4 mol·Lˉ1 浓 HSO 10 mL 60℃
2 4
D Zn 0.1 mol 3 mol·Lˉ1 CHCOOH 10 mL 30℃
3
【答案】B
【解析】Al和浓硫酸发生在加热条件下反应生成二氧化硫,不是氢气,选项A错误;Fe与浓硫酸发生钝
化,加热也无氢气生成,选项C错误;而B和D相比较,反应温度相同,均为活泼性相同的金属,但B中
盐酸为强酸,氢离子浓度较大,则B反应速率最大;
答案选B。
6.下列有关碰撞理论的说法正确的是
A.活化分子数目越多,反应速率越快 B.反应速率与有效碰撞次数成正比
C.活化分子的平均能量就是活化能 D.升高温度,活化分子百分数增大,反应速率加快
【答案】D
【解析】A.单位体积的活化分子数越多,单位时间内有效碰撞次数越多,反应速率越快,A错误;
B.反应速率与单位时间内有效碰撞次数成正比,B错误;
C.活化分子的平均能量与所有分子的平均能量之差称为活化能,C错误;
D.升高温度,活化分子百分数增大,单位体积活化分子数增多,反应速率加快,D正确;
故选D。
7.在一定温度下,某密闭容器中发生反应:2C(g) A(g)+2B(s) ΔH>0,若0~10 s内c(C)由0.1 mol·L-1
降到0.08 mol·L-1,则下列说法正确的是
A.0~10 s内用B表示的平均反应速率为v(B)=0.002 mol·L-1·s-1
B.c(C)由0.1 mol·L-1降到0.04 mol·L-1所需的反应时间小于5 s
C.升高温度正反应速率加快,逆反应速率减慢
D.减小反应体系的体积,化学反应速率加快
【答案】D
【解析】A.B为固体,不能用固体的浓度变化表示反应速率,A错误;
B.c(C)由0.1 mol·L-1降到0.08 mol·L-1,所需的反应时间为10s,浓度越小,反应速率越慢,所以c(C)由
0.1 mol·L-1降到0.04 mol·L-1所需的反应时间一定大于5 s,B错误;
C.升高温度,反应物分子碰撞的次数增多,正、逆反应速率均加快,C错误;D.减小反应体系的体积,各气体的浓度增大,化学反应速率加快,D正确;
故选D。
8.一定条件下,酸性 溶液与 发生反应, (Ⅱ)起催化作用,过程中不同价态含 粒子
的浓度随时间变化如下图所示。下列说法正确的是
A. (Ⅲ)不能氧化
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下, (Ⅱ)和 (Ⅶ)不能大量共存
D.总反应为:
【答案】C
【分析】开始一段时间(大约13min前)随着时间的推移Mn(Ⅶ)浓度减小直至为0,Mn(Ⅲ)浓度增大直至
达到最大值,结合图像,此时间段主要生成Mn(Ⅲ),同时先生成少量Mn(Ⅳ)后Mn(Ⅳ)被消耗;后来(大
约13min后)随着时间的推移Mn(Ⅲ)浓度减少,Mn(Ⅱ)的浓度增大;据此作答。
【解析】A.由图像可知,随着时间的推移Mn(Ⅲ)的浓度先增大后减小,说明开始反应生成Mn(Ⅲ),后
Mn(Ⅲ)被消耗生成Mn(Ⅱ),Mn(Ⅲ)能氧化HC O,A项错误;
2 2 4
B.随着反应物浓度的减小,到大约13min时开始生成Mn(Ⅱ),Mn(Ⅱ)对反应起催化作用,13min后反应
速率会增大,B项错误;
C.由图像可知,Mn(Ⅶ)的浓度为0后才开始生成Mn(Ⅱ),该条件下Mn(Ⅱ)和Mn(Ⅶ)不能大量共存,C项
正确;
D.HC O 为弱酸,在离子方程式中应以化学式保留,总反应为2 +5H C O+6H+=2Mn2+
2 2 4 2 2 4
+10CO ↑+8H O,D项错误;答案选C。
2 2
9.某研究小组以反应 为例探究外界条件对化学反应速率的影响。实验时,分别量取 溶液和酸性 溶液,迅速混合并开始计时,通过测定溶液褪色
所需时间来判断反应的快慢。下列说法错误的是
酸性溶液 溶液
实验序 实验温 溶液颜色褪至无色所用时
号 度/℃ 间/s
V/mL V/mL V/mL
① 20 2 0.02 4 0.1 0
② 20 2 0.02 2 0.1 2 8
③ 45 2 0.02 2 0.1 x
A.
B. ,
C.配制 溶液时可用硫酸酸化
D.利用实验②③探究温度对化学反应速率的影响
【答案】B
【解析】A.实验②和③只是温度不同,目的是探究温度对反应速率的影响,除温度外,其它条件应相
同,则水的体积需要保持一致,因此x=2,故A正确;
B.分析表中数据可知,实验①和实验②只是浓度不同,则实验①和实验②是探究反应物浓度对化学反应
速率的影响,且浓度越大,反应速率越大,可知t<8,实验②和③只是温度不同,目的是探究温度对反应
1
速率的影响,温度越高,反应速率越快,则t<8,故B错误;
2
C.高锰酸钾能氧化氯离子生成氯气,配制KMnO 溶液时不能用盐酸酸化,应该用稀硫酸,故C正确;
4
D.实验①③中温度和草酸的浓度均是变量,不能利用实验①③探究温度对化学反应速率的影响,应该用
实验②和③,故D正确;故选B。
10.一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列
描述正确的是A.反应开始到10 s时,用Z表示的反应速率为0.158 mol·L-1·s-1
B.反应开始到10 s时,X的物质的量浓度减少了0.79 mol·L-1
C.反应到达10 s时,c(Y)=0.105 mol·L-1·s-1
D.反应的化学方程式为X(g)+Y(g) 2Z(g)
【答案】D
【分析】各物质相关物理量的变化如表所示: 反应的化学方程式为X(g)+Y(g) 2Z(g)。
X Y Z
物质的量变化/mol 1.20-0.41=0.79 1.00-0.21=0.79 1.58-0=1.58
浓度变化/mol·L-1 =0.395 =0.395 =0.79
反应速率/mol·L-1·s-1 0.039 5 0.039 5 0.079
反应速率之比 1∶1∶2
【解析】A.由图可知,10s内Z的物质的量变化量为1.58mol,用Z表示的反应速率为v(Z)=0.079moL/
(L·s),故A错误;
B.由图可知,10s内X的物质的量变化量为0.79mol,X的物质的量浓度减少了△c=
=0.395mol·L-1,故B错误;
C.10s内,用Y表示的反应速率为v(Y)= =0.0395moL/(L·s),故C错误;
D.由图像可以看出,由图表可知,随反应进行X、Y的物质的量减小,Z的物质的量增大,所以X、Y是
反应物,Z是生产物,l0s后X、Y、Z的物质的量为定值,不为0,反应是可逆反应,且△n(X):△n(Y):
△n(Z)=(1.20-0.41)mol:(1.00-0.21)mol:1.58mol=1:1:2,参加反应的物质的物质的量之比等于化学计量
数之比,故反应化学方程式为X(g)+Y(g) 2Z(g),故D正确;故选D。11.下列有关化学反应速率的实验探究方案设计合理的是
选
实验方案 实验目的
项
比较Cu2+
向等体积等浓度的HO 溶液中分别加入5滴等浓度的CuSO 和FeCl 溶液,观察气体产
A 2 2 4 3 和Fe3+的
生的速度
催化效果
探究草酸
两支试管,都加入2mL1mol/L的酸性KMnO 溶液,再同时向两支试管分别加入
4 浓度对反
B 2mL0.1mol/L的HC O 溶液和2mL0.05mol/L的HC O 溶液,观察高锰酸钾溶液褪色所
2 2 4 2 2 4 应速率影
需时间
响
在锥形瓶内各盛有2g锌粒(颗粒大小基本相同),然后通过分液漏斗分别加入
40mL1mol/L和40mL18mol/L的硫酸。比较两者收集10mL氢气所用的时间
探究硫酸
浓度对反
C
应速率影
响
探究温度
D 对反应速
率的影响
【答案】D
【解析】A.阴离子不同,无法比较Cu2+和Fe3+的催化效率,A错误;
B.两组实验中草酸均不足量,高锰酸钾均无法褪色,B错误;
C.18mol·L-1的硫酸为浓硫酸,浓硫酸锌粒反应生成物为SO ,无H 产生,无法比较产生H 的速率,C错
2 2 2
误;
D.反应物浓度和压强均相同,只有温度不同,可以用来探究温度对反应速率的影响,D正确;
故选D。
12.采取下列措施对增大化学反应速率有明显效果的是
A.N 和H 合成NH 时,不断分离出产物NH
2 2 3 3
B.Fe与稀硫酸反应制取H 时,改用浓硫酸
2
C.NaSO 溶液与BaCl 溶液反应时,增大压强
2 4 2
D.大理石与盐酸反应制取CO 时,将块状大理石改为粉末状大理石
2
【答案】D【解析】A.N 和H 合成NH 时,不断分离出NH ,生成物的浓度降低,且随着反应进行反应物浓度也降
2 2 3 3
低,化学反应速率降低,A错误;
B.常温下Fe遇浓硫酸发生钝化,无法增大反应速率,B错误;
C.NaSO 溶液和BaCl 溶液反应,两者都是溶液,反应速率不受压强的影响,增大压强反应速率不变,C
2 4 2
错误;
D.大理石与盐酸反应制备CO,将块状大理石换成粉末状大理石,大理石与盐酸的接触面积增大,反应
2
速率增大,D正确;
故选D。
13.实验室中利用锌粒和稀硫酸反应制备氢气,下列措施不能增大氢气生成速率的是
A.用98%的浓硫酸代替稀硫酸 B.用锌粉代替锌粒
C.用镁粒代替锌粒 D.升高温度
【答案】A
【解析】A.锌和浓硫酸反应不生成氢气,用98%的浓硫酸代替稀硫酸不能增大氢气生成速率,故A选;
B.用锌粉代替锌粒可以增大接触面积,增大反应速率,故B不选;
C.镁的活泼性比锌强,用镁粒代替锌粒,可以加快反应速率,故C不选;
D.升高温度,可以加快反应速率,故D不选;
故选A。
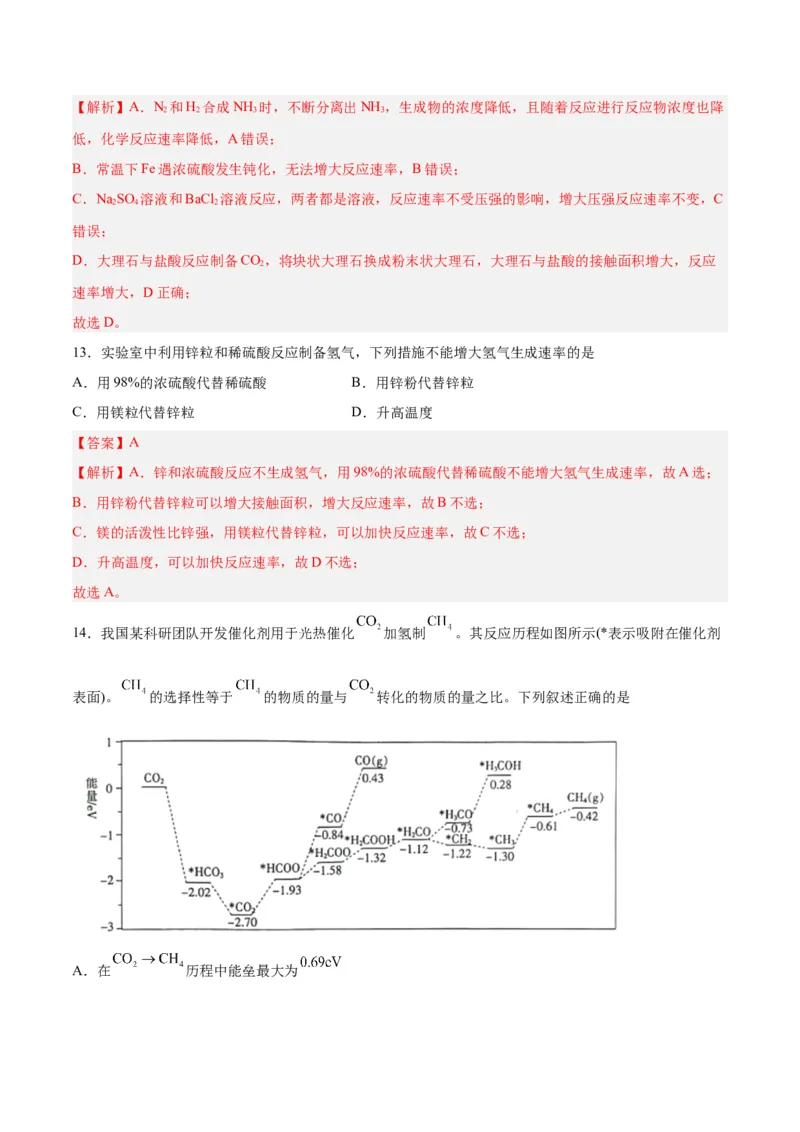
14.我国某科研团队开发催化剂用于光热催化 加氢制 。其反应历程如图所示(*表示吸附在催化剂
表面)。 的选择性等于 的物质的量与 转化的物质的量之比。下列叙述正确的是
A.在 历程中能垒最大为B.该反应历程中, 的选择性为100%
C.催化剂表面上 、CO脱附都会放出能量
D.反应历程中有极性键的断裂与形成
【答案】D
【解析】A.由图可知,在 历程中能垒最大的是 的能垒为0.77eV,故A错
误;
B.CO 加氢生成了副产物CO、CHOH、CH 的选择性小于100%,B项错误;
2 3 4
C.由图可知, 是脱附过程,需要吸收能量,C项错误;
D.反应历程中 过程中有极性键的断裂, 过程中有极性键的生成,故D
正确;故选D。
15.在一定条件下,发生反应:CO(g)+3H(g)﹦CH OH(g)+ HO(g),前10s内,H 的平均反应速率为
2 2 3 2 2
,则10s末,容器中CHOH的物质的量浓度为
3
A.0.4mol·L-1 B.0.8mol·L-1 C.1.2 mol·L-1 D.1.8 mol·L-1
【答案】A
【解析】根据题干信息可知,前10s内,H 消耗的物质的量浓度为 ,因体
2
积不变,反应的浓度之比等于系数之比,设生成的CHOH的物质的量浓度为x,则有 ,解x=
3
,故选A。
16.一定温度下,利用测压法在刚性反应器中研究固体催化剂作用下的A的分解反应:
。体系的总压强p随时间t的变化如表所示:
t/min 0 100 150 250 420 500 580
p/kPa 12.1 13.3 13.9 15.1 17.14 x 19.06
下列说法不正确的是
A.100~150min,消耗A的平均速率为B.其他条件不变,420min时向刚性容器中再充入少量A,反应速率比原420min时大
C.推测x为18.1
D.升高体系温度,不一定能加快反应速率
【答案】B
【解析】A.反应 ,反应前后气体压强变化和生成C的量成正比,同时A的变化为
变化量的 ,用压强代表浓度,则100~150min体系压强变化=13.9kPa-13.3kPa=0.06kPa,消耗A的平均速
率= =0.006kPamin-1,故A正确;
⋅
B.其他条件不变,420min时向刚性容器中再充入少量A,相当于增大压强,反应在固体催化剂表面进
行,固体表面积一定,反应速率不变,故B错误;
C.0~100min,压强变化为1.2kPa,150min~250min,压强变化1.2kPa,则100kPa~500kPa,体系压强变
化1.2×4kPa=4.8kPa,则500min时,体系压强=13.3kPa+4.8kPa=18.1kPa,故C正确;
D.反应在催化剂表面反应,升高体系温度,催化剂活性减小时,反应速率减小,不一定能加快反应速
率,故D正确;
故选B。
17.反应C(s) +H O(g) CO(g) +H (g) ΔH >0,下列说法正确的是
2 2
A.其他条件不变时,增加碳的量,化学反应速率增大
B.其他条件不变时,升高温度,正反应速率增大,逆反应速率减小
C.其他条件不变时,缩小容器的容积,增大压强,化学反应速率增大
D.其他条件不变时,向容积不变的密闭容器中充入HO(g),正反应速率增大,逆反应速率减小
2
【答案】C
【解析】A.碳是固体,浓度为定值,只增大碳的量时化学反应速率不变,故A错误;
B.温度升高时,正、逆反应速率均增大,故B错误;
C.其他条件不变时,缩小容器的容积,增大压强,各物质浓度增大,化学反应速率增大,故C正确;
D.其他条件不变时,向容积不变的密闭容器中充入HO(g),等效为加压,则正反应速率增大,逆反应速
2
率相对原来的也增大,故D错误;故选C。
18.反应 在一容积可调的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
A.保持体积不变,冲入氮气使体系压强增大
B.将容器的体积缩小一半
C.增加水蒸气的量
D.保持压强不变。冲入氮气使容器体积变大
【答案】A
【解析】A.保持体积不变,冲入氮气使体系压强增大,但反应物浓度不变,反应速率不变,A符合;
B.将容器的体积缩小一半,浓度增大,反应速率加快,B不符合;
C.增加水蒸气的量,容器容积增大,生成物浓度减小,反应速率减小,C不符合;
D.保持压强不变,冲入氮气使容器体积变大,反应物浓度减小,反应速率减小,D不符合;
答案选A。
19.某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】
【实验内容及记录】
试管中所加试剂及其用量/mL
实验温
实验编号 0.6mol/L 3mol/L 0.05mol/L 溶液褪至无色所需时间/min
度
溶液 稀 溶液 溶液
① 25 5.0 3.0 2.0 5.0 1.4
② 25 4.0 2.0 5.0 2.6
③ 50 5.0 3.0 2.0 5.0 0.9
(1)请完成此实验设计,其中: 。
(2)探究浓度对化学反应速率的影响,应选择 (填实验编号)。
(3)根据上表中实验①、③的数据,可以得到的结论是 。
(4)该小组同学根据经验绘制了 随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发
现,该实验过程中 随时间变化的实际趋势如图2所示。该小组同学根据图2所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
试管中所加试剂及其用量/mL
实验 实验温 0.6mol/L 3mol/L 再向试管中加入 溶液褪至无色
编号 度/℃ 0.05mol/L 某种固体 所需时间/min
溶 稀 溶液
液 溶液
④ 25 5.0 3.0 2.0 5.0 t
①该小组同学提出的假设是 。
②若该小组同学提出的假设成立,t的大小范围是 。
(5)某研究小组同学要测定市售草酸晶体样品的纯度,先称取5.0g样品配成100mL溶液,分别量取25.00mL
溶液于锥形瓶中,用0.2mol/L 标准溶液滴定,滴定到达终点的现象是 ,若三次滴定消耗
标准溶液的平均体积为25.00mL,则该草酸样品的纯度为 。
【答案】(1)4.0
(2)①②
(3)其他条件不变时,升高(降低)温度,化学反应速率加快(减慢)
(4) 生成物中的 为该反应的催化剂(或 对该反应有催化作用) t<1.4min
(5) 当滴入最后半滴酸性 溶液后溶液由无色变为浅紫色,且半分钟内不褪色 90.0%
【解析】(1)实验①② 浓度不同,探究的是草酸浓度对反应速率的影响,需要保持溶液总体积相
同,由于所加硫酸的体积相同,则 5.0+3.0-4.0=4.0;(2)实验①② 浓度不同,其他条件相同,则探究浓度对化学反应速率的影响,应选择①②;
(3)实验①、③的温度不同,其他条件相同,根据溶液褪色时间,可以得到的结论是其他条件不变时,
升高(降低)温度,化学反应速率加快(减慢);
(4)①根据锰离子物质的量的变化曲线,该小组同学提出的假设是生成物中的 为该反应的催化剂
(或 对该反应有催化作用);
②若锰离子为反应的催化剂,反应速率加快,溶液褪色时间变短,若该小组同学提出的假设成立,t<
1.4min;
(5) 标准溶液为紫红色,滴定到达终点时的现象是当滴入最后半滴酸性 溶液后溶液由无
色变为浅紫色,且半分钟内不褪色;根据
,若三次滴定消耗 标准溶液的平
均体积为25.00mL,则该草酸样品的纯度为 ×100%=90.0%。
20.硫代硫酸钠( )俗称大苏打或海波,在碱性条件下稳定,遇酸易分解。将 通入按一定比例配
成的 和 的混合溶液中,便可得到 ,同时生成 。
Ⅰ.制备
(1)仪器A的名称为 ,装置D的作用是 ,B中的试剂最好选用 (填序号)。
A.稀 B.NaOH溶液
C.饱和 溶液 D.饱和 溶液
(2)写出C中反应的离子方程式为 。
(3)写出一种可以提高装置C中 吸收效率的方法 。
(4)为保证硫代硫酸钠的产量,实验中产生的 不能过量,原因是 ;
Ⅱ.探究 的部分化学性质
(5)从S的化合价推测 具有较强的还原性。请设计实验验证 具有还原性 。
Ⅲ. 的应用
已知: 。
某同学探究 与稀 反应的速率影响因素时,设计了如下系列实验:
溶液 稀
实验序号 反应温度/℃
① 20 10.0 0.10 10.0 0.50 0
② 40 10.0 0.10 0.50 0
③ 20 0.10 4.0 0.50
(6)实验①、②可探究 对反应速率的影响,因此 ;
(7)实验①、③可探究 对反应速率的影响,因此 , 。
【答案】(1)圆底烧瓶 安全瓶(或防倒吸) C
(2)
(3)控制二氧化硫的流速、适当增大C中混合液的浓度、适当升高C中溶液温度等(4)若 过量,溶液显酸性,产物 分解,产率降低
(5)取适量酸性 溶液(或加有淀粉溶液的碘水)于试管中,滴加 溶液,若溶液褪色,则说明
有还原性(或取适量 溶液于试管中,滴加几滴酸性 溶液(或加有淀粉溶液的碘水),
若溶液褪色,则说明 有还原性)
(6) 温度 10.0
(7) 浓度 10.0 6.0
【分析】利用亚硫酸钠固体与70%的硫酸反应制备二氧化硫,所得二氧化硫通入硫化钠和碳酸钠的混合溶
液中反应,制备 ,产生的二氧化硫利用装置E吸收;再利用 与稀硫酸反应探究浓度等条
件对化学反应速率的影响;
【解析】(1)根据仪器的构造可知,仪器A为圆底烧瓶;装置D是为了防止装置E中的溶液进入装置
D,其作用是安全瓶(或防倒吸),B装置主要为平衡气压、控制气流速度,以及防止倒吸的作用,试剂最好
选用饱和 溶液,答案选C;
(2)C中硫化钠、碳酸钠与二氧化硫反应生成硫代硫酸钠和二氧化碳,反应的离子方程式为
;
(3)控制二氧化硫的流速、适当增大C中混合液的浓度、适当升高C中溶液温度等都可以提高装置C中
吸收效率;
(4)为保证硫代硫酸钠的产量,实验中产生的 不能过量,原因是若 过量,溶液显酸性,产物
分解,产率降低;
(5)取适量酸性 溶液(或加有淀粉溶液的碘水)于试管中,滴加 溶液,若溶液褪色,则说
明 有还原性(或取适量 溶液于试管中,滴加几滴酸性 溶液(或加有淀粉溶液的碘水),若溶液褪色,则说明 有还原性);
(6)分析实验①、②可知,温度不同,则实验①、②可探究温度对反应速率的影响,其他条件应相同,
故 10.0;
(7)分析实验①、③可知,硫酸所用体积不同,故其他条件应该相同,故实验①、③可探究 浓度
对反应速率的影响,满足除硫酸的用量不同,但所用溶液的总体积相等,因此10.0, 6.0。