文档内容
第 19 讲 化学平衡
1. ,是工业制硫酸中的一步重要反应。在一定条件下,当反应达到平
衡状态时,下列叙述正确的是
A. 的浓度保持不变 B. 能全部转化为
C.正、逆反应速率均为零 D.使用合适的催化剂是为了提高 的平衡转化率
2.一定温度下,在 恒容密闭容器中加入足量铁粉并充入一定量的 气体,发生反应
。下列说法不正确的是
A. 时, 的平均反应速率为
B.充入 ,容器内压强增大,则化学反应速率增大
C. 时, ,反应未达到平衡状态
D. 后,混合气体的平均分子量为35.1
3.在一定温度下,恒容密闭容器中进行反应 ,下列说法正确的是
A.反应一段时间后 只存在于 和 中
B.向容器中通入少量 ,反应速率增大
C.达到平衡状态时, 与 物质的量之比一定为1∶1D.容器内密度不再变化时,判定反应已经达到平衡状态
4.一定温度下,在 NO 的四氯化碳溶液(100 mL)中发生分解反应:2NO 4NO +O 。在不同时刻测量
2 5 2 5 2 2
放出的 O 体积,换算成 NO 浓度如表:
2 2 5
t/s 0 600 1 200 1 710 2 220 2 820 x
c(NO)/(mol·L-1) 1.40 0.96 0.66 0.48 0.35 0.24 0.12
2 5
下列说法正确的是
A.600~1 200 s,生成 NO 的平均速率为 5.0×10-4mol·L-1·s-1
2
B.反应 2220 s 时,放出的 O 体积为 11.8 L(标准状况)
2
C.反应达到平衡时,2v 正(N O)=v 逆(NO )
2 5 2
D.推测上表中的 x 为 4930
5.在一恒容密闭容器中放入一定量的 ,发生反应
,下列说法正确的是
A.当 质量不变时,该反应达到平衡状态
B.若 ,则反应达到平衡状态
C.反应达到平衡时,升高温度,正反应速率大于逆反应速率
D.反应物的总能量小于生成物的总能量
6.含氮物质可发生如下反应:①
②
③
下列说法正确的是
A.常温下,NO与 混合能立即看到红棕色气体,说明该反应已达平衡
B.反应②的
C.反应③消耗 ,理论上会生成标准状况下约
D.利用反应①、②、③可以同时处理 含量较高的废气和含 的废水7.在恒温恒容下,可逆反应N(g)+ 3H (g) 2NH (g)达到平衡状态的标志是
2 2 3
A.N、H、NH 在容器中共存 B.混合气体的密度不再发生变化
2 2 3
C.混合气体的压强不再发生变化 D.v (N )=2v (NH )
正 2 逆 3
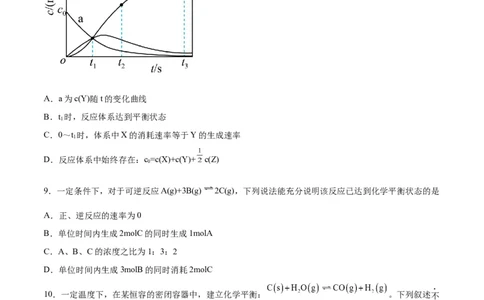
8.反应X→2Z经历两步:①X→Y;②Y→2Z。反应体系中X、Y、Z的浓度c随时间t的变化曲线如图所
示。下列说法正确的是
A.a为c(Y)随t的变化曲线
B.t 时,反应体系达到平衡状态
1
C.0~t 时,体系中X的消耗速率等于Y的生成速率
1
D.反应体系中始终存在:c=c(X)+c(Y)+ c(Z)
0
9.一定条件下,对于可逆反应A(g)+3B(g) 2C(g),下列说法能充分说明该反应已达到化学平衡状态的是
A.正、逆反应的速率为0
B.单位时间内生成2molC的同时生成1molA
C.A、B、C的浓度之比为1:3:2
D.单位时间内生成3molB的同时消耗2molC
10.一定温度下,在某恒容的密闭容器中,建立化学平衡: 。下列叙述不
能说明该反应已达到化学平衡状态的是
A.气体的密度不再发生变化 B.
C.气体的压强不再发生变化 D.生成 ,同时生成
11.在恒温恒容的密闭容器中,对于可逆反应 ,不能说明其已达到平衡状态的是
A.容器中固体质量不随时间而变化
B.容器中混合气体的总物质的量不随时间而变化
C.容器中气体的密度不随时间而变化
D. 的比值保持不变
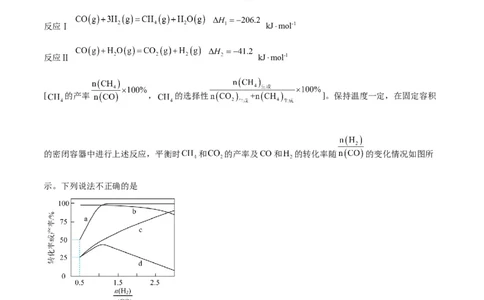
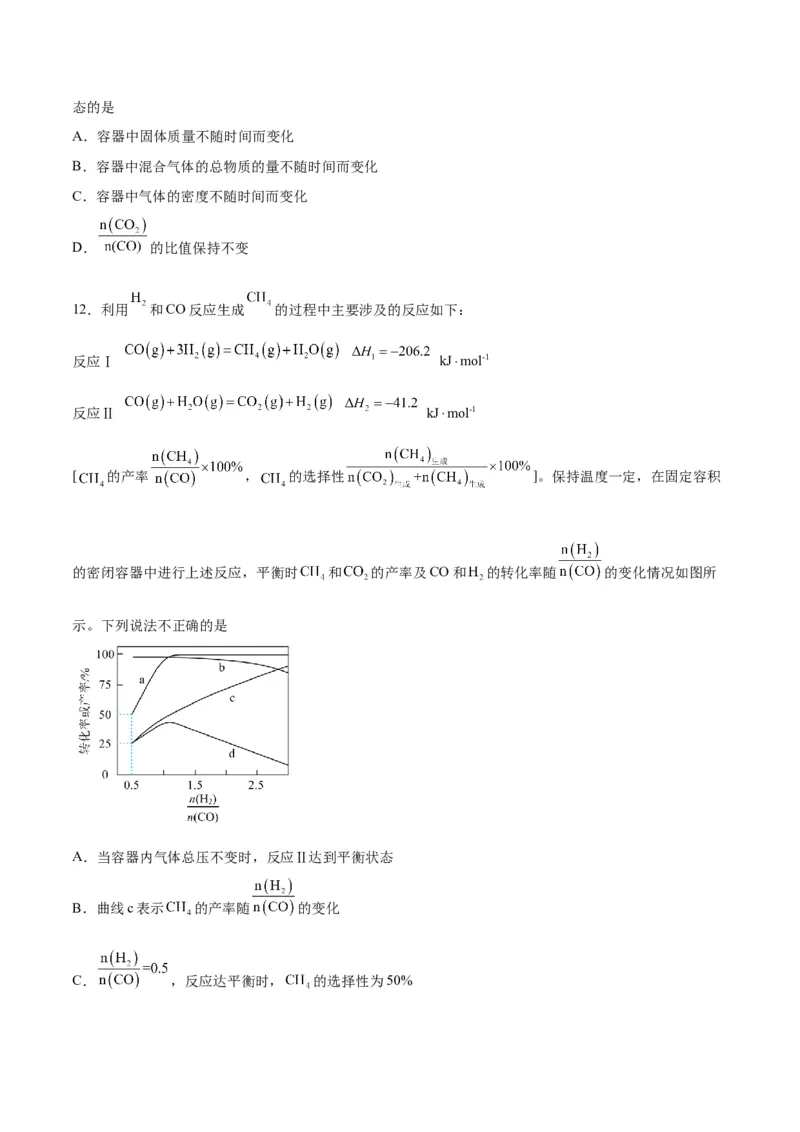
12.利用 和CO反应生成 的过程中主要涉及的反应如下:
反应Ⅰ kJ⋅mol-1
反应Ⅱ kJ⋅mol-1
[ 的产率 , 的选择性 ]。保持温度一定,在固定容积
的密闭容器中进行上述反应,平衡时 和 的产率及CO和 的转化率随 的变化情况如图所
示。下列说法不正确的是
A.当容器内气体总压不变时,反应Ⅱ达到平衡状态
B.曲线c表示 的产率随 的变化
C. ,反应达平衡时, 的选择性为50%D.随着 增大, 的选择性先增大后减小
13.在一定温度下的定容密闭容器中,取一定量的A、B于反应容器中,当下列物理量不再改变时,表明
反应:A(s)+2B(g) C(g)+D(g)已达平衡的是
A.混合气体的压强 B.混合气体的密度
C.A的浓度 D.气体的总物质的量
14.一定温度下,在体积为 的恒容密闭容器中,某一反应中 、 、 三种气体的物质的量随时间变
化的曲线如图所示,下列表述中正确的是
A.反应的化学方程式为
B. 时,正、逆反应都不再继续进行,反应达到化学平衡
C.若 ,则 内,X的化学反应速率为
D.温度、体积不变, 时刻充入 使压强增大,正、逆反应速率都增大
15.一定条件下,将CO与 以体积比 置于密闭容器中,发生可逆反应
,下列能说明反应达到平衡状态的是
A.体系压强保持不变 B.混合气体颜色保持不变
C. 和NO的体积比保持不变 D.每消耗 的同时消耗
16.设 为阿伏加德罗常数的值。工业上制备高纯度硅的反应有:
①
②③
已知:H、Si的电负性依次为2.1、1.8.下列有关说法正确的是
A.①中,30g氧化剂含极性键数目为 B.②中,生成1g 时转移电子数为
C.②和③互为可逆反应 D.②和③的目的是除去粗硅中的杂质
17.在恒容的密闭容器中,将CO和H 的混合气体在催化剂作用下转化为甲醇的反应为CO(g)+2H(g)
2 2
CHOH(g) ΔH <0。能说明该反应达到平衡状态的是
3
A.混合气体的密度不再变化
B.CO和H 的物质的量之比不再变化
2
C.2v (H )=v (CHOH)
正 2 逆 3
D.CO在混合气体中的质量分数保持不变
18.NH 、NH Cl、NO、NO 、HNO 等是氮的重要化合物,工业合成氨的反应为N(g)+3H(g )
3 4 2 3 2 2
2NH (g) ΔH=-92.4kJ•mol-1。NH 可与酸反应制得铵盐,也可通过催化氧化生成NO,用于生产HNO。浓
3 3 3
氨水加到生石灰中,放出大量热量,促进NH ·H O分解,可用于实验室制取NH 。对于工业合成氨的反
3 2 3
应:N (g)+3H(g ) 2NH (g) ΔH=-92.4kJ•mol-1。下列说法正确的是
2 2 3
A.该反应为吸热反应
B.升高温度能加快反应速率
C.0.1molN 与0.3molH 充分反应可释放9.24kJ的能量
2 2
D.若3v(N )=v(H),该反应处于平衡状态
2 2
19.“有序介孔碳”和“纳米限域催化”的研究双双获得国家自然科学奖一等奖。利用介孔限域催化温室
气体 加氢制甲醇,再通过甲醇制备燃料和化工原料等,是解决能源问题与实现双碳目标的主要技术之
一、反应如下:
i.
ii.
iii.
(1) 。(2)绝热条件下,将 以体积比2∶1充入恒容密闭容器中,若只发生反应ii,下列可作为反应ii达到平
衡的判据是_______。
A. 与 比值不变 B.容器内气体密度不变
C.容器内气体压强不变 D. 不变
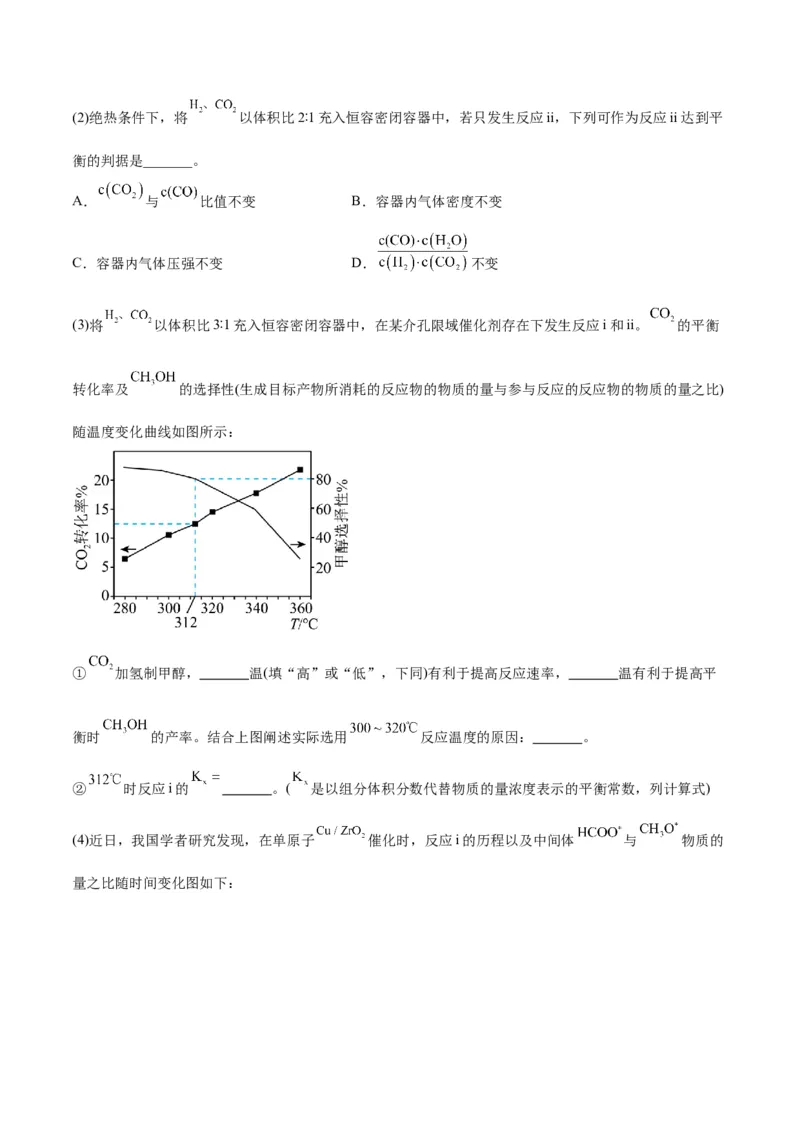
(3)将 以体积比3∶1充入恒容密闭容器中,在某介孔限域催化剂存在下发生反应i和ii。 的平衡
转化率及 的选择性(生成目标产物所消耗的反应物的物质的量与参与反应的反应物的物质的量之比)
随温度变化曲线如图所示:
① 加氢制甲醇, 温(填“高”或“低”,下同)有利于提高反应速率, 温有利于提高平
衡时 的产率。结合上图阐述实际选用 反应温度的原因: 。
② 时反应i的 。( 是以组分体积分数代替物质的量浓度表示的平衡常数,列计算式)
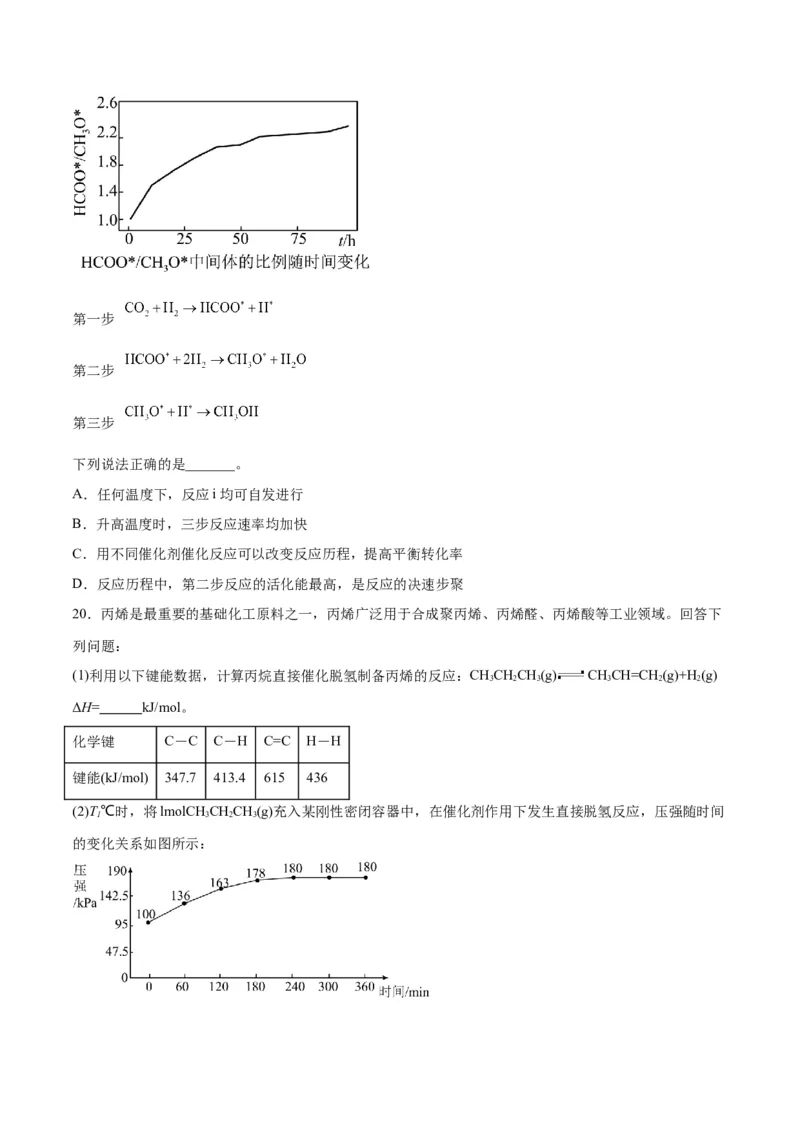
(4)近日,我国学者研究发现,在单原子 催化时,反应i的历程以及中间体 与 物质的
量之比随时间变化图如下:第一步
第二步
第三步
下列说法正确的是_______。
A.任何温度下,反应i均可自发进行
B.升高温度时,三步反应速率均加快
C.用不同催化剂催化反应可以改变反应历程,提高平衡转化率
D.反应历程中,第二步反应的活化能最高,是反应的决速步聚
20.丙烯是最重要的基础化工原料之一,丙烯广泛用于合成聚丙烯、丙烯醛、丙烯酸等工业领域。回答下
列问题:
(1)利用以下键能数据,计算丙烷直接催化脱氢制备丙烯的反应:CHCHCH(g ) CHCH=CH(g)+H(g)
3 2 3 3 2 2
ΔH= kJ/mol。
化学键 C-C C-H C=C H-H
键能(kJ/mol) 347.7 413.4 615 436
(2)T℃时,将lmolCHCHCH(g)充入某刚性密闭容器中,在催化剂作用下发生直接脱氢反应,压强随时间
1 3 2 3
的变化关系如图所示:①计算0~60min之间,H 分压的平均变化率为 kPa/min。
2
②T℃时,该反应的平衡常数K = kPa(分压=总压×物质的量分数)
1 p
(3)CO 是一种温和的氧化剂。研究发现CO 氧化丙烷脱氢的反应机理有两种:
2 2
①“一步法”:CO 与C H 催化作用下反应机理如图所示:
2 3 8
写出CO 与C H 反应的总化学方程式 。
2 3 8
②“二步法”:丙烷分子先脱氢生成丙烯和氢气,再发生CO(g)+H(g ) CO(g)+HO(g) ΔH=+41kJ/mol。
2 2 2
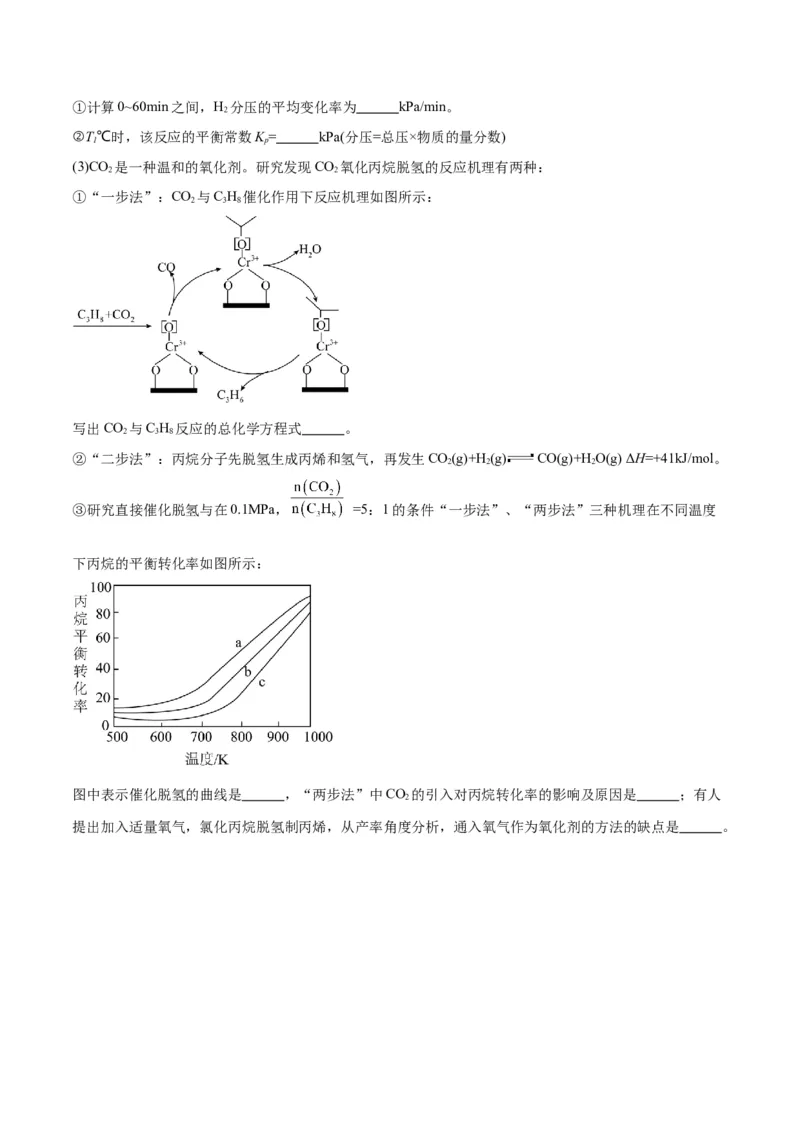
③研究直接催化脱氢与在0.1MPa, =5:1的条件“一步法”、“两步法”三种机理在不同温度
下丙烷的平衡转化率如图所示:
图中表示催化脱氢的曲线是 ,“两步法”中CO 的引入对丙烷转化率的影响及原因是 ;有人
2
提出加入适量氧气,氯化丙烷脱氢制丙烯,从产率角度分析,通入氧气作为氧化剂的方法的缺点是 。