文档内容
第 22 讲 水的电离与溶液的 pH
1.水是最宝贵的资源之一,下列表述正确的是
A.HO的电子式为
2
B.4℃时,纯水的pH=7
C.D16O中,质量数之和是质子数之和的两倍
2
D.273K、101kPa,22.4L水含有的原子个数为3N 个
A
2.下列关于溶液的酸碱性,说法正确的是
A.pH=7的溶液呈中性
B.中性溶液中一定有c(H+)=1.0×10-7 mol·L-1
C.若水电离出的c(OH- )=1.0×10-11mol·L-1,则溶液可能呈酸性,也可能呈碱性
D.在100℃时,纯水的pH<7,因此显酸性
3.用 试纸测定某无色溶液的 时,规范的操作是
A.将 试纸放入溶液中,观察其颜色变化,跟标准比色卡比较
B.将溶液倒在 试纸上,跟标准比色卡比较
C.用干燥的洁净玻璃棒蘸取溶液,滴在 试纸上,跟标准比色卡比较
D.在试管内放入少量溶液,把 试纸放在管口,观察颜色,跟标准比色卡比较
4.25℃时,水的电离达到平衡:H
2
O⇌H++OH-△H>0,下列叙述正确的是
A.向水中加入稀盐酸,水的电离平衡逆向移动,c(OH-)减小
B.向水中加入少量NaHSO 固体,c(H+)增大,K 增大
4 w
C.向水中加入少量固体Na,水的电离平衡逆向移动,c(H+)降低
D.将纯水加热,K 增大,pH不变
w
5.25℃时,水溶液中c(H+)与c(OH-)的变化关系如图中曲线所示,下列判断错误的是A.ac曲线上的任意一点都有c(H+)·c(OH-)=10-14
B.bd线段上任意一点对应的溶液都呈中性
C.d点对应的溶液pH<7
D.a点溶液可能是NaOH溶液
6.在相同温度下,0.01mol•L-1的醋酸溶液和0.01mol•L-1的盐酸相比,下列说法正确的是
A.由水电离出的c水(H+)相等
B.等体积两种溶液,与足量的锌粉反应产生的氢气物质的量不相同
C.两者都促进了水的电离
D.等体积两种溶液中和氢氧化钠能力相同
7.下列物质溶解于水时,电离出的阳离子能使水的电离平衡向右移动的是
A.NH Cl B.CHCOONa C.HSO D.KNO
4 3 2 4 3
8.室温下,下列各组离子在指定溶液中一定能大量共存的是
A.在 溶液中: 、 、 、
B.含大量 的溶液中: 、 、 、
C.加入Al产生 的溶液中: 、 、 、
D.由水电离的 的溶液中: 、 、 、
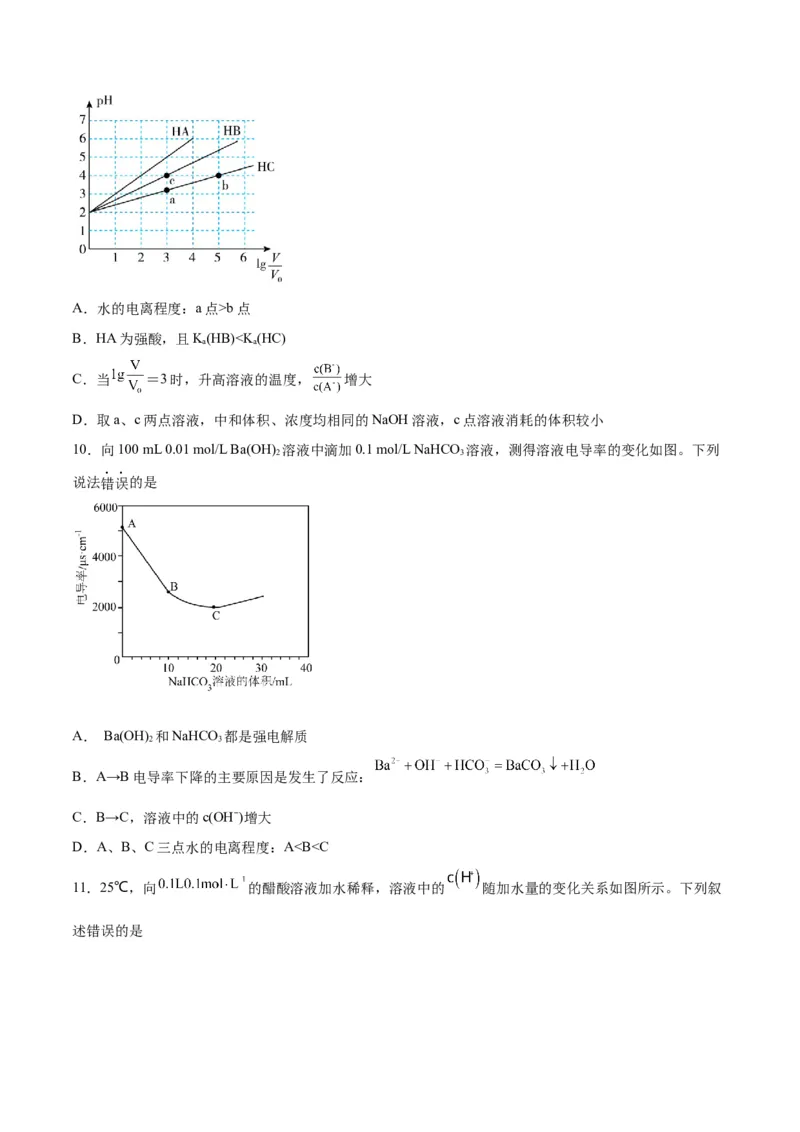
9.常温下,pH均为2、体积均为V 的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随
0
。的变化关系如图所示,下列叙述正确的是A.水的电离程度:a点>b点
B.HA为强酸,且K(HB)b>a B.水的电离程度:c>a
C.水的离子积 :b<c D.无限稀释后,pH趋近7
12.常温下,将0.2 mol/L氢氧化钠溶液与0.2 mol/L硫酸溶液等体积混合,该混合溶液的pH等于
A.1.0 B.3.0 C.7.0 D.13.0
13.常温下,pH=1的稀盐酸与pH=13的氢氧化钡溶液混合后pH=7,则V :V 为
酸 碱
A.1:1 B.2:1 C.1:2 D.1010:1
14. T℃时,水的离子积常数 ,该温度下, 的NaOH稀溶液与 的稀盐
酸充分反应(混合后的体积变化忽略不计),恢复到T℃,测得混合溶液的pH=3,则 的值为
A.9∶101 B.99∶101 C.1∶100 D.1∶1
15.T℃时,水的离子积常数 ,该温度下, 的NaOH稀溶液与 的稀盐酸
充分反应(混合后的体积变化忽略不计),恢复到T℃,测得混合溶液的 ,则 的值为
A.9∶101 B.99∶101 C.1∶100 D.1∶1
16.用标准的盐酸滴定未知浓度的NaOH溶液,下列各操作中,不会引起实验误差的是
A.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定
B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗后装入一定体积的NaOH溶液
C.取10.00 mL NaOH溶液放入洗净的锥形瓶中,再加入适量蒸馏水
D.取10.00 mL的NaOH溶液,放入锥形瓶后,把碱式滴定管尖嘴液滴吹去
17.实验小组进行实验检测菠菜中草酸和草酸盐的含量(均以草酸计),主要操作包括:
①菠菜样品研磨成汁,稀硫酸浸泡后取澄清溶液;
②转移定容①中的澄清溶液,得待测液;③移取20.00mL待测液,用 的酸性 溶液滴定。
上述操作中,未用到的仪器为
A. B. C. D.
18.用标准NaOH溶液滴定未知浓度的盐酸,若测定结果偏低,则原因可能是
A.用滴定管量取标准液时,先俯视后仰视
B.锥形瓶洗净后瓶内残留有少量蒸馏水
C.滴定到终点读数时,发现滴定管尖嘴处悬挂了一滴溶液
D.配制标准溶液的固体NaOH中混有NaO杂质
2
19.常温下,用 盐酸滴定 溶液,溶液中 、 、 的分布分数 随
变化曲线及滴定曲线如图。下列说法正确的是
已知:
A. B. 的 的值为
C.第一次突变,可选甲基橙作指示剂 D. 溶液呈酸性
20.向25 mL的滴定管中注入0.01 NaOH溶液至10.00 mL刻度处,再把管中的溶液全部放入锥
形瓶中,需用15.00 mL稀盐酸才能恰好中和,则所用稀盐酸的浓度为A.大于0.01 B.等于0.01
C.小于0.01 D.无法确定
21.酸碱中和滴定常见的误差分析 (标准液盐酸滴定待测液氢氧化钠)
V c
步骤 操作 标 待
准 测
酸式滴定管未用标准溶液润洗
碱式滴定管未用标准溶液润洗
洗涤
锥形瓶用待测溶液润洗
锥形瓶洗净后还留有蒸馏水
取液 放出碱液的滴定管开始有气泡,放出液体后气泡消失
酸式滴定管滴定前有气泡,滴定终点时气泡消失
振荡锥形瓶时部分液体溅出
滴定
部分酸液滴出锥形瓶外
溶液颜色较浅时滴入酸液过快,停止滴定后再加一滴NaOH溶液无变化
滴定前读数正确,滴定后俯视读数
读数
滴定前读数正确,滴定后仰视读数
22.图表是几种常见弱酸的电离平衡常数(25℃),回答下列各题:
酸 HCN HClO
电离平衡常数( )
(1)当温度升高时, 值 (填“增大”、“减小”或“不变”);
(2)结合表中给出的电离常数回答下列问题:
①上述四种酸中,酸性最弱、最强的酸分别是 、 (用化学式表示),
②下列能使醋酸溶液中 的电离程度增大,而电离平衡常数不变的操作是 (填序号),
A.升高温度 B.加水稀释 C.加少量的 固体 D.加少量冰醋酸③依据表中数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应
的离子方程式 。
(3)已知草酸是一种二元弱酸,其电离常数 , ,写出草酸的电离方程式
、 ,试从电离平衡移动的角度解释 的原因 。
(4)用食醋浸泡有水垢的水壶,可以清除其中的水垢,通过该事实 (填“能”或“不能”)比较醋酸与
碳酸的酸性强弱,请设计一个简单的实验验证醋酸与碳酸的酸性强弱。方案: 。