文档内容
第 23 讲 弱电解质的电离平衡
目录
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查弱电解质的电离特点
高频考点2 考查溶液导电性图像分析
高频考点3 考查外界条件对电离平衡的影响
高频考点4 考查强、弱电解质的判断与比较
高频考点5 考查电离常数的应用
高频考点6 考查电离平衡常数的有关计算
高频考点7 考查弱电解质的判断方法
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
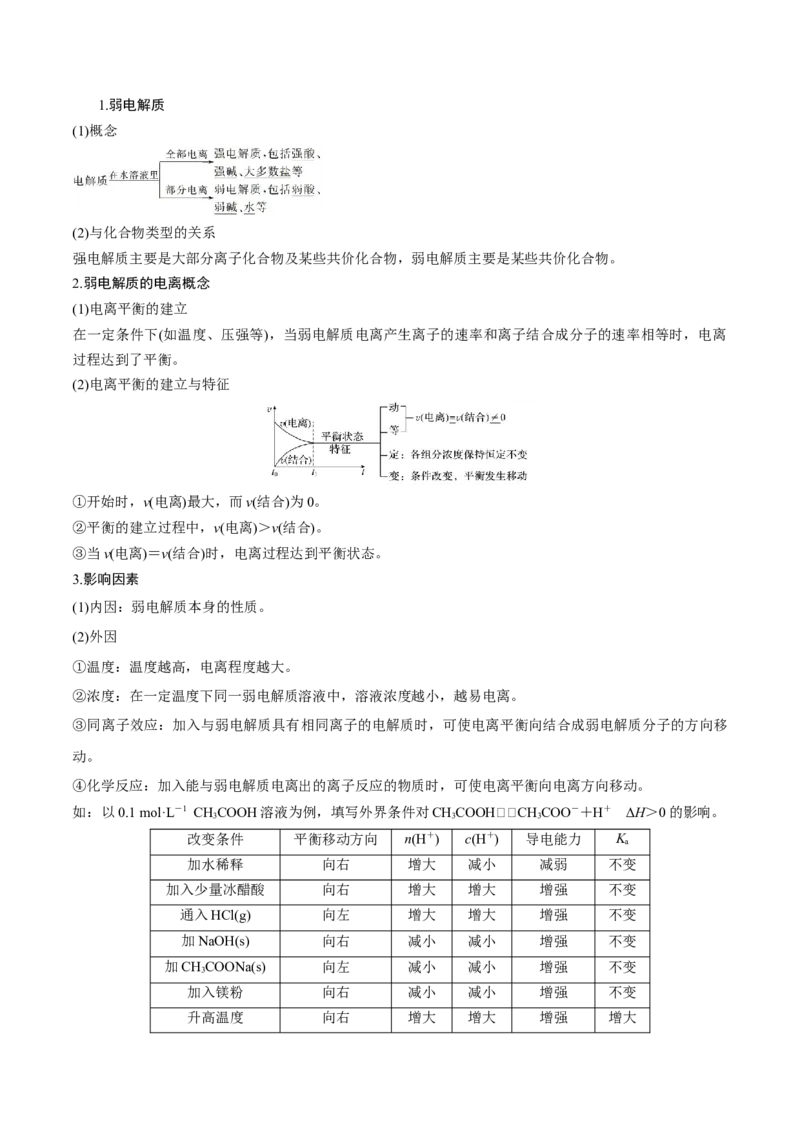
知识点一 弱电解质的电离平衡1.弱电解质
(1)概念
(2)与化合物类型的关系
强电解质主要是大部分离子化合物及某些共价化合物,弱电解质主要是某些共价化合物。
2.弱电解质的电离概念
(1)电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质电离产生离子的速率和离子结合成分子的速率相等时,电离
过程达到了平衡。
(2)电离平衡的建立与特征
①开始时,v(电离)最大,而v(结合)为0。
②平衡的建立过程中,v(电离)>v(结合)。
③当v(电离)=v(结合)时,电离过程达到平衡状态。
3.影响因素
(1)内因:弱电解质本身的性质。
(2)外因
①温度:温度越高,电离程度越大。
②浓度:在一定温度下同一弱电解质溶液中,溶液浓度越小,越易电离。
③同离子效应:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解质分子的方向移
动。
④化学反应:加入能与弱电解质电离出的离子反应的物质时,可使电离平衡向电离方向移动。
如:以0.1 mol·L-1 CHCOOH溶液为例,填写外界条件对CHCOOHCHCOO-+H+ ΔH>0的影响。
3 3 3
改变条件 平衡移动方向 n(H+) c(H+) 导电能力 K
a
加水稀释 向右 增大 减小 减弱 不变
加入少量冰醋酸 向右 增大 增大 增强 不变
通入HCl(g) 向左 增大 增大 增强 不变
加NaOH(s) 向右 减小 减小 增强 不变
加CHCOONa(s) 向左 减小 减小 增强 不变
3
加入镁粉 向右 减小 减小 增强 不变
升高温度 向右 增大 增大 增强 增大4.电离方程式的书写
(1)多元弱酸分步电离,且第一步电离程度远远大于第二步,如 HCO 的电离方程式:HCO H++
2 3 2 3
HCO,HCO H++CO。
(2)多元弱碱电离方程式一步写成,如Fe(OH) 的电离方程式:Fe(OH) Fe3++3OH-。
3 3
(3)强酸的酸式盐完全电离,如NaHSO 的电离方程式:NaHSO===Na++H++SO。
4 4
(4)弱酸的酸式盐中酸式酸根不能完全电离,如 NaHCO 的电离方程式:NaHCO ===Na++HCO,HCO
3 3
H++CO。
5.电解质溶液的导电性
(1)电解质导电的条件
电解质的导电条件是在水溶液中或高温熔融状态,共价化合物只能在水溶液中导电,离子化合物在熔融状
态和溶液中均可导电。
(2)导电性强弱
知识点二 电离度和电离平衡常数
1.电离度
(1)概念
在一定条件下的弱电解质达到电离平衡时,已经电离的电解质分子数占原电解质总数的百分比。
(2)表示方法
α=×100%
也可表示为α=×100%
(3)意义:衡量弱电解质的电离程度,在相同条件下(浓度、温度相同),不同弱电解质的电离度越大,弱电
解质的电离程度越大。
(4)影响因素
1)内因:弱电解质本身的性质。
2)外因:
①相同温度下,同一弱电解质,浓度越大,其电离度(α)越小。
②相同浓度下,同一弱电解质,温度越高,其电离度(α)越大。
2.电离常数
(1)表达式
①一元弱酸HA的电离常数:根据HA H++A-,可表示为K=。
a
②一元弱碱BOH的电离常数:根据BOH B++OH-,可表示为K =。
b
(2)特点
①电离常数与温度有关,与浓度无关。升高温度,K值增大。
②电离常数反映弱电解质电离程度的相对强弱,K越大,表示弱电解质越易电离,酸性或碱性越强。③多元弱酸的各级电离常数的大小关系是K K K ……,故其酸性取决于第一步电离。
1 2 3
(3)影响因素 ≫ ≫
①内因:弱电解质本身的性质。
②外因:温度越高,K值越大。
(4)电离常数的四大应用
①判断弱酸(或弱碱)的相对强弱,电离常数越大,酸性(或碱性)越强。
②判断盐溶液的酸性(或碱性)强弱,电离常数越大,对应的盐水解程度越小,酸性(或碱性)越弱。
③判断复分解反应能否发生,一般符合“强酸制弱酸”规律。
④计算弱酸、弱碱溶液中的c(H+)、c(OH-)。稀溶液中、弱酸溶液中,c(H+)=,弱碱溶液中c(OH-)=。
(5)电离度和电离常数的关系α≈或K≈cα2。
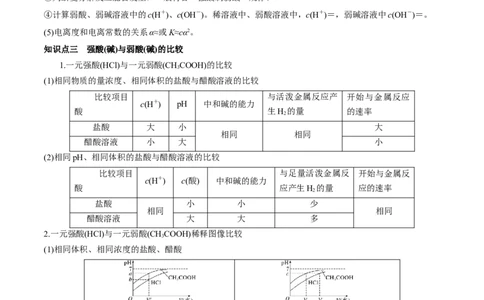
知识点三 强酸(碱)与弱酸(碱)的比较
1.一元强酸(HCl)与一元弱酸(CHCOOH)的比较
3
(1)相同物质的量浓度、相同体积的盐酸与醋酸溶液的比较
比较项目 与活泼金属反应产 开始与金属反应
c(H+) pH 中和碱的能力
酸 生H 的量 的速率
2
盐酸 大 小 大
相同 相同
醋酸溶液 小 大 小
(2)相同pH、相同体积的盐酸与醋酸溶液的比较
比较项目 与足量活泼金属反 开始与金属反
c(H+) c(酸) 中和碱的能力
酸 应产生H 的量 应的速率
2
盐酸 小 小 少
相同 相同
醋酸溶液 大 大 多
2.一元强酸(HCl)与一元弱酸(CHCOOH)稀释图像比较
3
(1)相同体积、相同浓度的盐酸、醋酸
加水稀释相同的倍数,醋酸的pH大 加水稀释到相同的pH,盐酸加入的水多
(2)相同体积、相同pH值的盐酸、醋酸
加水稀释相同的倍数,盐酸的pH大 加水稀释到相同的pH,醋酸加入的水多
3.判断HA为一元弱酸的两种常用方法(1)常温下,测量NaA溶液的pH,若pH>7,则证明HA为一元弱酸。
(2)配制0.01 mol·L-1的HA的溶液,测量溶液的pH,若pH>2,则证明HA为一元弱酸。
知识点四 自偶电离
1.定义:液态状况下溶剂分子在溶剂中自发发生的电离称为自偶电离。
2.条件:只要是液态极性共价分子化合物就可发生自偶电离,在部分酸的浓水溶液(如浓硝酸)也可发生
类似反应。分子的极性越强则自偶电离的程度越大。
3.实例
(1)极性共价化合物的自偶电离
HNO+HNO HNO ++NO-
3 3 2 3 3
BrF+BrF BrF⁻+ BrF ⁺
3 3 4 2
NH +NH NH ++NH-
3 3 4 2
CHCHOH+CH CHOH CHCHOH ++CH CHO-
3 2 3 2 3 2 2 3 2
HO+HO HO++OH-
2 2 3
SOCl SOCl++Cl⁻
2
NO NO++NO-
2 4 3
3HF HF++HF-
2 2
2SO SO2++SO2-
2 3
3HCl HCl++HCl -
2 2
(2)非极性共价分子在溶液中时也偶有自偶电离
例如:2PCl PCl - + PCl +
5 6 4
PBr PBr ++ Br_
5 4
第三部分:典型例题剖析
高频考点1 考查弱电解质的电离特点
例1.下列有关电离平衡的叙述中正确的是
A.电解质达到电离平衡后,各种离子的浓度相等
B.电离平衡时,由于分子和离子的浓度不断发生变化,所以说电离平衡是动态平衡
C.电离平衡是相对的、暂时的,外界条件改变时,平衡就会发生移动
D.电解质在溶液里达到电离平衡时,分子的浓度和离子的浓度相等
【易错警示】(1)电离平衡向右移动,电离程度不一定增大。
(2)加水稀释电解质,电解质分子的浓度不一定减小。
(3)溶液的导电能力(电导率)与电解质的强弱无关,它取决于溶液中自由移动的离子浓度大小以及离子所带电荷的多少。
【变式训练】在醋酸溶液中,CHCOOH电离达到平衡的标志是
3
A.溶液显电中性 B.氢离子浓度恒定不变
C.c(H+) = c(CHCOO¯) D.溶液中检测不出CHCOOH分子存在
3 3
高频考点2 考查溶液导电性图像分析
例2.(2022·北京一七一中三模)用0.100mol·L-1的NaOH溶液分别滴定体积均为10.00mL、浓度均为
0.100mol·L-1的HCl和CHCOOH溶液。利用传感器测得滴定过程中溶液的电导率(电导率越大表示溶液导
3
电性越强)变化如图所示。下列说法正确的是
A.曲线①代表向HCl中滴加NaOH B.A点溶液的pH小于C点溶液的pH
C.A、B两点水的电离程度:A>B D.C→D发生了反应:H++OH-=H O
2
【方法归纳】影响电解质溶液的导电能力的主要因素
电解质溶液的导电能力主要取决于离子的浓度、离子在电场中的运动速率以及离子所带的电荷数目。
(1)相同条件下溶液的离子浓度越大,其导电能力越强。
(2)相同离子浓度时,离子所带的电荷数越多,溶液的导电能力越强。
(3)温度越高,溶液的导电能力越强。
【变式训练】常温下,向 的HR溶液中逐滴滴入 的 溶液,所得溶液pH
及导电性变化如图所示。下列分析不正确的是
A.a~b点导电能力增强说明HR为弱酸B.c点溶液存在
C.b点溶液 ,此时溶液显酸性
D.b~c任意点溶液均有
高频考点3 考查外界条件对电离平衡的影响
例3.CHCOOH溶液存在电离平衡,下列有关叙述不正确的是
3
A.向CHCOOH溶液中加水稀释,溶液中c(OH−)减小
3
B.向CHCOOH溶液中加入少量的CHCOONa固体,电离平衡向左移动
3 3
C.CHCOOH溶液中离子浓度的关系:c(H+)=c(OH−)+c(CHCOO−)
3 3
D.常温下,pH=2的CHCOOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
3
【易错提醒】外界条件对电离平衡影响的四个“不一定”
(1)稀醋酸加水稀释时,溶液中不一定所有的离子浓度都减小。
因为温度不变,K =c(H+)·c(OH-)是定值,稀醋酸加水稀释时,溶液中的c(H+)减小,故c(OH-)增大。
w
(2)电离平衡右移,电解质分子的浓度不一定减小,离子的浓度不一定增大,电离程度也不一定增大。
如对于CHCOOH CHCOO-+H+,平衡后,加入冰醋酸,c(CHCOOH)增大,平衡右移,根据勒夏特
3 3 3
列原理,只能“减弱”而不能“消除”,再次平衡时,c(CHCOOH)比原平衡时大;加水稀释或加少量
3
NaOH固体,都会使平衡右移,但 c(CHCOOH)、c(H+)都比原平衡时要小;加水稀释或增大弱电解质的浓
3
度,都使平衡右移,但加水稀释时弱电解质的电离程度增大,而增大弱电解质的浓度时弱电解质的电离程
度减小。
【变式训练】HS水溶液中存在电离平衡HS H++HS-和HS- H++S2-。下列关于HS溶液的说法正
2 2 2
确的是
A.滴加新制氯水,平衡向左移动,溶液pH减小
B.加水,平衡向右移动,溶液中氢离子浓度增大
C.通入过量SO 气体,平衡向左移动,溶液pH增大
2
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子的浓度都减小
高频考点4 考查强、弱电解质的判断与比较
例4.(2022·北京昌平·高三期末)某温度下,将pH和体积均相同的HCl和CHCOOH溶液分别加水稀释,
3
其pH随加水体积的变化如图所示。下列叙述正确的是A.稀释前溶液的浓度:c(HCl) >c(CHCOOH)
3
B.溶液中水的电离程度:b点<c点
C.从b点到d点,溶液中c(H+)c(OH-)逐渐增大
D.在d点和e点均存在:c(H+)<c(酸根阴离子)
【名师助学】我们在做有关强酸、弱酸、强碱、弱碱的试题时,不妨用假设法给自己搭建一个平台,用这
个平台进行分析。如题中的A选项,分别加水稀释10倍,假设平衡不移动,那么①②溶液的浓度均为原
来的,然后再根据电离平衡移动进行分析,其它选项也可以采用类似的方法处理。
【变式训练】(2022·上海松江·二模)相同条件下,取pH=2的HCl溶液和pH=2的CHCOOH溶液各
3
100mL,分别加入0.65g锌粉充分反应,有关叙述正确的是
A.CHCOOH与锌反应起始速率快 B.HCl与锌粉反应放出H 多
3 2
C.HCl与锌反应起始速率快 D.CHCOOH与锌粉反应放出H 多
3 2
高频考点5 考查电离常数的应用
例5.部分弱酸的电离平衡常数如下表:
弱酸 HCOOH HCN HCO
2 3
电离平衡常数(25 ℃) K=1.77×10-4 K=4.9×10-10 K =4.3×10-7 K =5.6×10-11
i i i1 i2
下列选项错误的是
A.2CN-+HO+CO=2HCN+CO
2 2
B.2HCOOH+CO =2HCOO-+HO+CO↑
2 2
C.由数据可知酸性:HCOOH>H CO>HCN>HCO
2 3
D.25 ℃时,在等浓度的CHCOOH溶液和HCN溶液中,水的电离程度后者大
3
【规律总结】电离常数的应用
(1)判断弱酸(或弱碱)的相对强弱,电离常数越大,酸性(或碱性)越强。
(2)判断盐溶液的酸性(或碱性)强弱,电离常数越大,对应的盐水解程度越小,酸性(或碱性)越弱。
(3)判断复分解反应能否发生,一般符合“强酸制弱酸”规律。
【变式训练】常温下,CHCOOH、HCOOH(甲酸)的电离常数数值分别为1.7×10-5、1.8×10-4,以下关于
30.1mol/LCH COOH溶液、0.1mol/LHCOOH溶液的说法正确的是
3
A.c(H+):CHCOOH>HCOOH
3
B.等体积的两溶液中,分别加入过量的镁,产生氢气的体积:HCOOH>CHCOOH
3
C.HCOOH可能与NaOH发生反应:H++OH-=H O
2
D.将CHCOOH溶液稀释100倍过程中, 保持不变
3
高频考点6 考查电离平衡常数的有关计算
例6.(2022·河南开封·一模)25℃时,将1.0Lx mol ·L-1 CHCOOH溶液与0. 1 mol NaOH固体混合,使之充
3
分反应。然后向该混合溶液中通入HCl气体或加入NaOH固体(忽略体积和温度变化),溶液pH随通入(或
加入)物质的物质的量的变化如图所示。下列叙述正确的是
A.水的电离程度:①>②>③
B.点②对应的混合溶液中:c(CHCOOH)+c(CH COO-)=x mol·L-1
3 3
C.点③对应的混合溶液中:c(Na+)> c(CHCOO-)
3
D.该温度下,CHCOOH的电离平衡常数K=
3 a
【方法归纳】溶液中离子浓度比值变化的判断方法
(1)将浓度之比转化为物质的量之比;
(2)“凑常数”:将某些离子的浓度比值乘以或除以某些离子的浓度,转化为一个 K 或K 或K 等常数与某
a b W
种离子浓度乘积或相除的关系;
(3)“假设法”:假设无限稀释,则c(H+)、c(OH-)趋于不变,其他离子浓度趋于0。
【变式训练】常温下,用0.1mol·L-1的NaOH溶液滴定20mL0.1mol·L-1HA溶液。溶液中A-(或HA)的分布系
数δ、NaOH溶液体积V与pH的关系如图所示[已知:δ(HA)= ]。下列叙述错误的是A.曲线a表示的是HA的分布系数变化曲线
B.HA的电离平衡常数的数量级为10-6
C.p点对应的溶液中,c(A-)<3c(HA)
D.p、n、q中,水的电离程度最大的是q点
高频考点7 考查弱电解质的判断方法
例7.(2022·北京·北师大实验中学三模)常温下,下列实验事实能证明醋酸是一元酸的是
A.0.1mol·L-1醋酸溶液pH= 3
B.向醋酸钠溶液中滴加酚酞溶液,溶液变红
C.完全中和25mL 0.1mol·L-1醋酸溶液需要25mL 0.1mol·L-1NaOH溶液
D.等物质的量浓度时,醋酸溶液的导电性弱于盐酸
【方法归纳】判断弱电解质的三个思维角度
角度一:弱电解质的定义,即弱电解质不能完全电离,如0.1 mol·L-1的CHCOOH溶液的pH>1。
3
角度二:弱电解质溶液中存在电离平衡,条件改变,平衡移动,如pH=1的CHCOOH溶液加水稀释10倍
3
后,17。
【变式训练】下列事实中一定能证明 是弱电解质的是
①用 溶液做导电实验,灯炮很暗
② 溶液的
③等 等体积的硫酸、 溶液和足量锌反应, 放出的氢气较多
④ 醋酸溶液恰好与 溶液完全反应⑤ 的 溶液稀释至1000倍,
A.①②④⑤ B.②③⑤ C.②③④⑤ D.①②⑤