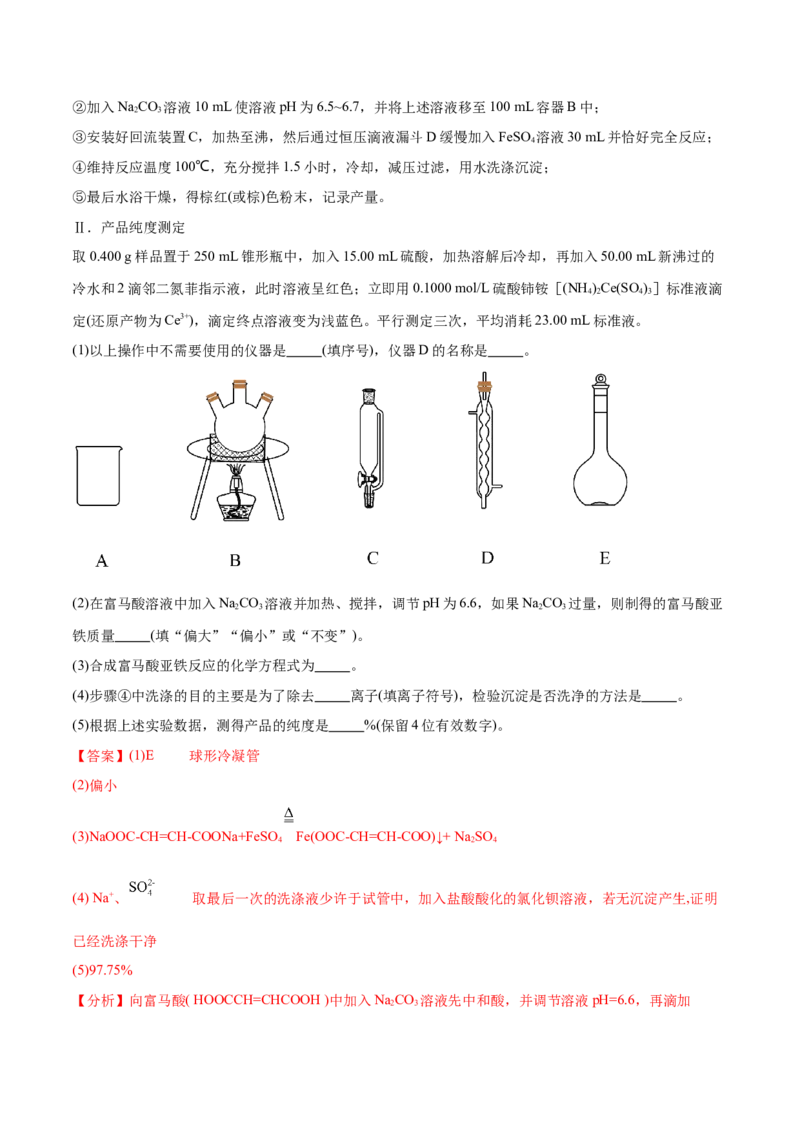文档内容
第 27 讲 物质的制备与性质实验
1.实验室制取少量干燥的氨气涉及下列装置,其中正确的是
A.①是氨气发生装置 B.②是氨气吸收装置
C.③是氨气发生装置 D.④是氨气收集、检验装置
【答案】C
【解析】①装置 加热分解生成 和 ,在试管口处 和 气体遇冷会再反应生成 ,
收集不到 ,A错误; 极易溶于水, 溶解导致导气管中气体压强减小而引发倒吸现象,因此②
不能用于 的吸收,②装置,防倒吸装置中漏斗口与液面应接触,但插入液面之下不能防止倒吸,B错
误;③装置用浓氨水加热可分解制得 ,C正确;由于 的密度比空气小,因此收集 可以采用向
下排空气法,为防止空气对流应在试管口塞一团棉花,D错误。答案为C。
2.实验室可利用苯和液溴在溴化铁的催化作用下制取溴苯,其制备及提纯过程为:制备→水洗分液→碱
洗分液→水洗分液→再分离,下列说法正确的是
A.制备装置a中长导管仅起导气作用
B.装置b可用于制备过程中吸收尾气
C.分液时,有机层由装置c的上口倒出D.可选择装置d进行再分离
【答案】D
【解析】铁做催化剂条件下,苯和液溴反应生成溴苯和溴化氢,该反应为放热反应,反应放出的热量会使
苯和液溴挥发,则制备装置a中长导管起导气兼冷凝回流的作用,故A错误;溴化氢极易溶于水,若用装
置b吸收溴化氢会产生倒吸,故B错误;溴苯是密度比水大的不溶于水的无色液体,分液时,密度比水大
的溴苯应该从下口放出,故C错误;由分析可知,水洗分液得到含有苯的粗溴苯,分离粗溴苯可以利用苯
与溴苯的沸点不同选择装置d进行蒸馏分离,故D正确;故选D。
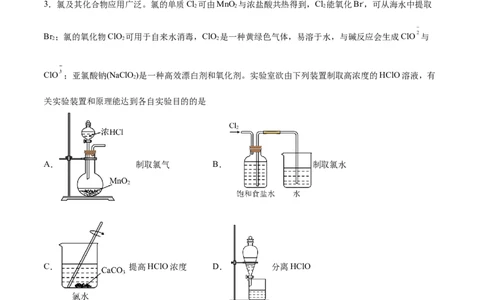
3.氯及其化合物应用广泛。氯的单质Cl 可由MnO 与浓盐酸共热得到,Cl 能氧化Br-,可从海水中提取
2 2 2
Br ;氯的氧化物ClO 可用于自来水消毒,ClO 是一种黄绿色气体,易溶于水,与碱反应会生成ClO 与
2 2 2
ClO ;亚氯酸钠(NaClO)是一种高效漂白剂和氧化剂。实验室欲由下列装置制取高浓度的HClO溶液,有
2
关实验装置和原理能达到各自实验目的的是
A. 制取氯气 B. 制取氯水
C. 提高HClO浓度 D. 分离HClO
【答案】C
【解析】浓盐酸与MnO 加热条件制取Cl,该装置中少了酒精灯,A项不能达到实验目的;制取的Cl 含
2 2 2
有HCl,需要用饱和氯化钠洗气装置长进短出,该装置达到无法除杂的目的,B项不能达到实验目的;氯
气溶于水存在平衡Cl+H O HCl+HClO,加入CaCO 消耗HCl使平衡正向HClO浓度增大,C项能达到
2 2 3
实验目的;最终得到浓的HClO中含有CaCO 固体,需要进行过滤除去,该装置错误,D项不能达到实验
3目的;故选C。
4.湿法制备高铁酸钾的过程:①将制得的Cl 通入一定体积分数的KOH溶液中得到KClO溶液;②将
2
KOH固体溶解在①中得到的KClO溶液中,加入一定质量的Fe(NO )·9H O,搅拌得到KFeO 溶液,继续
3 3 2 2 4
加KOH固体至溶液饱和;③减压过滤,滤渣经一系列操作得到KFeO 晶体。已知KFeO 性质:低温、碱
2 4 2 4
性环境稳定;具有强氧化性,能氧化烃、苯胺和80%以下的乙醇溶液。下列说法正确的是
A.②中两次使用KOH固体的作用相同
B.③中一系列操作含洗涤,洗涤时可用75%乙醇溶液
C.KFeO 消毒净水过程均利用它的氧化性
2 4
D.制备过程中涉及的主要化学反应都是氧化还原反应
【答案】D
【解析】KClO在碱性条件下反应,则在②中先加 KOH 固体的作用是:与反应液中过量的氯气继续反
应,营造碱性环境;生成KFeO 溶液后继续加KOH固体的作用是:增大K+浓度,促进KFeO 晶体析
2 4 2 4
出;两次使用KOH固体的作用不相同,故A错误;KFeO 能氧化80%以下的乙醇溶液,③中一系列操作
2 4
含洗涤,洗涤时不能用75%乙醇溶液,故B错误;KFeO 具有强氧化性,能够消毒杀菌;同时FeO 被还
2 4
原成Fe3+,Fe3+水解形成Fe(OH) 胶体,能够吸附水中悬浮杂质,KFeO 消毒净水过程利用它的氧化性和能
3 2 4
形成胶体的性质,故C错误;制备过程中涉及的主要离子反应为:Cl+2OH-=ClO-+Cl-+H O、2Fe(OH) +
2 2 3
3ClO-+4OH-=2FeO +3Cl-+5H O,都是氧化还原反应,故D正确;故选D。
2
5.能用如图所示装置完成气体制备、尾气处理(加热和夹持等装置略去)的是
气体 制备试剂 烧杯中试剂
A NO 铜与浓硝酸 NaOH溶液
2
B CO 大理石和硫酸 石灰水
2
C C H 电石与水 水
2 2D Cl MnO 与浓盐酸 饱和NaCl溶液
2 2
【答案】A
【解析】铜与浓硝酸反应生成硝酸铜、NO 、水,NO 采用排空法收集后,多余的尾气可以采用NaOH溶
2 2
液吸收,故A正确;实验室制取二氧化碳不选用大理石和硫酸,因为会生成硫酸钙覆盖在碳酸钙表面阻止
反应,应该选用稀盐酸和碳酸钙反应,故B错误;电石与水反应生成氢氧化钙和乙炔,乙炔与水不反应,
尾气乙炔应该用酸性高锰酸钾溶液吸收处理,故C错误;氯气与饱和NaCl溶液不反应,不能用饱和氯化
钠吸收尾气,应该选用氢氧化钠溶液进行吸收,故D错误;故选A。
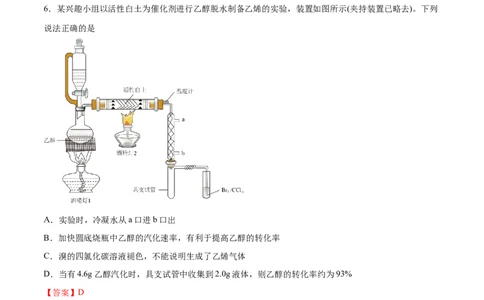
6.某兴趣小组以活性白土为催化剂进行乙醇脱水制备乙烯的实验,装置如图所示(夹持装置已略去)。下列
说法正确的是
A.实验时,冷凝水从a口进b口出
B.加快圆底烧瓶中乙醇的汽化速率,有利于提高乙醇的转化率
C.溴的四氯化碳溶液褪色,不能说明生成了乙烯气体
D.当有4.6g乙醇汽化时,具支试管中收集到2.0g液体,则乙醇的转化率约为93%
【答案】D
【解析】实验时,冷凝水应从下口进上口出,选项A错误;若乙醇的汽化速率过快,乙醇分子在催化剂表
面停留的时间过短,部分乙醇还来不及被吸附、活化、反应即被带出催化剂层,将导致转化率降低,选项
B错误;产生的乙烯能与溴发生加成反应,从而使溶液褪色,通过实验现象能说明有乙烯生成,选项C错
误;具支试管中收集的液体成分是乙醇和水,则生成乙烯气体的质量是 ,故乙醇的转化
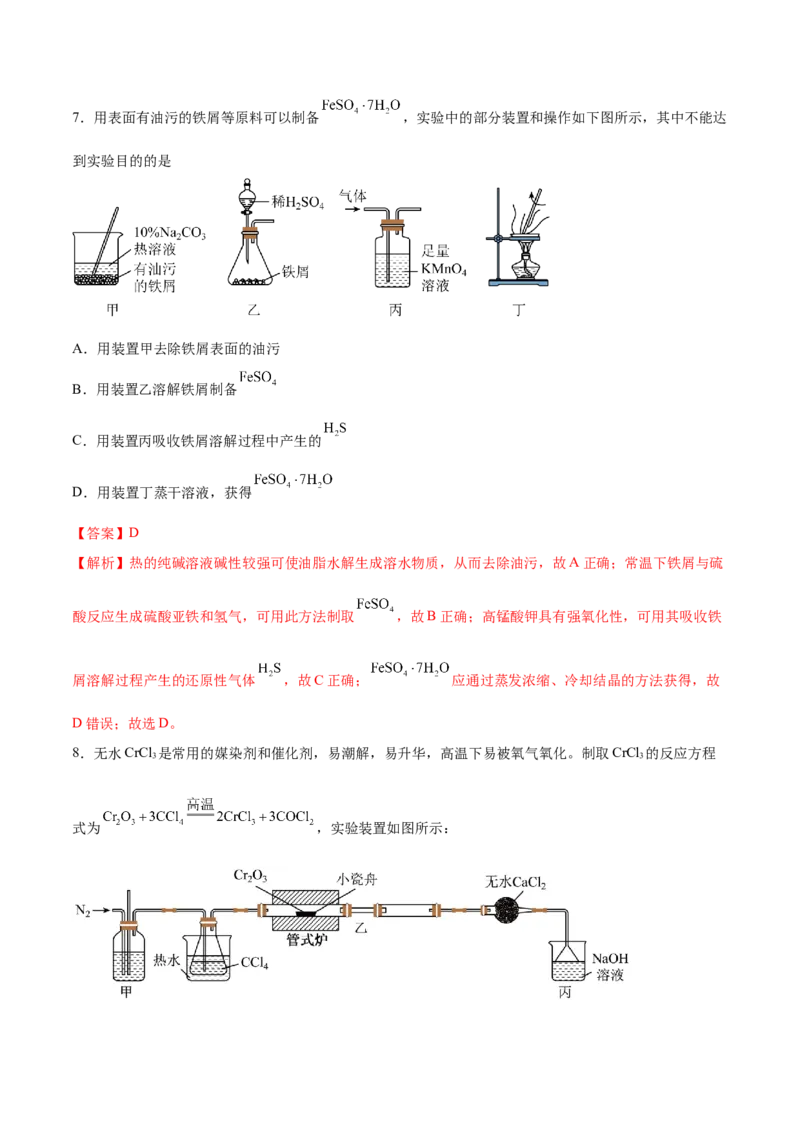
率为 ,选项D正确;故选D。7.用表面有油污的铁屑等原料可以制备 ,实验中的部分装置和操作如下图所示,其中不能达
到实验目的的是
A.用装置甲去除铁屑表面的油污
B.用装置乙溶解铁屑制备
C.用装置丙吸收铁屑溶解过程中产生的
D.用装置丁蒸干溶液,获得
【答案】D
【解析】热的纯碱溶液碱性较强可使油脂水解生成溶水物质,从而去除油污,故A正确;常温下铁屑与硫
酸反应生成硫酸亚铁和氢气,可用此方法制取 ,故B正确;高锰酸钾具有强氧化性,可用其吸收铁
屑溶解过程产生的还原性气体 ,故C正确; 应通过蒸发浓缩、冷却结晶的方法获得,故
D错误;故选D。
8.无水CrCl 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。制取CrCl 的反应方程
3 3
式为 ,实验装置如图所示:已知 有毒,遇水发生水解。下列说法错误的是
A.甲中的试剂为浓硫酸
B.若实验过程中乙处出现堵塞,用酒精灯加热乙处即可
C.丙中发生反应的离子方程式为
D.实验前、后均需通入一段时间的 ,其作用相同
【答案】D
【分析】结合装置图,反应前先通入氮气,排除空气的干扰,CrCl 易潮解、高温下易被氧气氧化,则实验
3
过程中必须保持干燥环境,甲中装浓HSO 可以干燥N 并防止空气中水蒸气进入装置,反应结束后继续通
2 4 2
入一段时间干燥的氮气,使CrCl 在氮气氛围中冷却,无水CaCl 防止丙中水蒸气进入乙装置;生成的
3 2
COCl 有毒,需要通过NaOH溶液吸收处理,据此分析解题。
2
【解析】由分析可知,甲中的试剂为浓硫酸,可以干燥N 并防止空气中水蒸气进入置,A正确;由题干信
2
息可知,CrCl 具有易升华的性质,故若实验过程中乙处出现堵塞,用酒精灯加热乙处即可,B正确;装置
3
丙中可以看做是COCl 先与水反应生成二氧化碳和氯化氢,二氧化碳和氯化氢再与氢氧化钠反应,所以最
2
终溶液中存在碳酸根离子和氯离子,故反应方程式为: ,C正确;由分析可
知,实验前、后均需通入一段时间的 ,反应前先通入氮气,排除空气的干扰,而反应结束后继续通入一
段时间干燥的氮气,使CrCl 在氮气氛围中冷却,即前后两次的作用不相同,D错误;故选D。
3
9.下列由废铁屑(除Fe外还含少量C、FeS等杂质)制取 的原理与装置不能达到实验目的的是
A.用装置甲制取 B.用装置乙吸收尾气中的C.用装置丙过滤得到 溶液 D.用装置丁蒸发结晶获得
【答案】D
【解析】由图可知,装置甲为铁屑与稀硫酸在80℃水浴中共热反应制备硫酸亚铁的装置,水浴加热的目的
是加快反应速率,故A正确;由图可知,装置乙中盛有的硫酸铜溶液用于吸收氯化亚铁与稀硫酸反应生成
的有毒的硫化氢,防止污染空气,故B正确;由图可知,装置丙为用抽滤的方法得到硫酸亚铁溶液,抽滤
的目的是加快过滤得速率,故C正确;蒸发结晶获得绿矾应选用蒸发皿,不能选用坩埚,故D错误;故选
D。
10.实验室制备下列气体所选装置,制备试剂、除杂试剂及所选装置均正确的是
(干燥、收集装置略)
气体 制备试剂 除杂试剂 所选装置
A NH NH Cl —— b、c
3 4
B Cl MnO +浓HCl 饱和NaCl溶液 a、c
2 2
C C H C HOH+浓HSO NaOH溶液 b、c
2 4 2 5 2 4
D C H 电石+饱和NaCl溶液 CuSO 溶液 a、c
2 2 4
【答案】D
【解析】实验室中不能采用直接加热氯化铵制取氨气,应用浓氨水加热制取,故A错误;二氧化锰与浓盐
酸加热生成氯气,氯气中混有挥发出的HCl气体,可用饱和食盐水除去,装置可选b、c,故B错误;乙醇
与浓硫酸发生消去反应生成乙烯需要控制温度迅速升至170℃,因此装置中需用温度计控制反应温度,故
C错误;电石和饱和食盐水常温下反应生成乙炔,因电石中含有硫化物,同时会生成硫化氢,可用硫酸铜
溶液将硫化氢沉淀除去,装置应选a、c,故D正确;故选D。
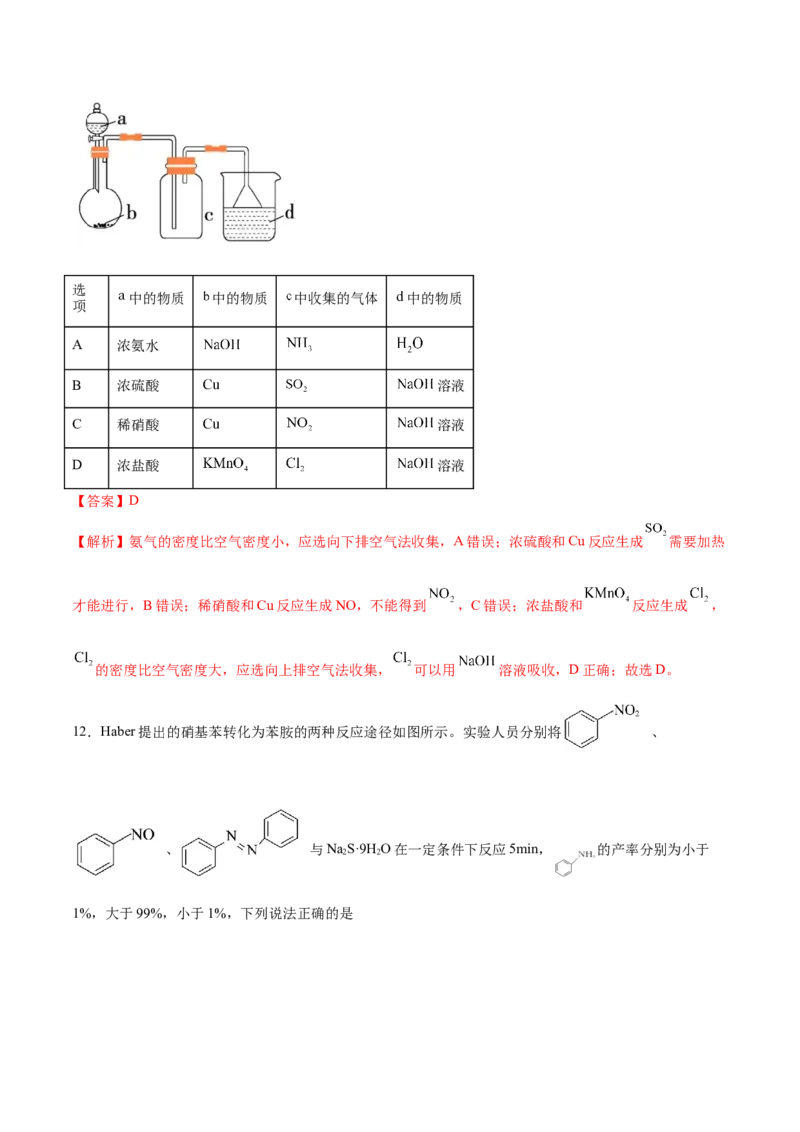
11.实验室中某些气体的制取、收集及尾气处理装置如图所示(省略净化装置)。仅用此装置和表中提供的
物质完成相关实验,最合理的选项是选
中的物质 中的物质 中收集的气体 中的物质
项
A 浓氨水
B 浓硫酸 溶液
C 稀硝酸 溶液
D 浓盐酸 溶液
【答案】D
【解析】氨气的密度比空气密度小,应选向下排空气法收集,A错误;浓硫酸和Cu反应生成 需要加热
才能进行,B错误;稀硝酸和Cu反应生成NO,不能得到 ,C错误;浓盐酸和 反应生成 ,
的密度比空气密度大,应选向上排空气法收集, 可以用 溶液吸收,D正确;故选D。
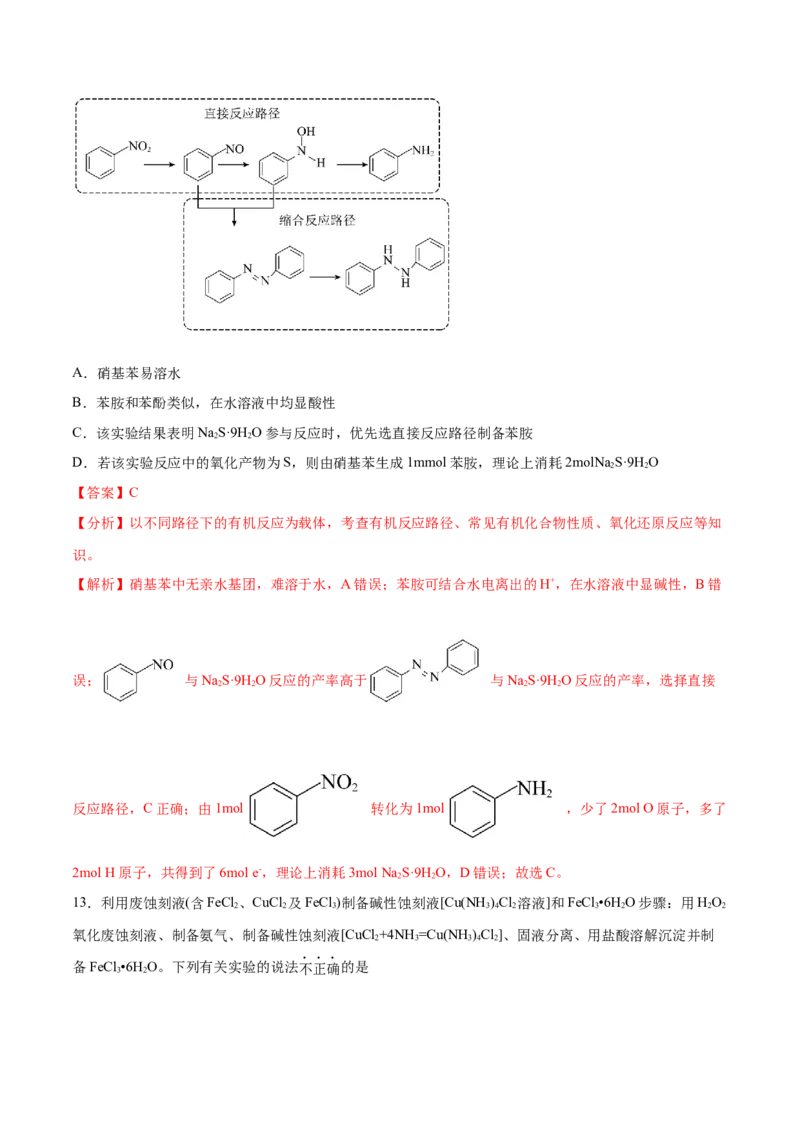
12.Haber提出的硝基苯转化为苯胺的两种反应途径如图所示。实验人员分别将 、
、 与NaS·9H O在一定条件下反应5min, 的产率分别为小于
2 2
1%,大于99%,小于1%,下列说法正确的是A.硝基苯易溶水
B.苯胺和苯酚类似,在水溶液中均显酸性
C.该实验结果表明NaS·9H O参与反应时,优先选直接反应路径制备苯胺
2 2
D.若该实验反应中的氧化产物为S,则由硝基苯生成1mmol苯胺,理论上消耗2molNa S·9H O
2 2
【答案】C
【分析】以不同路径下的有机反应为载体,考查有机反应路径、常见有机化合物性质、氧化还原反应等知
识。
【解析】硝基苯中无亲水基团,难溶于水,A错误;苯胺可结合水电离出的H+,在水溶液中显碱性,B错
误; 与NaS·9H O反应的产率高于 与NaS·9H O反应的产率,选择直接
2 2 2 2
反应路径,C正确;由1mol 转化为1mol ,少了2mol O原子,多了
2mol H原子,共得到了6mol e-,理论上消耗3mol Na S·9H O,D错误;故选C。
2 2
13.利用废蚀刻液(含FeCl 、CuCl 及FeCl )制备碱性蚀刻液[Cu(NH )Cl 溶液]和FeCl •6H O步骤:用HO
2 2 3 3 4 2 3 2 2 2
氧化废蚀刻液、制备氨气、制备碱性蚀刻液[CuCl +4NH=Cu(NH)Cl]、固液分离、用盐酸溶解沉淀并制
2 3 3 4 2
备FeCl •6H O。下列有关实验的说法不正确的是
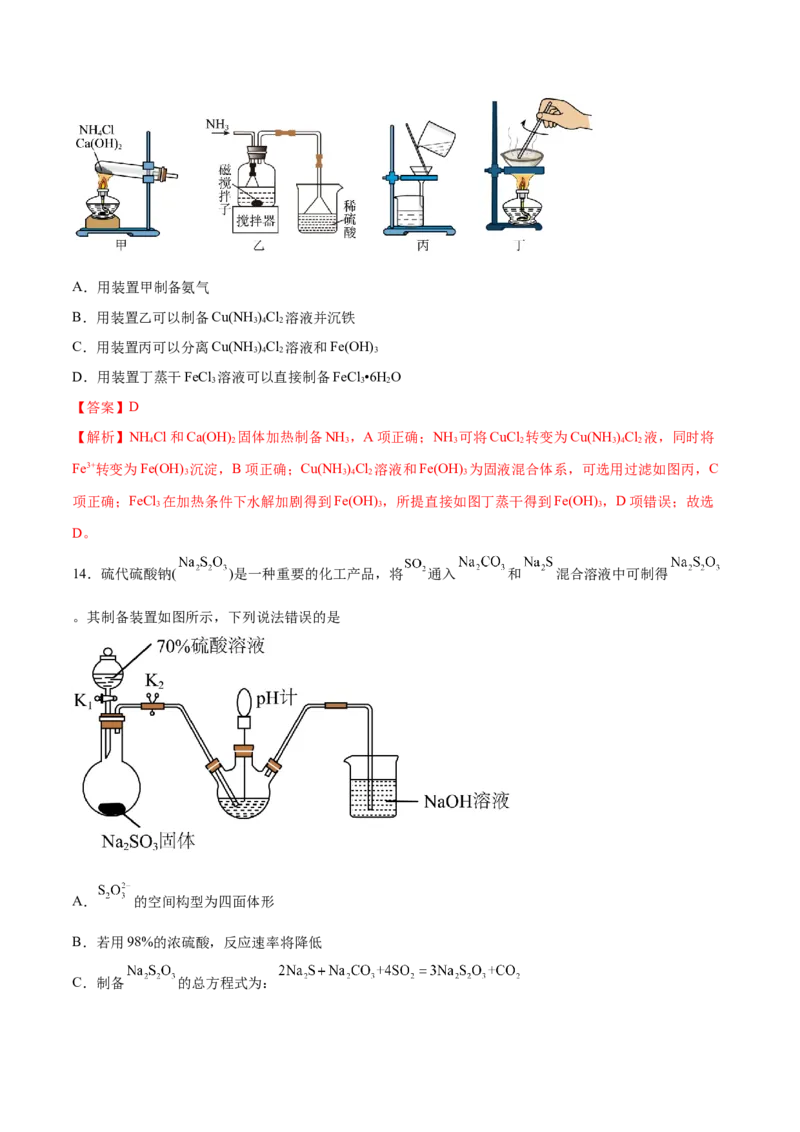
3 2A.用装置甲制备氨气
B.用装置乙可以制备Cu(NH )Cl 溶液并沉铁
3 4 2
C.用装置丙可以分离Cu(NH )Cl 溶液和Fe(OH)
3 4 2 3
D.用装置丁蒸干FeCl 溶液可以直接制备FeCl •6H O
3 3 2
【答案】D
【解析】NH Cl和Ca(OH) 固体加热制备NH ,A项正确;NH 可将CuCl 转变为Cu(NH )Cl 液,同时将
4 2 3 3 2 3 4 2
Fe3+转变为Fe(OH) 沉淀,B项正确;Cu(NH )Cl 溶液和Fe(OH) 为固液混合体系,可选用过滤如图丙,C
3 3 4 2 3
项正确;FeCl 在加热条件下水解加剧得到Fe(OH) ,所提直接如图丁蒸干得到Fe(OH) ,D项错误;故选
3 3 3
D。
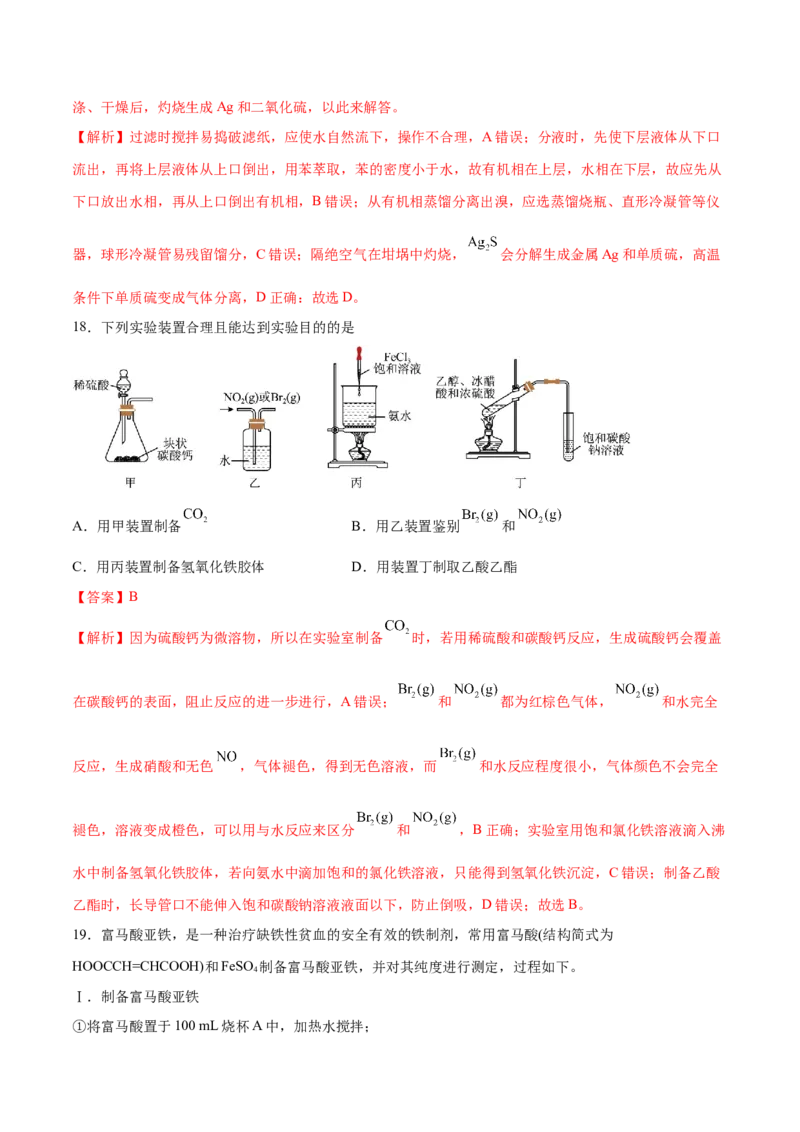
14.硫代硫酸钠( )是一种重要的化工产品,将 通入 和 混合溶液中可制得
。其制备装置如图所示,下列说法错误的是
A. 的空间构型为四面体形
B.若用98%的浓硫酸,反应速率将降低
C.制备 的总方程式为:D.为增大三颈烧瓶中加入原料的利用率,可通入过量
【答案】D
【分析】由实验装置图可知,圆底烧瓶中亚硫酸钠固体与70%较浓硫酸反应制备二氧化硫,三颈烧瓶中二
氧化硫与硫化钠和碳酸钠的混合溶液反应制备硫代硫酸钠,烧杯中盛有的氢氧化钠溶液用于吸收二氧化碳
和未反应的二氧化硫,防止污染空气。
【解析】硫代硫酸根离子中中心原子为硫原子,硫原子的价层电子对数为4、孤对电子对数为0,离子的空
间构型为四面体形,故A正确;98%的浓硫酸的主要成分是硫酸分子,溶液中氢离子浓度小,与亚硫酸钠
固体的反应速率慢,则若用98%的浓硫酸,反应速率将降低,故B正确;制备硫代硫酸的反应为二氧化硫
与硫化钠和碳酸钠的混合溶液反应生成硫代硫酸钠和二氧化碳,反应的化学方程式为
,故C正确;二氧化硫与水反应生成亚硫酸,亚硫酸电离出的氢
离子能与硫代硫酸钠溶液反应,导致产率降低,所以制备硫代硫酸钠时,不能通入过量的二氧化硫,故D
错误;故选D。
15.实验室从废定影液[含 和 等]中回收 和 的主要步骤如下。下列说法正确的是
A.为加快过滤速度,可以用玻璃棒轻轻搅拌漏斗中的液体
B.分液时先从下口放出有机相,再从上口倒出水相
C.从有机相提取 的操作中需要的玻璃仪器有酒精灯、蒸馏烧瓶、球形冷凝管等
D.由 制备金属银时,需将 置于坩埚中隔绝空气高温焙烧
【答案】D
【分析】由流程可知,加入NaS溶液会和 反应生成Ag S沉淀和 ,过滤分离出滤液中含
2 2
Br-、 ,通入氯气能将Br-氧化为Br ,利用苯将溴单质萃取后分液得到有机相,蒸馏分离出溴;滤渣洗
2涤、干燥后,灼烧生成Ag和二氧化硫,以此来解答。
【解析】过滤时搅拌易捣破滤纸,应使水自然流下,操作不合理,A错误;分液时,先使下层液体从下口
流出,再将上层液体从上口倒出,用苯萃取,苯的密度小于水,故有机相在上层,水相在下层,故应先从
下口放出水相,再从上口倒出有机相,B错误;从有机相蒸馏分离出溴,应选蒸馏烧瓶、直形冷凝管等仪
器,球形冷凝管易残留馏分,C错误;隔绝空气在坩埚中灼烧, 会分解生成金属Ag和单质硫,高温
条件下单质硫变成气体分离,D正确:故选D。
18.下列实验装置合理且能达到实验目的的是
A.用甲装置制备 B.用乙装置鉴别 和
C.用丙装置制备氢氧化铁胶体 D.用装置丁制取乙酸乙酯
【答案】B
【解析】因为硫酸钙为微溶物,所以在实验室制备 时,若用稀硫酸和碳酸钙反应,生成硫酸钙会覆盖
在碳酸钙的表面,阻止反应的进一步进行,A错误; 和 都为红棕色气体, 和水完全
反应,生成硝酸和无色 ,气体褪色,得到无色溶液,而 和水反应程度很小,气体颜色不会完全
褪色,溶液变成橙色,可以用与水反应来区分 和 ,B正确;实验室用饱和氯化铁溶液滴入沸
水中制备氢氧化铁胶体,若向氨水中滴加饱和的氯化铁溶液,只能得到氢氧化铁沉淀,C错误;制备乙酸
乙酯时,长导管口不能伸入饱和碳酸钠溶液液面以下,防止倒吸,D错误;故选B。
19.富马酸亚铁,是一种治疗缺铁性贫血的安全有效的铁制剂,常用富马酸(结构简式为
HOOCCH=CHCOOH)和FeSO 制备富马酸亚铁,并对其纯度进行测定,过程如下。
4
Ⅰ.制备富马酸亚铁
①将富马酸置于100 mL烧杯A中,加热水搅拌;②加入NaCO 溶液10 mL使溶液pH为6.5~6.7,并将上述溶液移至100 mL容器B中;
2 3
③安装好回流装置C,加热至沸,然后通过恒压滴液漏斗D缓慢加入FeSO 溶液30 mL并恰好完全反应;
4
④维持反应温度100℃,充分搅拌1.5小时,冷却,减压过滤,用水洗涤沉淀;
⑤最后水浴干燥,得棕红(或棕)色粉末,记录产量。
Ⅱ.产品纯度测定
取0.400 g样品置于250 mL锥形瓶中,加入15.00 mL硫酸,加热溶解后冷却,再加入50.00 mL新沸过的
冷水和2滴邻二氮菲指示液,此时溶液呈红色;立即用0.1000 mol/L硫酸铈铵[(NH )Ce(SO)]标准液滴
4 2 4 3
定(还原产物为Ce3+),滴定终点溶液变为浅蓝色。平行测定三次,平均消耗23.00 mL标准液。
(1)以上操作中不需要使用的仪器是 (填序号),仪器D的名称是 。
(2)在富马酸溶液中加入NaCO 溶液并加热、搅拌,调节pH为6.6,如果NaCO 过量,则制得的富马酸亚
2 3 2 3
铁质量 (填“偏大”“偏小”或“不变”)。
(3)合成富马酸亚铁反应的化学方程式为 。
(4)步骤④中洗涤的目的主要是为了除去 离子(填离子符号),检验沉淀是否洗净的方法是 。
(5)根据上述实验数据,测得产品的纯度是 %(保留4位有效数字)。
【答案】(1)E 球形冷凝管
(2)偏小
(3)NaOOC-CH=CH-COONa+FeSO Fe(OOC-CH=CH-COO)↓+ Na SO
4 2 4
(4) Na+、 取最后一次的洗涤液少许于试管中,加入盐酸酸化的氯化钡溶液,若无沉淀产生,证明
已经洗涤干净
(5)97.75%
【分析】向富马酸( HOOCCH=CHCOOH )中加入NaCO 溶液先中和酸,并调节溶液pH=6.6,再滴加
2 3FeSO 溶液可合成得到富马酸亚铁,然后过滤、洗涤、干燥后得到产品,再根据富马酸亚铁(C HOFe)有
4 4 2 4
Fe2+,溶液中的Fe2+被Ce4+氧化为Fe3+,Ce4+被还原为Ce3+,反应为:Fe2++Ce4+=Fe3++Ce3+,可得富马酸亚铁
与Ce4+的关系式:富马酸亚铁~ Ce4+,根据滴定消耗硫酸铈铵[(NH )Ce(SO)]标准液的体积计算富马酸
4 2 4 3
亚铁的物质的量,再根据理论产量和产品的实际质量计算产品纯度。
【解析】(1)在步骤①溶解富马酸需使用烧杯;在步骤②中需使用装置B;在步骤③回流装置中需要使用
装置D和装置C;过滤需要烧杯和漏斗,滴定需要滴定管,不需使用容量瓶,故合理选项为E;
根据图示可知仪器D为球形冷凝管;
(2)在富马酸溶液中加入NaCO 并加热、搅拌,调节pH为6.6。如果NaCO 过量,过量的碳酸钠会消耗
2 3 2 3
亚铁离子,导致制得的富马酸亚铁质量偏小;
(3)富马酸首先和碳酸钠反应生成NaOOC-CH=CH-COONa,然后NaOOC-CH=CH-COONa和硫酸亚铁反
应合成富马酸亚铁,反应的化学反应方程式为:NaOOC-CH=CH-COONa+FeSO Fe(OOC-CH=CH-
4
COO)↓+ Na SO ;
2 4
(4)步骤④中洗涤沉淀目的主要是为了除去沉淀表面的可溶物,即反应产生的NaSO 电离产生的Na+、
2 4
; 可通过检验洗涤液中是否含有 来判断沉淀是否洗涤干净。故检验沉淀是否洗净的方法是:取
最后一次的洗涤液少许于试管中,加入盐酸酸化的氯化钡溶液,若无沉淀产生,证明已经洗涤干净;
(5)根据富马酸亚铁( C HOFe)有Fe2+,关系式为富马酸亚铁~ Fe2+,溶液中的Fe2+被Ce4+氧化为Fe3+,
4 2 4
Ce4+被还原为Ce3+,反应为: Fe2++Ce4+=Fe3++Ce3+,故富马酸亚铁~Ce4+,富马酸亚铁的物质的量是n(富马
酸亚铁)=n(Ce4+)=0.l mol/L×0.023 L=0.0023 mol,故所得产品的纯度为:
×100%=97.75%。
20.环己酮是重要化工原料,是制造尼龙的主要中间体,也是重要的工业溶剂,实验室利用如下反应原理
和实验装置制备环己酮(夹持、加热装置略,C 、C 处有仪器未画出):
1 2环己醇、环己酮和饱和食盐水的部分物理性质见表(括号中的数据表示该有机物与水形成的具有固定组成的
混合物的沸点)
物质 密度/(g/cm3) 沸点/℃ 部分性质
环己醇 0.90 161.1(97.8) 能溶于水,具有还原性,易被氧化
环己酮 0.88 155.6(95) 微溶于水,遇氧化剂易发生开环反应
饱和食盐水 1.33 108.0
实验步骤:
Ⅰ.实验中通过装置B将酸性NaCr O 溶液分批滴加到盛有30mL环己醇的A中,加入第一批NaCr O 溶液
2 2 7 2 2 7
后,待反应物的橙红色消失后再加入第二批……依次进行下去,直至反应结束,控制反应在55~65℃进
行。反应结束后,向反应液中加入适量的草酸。
Ⅱ.反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
Ⅲ.进一步分离提纯得到精环已酮18.0g。
(1)实验装置图中C 处应放置的仪器名称为 。
1
(2)A中发生反应的离子方程式为 ,用蒸馏不能分离环己酮和水的原因是 。
(3)实验过程中NaCr O 溶液分批加入的原因是 。
2 2 7
(4)步骤Ⅰ加入适量草酸为了将剩余的NaCr O 完全反应,草酸与NaCr O 的物质的量之比为 时反
2 2 7 2 2 7
应恰好进行完全。
(5)环己酮的提纯需要经过以下一系列的操作:a.蒸馏,收集151-156℃馏分,得到精品b.过滤c.在收集到的
粗品中加NaCl固体至饱和,静置,分液d.加入无水MgSO 固体,除去有机物中少量水。上述操作的正确
4
顺序是 (填序号)。上述操作c中,加入NaCl固体的作用是 。
(6)计算环己酮的产率 。(保留整数)
【答案】(1)温度计(2) 3 +Cr O +8H+ 3 +2Cr3++7H O 环己酮和水形成具有固定组成的混合物
2 2
一起蒸出
(3)避免氧化剂NaCr O 溶液过量而加剧了环己酮的开环反应
2 2 7
(4)3:1
(5)cdba 降低环己酮在水中的溶解度,减少产物损失;增加水层密度,有利于分层
(6)68%
【分析】通过装置B将酸性NaCr O 溶液分批滴加到盛有30mL环己醇的A中,反应生成环己酮,反应后
2 2 7
加入草酸除去过量的重铬酸钠,蒸馏得到环己酮粗品,粗品干燥、蒸馏得到精品;
【解析】(1)实验中加热温度需要控制在合适的反应温度,故图中C 处应放置的仪器名称为温度计;
1
(2)重铬酸钠具有强氧化性,A中发生反应为环己醇被重铬酸钠氧化为环己酮和三价铬离子、同时生成
水,反应为:3 +Cr O +8H+ 3 +2Cr3++7H O,由题干可知用蒸馏不能分离
2 2
环己酮和水的原因是:环己酮和水形成具有固定组成的混合物一起蒸出;
(3)重铬酸钠具有强氧化性,已知:环己酮遇氧化剂易发生开环反应;故实验过程中NaCr O 溶液分批
2 2 7
加入的原因是:避免氧化剂NaCr O 溶液过量而加剧了环己酮的开环反应;
2 2 7
(4)草酸与NaCr O 反应中碳元素化合价由+3变为+4、铬元素化合价由+6变为+3,根据电子守恒可知,
2 2 7
草酸与NaCr O 的物质的量之比为3:1时反应恰好进行完全。
2 2 7
(5)环己酮会和水形成具有固定组成的混合物一起蒸出,环己酮的提纯操作过程为:c.在收集到的粗品中
加NaCl固体至饱和降低环己酮的溶解度利于其分层,静置,分液分离出有机相;d.加入无水MgSO 固
4
体,除去有机物中少量水,防止形成混合物一起蒸出;b.过滤,除去干燥剂;a.蒸馏,收集151-156℃馏
分,利于物质沸点不同得到精品;故为cdba;操作c中,加入NaCl固体的作用是降低环己酮在水中的溶解
度,减少产物损失且可增加水层密度,有利于分层;
(6)30mL环己醇的物质的量为 ,则理论生成0.27mol环己酮,环己酮的产率。