文档内容
第 2 讲 物质的量浓度
课 程 标 准 知 识 建 构
1.配制一定物质的量浓度的溶液。
2.运用物质的量、物质的量浓度之间的相互
关系进行简单计算。
一、物质的量浓度
1.基本概念
2.对物质的量浓度表达式的理解
(1)正确判断溶液的溶质
①与水发生反应生成新的物质:如
Na、Na O、Na O ――→NaOH,SO ――→H SO ,NO ――→HNO 。
2 2 2 3 2 4 2 3
②特殊物质:如NH 溶于水后溶质为NH ·H O,但计算浓度时仍以NH 作为
3 3 2 3
溶质。
③含结晶水的物质:
CuSO ·5H O→CuSO ,Na CO ·10H O→Na CO 。
4 2 4 2 3 2 2 3
(2)准确计算溶液的体积
表达式c=中的V是溶液的体积,不是溶剂的体积,也不是溶质和溶剂的体积
之和,不能用水的体积代替溶液的体积,应根据V=计算。
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)1 mol·L-1 NaCl溶液是指此溶液中含有1 mol NaCl( )
(2)从100 mL 5 mol·L-1 H SO 溶液中取出了10 mL,所得硫酸的物质的量浓
2 4
度为0.5 mol·L-1( )
(3)用 100 mL 水吸收 0.1 mol HCl 气体所得溶液的物质的量浓度恰好是 1
mol·L-1( )
(4)将 62 g Na O 溶于水中,配成 1 L 溶液,所得溶质的物质的量浓度为 1
2
mol·L-1( )
(5)0.5 mol·L-1的稀H SO 溶液中c(H+)为1.0 mol·L-1( )
2 4(6)31 g Na O溶于水,配成1 L溶液,c(Na O)=0.5 mol·L-1( )
2 2
答案 (1)× (2)× (3)× (4)× (5)√ (6)×
二、一定物质的量浓度溶液的配制
1.容量瓶
(1)构造及用途
(2)查漏操作
2.溶液的配制
以配制500 mL 1.0 mol·L-1 NaCl溶液为例:
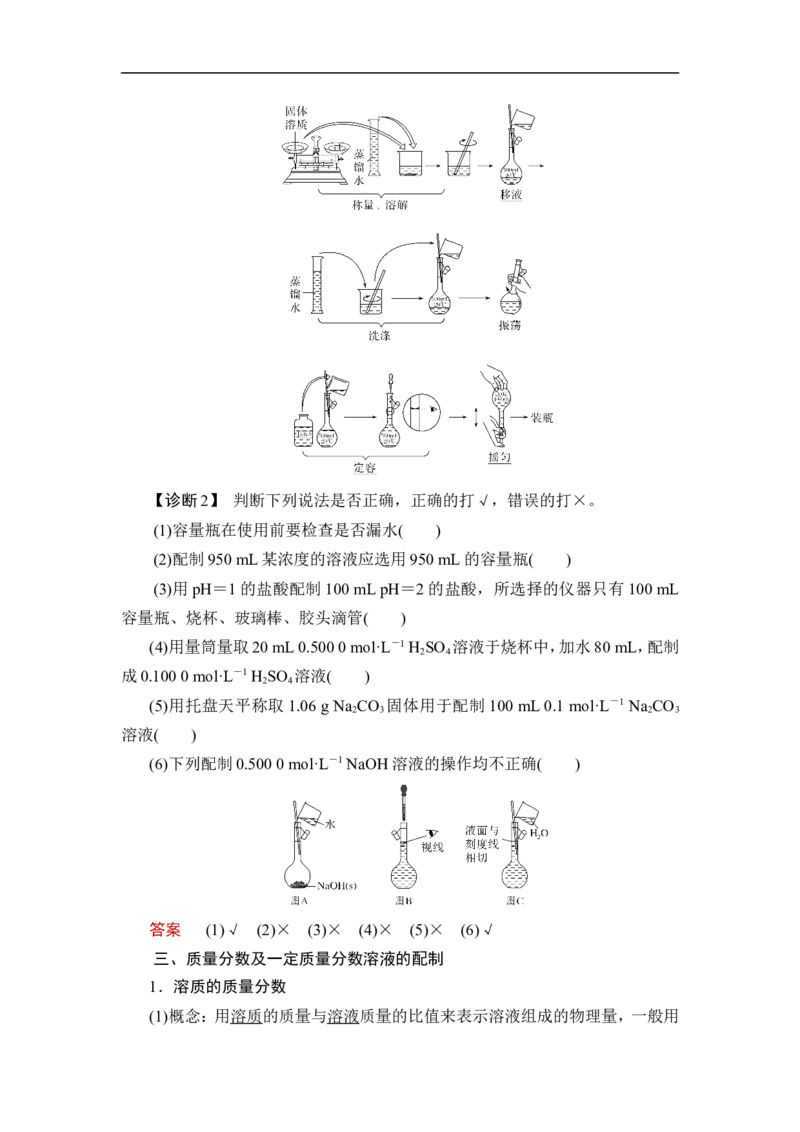
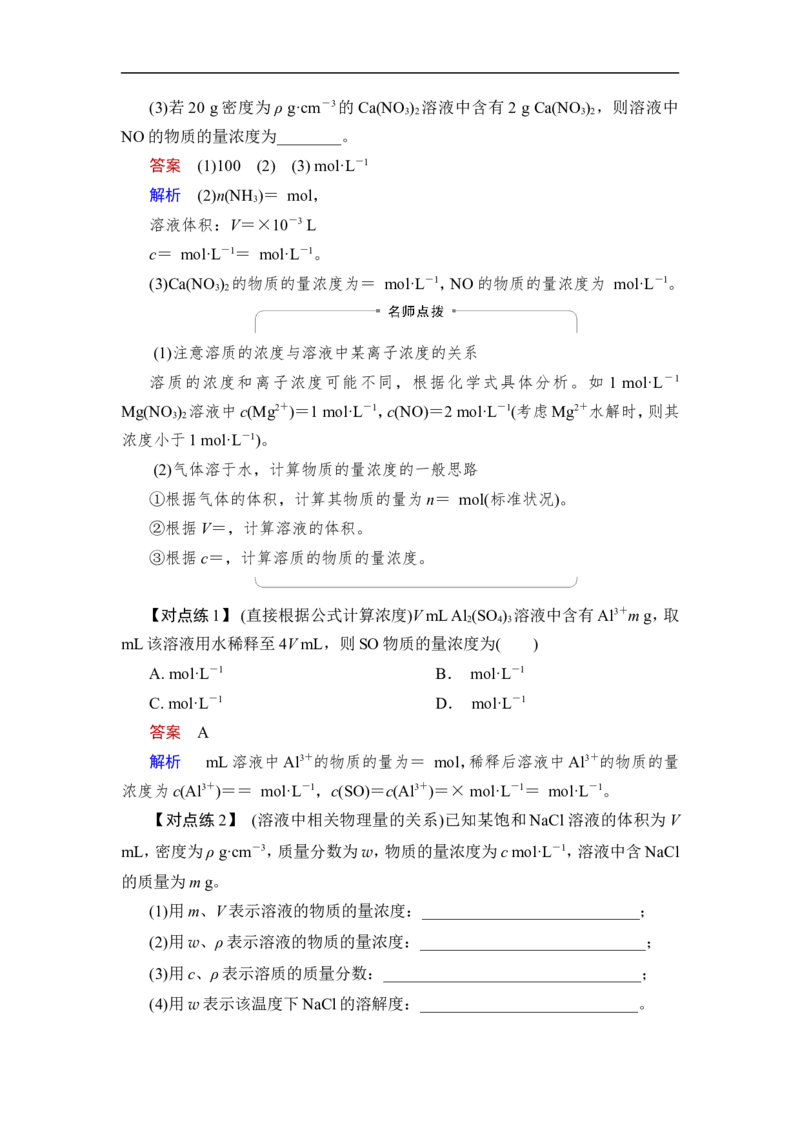
(1)配制过程
(2)图示【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)容量瓶在使用前要检查是否漏水( )
(2)配制950 mL某浓度的溶液应选用950 mL的容量瓶( )
(3)用pH=1的盐酸配制100 mL pH=2的盐酸,所选择的仪器只有100 mL
容量瓶、烧杯、玻璃棒、胶头滴管( )
(4)用量筒量取20 mL 0.500 0 mol·L-1 H SO 溶液于烧杯中,加水80 mL,配制
2 4
成0.100 0 mol·L-1 H SO 溶液( )
2 4
(5)用托盘天平称取1.06 g Na CO 固体用于配制100 mL 0.1 mol·L-1 Na CO
2 3 2 3
溶液( )
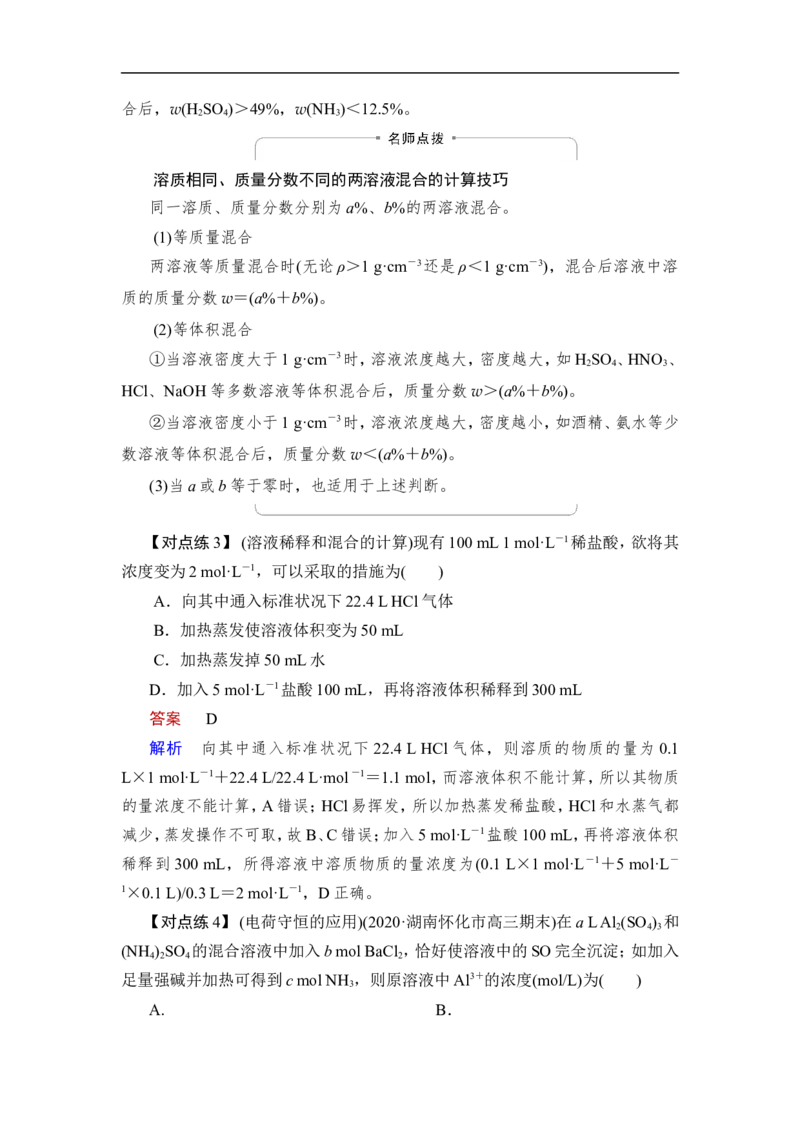
(6)下列配制0.500 0 mol·L-1 NaOH溶液的操作均不正确( )
答案 (1)√ (2)× (3)× (4)× (5)× (6)√
三、质量分数及一定质量分数溶液的配制
1.溶质的质量分数
(1)概念:用溶质的质量与溶液质量的比值来表示溶液组成的物理量,一般用百分数表示。
(2)表达式:w(B)= × 100% 。
2.质量分数与物质的量浓度的关系
c=。
3.一定质量分数溶液的配制
以配制100 g 5% NaOH溶液为例:
(1)步骤:计算→称量(量取)→溶解(稀释)。
(2)仪器:托盘天平、量筒、烧杯、玻璃棒。
4.体积比浓度溶液的配制
如用浓硫酸配制1∶4的稀硫酸50 mL:用50 mL的量筒量取40.0 mL的水注
入100 mL的烧杯中,再用10 mL的量筒量取10.0 mL浓硫酸,然后沿烧杯内壁缓
缓注入烧杯中,并用玻璃棒不停地搅拌。
【诊断3】 判断下列说法是否正确,正确的打√,错误的打×。
(1)“5%硫酸铜溶液”表示100 g硫酸铜溶液中含有5 g硫酸铜溶质( )
(2)要配制100 g溶质质量分数为10%的氯化钠溶液,应将10 g氯化钠固体溶
于100 mL水( )
(3)将25 g CuSO ·5H O晶体溶于75 g水中所得溶质的质量分数为25%( )
4 2
(4)将40 g SO 溶于60 g水中所得溶质的质量分数为49%( )
3
(5)配制氯化钠溶液称量氯化钠时可直接放在天平的托盘上称量( )
(6)应将配好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签( )
答案 (1)√ (2)× (3)× (4)√ (5)× (6)√
考点一 物质的量浓度的相关计算
【典例1】 根据题目条件计算下列溶液的相关量:
(1)2 mol·L - 1 Mg(NO ) 溶 液 中 含 有 0.4 mol NO , 则 溶 液 的 体 积 为
3 2
________mL。
(2)在标准状况下,将V L氨气溶于0.1 L水中,所得溶液的密度为ρ g·cm-3,
则此氨水的物质的量浓度为________ mol·L-1。(3)若20 g密度为ρ g·cm-3的Ca(NO ) 溶液中含有2 g Ca(NO ) ,则溶液中
3 2 3 2
NO的物质的量浓度为________。
答案 (1)100 (2) (3) mol·L-1
解析 (2)n(NH )= mol,
3
溶液体积:V=×10-3 L
c= mol·L-1= mol·L-1。
(3)Ca(NO ) 的物质的量浓度为= mol·L-1,NO的物质的量浓度为 mol·L-1。
3 2
(1)注意溶质的浓度与溶液中某离子浓度的关系
溶质的浓度和离子浓度可能不同,根据化学式具体分析。如 1 mol·L-1
Mg(NO ) 溶液中c(Mg2+)=1 mol·L-1,c(NO)=2 mol·L-1(考虑Mg2+水解时,则其
3 2
浓度小于1 mol·L-1)。
(2)气体溶于水,计算物质的量浓度的一般思路
①根据气体的体积,计算其物质的量为n= mol(标准状况)。
②根据V=,计算溶液的体积。
③根据c=,计算溶质的物质的量浓度。
【对点练1】 (直接根据公式计算浓度)V mL Al (SO ) 溶液中含有Al3+m g,取
2 4 3
mL该溶液用水稀释至4V mL,则SO物质的量浓度为( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
答案 A
解析 mL溶液中Al3+的物质的量为= mol,稀释后溶液中Al3+的物质的量
浓度为c(Al3+)== mol·L-1,c(SO)=c(Al3+)=× mol·L-1= mol·L-1。
【对点练2】 (溶液中相关物理量的关系)已知某饱和NaCl溶液的体积为V
mL,密度为ρ g·cm-3,质量分数为w,物质的量浓度为c mol·L-1,溶液中含NaCl
的质量为m g。
(1)用m、V表示溶液的物质的量浓度:___________________________;
(2)用w、ρ表示溶液的物质的量浓度:____________________________;
(3)用c、ρ表示溶质的质量分数:________________________________;
(4)用w表示该温度下NaCl的溶解度:___________________________。答案 (1) mol·L-1 (2) mol·L-1 (3)×100% (4) g
解析 (1)c(NaCl)= mol·L-1= mol·L-1。
(2)c(NaCl)== mol·L-1。
(3)w=×100%=×100%。
(4)=,S= g。
溶液中c、w、S等相关量的关系
(1)溶质的物质的量浓度c与溶质的质量分数w的关系:
c=,w=。
(2)物质的量浓度(c)与溶解度(S)的换算
若某饱和溶液的密度为ρ g·cm-3,溶质的摩尔质量为M g·mol-1,溶解度为S
g,则溶解度与物质的量浓度的表达式分别为:
S=,c===。
【典例2】 下图是某学校实验室从市场买回的试剂标签上的部分内容。
按要求回答下列问题:
(1)硫酸的物质的量浓度为________,氨水的物质的量浓度为________。
(2)各取 5 mL 与等质量的水混合后,c(H SO )________9.2 mol·L-1,
2 4
c(NH )________6.45 mol·L-1(填“>”“<”或“=”,下同)。
3
(3) 各 取 5 mL 与 等 体 积 水 混 合 后 , w(H SO )________49% ,
2 4
w(NH )________12.5%。
3
答案 (1)18.4 mol·L-1 12.9 mol·L-1
(2)< > (3)> <
解析 (1)利用c=计算,c(H SO )= mol·L-1=18.4 mol·L-1,c(NH )= mol·L
2 4 3
-1≈12.9 mol·L-1。
(2)硫酸的密度大于水,氨水的密度小于水,各取5 mL与等质量的水混合后,
所得稀硫酸的体积大于 10 mL,稀氨水的体积小于 10 mL,故有c(H SO )<9.2
2 4
mol·L-1,c(NH )>6.45 mol·L-1。
3
(3)5 mL浓硫酸和5 mL浓氨水的质量分别为1.84 g·cm-3×5 mL=9.2 g、0.88
g·cm-3×5 mL=4.4 g,而5 mL水的质量约为5 g,故各取5 mL与等体积的水混合后,w(H SO )>49%,w(NH )<12.5%。
2 4 3
溶质相同、质量分数不同的两溶液混合的计算技巧
同一溶质、质量分数分别为a%、b%的两溶液混合。
(1)等质量混合
两溶液等质量混合时(无论ρ>1 g·cm-3还是ρ<1 g·cm-3),混合后溶液中溶
质的质量分数w=(a%+b%)。
(2)等体积混合
①当溶液密度大于1 g·cm-3时,溶液浓度越大,密度越大,如H SO 、HNO 、
2 4 3
HCl、NaOH等多数溶液等体积混合后,质量分数w>(a%+b%)。
②当溶液密度小于1 g·cm-3时,溶液浓度越大,密度越小,如酒精、氨水等少
数溶液等体积混合后,质量分数w<(a%+b%)。
(3)当a或b等于零时,也适用于上述判断。
【对点练3】 (溶液稀释和混合的计算)现有100 mL 1 mol·L-1稀盐酸,欲将其
浓度变为2 mol·L-1,可以采取的措施为( )
A.向其中通入标准状况下22.4 L HCl气体
B.加热蒸发使溶液体积变为50 mL
C.加热蒸发掉50 mL水
D.加入5 mol·L-1盐酸100 mL,再将溶液体积稀释到300 mL
答案 D
解析 向其中通入标准状况下 22.4 L HCl 气体,则溶质的物质的量为 0.1
L×1 mol·L-1+22.4 L/22.4 L·mol -1=1.1 mol,而溶液体积不能计算,所以其物质
的量浓度不能计算,A错误;HCl易挥发,所以加热蒸发稀盐酸,HCl和水蒸气都
减少,蒸发操作不可取,故B、C错误;加入5 mol·L-1盐酸100 mL,再将溶液体积
稀释到300 mL,所得溶液中溶质物质的量浓度为(0.1 L×1 mol·L-1+5 mol·L-
1×0.1 L)/0.3 L=2 mol·L-1,D正确。
【对点练4】 (电荷守恒的应用)(2020·湖南怀化市高三期末)在a L Al (SO ) 和
2 4 3
(NH ) SO 的混合溶液中加入b mol BaCl ,恰好使溶液中的SO完全沉淀;如加入
4 2 4 2
足量强碱并加热可得到c mol NH ,则原溶液中Al3+的浓度(mol/L)为( )
3
A. B.C. D.
答案 B
解析 加入 BaCl 反应的离子方程式为:Ba2++SO===BaSO ↓,溶液中
2 4
n(SO)=n(Ba2+)=b mol;根据N原子守恒,溶液中n(NH)=n(NH )=c mol;原溶
3
液中的电荷守恒为:3n(Al3+)+n(NH)=2n(SO),原溶液中n(Al3+)= mol,c(Al3+)
= mol÷a L= mol/L。
(1)溶液稀释规律(守恒观点)
①溶质的质量在稀释前后保持不变,即m w =m w 。
1 1 2 2
②溶质的物质的量在稀释前后保持不变,即c V =c V 。
1 1 2 2
③溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。
(2)同溶质不同物质的量浓度溶液混合的计算
①混合后溶液体积保持不变时,c V +c V =c ×(V +V )。
1 1 2 2 混 1 2
②混合后溶液体积发生变化时,c V +c V =c V ,其中V =。
1 2 2 2 混 混 混
考点二 一定物质的量浓度溶液的配制和分析
【典例3】 (2020·福建福清高三月考)某实验需要1.84 mol·L-1的稀硫酸450
mL,回答下列问题:
(1)配制时需要98%密度为1.84 g·cm-3的浓硫酸________mL。
(2)配制时,必须使用的仪器有________(填代号),还缺少的仪器是________。
①烧杯 ②50 mL量筒 ③100 mL量筒
④1000 mL容量瓶 ⑤500 mL容量瓶 ⑥托盘天平(带砝码) ⑦玻璃棒
(3)配制时,该实验两次用到玻璃棒,其作用分别是________、________。
(4)下列操作的顺序是(用字母表示)________。
A.冷却 B.量取
C.洗涤两次 D.定容
E.稀释 F.摇匀
G.转移
(5)下列操作中,容量瓶所不具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液C.用来加热溶解固体溶质
D.作为反应容器
答案 (1)50 (2)①②⑤⑦ 胶头滴管 (3)搅拌 引流
(4)BEAGCGDF (5)BCD
解析 (1)98%密度为1.84 g·cm-3的浓硫酸的物质的量浓度是 mol/L=18.4
mol/L,根据稀释规律得1.84 mol/L×0.5 L÷18.4 mol/L=0.05 L=50 mL;
(2)配制500 mL的溶液,需要的仪器是:50 mL量筒量取浓硫酸、烧杯用于稀
释浓硫酸、500 mL的容量瓶、玻璃棒用于搅拌,定容时还缺少胶头滴管;
(3)第一次用到玻璃棒是稀释浓硫酸时用于搅拌,第二次用玻璃棒是在移液
时起到引流作用;
(4)根据溶液配制的一般步骤,先量取浓硫酸,然后在烧杯中稀释、冷却后将
溶液移入容量瓶中,洗涤烧杯、玻璃棒两次,也把洗涤液移入容量瓶中,然后定容
摇匀,所以答案是BEAGCGDF;
(5)容量瓶只能用来配制一定浓度、一定体积的溶液,不能用来长期贮存溶液
作反应容器和加热容器,所以答案选BCD。
容量瓶的选择和使用
(1)选用容量瓶的原则——“大而近”,如需90 mL溶液,则选用100 mL容量
瓶配制。
(2)选用容量瓶时,应指明其规格。
(3)往容量瓶中转移液体时,用玻璃棒引流,玻璃棒末端应在容量瓶刻度线以
下。
【对点练5】 (配制溶液的规范操作)(2020·山西太原模拟)配制一定物质的量
浓度的NaCl溶液时,下列操作不正确的是( )答案 C
【对点练6】 (固体溶质溶液的配制)实验室需要配制0.50 mol·L-1 NaCl溶液
480 mL。
按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(带砝码、最小砝码为5
g)、药匙、烧杯、________、________、________以及等质量的两片同种纸片。
(2)计算。配制该溶液需要NaCl晶体________g。
(3)称量。
①天平调平之后,应将天平的游码调至某个位置,请在下图中用一根竖线标
出游码左边缘所处的位置:
②称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
(4) 溶 解 、 冷 却 。 该 步 实 验 中 需 要 使 用 玻 璃 棒 , 目 的 是
__________________________________________________。
(5)转移、洗涤。在转移时应使用玻璃棒引流,需要洗涤烧杯和玻璃棒2~3次
是为了_____________________________。
(6)定容。向容量瓶中加水至液面接近刻度线________处,改用________加水
使溶液凹液面与刻度线相切。
(7)摇匀、装瓶。
答案 (1)500 mL容量瓶 胶头滴管 玻璃棒
(2)14.6(3)①
②左盘
(4)搅拌,加速NaCl溶解
(5)保证溶质全部转入容量瓶中
(6)1~2 cm 胶头滴管
配制一定物质的量浓度溶液时注意事项
(1)解答需要补充仪器的实验题时,要学会“有序思考”——即按照实验的先
后顺序、步骤,思考每一步所需仪器,然后与已知仪器比较,寻找要补充的仪器。
(2)所用定量仪器的精确度:量筒(精确到0.1 mL)、托盘天平(精确到0.1 g)。
【典例4】 分析误差填空。(用“偏大”“偏小”或“无影响”填空)。
(1)配制450 mL 0.1 mol·L-1的NaOH溶液,用托盘天平称取NaOH固体1.8
g:________。
(2)配制 500 mL 0.1 mol·L-1的硫酸铜溶液,用托盘天平称取胆矾 8.0 g:
________。
(3)配制NaOH溶液时,托盘天平的两个托盘上放两张质量相等的纸片,其他
操作均正确:________。
(4)配制一定物质的量浓度的NaOH溶液,需称量溶质4.4 g,称量时物码放置
颠倒:________。
(5)用量筒量取浓硫酸时,仰视读数:________。
(6)定容时,加水超过刻度线,用胶头滴管吸取多余的液体至刻度线:
________。
(7)未经洗涤烧杯及玻璃棒:________。
(8)配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却
立即转移到容量瓶中并定容:________。
(9)定容摇匀后,发现液面下降,继续加水至刻度线:________。
(10)定容时仰视刻度线:________。
(11)定容摇匀后少量溶液外流:________。
(12)容量瓶中原有少量蒸馏水:________。
答案 (1)偏小 (2)偏小 (3)偏小 (4)偏小 (5)偏大(6)偏小 (7)偏小 (8)偏大 (9)偏小 (10)偏小
(11)无影响 (12)无影响
解析 (1)配制时应选用500 mL容量瓶,所需NaOH固体质量为0.5 L×0.1
mol·L-1×40 g·mol-1=2.0 g。(2)胆矾的摩尔质量为250 g·mol-1,所需质量为0.5
L×0.1 mol·L-1×250 g·mol-1=12.5 g。(3)NaOH易吸水潮解,会沾在纸片上,不
能全部转移到烧杯中。(4)实际称量NaOH的质量为4.0 g-0.4 g=3.6 g。(8)NaOH
溶于水放热,未冷却时溶液的体积比室温时大,应恢复室温后再移液、定容。(9)溶
液的总体积超出了刻度线。
配制误差分析的思维流程
【对点练7】 (溶液配制的误差分析)在配制一定物质的量浓度的盐酸时,下列
操作可使所配溶液浓度偏高的是( )
A.未将洗涤烧杯和玻璃棒的溶液移入容量瓶
B.用量筒量取浓盐酸时,仰视读数
C.定容时仰视刻度线
D.溶解搅拌时造成液体溅出
答案 B
解析 未将洗涤烧杯和玻璃棒的溶液移入容量瓶中,溶质的物质的量减少,
所配溶液的浓度偏低,A项错误;用量筒量取浓盐酸时,仰视读数,量取的浓盐酸
体积偏大,所配溶液浓度偏高,B项正确;定容时仰视刻度线,会造成水量偏多,
所以溶液浓度偏低,C项错误;溶解搅拌时造成液体溅出,溶质的物质的量减少,
所配溶液的浓度偏低,D项错误。
【对点练8】 (仪器读数的误差分析)试分析下列情况的误差:
(1)用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度________(填“偏
高”、“偏低”或“无影响”)。
(2)某同学用标准氢氧化钠溶液滴定待测盐酸的物质的量浓度时,若滴定前,
读碱液体积时仰视碱式滴定管液面;滴定后,读碱液体积时俯视碱式滴定管液面
上述操作会使盐酸浓度的测定值________(填“偏高”、“偏低”或“无影响”)。(3)量筒内有95 mL水,读数时仰视,则读数________(填“偏高”、“偏低”或
“无影响”);若量取95 mL水时仰视刻度,则实际量取的水的体积________(填
“大于”、“小于”或“等于”)95 mL。
答案 (1)偏高 (2)偏低 (3)偏低 大于
(1)配制溶液定容时,视线引起误差分析
①仰视刻度线(图1),导致溶液体积偏大,溶液浓度偏低。
②俯视刻度线(图2),导致溶液体积偏小,溶液浓度偏高。
(2)不同仪器的仰视和俯视
量取一定体积的液体时:
仪器类型 观察方法 误差
仰视 偏高(偏大)
“0”刻度在下边
俯视 偏低(偏小)
仰视 偏低(偏小)
“0”刻度在上边
俯视 偏高(偏大)
微专题3 化学计算的常用方法
方法一 守恒法
1.含义
所谓“守恒”就是物质在发生“变化”或两物质在发生“反应”的过程中
某些物理量的总量保持“不变”。在化学变化中存在各种守恒,如质量守恒、原子
守恒、得失电子守恒、电荷守恒、能量守恒、物料守恒等。
2.解题步骤
类型(一) 原子守恒1.密胺是重要的工业原料,结构简式如图所示。工业上以液氨和二氧化碳为
原料,以硅胶为催化剂,在一定条件下通过系列反应生成密胺。若原料完全反应
生成密胺,则NH 和CO 的质量之比应为( )
3 2
A.17∶44 B.22∶17
C.17∶22 D.2∶1
答案 C
解析 根据密胺的结构简式和原子守恒可知,一个密胺分子中有三个碳原子
和六个氮原子,所以合成1 mol密胺需要3 mol CO 和6 mol NH ,NH 和CO 的
2 3 3 2
质量之比应为(6×17)∶(3×44)=17∶22。
2.28 g铁粉溶于稀盐酸中,然后加入足量的Na O 固体,充分反应后过滤,将
2 2
滤渣加强热,最终得到的固体质量为( )
A.36 g B.40 g
C.80 g D.160 g
答案 B
解析 28 g铁粉溶于稀盐酸中生成氯化亚铁溶液,然后加入足量的Na O 固
2 2
体,由于Na O 固体溶于水后生成氢氧化钠和氧气,本身也具有强氧化性,所以充
2 2
分反应后生成氢氧化铁沉淀,过滤,将滤渣加强热,最终得到的固体为Fe O ,根
2 3
据铁原子守恒,n(Fe O )=n(Fe)=×=0.25 mol,所得Fe O 固体的质量为:0.25
2 3 2 3
mol×160 g·mol-1=40 g。
类型(二) 电荷守恒
3.将a g Fe O 、Al O 样品溶解在过量的200 mL pH=1的硫酸溶液中,然后
2 3 2 3
向其中加入NaOH溶液,使Fe3+、Al3+刚好沉淀完全,用去NaOH溶液100 mL,
则NaOH溶液的浓度为________。
答案 0.2 mol·L-1
解析 当Fe3+、Al3+刚好沉淀完全时,溶液中溶质只有硫酸钠,而Na+全部来
源于NaOH,且变化过程中Na+的量不变。根据电荷守恒可知:=,所以,n(NaOH)
=n(Na+)=2n(SO)=n(H+)=0.1 mol·L-1×0.2 L=0.02 mol,c(NaOH)==0.2
mol·L-1。
4.若测得雨水所含水溶性无机离子的化学组分及其平均浓度如下表:离子 K+ Na+ NH SO NO Cl-
浓度/
4×10-6 6×10-6 2×10-5 4×10-5 3×10-5 2×10-5
mol·L-1
根据表中数据判断试样的pH=________。
答案 4
解析 根据表格提供的离子可知,NH水解导致试样溶液呈酸性,再根据电荷
守恒可知,c(K+)+c(NH)+c(Na+)+c(H+)=2c(SO)+c(Cl-)+c(NO),将表格中的
数据代入得H+浓度为10-4 mol·L-1,则pH为4。
方法二 关系式法
关系式是表示两种或多种物质之间“量”的关系的一种简化式子,在多步反
应中,它可以把始态的反应物与终态的生成物之间“量”的关系表示出来,把多
步计算简化成一步计算。高考题量大,时间紧,对于涉及多步计算的问题,如滴定
实验的有关计算,巧妙运用关系式法,可以缩短答题时间;解题的关键是正确书
写关系式。
类型(一) 根据多步反应的方程式找关系式
1.为测定某石灰石中CaCO 的质量分数,称取W g石灰石样品,加入过量的
3
浓度为6 mol·L-1的盐酸,使它完全溶解,加热煮沸,除去溶解的CO ,再加入足
2
量的草酸铵[(NH ) C O ]溶液后,慢慢加入氨水降低溶液的酸度,则析出草酸钙沉
4 2 2 4
淀,离子方程式为C O+Ca2+===CaC O ↓,过滤出CaC O 后,用稀硫酸溶解:
2 2 4 2 4
CaC O +H SO ===H C O +CaSO ,再用蒸馏水稀释溶液至V mL。取出V mL
2 4 2 4 2 2 4 4 0 1
用a mol·L-1的酸性KMnO 溶液滴定,此时发生反应:2MnO+5H C O +6H+
4 2 2 4
===2Mn2++10CO ↑+8H O。若滴定终点时消耗a mol·L-1的KMnO V mL,计
2 2 4 2
算样品中CaCO 的质量分数。
3
答案 %
解析 本题涉及的化学方程式或离子方程式为
CaCO +2H+===Ca2++2CO ↑+H O
3 2 2
C O+Ca2+===CaC O ↓
2 2 4
CaC O +H SO ===H C O +CaSO
2 4 2 4 2 2 4 4
2MnO+5H C O +6H+===2Mn2++10CO ↑+8H O
2 2 4 2 2
由方程式可以得出相应的关系式样品中n(CaCO )=2.5aV ×10-3× mol
3 2
则w(CaCO )=×100%=%。
3
2.(2018·课标全国Ⅲ节选)硫代硫酸钠晶体(Na S O ·5H O,M=248 g·mol-1)
2 2 3 2
可用作定影剂、还原剂。
利用K Cr O 标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
2 2 7
滴定:取0.009 50 mol·L-1的K Cr O 标准溶液20.00 mL,硫酸酸化后加入过
2 2 7
量KI,发生反应:Cr O+6I-+14H+===3I +2Cr3++7H O。然后用硫代硫酸钠样
2 2 2
品溶液滴定至淡黄绿色,发生反应:I +2S O===S O+2I-。加入淀粉溶液作为指
2 2 4
示剂,继续滴定,当溶液________,即为终点。平行滴定3次,样品溶液的平均用
量为24.80 mL,则样品纯度为________%(保留1位小数)。
答案 蓝色褪去 95.0
解析 利用I 遇淀粉溶液显蓝色来判断滴定终点时,当溶液蓝色褪去,且半
2
分钟内不恢复即可说明达到滴定终点。根据题中反应可得:Cr O~3I ~6S O,则
2 2 2
1.200 0 g样品中含有Na S O ·5H O的质量=××248 g·mol-1=1.140 g,样品纯
2 2 3 2
度=×100%=95.0%。
多步反应找关系式的解题步骤
类型(二) 根据不同物质中所含同种元素的原子个数找关系式
3.银铜合金广泛用于航空工业,从切割废料中回收银并制备铜化工产品的
工艺如下:[注:Al(OH) 和Cu(OH) 开始分解的浓度分别为450 ℃和80℃]。若铜银合金
3 2
中铜的质量分数为63.5%,理论上5.0 kg废料中的铜可完全转化为________ mol
CuAlO ,至少需要1.0 mol·L-1的Al (SO ) 溶液________ L。(已知Cu相对原子质
2 2 4 2
量为63.5)
答案 50 25.0
解析 5.0 kg银铜合金中铜的物质的量为
n(Cu)==50 mol
根据流程图分析再由Cu原子守恒可得如下关系
4Cu~4CuO~2Al (SO ) ~4CuAlO
2 4 3 2
即,2Cu,~,Al (SO ) ,~,2CuAlO ,,2,,1,,2)
2 4 3 2
所以可完全转化生成50 mol CuAlO ,
2
至少需要Al (SO ) 的体积为=25.0 L。
2 4 3
用原子守恒找关系式的方法
(1)实际化工生产中往往涉及多步反应,但原料和产品中的某种主要元素是相
同的,据此可以找出关系式,如利用转化反应中Cu原子守恒可得出关系式:Cu~
CuO~CuSO ~CuAlO ,这样可避免书写化学方程式,缩短解题时间。
4 2
(2)寻找关系式时,要特别注意原料中的主要元素是否全部转化为产物,如不
能完全转化,可以将分步转化率换算成总转化率进行计算。
方法三 热重分析法
1.设晶体为1 mol,其质量为m。
2.失重一般是先失水,再失非金属氧化物。
3.计算每步固体剩余的质量(m )
余
×100%=固体残留率。
4.晶体中金属质量不再减少,仍在m 中。
余5.失重最后一般为金属氧化物,由质量守恒得m ,由n ∶n ,即可求出
氧 金属 氧
失重后物质的化学式。
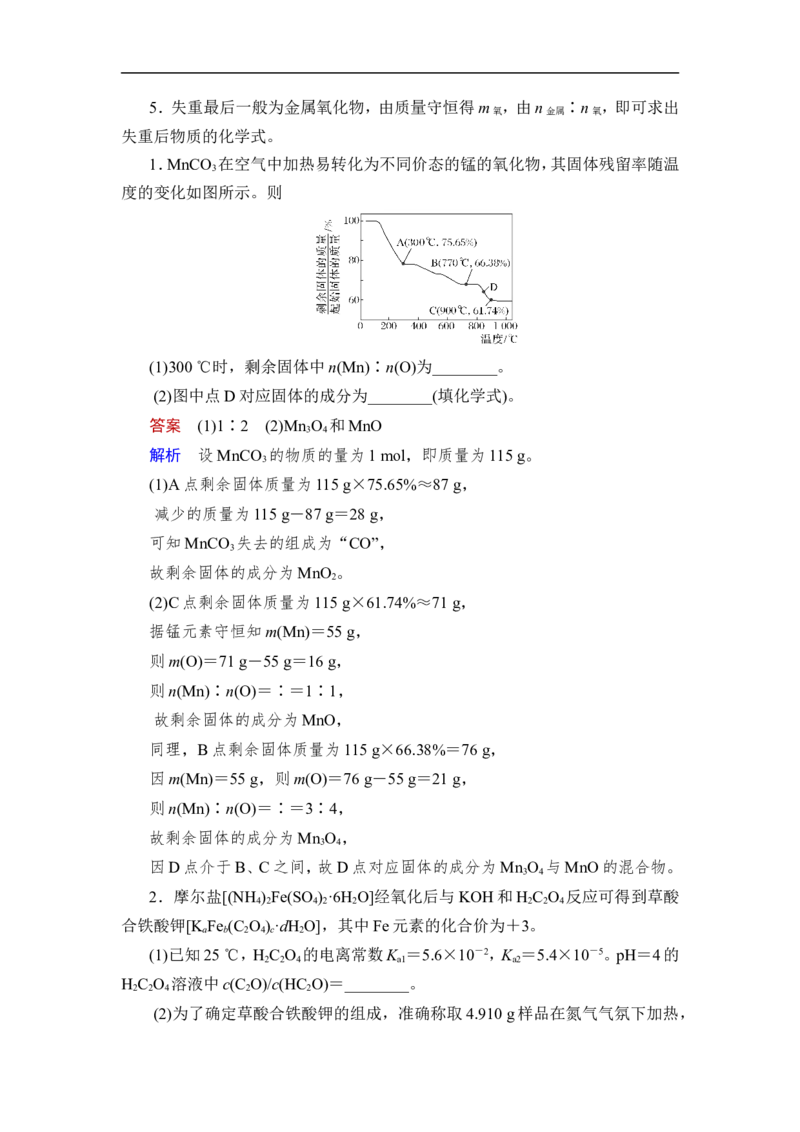
1.MnCO 在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温
3
度的变化如图所示。则
(1)300 ℃时,剩余固体中n(Mn)∶n(O)为________。
(2)图中点D对应固体的成分为________(填化学式)。
答案 (1)1∶2 (2)Mn O 和MnO
3 4
解析 设MnCO 的物质的量为1 mol,即质量为115 g。
3
(1)A点剩余固体质量为115 g×75.65%≈87 g,
减少的质量为115 g-87 g=28 g,
可知MnCO 失去的组成为“CO”,
3
故剩余固体的成分为MnO 。
2
(2)C点剩余固体质量为115 g×61.74%≈71 g,
据锰元素守恒知m(Mn)=55 g,
则m(O)=71 g-55 g=16 g,
则n(Mn)∶n(O)=∶=1∶1,
故剩余固体的成分为MnO,
同理,B点剩余固体质量为115 g×66.38%=76 g,
因m(Mn)=55 g,则m(O)=76 g-55 g=21 g,
则n(Mn)∶n(O)=∶=3∶4,
故剩余固体的成分为Mn O ,
3 4
因D点介于B、C之间,故D点对应固体的成分为Mn O 与MnO的混合物。
3 4
2.摩尔盐[(NH ) Fe(SO ) ·6H O]经氧化后与KOH和H C O 反应可得到草酸
4 2 4 2 2 2 2 4
合铁酸钾[K Fe (C O ) ·dH O],其中Fe元素的化合价为+3。
a b 2 4 c 2
(1)已知25 ℃,H C O 的电离常数K =5.6×10-2,K =5.4×10-5。pH=4的
2 2 4 a1 a2
H C O 溶液中c(C O)/c(HC O)=________。
2 2 4 2 2
(2)为了确定草酸合铁酸钾的组成,准确称取4.910 g样品在氮气气氛下加热,固体样品的剩余质量随温度的变化如图所示。
已知:a.120 ℃时样品已完全失去结晶水;
b.200~580 ℃样品分解产生的 CO和CO 恢复至标准状况下体积为 1.008
2
L;
c.580 ℃以上残留固体为FeO和K CO 的混合物。
2 3
根据以上实验数据计算草酸合铁酸钾的化学式为________。
答案 (1)0.54 (2)K Fe(C O ) ·3H O
3 2 4 3 2
解析 (1)已知25 ℃,H C O 的电离常数K =5.6×10-2,K =5.4×10-5。pH
2 2 4 a1 a2
=4 的 H C O 溶液中====0.54。(2)120 ℃时样品已完全失去结晶水,则
2 2 4
m(H O)=4.910 g-4.37 g=0.54 g,n(H O)=3×10-2 mol;又已知分解产生的CO
2 2
和 CO 满足 n(CO)+n(CO )==4.5×10-2 mol,根据原子守恒有 2n(C O)=
2 2 2
n(K CO )+n(CO)+n(CO )=n(K CO )+4.5×10-2 mol,由已知信息c及题图可知
2 3 2 2 3
m(FeO)+m(K CO )=n(Fe3+)×72 g·mol-1+n(K+)×138 g·mol-1=2.79 g,又
2 3
K Fe (C O ) 呈电中性,则 3n(Fe3+)+n(K+)=2×n(C O)=n(K CO )+n(CO)+
a b 2 4 c 2 2 3
n(CO )=n(K CO )+4.5×10-3=n(K+)+4.5×10-2 mol,解得n(Fe3+)=1×10-2
2 2 3
mol,n(K+)=3×10-2 mol,n(C O)=3×10-2 mol,则样品中 n(K+)∶n(Fe3
2
+)∶n(C O)∶n(H O)=(3×10-2 mol)∶(1×10-2 mol)∶(3×10-2 mol)∶(3×10-2
2 2
mol)=3∶1∶3∶3,故草酸合铁酸钾的化学式为K Fe(C O ) ·3H O。
3 2 4 3 2
1.金属锡的纯度可以通过下述方法测定:将试样溶于盐酸,反应的化学方程
式为Sn+2HCl===SnCl +H ↑,再加入过量的FeCl 溶液,发生如下反应:SnCl
2 2 3 2
+2FeCl ===SnCl +2FeCl ,最后用已知浓度的K Cr O 溶液滴定生成的Fe2+,反
3 4 2 2 2 7
应的化学方程式为6FeCl +K Cr O +14HCl===6FeCl +2KCl+2CrCl +7H O。
2 2 2 7 3 3 2
现有金属锡试样0.613 g,经上述反应后,共用去0.100 mol·L-1 K Cr O 溶液16.0
2 2 7
mL。求试样中锡的百分含量________(假定杂质不参加反应,锡的相对原子质量
为119)。
答案 93.2%
解析 设Sn的质量为x,Sn与K Cr O 物质的量的关系:
2 2 73Sn~3SnCl ~6FeCl ~K Cr O
2 2 2 2 7
3×119 g 1 mol
x 0.100×0.016 mol
x==0.571 2 g
w(Sn)=×100%≈93.2%。
2.Ba2+是一种重金属离子,有一环境监测小组欲利用Na S O 、KI、K Cr O 等
2 2 3 2 2 7
试剂测定某工厂废水中Ba2+的物质的量浓度,取废水50.00 mL,控制适当的酸度
加入足量的K Cr O 溶液,得到BaCrO 沉淀;沉淀经洗涤、过滤后,用适量稀硫酸
2 2 7 4
处理,此时CrO全部转化为Cr O;再加入过量KI溶液进行反应,然后在反应液中
2
滴加0.100 mol·L-1的标准Na S O 溶液,反应完全时,消耗Na S O 溶液36.00
2 2 3 2 2 3
mL。已知有关反应的离子方程式为①Cr O+6I-+14H+===2Cr3++3I +7H O;
2 2 2
②2S O+I ===2I-+S O。则该工厂废水中Ba2+的物质的量浓度为________。
2 2 4
答案 0.024 mol·L-1
解析 设Ba2+的物质的量为x,则根据相关反应可得以下关系式:
Ba2+~BaCrO ~Cr O~I ~3S O
4 2 2 2
1 mol 3 mol
x 0.036 L×0.100 mol·L-1
解得x=1.2×10-3 mol,则c(Ba2+)==0.024 mol·L-1。
3.BaCrO 常用于制备颜料、陶瓷、玻璃、安全火柴等。为了测定某铬酸钡样品
4
中BaCrO 的含量,进行如下实验:
4
w g样品――→I 、Cr3+、Ba2+、Cl-
2
――→终点
已知:杂质不参与反应;滴定反应为I +2S O===2I-+S O。
2 2 4
(1) 写 出 BaCrO 与 过 量 HI 溶 液 反 应 的 离 子 方 程 式 :
4
____________________________________________。
(2)BaCrO 的摩尔质量为 M g·mol-1,则样品中 BaCrO 的质量分数为
4 4
________%(用代数式表示)。
答案 (1)2BaCrO +6I-+16H+===2Ba2++2Cr3++3I +8H O (2)
4 2 2
解析 根据题示信息,BaCrO 中+6价Cr元素被还原成Cr3+,HI中I-被氧
4
化成I ,根据得失电子守恒配平离子方程式 2BaCrO +6I-+16H+===2Ba2++
2 4
2Cr3++3I +8H O,由滴定反应知,2BaCrO ~3I ~6Na S O ,3n(BaCrO )=
2 2 4 2 2 2 3 4
n(Na S O ),则样品中BaCrO 的质量分数为×100%=%。
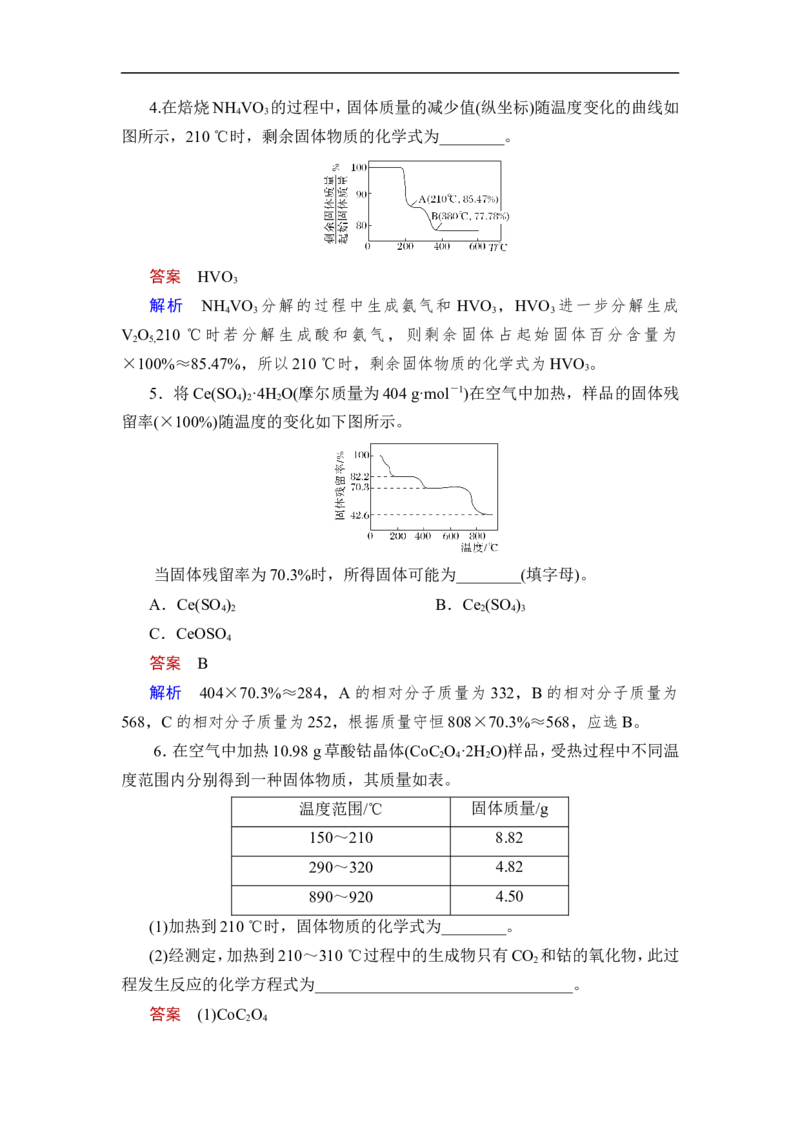
2 2 3 44.在焙烧NH VO 的过程中,固体质量的减少值(纵坐标)随温度变化的曲线如
4 3
图所示,210 ℃时,剩余固体物质的化学式为________。
答案 HVO
3
解析 NH VO 分解的过程中生成氨气和 HVO ,HVO 进一步分解生成
4 3 3 3
V O 210 ℃时若分解生成酸和氨气,则剩余固体占起始固体百分含量为
2 5,
×100%≈85.47%,所以210 ℃时,剩余固体物质的化学式为HVO 。
3
5.将Ce(SO ) ·4H O(摩尔质量为404 g·mol-1)在空气中加热,样品的固体残
4 2 2
留率(×100%)随温度的变化如下图所示。
当固体残留率为70.3%时,所得固体可能为________(填字母)。
A.Ce(SO ) B.Ce (SO )
4 2 2 4 3
C.CeOSO
4
答案 B
解析 404×70.3%≈284,A的相对分子质量为 332,B的相对分子质量为
568,C的相对分子质量为252,根据质量守恒808×70.3%≈568,应选B。
6.在空气中加热10.98 g草酸钴晶体(CoC O ·2H O)样品,受热过程中不同温
2 4 2
度范围内分别得到一种固体物质,其质量如表。
温度范围/℃ 固体质量/g
150~210 8.82
290~320 4.82
890~920 4.50
(1)加热到210 ℃时,固体物质的化学式为________。
(2)经测定,加热到210~310 ℃过程中的生成物只有CO 和钴的氧化物,此过
2
程发生反应的化学方程式为________________________________。
答案 (1)CoC O
2 4(2)3CoC O +2O =====Co O +6CO
2 4 2 3 4 2
解析 (1)CoC O ·2H O失去全部结晶水的质量为10.98× g=8.82 g,即加热
2 4 2
到210 ℃时,固体物质是CoC O 。(2)根据元素守恒,n(CO )=×2 mol=0.12 mol,
2 4 2
质量为0.12 mol×44 g·mol-1=5.28 g,而固体质量减少为(8.82-4.82) g=4.00 g,
说明有气体参加反应,即氧气参加,氧气的质量为(5.28-4.00) g=1.28 g,其物质
的量为 mol=0.04 mol,n(CoC O )∶n(O )∶n(CO )=∶0.04∶0.12=3∶2∶6,依
2 4 2 2
据原子守恒,3CoC O +2O =====Co O +6CO 。微专题4 溶解度及溶解度曲线
2 4 2 3 4 2
1.固体物质的溶解度
(1)概念:在一定温度下,某固体物质在100 g溶剂(通常是水)里达到饱和状
态时所溶解的质量,叫作这种物质在该溶剂里的溶解度,其单位为“g”。
(2)计算:饱和溶液中存在的两比例:①=;
②=。
(3)影响溶解度大小的因素
①内因:物质本身的性质(由结构决定)。
②外因:
a.溶剂的影响(如NaCl易溶于水而不易溶于汽油)。
b.温度的影响:升温,大多数固体物质在水中的溶解度增大,少数物质溶解度
减小,如Ca(OH) ;温度对NaCl的溶解度影响不大。
2
2.气体物质的溶解度
(1)表示方法:通常指该气体(其压强为101 kPa)在一定温度时溶解于1体积水
里达到饱和状态时气体的体积,常记为1∶x。如NH 、HCl、SO 、CO 气体常温时
3 2 2
在水中的溶解度分别为1∶700、1∶500、1∶40、1∶1。
(2)影响因素:气体物质溶解度的大小与温度和压强有关,温度升高,溶解度
减小;压强增大,溶解度增大。
3.溶解度曲线
(1)常见物质的溶解度曲线(g/100 g水)(2)溶解度曲线的意义
①点:曲线上的点叫饱和点。
a.曲线上任一点表示对应温度下该物质的溶解度;
b.两曲线的交点表示两物质在该交点的温度下溶解度相等。
②线:溶解度曲线表示物质的溶解度随温度变化的趋势,其变化趋势分为三
种:
a.陡升型:大部分固体物质的溶解度随温度升高而增大,且变化较大,如硝
酸钾,提纯时常采用降温结晶(冷却热饱和溶液)的方法;
b.下降型:极少数物质的溶解度随温度升高反而减小,如熟石灰的饱和溶液
升温时变浑浊;
c.缓升型:少数物质的溶解度随温度变化不大,如氯化钠,提纯时常采用蒸
发结晶(蒸发溶剂)的方法。
③面:
a.溶解度曲线下方的面表示相应温度下该物质的不饱和溶液;
b.溶解度曲线上方的面表示相应温度下该物质的过饱和溶液,可以结晶析
出晶体。
(3)溶解度曲线的应用
利用溶解度曲线选择不同的物质分离方法:
①溶解度受温度影响较小的物质(如NaCl)采取蒸发结晶的方法;若NaCl溶液中含有KNO ,应采取蒸发结晶,趁热过滤的方法。
3
②溶解度受温度影响较大的物质(或带有结晶水)采取蒸发浓缩、冷却结晶的
方法;若KNO 溶液中含有NaCl,应采取加热浓缩、冷却结晶、过滤的方法。
3
【案例1】 溶解度曲线的意义MgSO 、NaCl的溶解度曲线如图所示。下列说
4
法正确的是( )
A.MgSO 的溶解度随温度升高而升高
4
B.NaCl的溶解度比MgSO 的溶解度大
4
C.T ℃时,MgSO 饱和溶液溶质的质量分数最大
2 4
D.将MgSO 饱和溶液的温度从T ℃降至T ℃时,有晶体析出
4 3 2
答案 C
解析 温度低于T ℃时,MgSO 的溶解度随温度升高而增大,高于T ℃时,
2 4 2
MgSO 的溶解度随温度升高而降低,A错误;T ℃、T ℃时,NaCl、MgSO 的溶解
4 1 3 4
度相等,B错误;w=×100%,S越大,w越大,C正确;将MgSO 饱和溶液的温度
4
从T ℃降至T ℃时,MgSO 的溶解度增大,由饱和溶液变成不饱和溶液,不会有
3 2 4
晶体析出,D错误。
【案例2】 根据溶解度曲线进行分离提纯
(2017·课标全国Ⅲ,27)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,
铬铁矿的主要成分为FeO·Cr O ,还含有硅、铝等杂质。制备流程如图所示:
2 3
回答下列问题:
已知:有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,
冷却结晶,过滤得到K Cr O 固体。冷却到________(填标号)得到的K Cr O 固体
2 2 7 2 2 7
产品最多。a.80 ℃ b.60 ℃
c.40 ℃ d.10 ℃
步骤⑤的反应类型是________。
答案 d 复分解反应
解析 由溶解度曲线图可知,10 ℃时K Cr O 溶解度最小,而Na Cr O 、
2 2 7 2 2 7
KCl、NaCl此时溶解度均大于K Cr O ,三者均存在于溶液当中,故冷却到10 ℃
2 2 7
时 得 到 的 K Cr O 固 体 最 多 , 该 步 骤 的 反 应 化 学 方 程 式 为 2KCl +
2 2 7
Na Cr O ===2NaCl+K Cr O ,该反应为复分解反应。
2 2 7 2 2 7
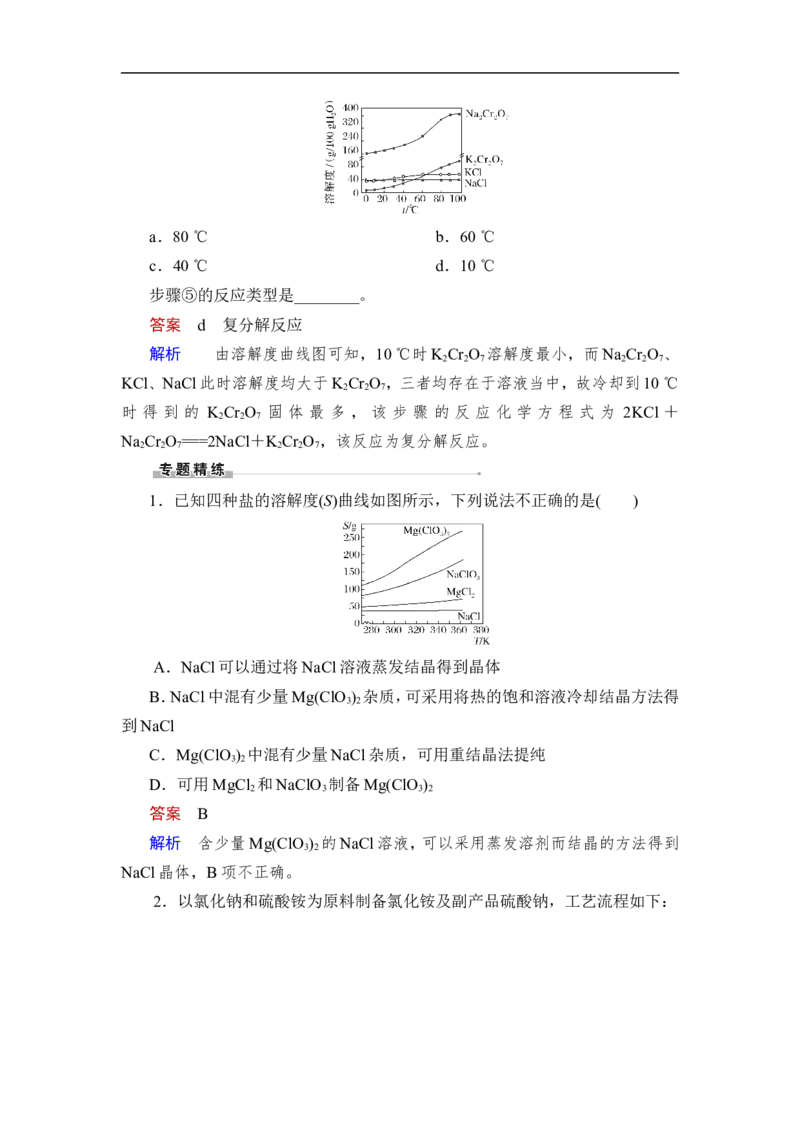
1.已知四种盐的溶解度(S)曲线如图所示,下列说法不正确的是( )
A.NaCl可以通过将NaCl溶液蒸发结晶得到晶体
B.NaCl中混有少量Mg(ClO ) 杂质,可采用将热的饱和溶液冷却结晶方法得
3 2
到NaCl
C.Mg(ClO ) 中混有少量NaCl杂质,可用重结晶法提纯
3 2
D.可用MgCl 和NaClO 制备Mg(ClO )
2 3 3 2
答案 B
解析 含少量Mg(ClO ) 的NaCl溶液,可以采用蒸发溶剂而结晶的方法得到
3 2
NaCl晶体,B项不正确。
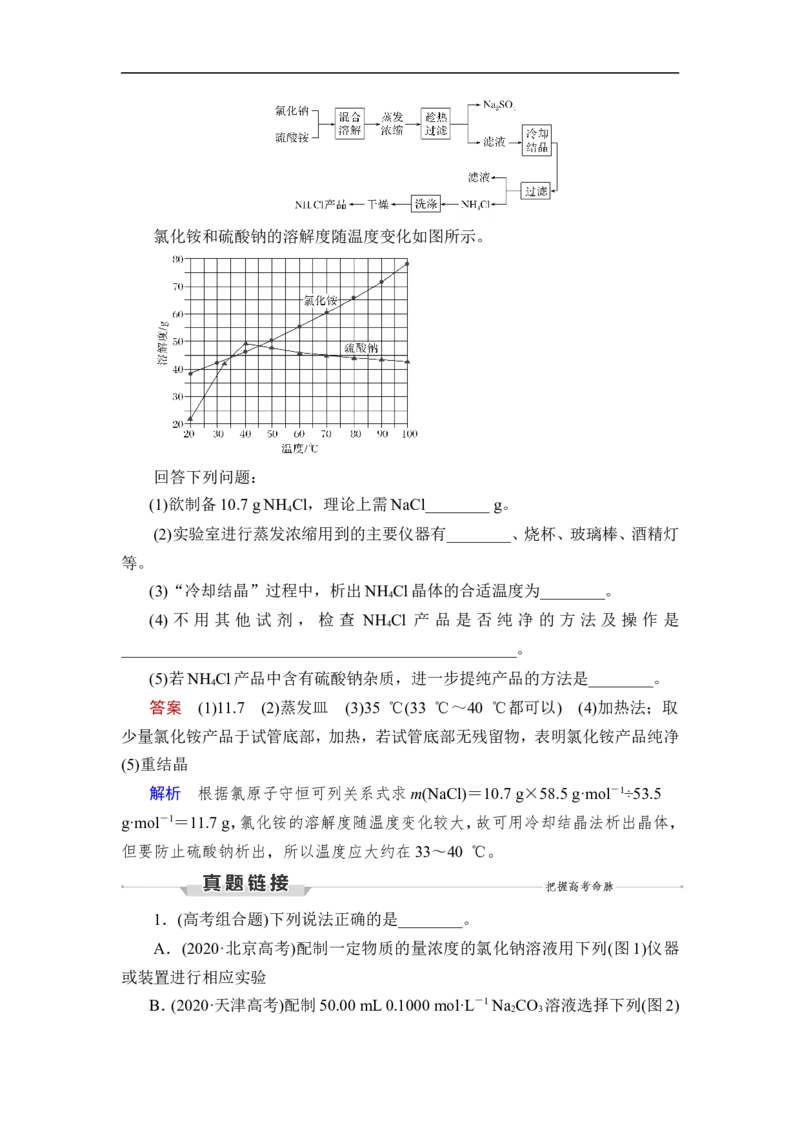
2.以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:氯化铵和硫酸钠的溶解度随温度变化如图所示。
回答下列问题:
(1)欲制备10.7 g NH Cl,理论上需NaCl________ g。
4
(2)实验室进行蒸发浓缩用到的主要仪器有________、烧杯、玻璃棒、酒精灯
等。
(3)“冷却结晶”过程中,析出NH Cl晶体的合适温度为________。
4
(4) 不 用 其 他 试 剂 , 检 查 NH Cl 产 品 是 否 纯 净 的 方 法 及 操 作 是
4
_________________________________________________。
(5)若NH Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是________。
4
答案 (1)11.7 (2)蒸发皿 (3)35 ℃(33 ℃~40 ℃都可以) (4)加热法;取
少量氯化铵产品于试管底部,加热,若试管底部无残留物,表明氯化铵产品纯净
(5)重结晶
解析 根据氯原子守恒可列关系式求m(NaCl)=10.7 g×58.5 g·mol-1÷53.5
g·mol-1=11.7 g,氯化铵的溶解度随温度变化较大,故可用冷却结晶法析出晶体,
但要防止硫酸钠析出,所以温度应大约在33~40 ℃。
1.(高考组合题)下列说法正确的是________。
A.(2020·北京高考)配制一定物质的量浓度的氯化钠溶液用下列(图1)仪器
或装置进行相应实验
B.(2020·天津高考)配制50.00 mL 0.1000 mol·L-1 Na CO 溶液选择下列(图2)
2 3实验仪器或装置
C.(2019·江苏高考)将4.0 g NaOH固体置于100 mL容量瓶中,加水至刻度,
配制1.000 mol·L-1NaOH溶液
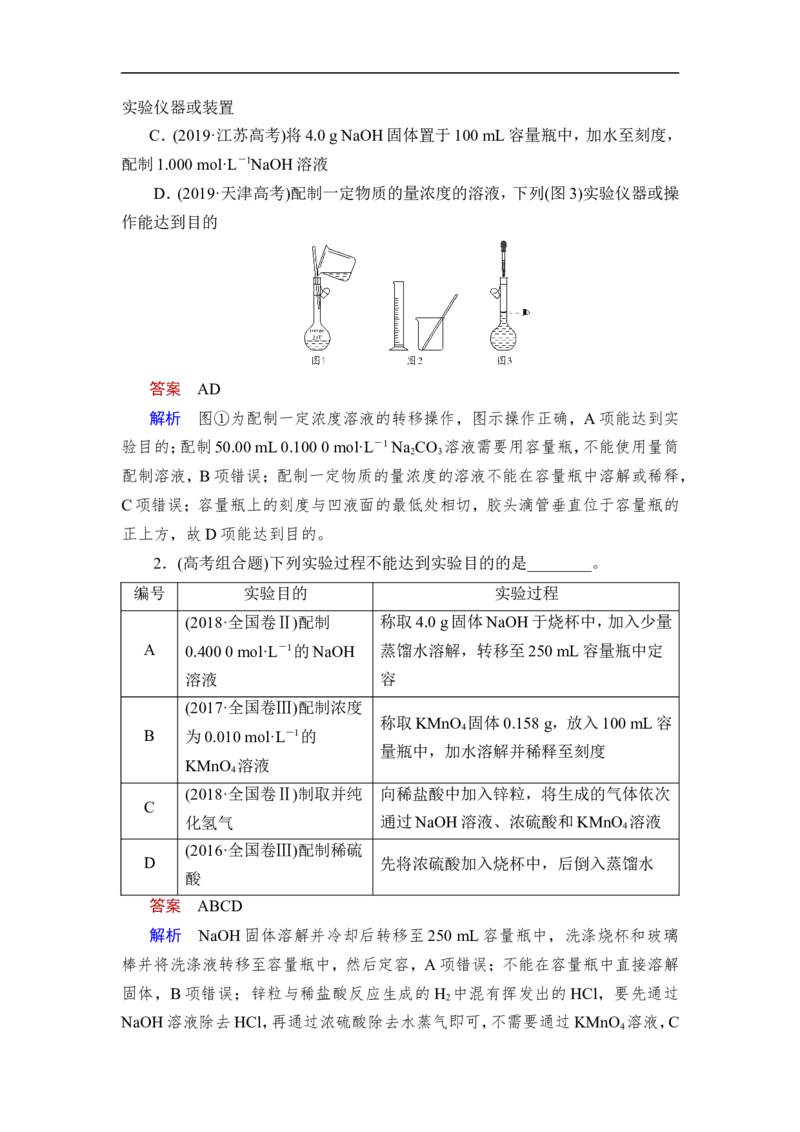
D.(2019·天津高考)配制一定物质的量浓度的溶液,下列(图3)实验仪器或操
作能达到目的
答案 AD
解析 图①为配制一定浓度溶液的转移操作,图示操作正确,A项能达到实
验目的;配制50.00 mL 0.100 0 mol·L-1 Na CO 溶液需要用容量瓶,不能使用量筒
2 3
配制溶液,B项错误;配制一定物质的量浓度的溶液不能在容量瓶中溶解或稀释,
C项错误;容量瓶上的刻度与凹液面的最低处相切,胶头滴管垂直位于容量瓶的
正上方,故D项能达到目的。
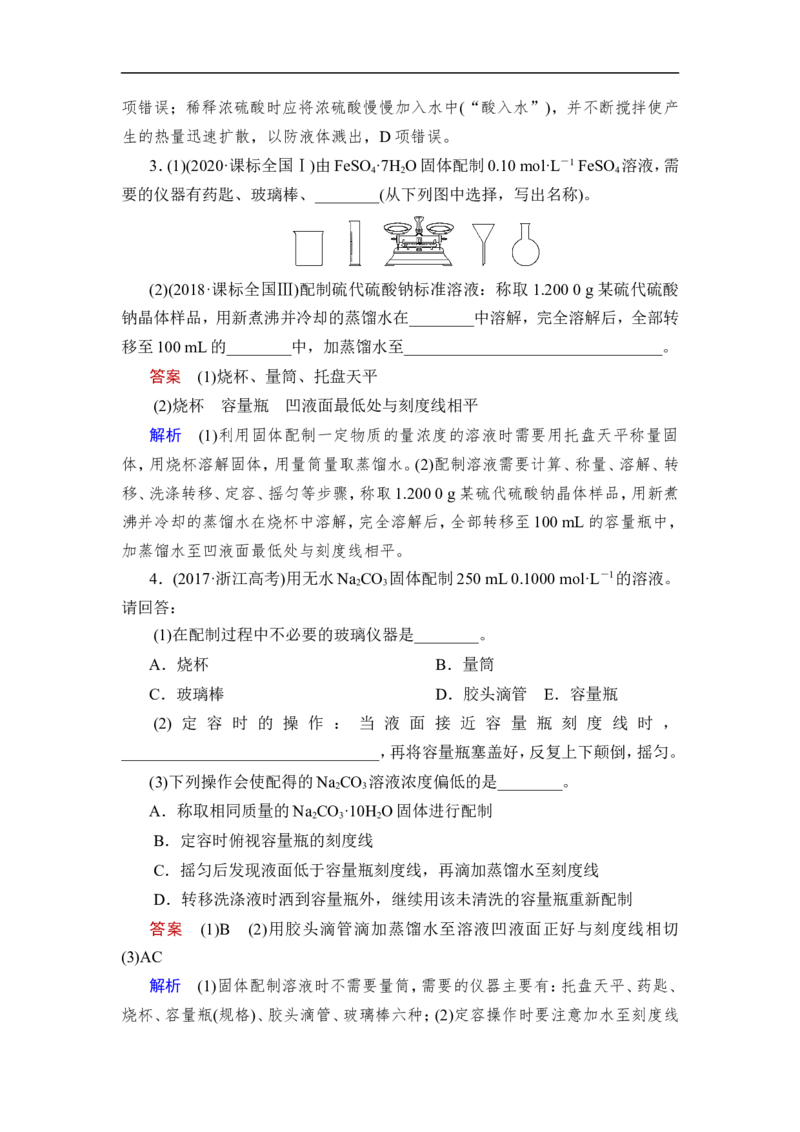
2.(高考组合题)下列实验过程不能达到实验目的的是________。
编号 实验目的 实验过程
(2018·全国卷Ⅱ)配制 称取4.0 g固体NaOH于烧杯中,加入少量
A 0.400 0 mol·L-1的NaOH 蒸馏水溶解,转移至250 mL容量瓶中定
溶液 容
(2017·全国卷Ⅲ)配制浓度
称取KMnO 固体0.158 g,放入100 mL容
4
B 为0.010 mol·L-1的
量瓶中,加水溶解并稀释至刻度
KMnO 溶液
4
(2018·全国卷Ⅱ)制取并纯 向稀盐酸中加入锌粒,将生成的气体依次
C
化氢气 通过NaOH溶液、浓硫酸和KMnO 溶液
4
(2016·全国卷Ⅲ)配制稀硫
D 先将浓硫酸加入烧杯中,后倒入蒸馏水
酸
答案 ABCD
解析 NaOH固体溶解并冷却后转移至250 mL容量瓶中,洗涤烧杯和玻璃
棒并将洗涤液转移至容量瓶中,然后定容,A项错误;不能在容量瓶中直接溶解
固体,B项错误;锌粒与稀盐酸反应生成的H 中混有挥发出的HCl,要先通过
2
NaOH溶液除去HCl,再通过浓硫酸除去水蒸气即可,不需要通过KMnO 溶液,C
4项错误;稀释浓硫酸时应将浓硫酸慢慢加入水中(“酸入水”),并不断搅拌使产
生的热量迅速扩散,以防液体溅出,D项错误。
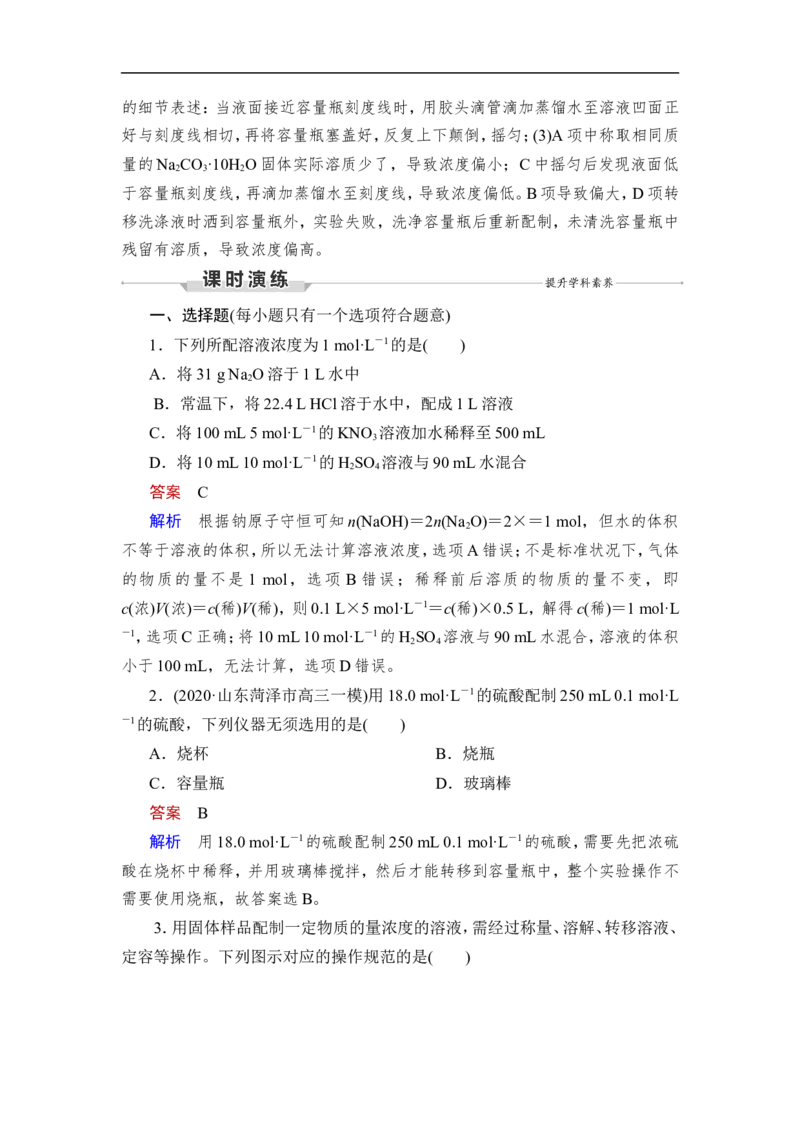
3.(1)(2020·课标全国Ⅰ)由FeSO ·7H O固体配制0.10 mol·L-1 FeSO 溶液,需
4 2 4
要的仪器有药匙、玻璃棒、________(从下列图中选择,写出名称)。
(2)(2018·课标全国Ⅲ)配制硫代硫酸钠标准溶液:称取 1.200 0 g某硫代硫酸
钠晶体样品,用新煮沸并冷却的蒸馏水在________中溶解,完全溶解后,全部转
移至100 mL的________中,加蒸馏水至________________________________。
答案 (1)烧杯、量筒、托盘天平
(2)烧杯 容量瓶 凹液面最低处与刻度线相平
解析 (1)利用固体配制一定物质的量浓度的溶液时需要用托盘天平称量固
体,用烧杯溶解固体,用量筒量取蒸馏水。(2)配制溶液需要计算、称量、溶解、转
移、洗涤转移、定容、摇匀等步骤,称取1.200 0 g某硫代硫酸钠晶体样品,用新煮
沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至100 mL的容量瓶中,
加蒸馏水至凹液面最低处与刻度线相平。
4.(2017·浙江高考)用无水Na CO 固体配制250 mL 0.1000 mol·L-1的溶液。
2 3
请回答:
(1)在配制过程中不必要的玻璃仪器是________。
A.烧杯 B.量筒
C.玻璃棒 D.胶头滴管 E.容量瓶
(2) 定 容 时 的 操 作 : 当 液 面 接 近 容 量 瓶 刻 度 线 时 ,
________________________________,再将容量瓶塞盖好,反复上下颠倒,摇匀。
(3)下列操作会使配得的Na CO 溶液浓度偏低的是________。
2 3
A.称取相同质量的Na CO ·10H O固体进行配制
2 3 2
B.定容时俯视容量瓶的刻度线
C.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线
D.转移洗涤液时洒到容量瓶外,继续用该未清洗的容量瓶重新配制
答案 (1)B (2)用胶头滴管滴加蒸馏水至溶液凹液面正好与刻度线相切
(3)AC
解析 (1)固体配制溶液时不需要量筒,需要的仪器主要有:托盘天平、药匙、
烧杯、容量瓶(规格)、胶头滴管、玻璃棒六种;(2)定容操作时要注意加水至刻度线的细节表述:当液面接近容量瓶刻度线时,用胶头滴管滴加蒸馏水至溶液凹面正
好与刻度线相切,再将容量瓶塞盖好,反复上下颠倒,摇匀;(3)A项中称取相同质
量的Na CO ·10H O固体实际溶质少了,导致浓度偏小;C中摇匀后发现液面低
2 3 2
于容量瓶刻度线,再滴加蒸馏水至刻度线,导致浓度偏低。B项导致偏大,D项转
移洗涤液时洒到容量瓶外,实验失败,洗净容量瓶后重新配制,未清洗容量瓶中
残留有溶质,导致浓度偏高。
一、选择题(每小题只有一个选项符合题意)
1.下列所配溶液浓度为1 mol·L-1的是( )
A.将31 g Na O溶于1 L水中
2
B.常温下,将22.4 L HCl溶于水中,配成1 L溶液
C.将100 mL 5 mol·L-1的KNO 溶液加水稀释至500 mL
3
D.将10 mL 10 mol·L-1的H SO 溶液与90 mL水混合
2 4
答案 C
解析 根据钠原子守恒可知n(NaOH)=2n(Na O)=2×=1 mol,但水的体积
2
不等于溶液的体积,所以无法计算溶液浓度,选项A错误;不是标准状况下,气体
的物质的量不是 1 mol,选项 B 错误;稀释前后溶质的物质的量不变,即
c(浓)V(浓)=c(稀)V(稀),则0.1 L×5 mol·L-1=c(稀)×0.5 L,解得c(稀)=1 mol·L
-1,选项C正确;将10 mL 10 mol·L-1的H SO 溶液与90 mL水混合,溶液的体积
2 4
小于100 mL,无法计算,选项D错误。
2.(2020·山东菏泽市高三一模)用18.0 mol·L-1的硫酸配制250 mL 0.1 mol·L
-1的硫酸,下列仪器无须选用的是( )
A.烧杯 B.烧瓶
C.容量瓶 D.玻璃棒
答案 B
解析 用18.0 mol·L-1的硫酸配制250 mL 0.1 mol·L-1的硫酸,需要先把浓硫
酸在烧杯中稀释,并用玻璃棒搅拌,然后才能转移到容量瓶中,整个实验操作不
需要使用烧瓶,故答案选B。
3.用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、
定容等操作。下列图示对应的操作规范的是( )答案 B
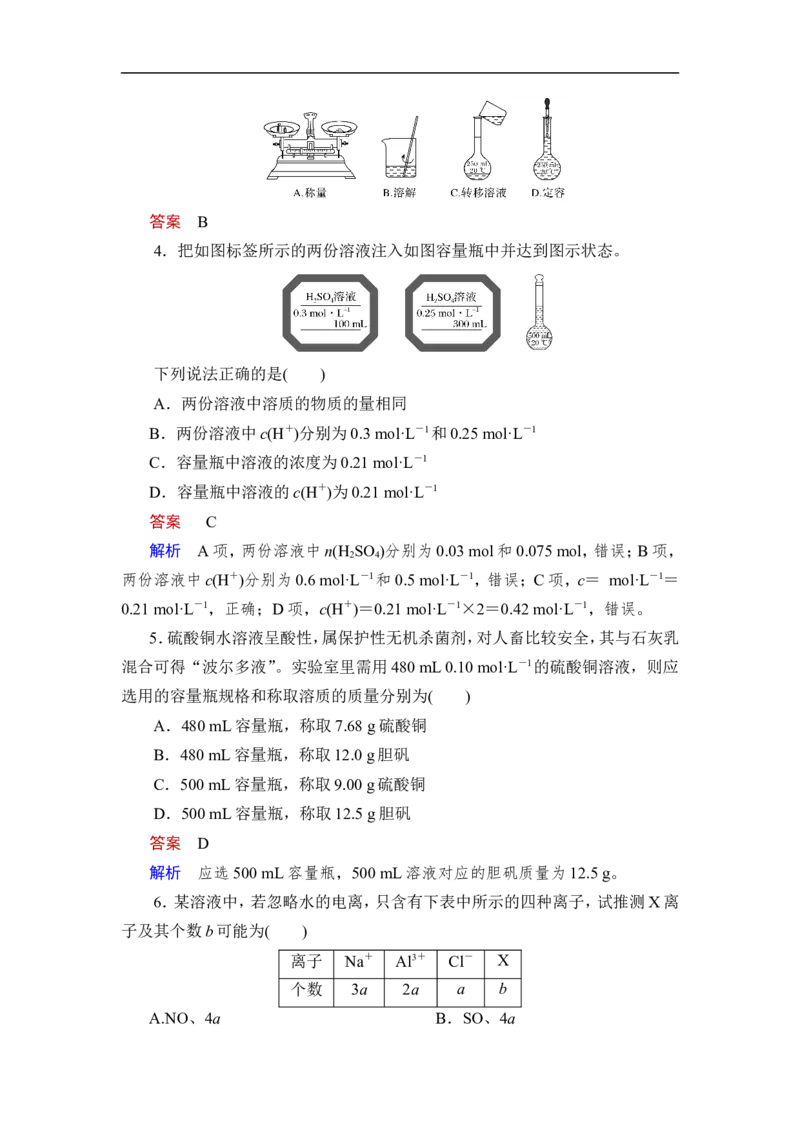
4.把如图标签所示的两份溶液注入如图容量瓶中并达到图示状态。
下列说法正确的是( )
A.两份溶液中溶质的物质的量相同
B.两份溶液中c(H+)分别为0.3 mol·L-1和0.25 mol·L-1
C.容量瓶中溶液的浓度为0.21 mol·L-1
D.容量瓶中溶液的c(H+)为0.21 mol·L-1
答案 C
解析 A项,两份溶液中n(H SO )分别为0.03 mol和0.075 mol,错误;B项,
2 4
两份溶液中c(H+)分别为0.6 mol·L-1和0.5 mol·L-1,错误;C项,c= mol·L-1=
0.21 mol·L-1,正确;D项,c(H+)=0.21 mol·L-1×2=0.42 mol·L-1,错误。
5.硫酸铜水溶液呈酸性,属保护性无机杀菌剂,对人畜比较安全,其与石灰乳
混合可得“波尔多液”。实验室里需用480 mL 0.10 mol·L-1的硫酸铜溶液,则应
选用的容量瓶规格和称取溶质的质量分别为( )
A.480 mL容量瓶,称取7.68 g硫酸铜
B.480 mL容量瓶,称取12.0 g胆矾
C.500 mL容量瓶,称取9.00 g硫酸铜
D.500 mL容量瓶,称取12.5 g胆矾
答案 D
解析 应选500 mL容量瓶,500 mL溶液对应的胆矾质量为12.5 g。
6.某溶液中,若忽略水的电离,只含有下表中所示的四种离子,试推测X离
子及其个数b可能为( )
离子 Na+ Al3+ Cl- X
个数 3a 2a a b
A.NO、4a B.SO、4aC.OH-、4a D.SO、8a
答案 B
解析 设 X 的电荷数为 n,溶液呈电中性,则溶液中存在 3a×N(Na+)+
2a×3N(Al3 + ) = a×N(Cl - ) + nb×N(X) , 则 A.3a×N(Na + ) + 2a×3N(Al3
+)≠a×N(Cl-)+4a×N(NO),电荷不守恒,故 A 错误;B.3a×N(Na+)+
2a×3N(Al3+)=a×N(Cl-)+4a×2×N(SO),电荷守恒,故B正确;C.3a×N(Na+)
+2a×3N(Al3+)≠a×N(Cl-)+4a×N(OH-),电荷不守恒,Al3+、OH-不能大量共
存,故C错误;D.3a×N(Na+)+2a×3N(Al3+)≠a×N(Cl-)+8a×2×N(SO),电荷
不守恒,故D错误。
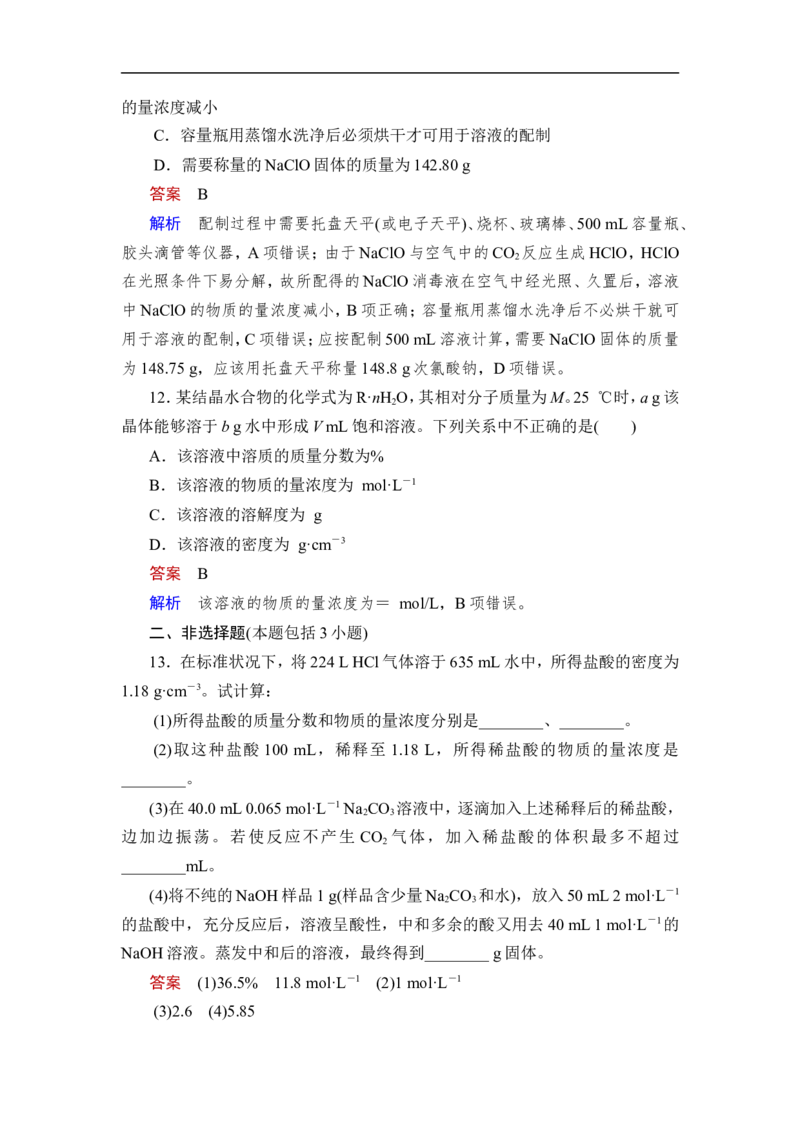
7.某兴趣小组需要500 mL 2 mol·L-1的H SO 溶液,若用98%密度为1.84
2 4
g·mL-1的浓硫酸配制该溶液。下列操作正确的是( )
答案 D
解析 A.图中量取液体时仰视刻度线,导致量取浓硫酸体积偏大,操作错误,
故A错误;B.图中浓硫酸稀释将水注入浓硫酸,容易产生酸飞溅伤人,操作错误,
故B错误;C.图中移液操作未用玻璃棒引流,操作错误,故C错误;D.图中为定容
操作,眼睛平视刻度线,操作正确,故D正确。
8.(2020·郑州模拟)将质量分数为a%、物质的量浓度为c mol·L-1的稀H SO
1 2 4
蒸发掉一定量的水,使其质量分数变为2a%,此时溶液中溶质的物质的量浓度为
c mol·L-1。则c 和c 的关系是( )
2 1 2
A.c =2c mol·L-1 B.c <2c mol·L-1
1 2 2 1
C.c >2c mol·L-1 D.c =2c mol·L-1
2 1 2 1
答案 C
解析 由c=可知,==,由于ρ <ρ ,所以c >2c 。
1 2 2 1
9.下列有关实验原理或操作正确的是( )
A.用20 mL量筒量取15 mL酒精,加5 mL水,配制质量分数为75%的酒精
溶液
B.在200 mL某硫酸盐溶液中,含有1.5N 个硫酸根离子和N 个金属离子,
A A则该硫酸盐的物质的量浓度为2.5 mol·L-1
C.实验中需用950 mL 2.0 mol·L-1 Na CO 溶液,配制时称取的Na CO 的质
2 3 2 3
量为201.4 g
D.实验室配制500 mL 0.2 mol·L-1硫酸亚铁溶液,其操作是:用天平称15.2 g
绿矾(FeSO ·7H O),放入小烧杯中加水溶解,转移到500 mL容量瓶,洗涤、稀释、
4 2
定容、摇匀
答案 B
解析 不能用量筒来配制溶液,应用烧杯,且15 mL酒精的质量不是5 mL水
的质量的3倍,A项错误;1.5N 个硫酸根离子的物质的量为1.5 mol,N 个金属阳
A A
离子的物质的量为1 mol,设金属离子的化合价为x,根据电荷守恒可知,x=
1.5×2=3,故金属阳离子为+3价,所以该硫酸盐可以表示为M (SO ) ,根据硫酸
2 4 3
根离子守恒可知,硫酸盐为0.5 mol,所以该硫酸盐的物质的量浓度为=2.5 mol·L
-1,B项正确;没有950 mL的容量瓶,应用1 000 mL的容量瓶进行配制,则
m(Na CO )=cVM=1 L×2 mol·L-1×106 g·mol-1=212 g,C项错误;配制500 mL
2 3
0.2 mol·L-1硫酸亚铁溶液,需要绿矾(FeSO ·7H O)的物质的量为 0.5 L×0.2
4 2
mol·L-1=0.1 mol,质量为27.8 g,D项错误。
10.把含硫酸铵和硝酸铵的混合溶液 a L 分成两等份,一份加入含 b mol
NaOH的溶液并加热,恰好把NH 全部赶出;另一份需消耗c mol BaCl 才能使
3 2
SO完全沉淀,则原溶液中NO的物质的量浓度(mol·L-1)为( )
A. B.
C. D.
答案 B
解析 b mol NaOH恰好将NH 全部赶出,根据NH+OH-=====NH ↑+H O
3 3 2
可知,每份中含有b mol NH;与氯化钡溶液完全反应消耗c mol BaCl 才能使SO
2
完全沉淀,根据Ba2++SO===BaSO ↓可知每份含有SOc mol,设每份中含有NO
4
的物质的量为x mol,根据溶液呈电中性,则b mol×1=c mol×2+x mol×1,得x
=b-2c,因将a L混合溶液分成两等份,则每份的体积是0.5a L,所以每份溶液
中c(NO)== mol·L-1,即原溶液中NO的浓度是 mol·L-1,故选B。
11.某同学参阅了“84消毒液”说明书中的配方,欲用NaClO固体自己配制
480 mL含NaClO 25%、密度为1.19 g·cm-3的消毒液。下列说法正确的是( )
A.配制过程中只需要三种仪器即可完成
B.所配得的NaClO消毒液在空气中经光照、久置后,溶液中NaClO的物质的量浓度减小
C.容量瓶用蒸馏水洗净后必须烘干才可用于溶液的配制
D.需要称量的NaClO固体的质量为142.80 g
答案 B
解析 配制过程中需要托盘天平(或电子天平)、烧杯、玻璃棒、500 mL容量瓶、
胶头滴管等仪器,A项错误;由于NaClO与空气中的CO 反应生成HClO,HClO
2
在光照条件下易分解,故所配得的NaClO消毒液在空气中经光照、久置后,溶液
中NaClO的物质的量浓度减小,B项正确;容量瓶用蒸馏水洗净后不必烘干就可
用于溶液的配制,C项错误;应按配制500 mL溶液计算,需要NaClO固体的质量
为148.75 g,应该用托盘天平称量148.8 g次氯酸钠,D项错误。
12.某结晶水合物的化学式为R·nH O,其相对分子质量为M。25 ℃时,a g该
2
晶体能够溶于b g水中形成V mL饱和溶液。下列关系中不正确的是( )
A.该溶液中溶质的质量分数为%
B.该溶液的物质的量浓度为 mol·L-1
C.该溶液的溶解度为 g
D.该溶液的密度为 g·cm-3
答案 B
解析 该溶液的物质的量浓度为= mol/L,B项错误。
二、非选择题(本题包括3小题)
13.在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为
1.18 g·cm-3。试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是________、________。
(2)取这种盐酸 100 mL,稀释至 1.18 L,所得稀盐酸的物质的量浓度是
________。
(3)在40.0 mL 0.065 mol·L-1 Na CO 溶液中,逐滴加入上述稀释后的稀盐酸,
2 3
边加边振荡。若使反应不产生 CO 气体,加入稀盐酸的体积最多不超过
2
________mL。
(4)将不纯的NaOH样品1 g(样品含少量Na CO 和水),放入50 mL 2 mol·L-1
2 3
的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去 40 mL 1 mol·L-1的
NaOH溶液。蒸发中和后的溶液,最终得到________ g固体。
答案 (1)36.5% 11.8 mol·L-1 (2)1 mol·L-1
(3)2.6 (4)5.85解析 (1)n(HCl)==10 mol,m(HCl)=10 mol×36.5 g·mol-1=365 g,盐酸的
质量分数w=×100%=36.5%,c(HCl)===11.8 mol·L-1。
(2)由c(浓)·V(浓)=c(稀)·V(稀)可知,c(稀)=11.8 mol·L-1×=1 mol·L-1。
(3)n(Na CO )=0.040 L×0.065 mol·L-1=0.002 6 mol,设加入稀盐酸的体积最
2 3
多不超过x mL,则n(HCl)=1 mol·L-1×0.001x L=0.001x mol,根据反应Na CO
2 3
+HCl===NaHCO +NaCl得0.002 6=0.001x,x=2.6。
3
(4)经过反应,蒸发中和后的溶液,最后所得固体为NaCl,根据氯原子守恒:
n(NaCl)=n(HCl)=0.050 L×2 mol·L-1=0.1 mol,m(NaCl)=0.1 mol×58.5 g·mol-
1=5.85 g。
14.在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。下表是1 L“鲜花保鲜
剂”的成分,阅读后回答下列问题:
成分 质量/g 摩尔质量/(g·mol-1)
蔗糖 50.00 342
硫酸钾 0.50 174
阿司匹林 0.35 180
高锰酸钾 0.50 158
硝酸银 0.04 170
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是________(填写名称)。
(2)“鲜花保鲜剂”中 K+的物质的量浓度为 (阿司匹林中不含 K
+)________(只要求写表达式,不需计算)mol·L-1。
(3)下图所示的仪器中,在配制“鲜花保鲜剂”溶液时肯定不需要的是
________(填字母),还缺少的仪器有________(填仪器名称)。
(4)配制过程中,下列操作对配制结果没有影响的是________(填选项字母)。
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,则加入的试剂中应含有
________(填化学符号)。答案 (1)蔗糖 (2)(2×+)
(3)ac 托盘天平、玻璃棒、烧杯 (4)AD (5)Cl-
解析 (2)“鲜花保鲜剂”中K+的物质的量为n(K+)=2n(K SO )+n(KMnO )
2 4 4
=(2×+)mol,所以c(K+)=(+) mol·L-1。(3)配制一定浓度的溶液必需的仪器:烧
杯、玻璃棒、胶头滴管、容量瓶,不需要圆底烧瓶和分液漏斗,还缺少的仪器有托
盘天平、烧杯、玻璃棒。(4)容量瓶在使用前未干燥,里面有少量蒸馏水,对溶液的
浓度不产生任何影响,A项正确;定容时仰视液面,溶液的体积偏大,使溶液的浓
度偏低,B项错误;容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而
未洗净,NaCl与AgNO 反应,会使溶液的浓度偏小,C项错误;定容摇匀后发现
3
液面低于容量瓶的刻度线,但未做任何处理,对配制溶液的浓度不产生任何影响
D项正确;(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,可利用反应:Ag++Cl-
===AgCl↓,加入的试剂中需含有Cl-。
15.人体血液里Ca2+的浓度一般采用mg·cm-3来表示。抽取一定体积的血样,
加适量的草酸铵[(NH ) C O ]溶液,可析出草酸钙(CaC O )沉淀,将此草酸钙沉淀
4 2 2 4 2 4
洗涤后溶于强酸可得草酸(H C O ),再用KMnO 溶液滴定即可测定血液样品中
2 2 4 4
Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
【配制KMnO 标准溶液】如图是配制50 mL KMnO 标准溶液的过程示意图。
4 4
(1)请你观察图示判断,其中不正确的操作有________(填序号)。
(2)其中确定50 mL溶液体积的容器是________(填名称)。
(3)如果用图示的操作所配制的溶液进行实验,在其他操作正确的情况下,所
配制的溶液浓度将________(填“偏大”或“偏小”)。
【测定血液样品中Ca2+的浓度】抽取血样20.00 mL,经过上述处理后得到草
酸,再用0.020 mol·L-1 KMnO 溶液滴定,使草酸转化成CO 逸出,这时共消耗
4 2
12.00 mL KMnO 溶液。
4
(4)已知草酸与KMnO 反应的离子方程式为:
42MnO+5H C O +6H+===2Mnx++10CO ↑+8H O
2 2 4 2 2
则方程式中的x=________。
(5)经过计算,血液样品中Ca2+的浓度为________ mg·cm-3。
答案 (1)①②⑤ (2)50 mL容量瓶 (3)偏小 (4)2 (5)1.2
解析 (1)由图示可知①②⑤操作不正确,②不能在量筒中溶解固体,⑤定容
时应平视刻度线,至溶液凹液面与刻度线相切。
(3)如果用按照图示的操作所配制的溶液进行实验,在其他操作正确的情况
下,由于仰视刻度线,会使溶液体积偏大,所配制的溶液浓度将偏小。
(5)血液样品中Ca2+的浓度为
=1.2 mg·cm-3。