文档内容
训练(五十) 物质的制备及性质探究
1.(2021·山东临沂质检)过硫酸钠(Na SO)常用作漂白剂、氧化剂等。某研究小组利用下
2 2 8
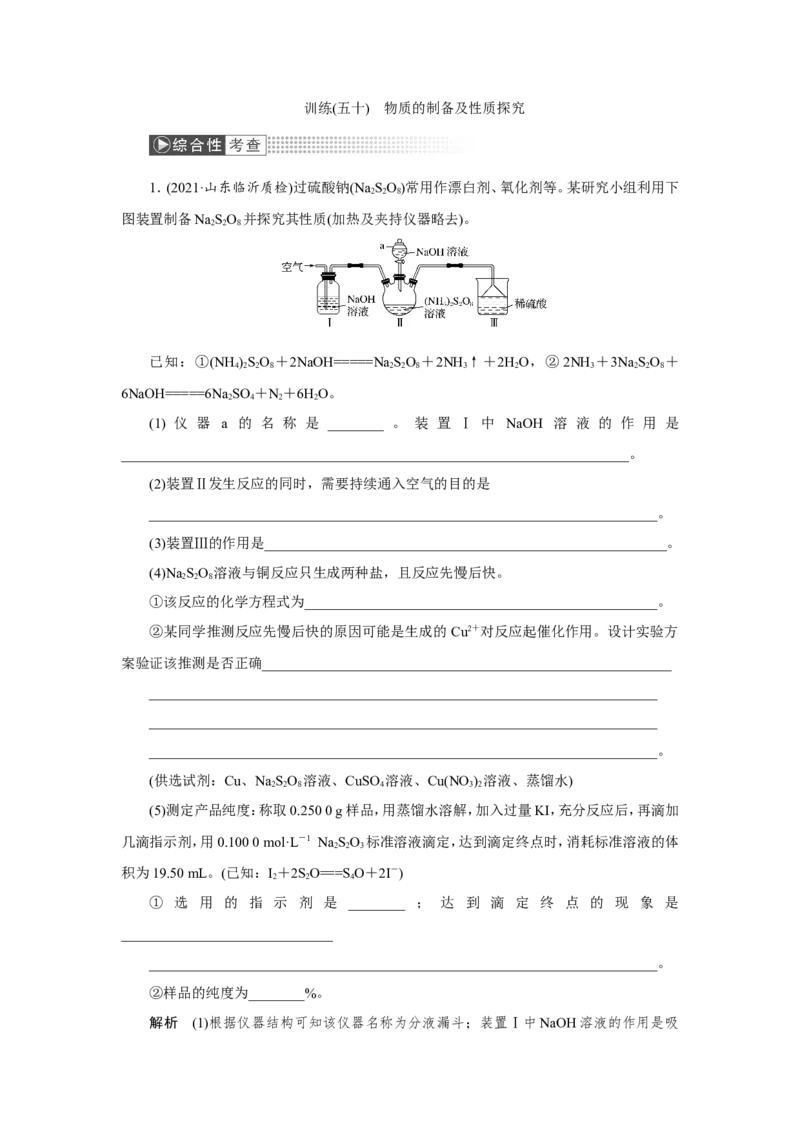
图装置制备NaSO 并探究其性质(加热及夹持仪器略去)。
2 2 8
已知:①(NH )SO +2NaOH=====NaSO +2NH ↑+2HO,②2NH +3NaSO +
4 2 2 8 2 2 8 3 2 3 2 2 8
6NaOH=====6NaSO +N+6HO。
2 4 2 2
(1) 仪 器 a 的 名 称 是 ________ 。 装 置 Ⅰ 中 NaOH 溶 液 的 作 用 是
________________________________________________________________________。
(2)装置Ⅱ发生反应的同时,需要持续通入空气的目的是
________________________________________________________________________。
(3)装置Ⅲ的作用是_________________________________________________________。
(4)Na SO 溶液与铜反应只生成两种盐,且反应先慢后快。
2 2 8
①该反应的化学方程式为__________________________________________________。
②某同学推测反应先慢后快的原因可能是生成的 Cu2+对反应起催化作用。设计实验方
案验证该推测是否正确__________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(供选试剂:Cu、NaSO 溶液、CuSO 溶液、Cu(NO ) 溶液、蒸馏水)
2 2 8 4 3 2
(5)测定产品纯度:称取0.250 0 g样品,用蒸馏水溶解,加入过量KI,充分反应后,再滴加
几滴指示剂,用0.100 0 mol·L-1 NaSO 标准溶液滴定,达到滴定终点时,消耗标准溶液的体
2 2 3
积为19.50 mL。(已知:I+2SO===S O+2I-)
2 2 4
① 选 用 的 指 示 剂 是 ________ ; 达 到 滴 定 终 点 的 现 象 是
______________________________
________________________________________________________________________。
②样品的纯度为________%。
解析 (1)根据仪器结构可知该仪器名称为分液漏斗;装置Ⅰ中NaOH溶液的作用是吸收空气中的CO,防止干扰实验。
2
(2)在装置Ⅱ中NaOH溶液与(NH )SO 反应会产生氨气,NH 可进一步与NaSO 反应,
4 2 2 8 3 2 2 8
故在装置Ⅱ发生反应的同时,需要持续通入空气将装置中的NH 及时排出,减少副反应的发
3
生。
(3)装置Ⅲ中稀硫酸,可吸收NH ,由于使用了倒置漏斗,因此使气体被充分吸收的同时
3
也可防止倒吸现象的发生。
(4)①过硫酸钠(Na SO)具有强的氧化性,能将Cu氧化为Cu2+,SO被还原为SO,根据
2 2 8 2
得失电子守恒、原子守恒可得反应的方程式为NaSO+Cu===Na SO +CuSO 。
2 2 8 2 4 4
(5)①根据I 遇淀粉溶液变蓝色,可选用淀粉溶液为指示剂;若滴定达到终点,会看到溶
2
液由蓝色变为无色,且半分钟内不恢复。
②NaSO 作氧化剂,1 mol NaSO 得到2 mol电子,KI被氧化变为I,生成1 mol I 转
2 2 8 2 2 8 2 2
移2 mol电子;I 与NaSO 反应的方程式为I+2NaSO===Na SO+2NaI,可得关系式:
2 2 2 3 2 2 2 3 2 4 6
NaSO ~I ~2NaSO ,n(Na SO)=0.100 0 mol·L-1×19.50×10-3L=1.95×10-3mol,则
2 2 8 2 2 2 3 2 2 3
n(Na SO)=n(Na SO)=9.75×10-4mol,m(Na SO)=9.75×10-4mol×238 g·mol-1=0.232
2 2 8 2 2 3 2 2 8
05 g,则该样品的纯度为(0.232 05 g÷0.250 0 g)×100%=92.82%。
答案 (1)分液漏斗 吸收空气中CO
2
(2)将三颈烧瓶中产生的NH 及时排出,减少副反应的发生
3
(3)吸收NH ,防止倒吸
3
(4)①NaSO+Cu===Na SO +CuSO
2 2 8 2 4 4
②向盛有等质量铜粉的试管中,分别加入等体积的硫酸铜溶液和蒸馏水,再加入等体积
等浓度的NaSO 溶液,若加入硫酸铜溶液的试管中反应快,则该推测正确
2 2 8
(5)① 淀粉溶液 滴入最后一滴标准溶液,溶液的蓝色褪去,且半分钟内不恢复
②92.82
2.(2021·福建南安一中检测)亚氯酸钠(NaClO)常用于纺织、造纸业漂白,也用于食品消
2
毒、水处理等。
已知:①亚氯酸钠(NaClO)受热易分解;
2
②纯ClO 易分解爆炸,一般用稀有气体或空气稀释到10%以下。
2
Ⅰ:制取NaClO 晶体
2(1)实验过程中需要持续通入空气,目的是________________________________。
(2)装置A中产生ClO 的化学方程式为_______________________________________。
2
(3)装置B中氧化剂和还原剂的物质的量之比为___________________________,氧化产
物为________________;反应结束后,为从溶液中得到NaClO 固体,采取减压蒸发而不用常
2
压蒸发,原因是_______________________________________________________。
(4)装置C的作用是_________________________________________________。
Ⅱ:测定亚氯酸钠的含量
实验步骤:①准确称取所得亚氯酸钠样品m g于小烧杯中,加入适量蒸馏水和过量的碘
化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液配成250 mL待测溶液。②移取
25.00 mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1NaSO 标准溶液滴定至终点,
2 2 3
重复2次,测得消耗NaSO 标准溶液体积的平均值为 V mL。(已知:ClO+4I-+4H+
2 2 3
===2H O+2I+Cl-、I+2SO===2I-+SO)
2 2 2 2 4
(5)达到滴定终点时的现象为_________________________________________________
________________________________________________________________________。
(6)该样品中NaClO 的质量分数为____________(用含m、c、V的代数式表示,结果化简
2
成最简式)。在滴定操作正确的情况下,此实验测得结果偏高,可能原因为
____________________________________(用离子方程式表示)。
解析 (1)根据题给信息“纯ClO 易分解爆炸,一般用稀有气体或空气稀释到10%以下”,
2
可知实验过程中持续通入空气的目的是稀释ClO ,以防止发生爆炸。
2
(2)装置A中NaClO 被还原为ClO ,NaSO 被氧化为NaSO ;根据得失电子守恒和元素
3 2 2 3 2 4
守恒,可知装置A中产生ClO 的化学方程式为2NaClO +NaSO +HSO ===2ClO ↑+
2 3 2 3 2 4 2
2NaSO +HO。
2 4 2
(3)装置B中ClO 参加反应生成NaClO,Cl元素的化合价降低,作氧化剂,HO 作还原
2 2 2 2
剂,有氧气生成,根据得失电子守恒可得关系式:2ClO ~HO,故装置B中氧化剂和还原剂
2 2 2
的物质的量之比为2∶1,氧化产物为O。根据题给信息“亚氯酸钠(NaClO)受热易分解”,可
2 2
知反应结束后为从溶液中得到NaClO 固体,应采取减压蒸发而不用常压蒸发,原因是常压
2蒸发温度过高,亚氯酸钠容易分解。
(4)装置C的作用是吸收ClO ,防止污染空气。
2
(5)用NaSO 标准溶液滴定待测溶液,发生反应:I+2SO===2I-+SO,指示剂淀粉溶
2 2 3 2 2 4
液遇I 变为蓝色,故滴定终点的现象为滴入最后一滴标准溶液时,溶液由蓝色变成无色,且
2
30 s内颜色不恢复。
(6)①由反应中的I元素守恒可知:ClO~2I~4SO,故25.00 mL待测溶液中n(NaClO)
2 2 2
=×cV×10-3mol,m(NaClO)=×90.5cV×10-3g;样品m g配成250 mL待测溶液,故样品中
2
NaClO 的质量分数为×100%=%。②实验测得结果偏高,说明滴定消耗的NaSO 标准溶液
2 2 2 3
体积偏大,则溶液中碘单质的含量偏高,可能原因为过量的碘离子被空气中的氧气氧化为碘
单质,反应的离子方程式为4I-+O+4H+===2I +2HO。
2 2 2
答案 (1)稀释ClO 以防爆炸
2
(2)2NaClO+NaSO +HSO ===2ClO ↑+2NaSO +HO
3 2 3 2 4 2 2 4 2
(3)2∶1 O 常压蒸发温度过高,亚氯酸钠容易分解
2
(4)吸收ClO ,防止污染空气
2
(5)当滴入最后一滴标准溶液时,溶液由蓝色变成无色,且30 s内颜色不恢复
(6)% 4I-+O+4H+===2I +2HO
2 2 2
3.(2021·山东烟台一中检测)以CuSO 溶液和不同酸根离子形成的钠盐溶液作为实验对
4
象,探究盐的性质和盐溶液间反应的多样性。
试剂 现象
实验
滴管 试管
0.2 mol·L-1
Ⅰ.产生白色沉淀和黄色溶液
NaI溶液
0.2 mol·L-1 0.2 mol·L-1
Ⅱ.产生绿色沉淀和无色无味气体
CuSO 溶液 NaCO 溶液
4 2 3
0.2 mol·L-1
Ⅲ.产生棕黄色沉淀
NaSO 溶液
2 3
(1)经检验,现象Ⅰ的白色沉淀为CuI,则反应的离子方程式为___________________
_____________________________________________________,
氧化产物与还原产物的物质的量之比为____________。
(2)经检验,现象Ⅱ中产生的气体是二氧化碳,绿色沉淀是碱式碳酸铜
[xCuCO·yCu(OH) ·zHO]。现采用氢气还原法测定碱式碳酸铜组成,请回答如下问题:
3 2 2
①写出xCuCO·yCu(OH) ·zHO与氢气反应的化学方程式:_____________________
3 2 2__________________________________________________________________________
。
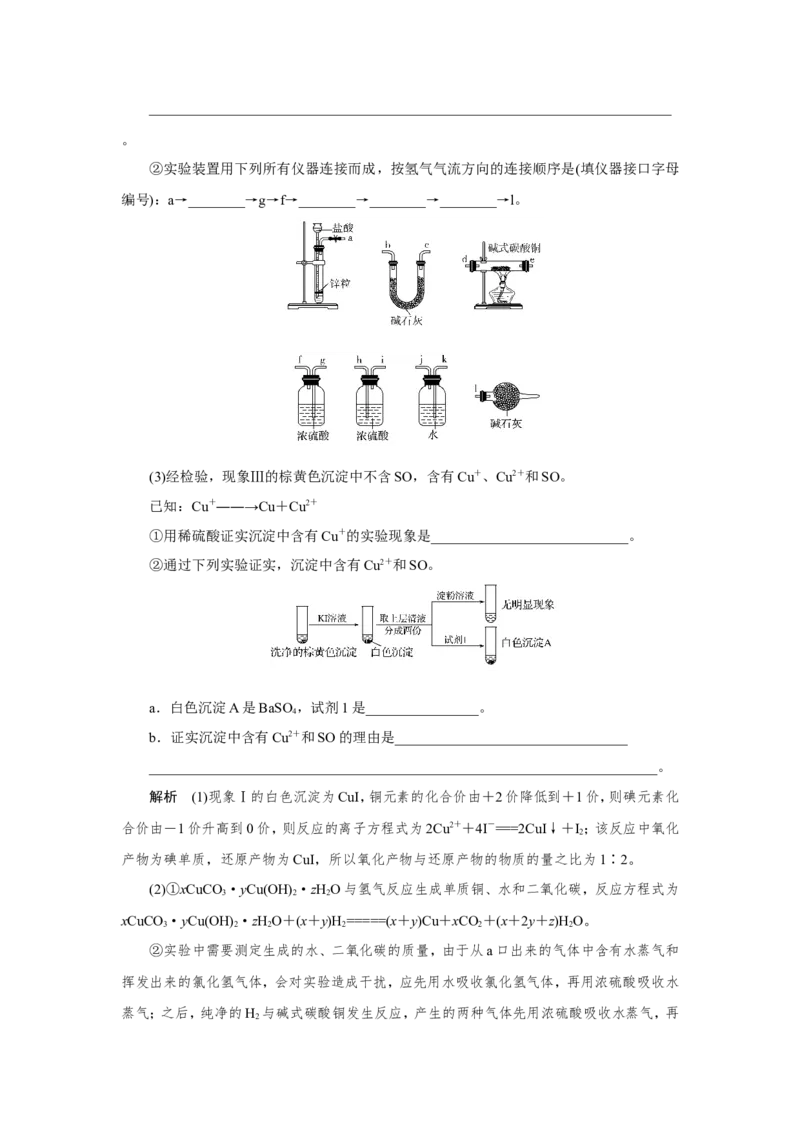
②实验装置用下列所有仪器连接而成,按氢气气流方向的连接顺序是(填仪器接口字母
编号):a→________→g→f→________→________→________→l。
(3)经检验,现象Ⅲ的棕黄色沉淀中不含SO,含有Cu+、Cu2+和SO。
已知:Cu+――→Cu+Cu2+
①用稀硫酸证实沉淀中含有Cu+的实验现象是____________________________。
②通过下列实验证实,沉淀中含有Cu2+和SO。
a.白色沉淀A是BaSO,试剂1是________________。
4
b.证实沉淀中含有Cu2+和SO的理由是_________________________________
________________________________________________________________________。
解析 (1)现象Ⅰ的白色沉淀为CuI,铜元素的化合价由+2价降低到+1价,则碘元素化
合价由-1价升高到0价,则反应的离子方程式为2Cu2++4I-===2CuI↓+I;该反应中氧化
2
产物为碘单质,还原产物为CuI,所以氧化产物与还原产物的物质的量之比为1∶2。
(2)①xCuCO·yCu(OH) ·zHO与氢气反应生成单质铜、水和二氧化碳,反应方程式为
3 2 2
xCuCO·yCu(OH) ·zHO+(x+y)H =====(x+y)Cu+xCO+(x+2y+z)H O。
3 2 2 2 2 2
②实验中需要测定生成的水、二氧化碳的质量,由于从a口出来的气体中含有水蒸气和
挥发出来的氯化氢气体,会对实验造成干扰,应先用水吸收氯化氢气体,再用浓硫酸吸收水
蒸气;之后,纯净的H 与碱式碳酸铜发生反应,产生的两种气体先用浓硫酸吸收水蒸气,再
2用U形管中的碱石灰吸收二氧化碳,同时连上装有碱石灰的球形干燥管,避免空气中的水和
二氧化碳进入U形管而产生误差,因此装置的连接顺序为a→kj→gf→de→hi→bc→l。
(3)①由已知信息可得Cu+和稀硫酸反应生成Cu和Cu2+,所以用稀硫酸证实沉淀中含
有Cu+的实验操作和现象为取一定量的沉淀于试管中,向其中加入稀硫酸,有红色固体析出。
②a.证明溶液中有SO,需要加入的试剂是盐酸和 BaCl 溶液,现象是生成白色沉淀
2
BaSO。
4
b.根据已知信息,加入KI溶液生成白色沉淀CuI,说明沉淀中有Cu2+;向清液中加入淀
粉溶液没有颜色变化,说明生成的I 被SO还原成I-,SO被氧化为SO,因此向清液中加入盐
2
酸和BaCl 溶液,产生BaSO 沉淀,则沉淀中含有Cu2+和SO。
2 4
答案 (1)2Cu2++4I-===2CuI↓+I 1∶2
2
(2)①xCuCO·yCu(OH) ·zHO+(x+y)H =====(x+y)Cu+xCO +(x+2y+z)H O ②kj
3 2 2 2 2 2
de hi bc
(3)①有红色固体析出 ②a.盐酸和BaCl 溶液 b.在I-作用下,Cu2+转化为白色沉淀
2
CuI,SO转化为SO
4.(2020·广西防城港二模)氢化铝锂(LiAlH )是有机合成中的重要还原剂。某课题组设计
4
实验制备氢化铝锂并测定其纯度。已知:氢化铝锂、氢化锂遇水都剧烈反应,并产生同一种气
体。回答下列问题:
Ⅰ.制备氢化锂(LiH):
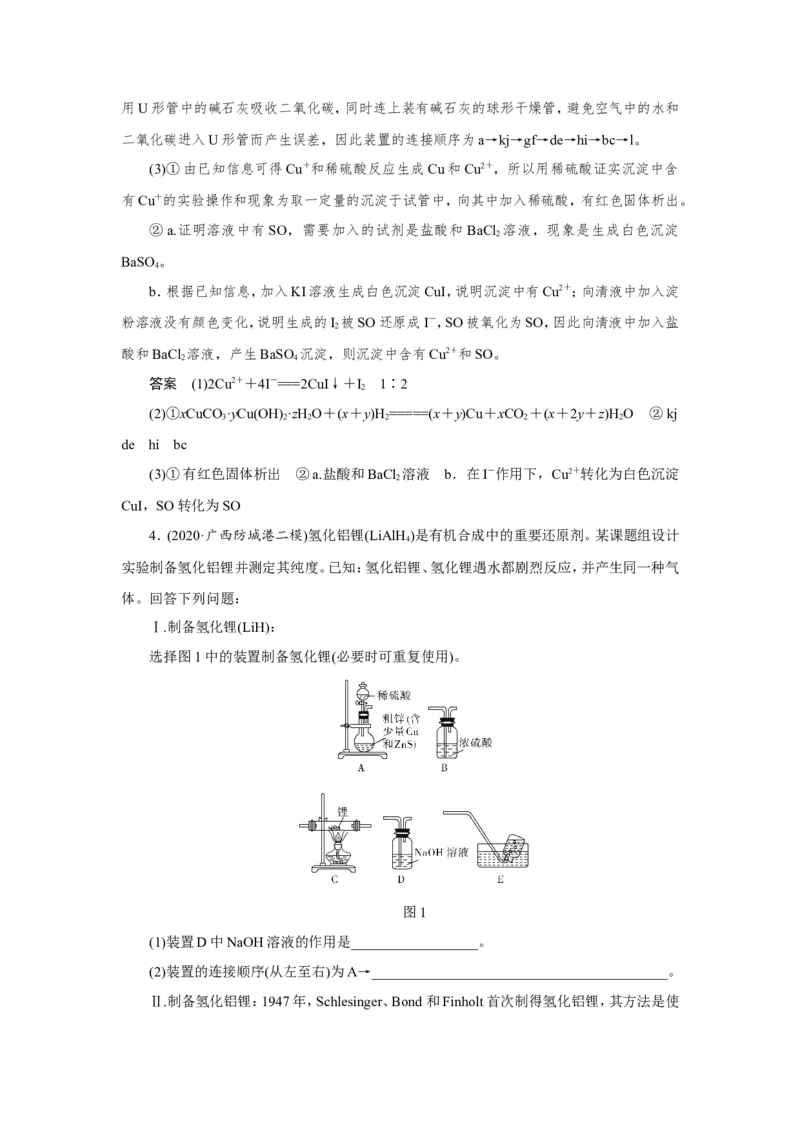
选择图1中的装置制备氢化锂(必要时可重复使用)。
图1
(1)装置D中NaOH溶液的作用是__________________。
(2)装置的连接顺序(从左至右)为A→__________________________________________。
Ⅱ.制备氢化铝锂:1947年,Schlesinger、Bond 和Finholt首次制得氢化铝锂,其方法是使氢化锂与无水三氯化铝按一定比例在乙醚中混合,搅拌,充分反应后,经一系列操作得到
LiAlH 晶体。
4
(3)将乙醚换为水是否可行,请简述理由:___________________________________
________________________________________________________________________。
(4)氢化锂与无水三氯化铝反应的化学方程式为______________________________。
Ⅲ.测定氢化铝锂产品(不含氢化锂)的纯度。
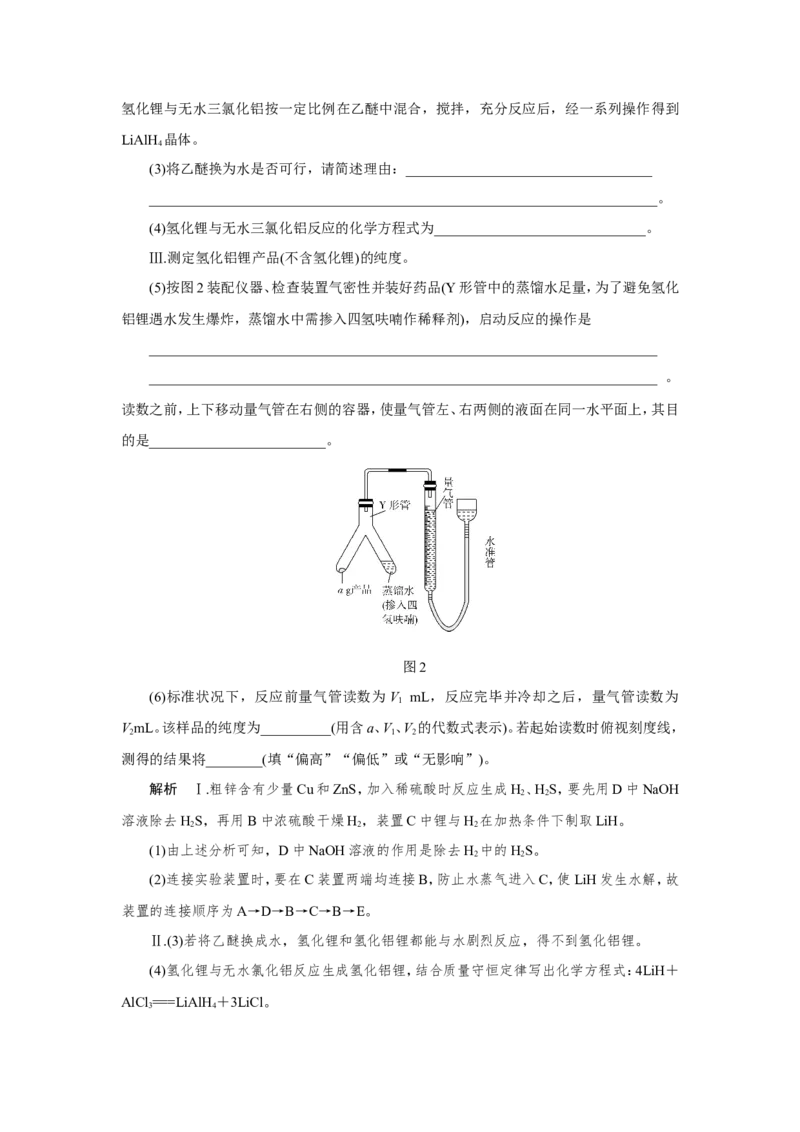
(5)按图2装配仪器、检查装置气密性并装好药品(Y形管中的蒸馏水足量,为了避免氢化
铝锂遇水发生爆炸,蒸馏水中需掺入四氢呋喃作稀释剂),启动反应的操作是
________________________________________________________________________
________________________________________________________________________ 。
读数之前,上下移动量气管在右侧的容器,使量气管左、右两侧的液面在同一水平面上,其目
的是_________________________。
图2
(6)标准状况下,反应前量气管读数为V mL,反应完毕并冷却之后,量气管读数为
1
VmL。该样品的纯度为__________(用含a、V、V 的代数式表示)。若起始读数时俯视刻度线,
2 1 2
测得的结果将________(填“偏高”“偏低”或“无影响”)。
解析 Ⅰ.粗锌含有少量Cu和ZnS,加入稀硫酸时反应生成H、HS,要先用D中NaOH
2 2
溶液除去HS,再用B中浓硫酸干燥H,装置C中锂与H 在加热条件下制取LiH。
2 2 2
(1)由上述分析可知,D中NaOH溶液的作用是除去H 中的HS。
2 2
(2)连接实验装置时,要在C装置两端均连接B,防止水蒸气进入C,使LiH发生水解,故
装置的连接顺序为A→D→B→C→B→E。
Ⅱ.(3)若将乙醚换成水,氢化锂和氢化铝锂都能与水剧烈反应,得不到氢化铝锂。
(4)氢化锂与无水氯化铝反应生成氢化铝锂,结合质量守恒定律写出化学方程式:4LiH+
AlCl ===LiAlH+3LiCl。
3 4Ⅲ.(5)分析装置可知,Y形管的左侧装有a g产品,右侧装有蒸馏水,使二者混合即可发
生反应,故启动反应的操作是将Y形管倾斜,将蒸馏水注入左侧产品中。实验结束量取气体
的体积时,要保持装置内外压强平衡,上下移动量气管在右侧的容器,使量气管左、右两侧的
液面在同一水平面上。
(6)产品LiAlH 中加入蒸馏水,发生反应:LiAlH +4HO===LiOH+Al(OH) +4H↑;反
4 4 2 3 2
应前量气管读数为V mL,反应完毕并冷却之后,量气管读数为V mL,则生成H 的体积为
1 2 2
(V -V)mL,则有n(LiAlH )=[(V -V)×10-3L]/(22.4 L·mol-1×4)=(V -V)/89 600 mol,
2 1 4 2 1 2 1
m(LiAlH )=(V-V)/89 600 mol×38 g·mol-1=19(V-V)/44 800 g,故该样品的纯度为[19(V
4 2 1 2 1 2
-V)/44 800 g]/a g×100%=%。若起始读数时俯视刻度线,引起V 的值偏小,则测得结果将
1 1
偏高。
答案 Ⅰ.(1) 除去H 中混有的HS (2)D→B→C→B→E
2 2
Ⅱ.(3)不可行,因为氢化铝锂、氢化锂遇水都剧烈反应
(4)4LiH+AlCl ===LiAlH+3LiCl
3 4
Ⅲ.(5)倾斜Y形管,将蒸馏水注入a g产品中 使量气管内气体的压强与大气压强相等
(6)% 偏高
5.(2021·湖南三湘名校联考)丙烯酸酯类物质广泛用于建筑、包装材料等,丙烯酸是合成
丙烯酸酯的原料之一。丙烯醇可用于生产甘油、塑料等。以丙烯醛为原料生产丙烯醇、丙烯酸
的流程如图所示:
已知:
①2CH===CH—CHO+NaOH――→CH===CHCHOH+CH===CHCOONa
2 2 2 2
②2CH===CHCOONa+HSO ―→2CH===CHCOOH+NaSO
2 2 4 2 2 4
③有关物质的相关性质如表:
物质 丙烯醛 丙烯醇 丙烯酸 四氯化碳
沸点/℃ 53 97 141 77
熔点/℃ -87 -129 13 -22.8
密度/g·cm-3 0.84 0.85 1.02 1.58溶于水和有机溶 溶于水和有机溶
溶解性(常温) 易溶于水和有机溶剂 难溶于水
剂 剂
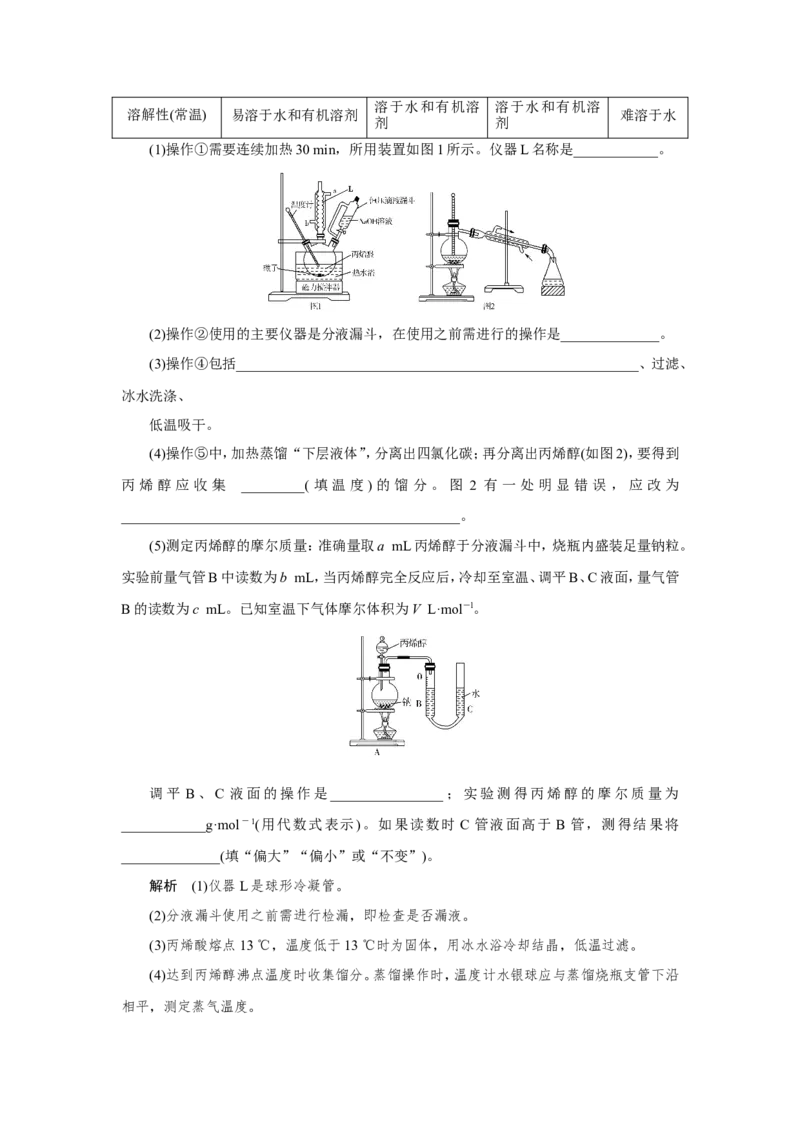
(1)操作①需要连续加热30 min,所用装置如图1所示。仪器L名称是____________。
(2)操作②使用的主要仪器是分液漏斗,在使用之前需进行的操作是______________。
(3)操作④包括_________________________________________________________、过滤、
冰水洗涤、
低温吸干。
(4)操作⑤中,加热蒸馏“下层液体”,分离出四氯化碳;再分离出丙烯醇(如图2),要得到
丙烯醇 应收 集 _________(填温 度)的馏分。图 2 有一处 明显错误 ,应改为
________________________________________________。
(5)测定丙烯醇的摩尔质量:准确量取a mL丙烯醇于分液漏斗中,烧瓶内盛装足量钠粒。
实验前量气管B中读数为b mL,当丙烯醇完全反应后,冷却至室温、调平B、C液面,量气管
B的读数为c mL。已知室温下气体摩尔体积为V L·mol-l。
调平 B、C 液面的操作是________________;实验测得丙烯醇的摩尔质量为
____________g·mol-1(用代数式表示)。如果读数时 C 管液面高于 B 管,测得结果将
______________(填“偏大”“偏小”或“不变”)。
解析 (1)仪器L是球形冷凝管。
(2)分液漏斗使用之前需进行检漏,即检查是否漏液。
(3)丙烯酸熔点13 ℃,温度低于13 ℃时为固体,用冰水浴冷却结晶,低温过滤。
(4)达到丙烯醇沸点温度时收集馏分。蒸馏操作时,温度计水银球应与蒸馏烧瓶支管下沿
相平,测定蒸气温度。(5)2CH ===CHCHOH+2Na―→2CH===CHCHONa+H↑,n(CH===CHCHOH)
2 2 2 2 2 2 2
===×2 mol,M(CH===CHCHOH)=== g·mol-1=== g·mol-1。若C管液面高于B管液面,测
2 2
得c偏小,结果偏大。
答案 (1)(球形)冷凝管
(2)检漏
(3)冰水浴冷却结晶(或降温结晶)
(4)97 ℃ 温度计水银球与蒸馏烧瓶支管口处相齐平
(5)上下移动C管 偏大
6.(2020·山东枣庄二模)氮化锶(Sr N)在工业上广泛用于生产荧光粉。锶与氮气在加热条
3 2
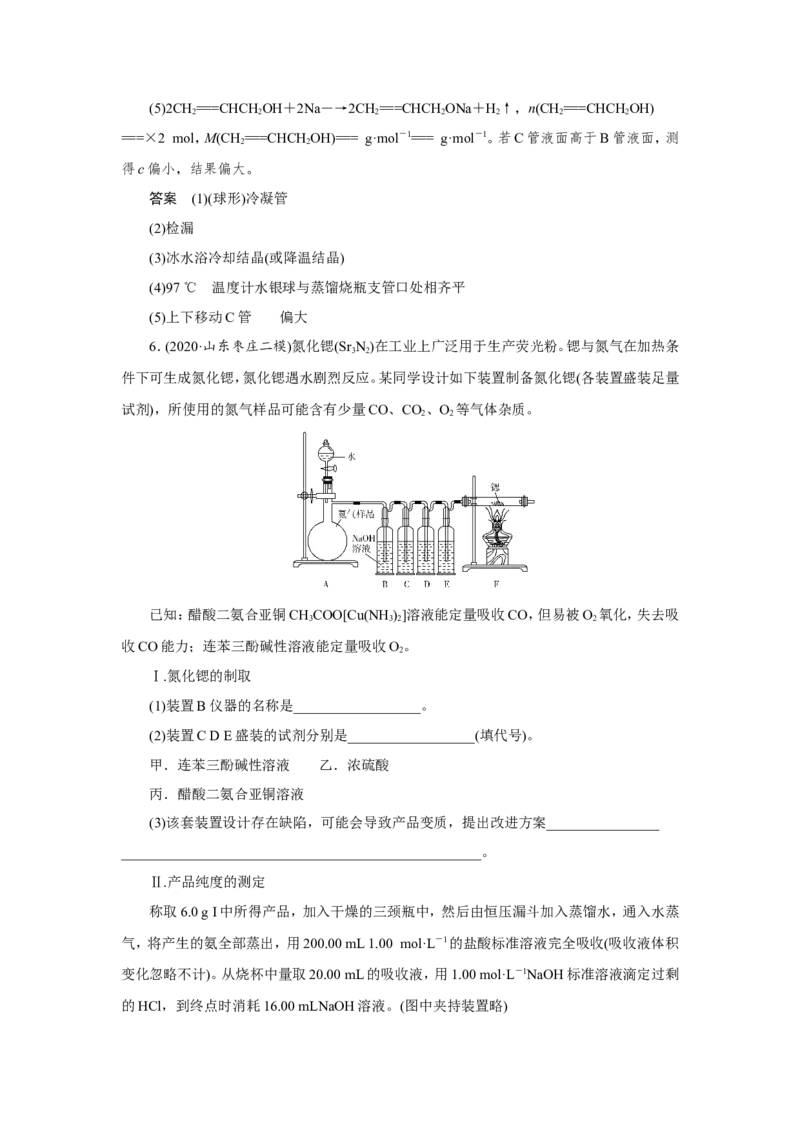
件下可生成氮化锶,氮化锶遇水剧烈反应。某同学设计如下装置制备氮化锶(各装置盛装足量
试剂),所使用的氮气样品可能含有少量CO、CO、O 等气体杂质。
2 2
已知:醋酸二氨合亚铜CHCOO[Cu(NH )]溶液能定量吸收CO,但易被O 氧化,失去吸
3 3 2 2
收CO能力;连苯三酚碱性溶液能定量吸收O。
2
Ⅰ.氮化锶的制取
(1)装置B仪器的名称是__________________。
(2)装置C D E盛装的试剂分别是__________________(填代号)。
甲.连苯三酚碱性溶液 乙.浓硫酸
丙.醋酸二氨合亚铜溶液
(3)该套装置设计存在缺陷,可能会导致产品变质,提出改进方案________________
___________________________________________________。
Ⅱ.产品纯度的测定
称取6.0 g I中所得产品,加入干燥的三颈瓶中,然后由恒压漏斗加入蒸馏水,通入水蒸
气,将产生的氨全部蒸出,用200.00 mL 1.00 mol·L-1的盐酸标准溶液完全吸收(吸收液体积
变化忽略不计)。从烧杯中量取20.00 mL的吸收液,用1.00 mol·L-1NaOH标准溶液滴定过剩
的HCl,到终点时消耗16.00 mLNaOH溶液。(图中夹持装置略)(4)三颈瓶中发生的化学反应方程式为____________________________________。
(5)装置中2的作用为_______________________________________________________。
(6)用1.00 mol·L-1NaOH标准溶液滴定过剩的HCl时所选指示剂为________(填字母)。
a.石蕊试液 b.酚酞试液 c.甲基橙
(7)产品纯度为__________________。
(8)下列实验操作可能使氮化锶(Sr N)测定结果偏高的是__________(填字母)。
3 2
a.滴定时未用NaOH标准溶液润洗滴定管
b.读数时,滴定前平视,滴定后俯视
c.摇动锥形瓶时有液体测出
解析 (2)氮气样品可能含有少量CO、CO、O 等气体杂质,醋酸二氨合亚铜溶液能吸收
2 2
CO,但易被O 氧化,失去吸收CO能力,连苯三酚碱性溶液能吸收O,故应先利用连苯三酚
2 2
碱性溶液吸收O 和CO,再利用醋酸二氨合亚铜溶液吸收CO,最后用浓硫酸干燥氮气。
2 2
(3)氮化锶遇水剧烈反应,装置F右端未接干燥装置,不能阻止空气中水蒸气进入F,可
在F后连接一个盛有碱石灰(无水氯化钙等)的干燥管或盛有浓硫酸的洗气瓶。
(7)Sr N 与水反应生成NH ,结合滴定时发生反应可得关系式:Sr N~2NH ~2HCl,则
3 2 3 3 2 3
有
n(Sr N)=n(HCl)=×(0.02 L×1.00 mol/L-0.016 L×1.00 mol/L)×=0.02 mol,
3 2
m(Sr N)=0.02 mol×290.8 g/mol=5.816 g,故产品的纯度为×100 %≈96.93%。
3 2
(8)滴定时未用NaOH标准溶液润洗滴定管,导致其浓度变小,消耗NaOH溶液的体积偏
大,则氮化锶(Sr N)的测定结果偏低,a错误;读数时,滴定前平视,滴定后俯视,读取消耗
3 2
NaOH溶液体积偏小,则氮化锶(Sr N)的测定结果偏高,b正确;摇动锥形瓶时有液体溅出,
3 2
消耗NaOH溶液体积偏小,则氮化锶(Sr N)的测定结果偏高,c正确。
3 2
答案 (1)洗气瓶
(2)甲 丙 乙
(3)在装置F后连接一盛有碱石灰的干燥管(或其他合理答案)
(4)Sr N+6HO===3Sr(OH) +2NH ↑
3 2 2 2 3(5)平衡气压,防止倒吸
(6)c
(7)96.93%
(8)b、c
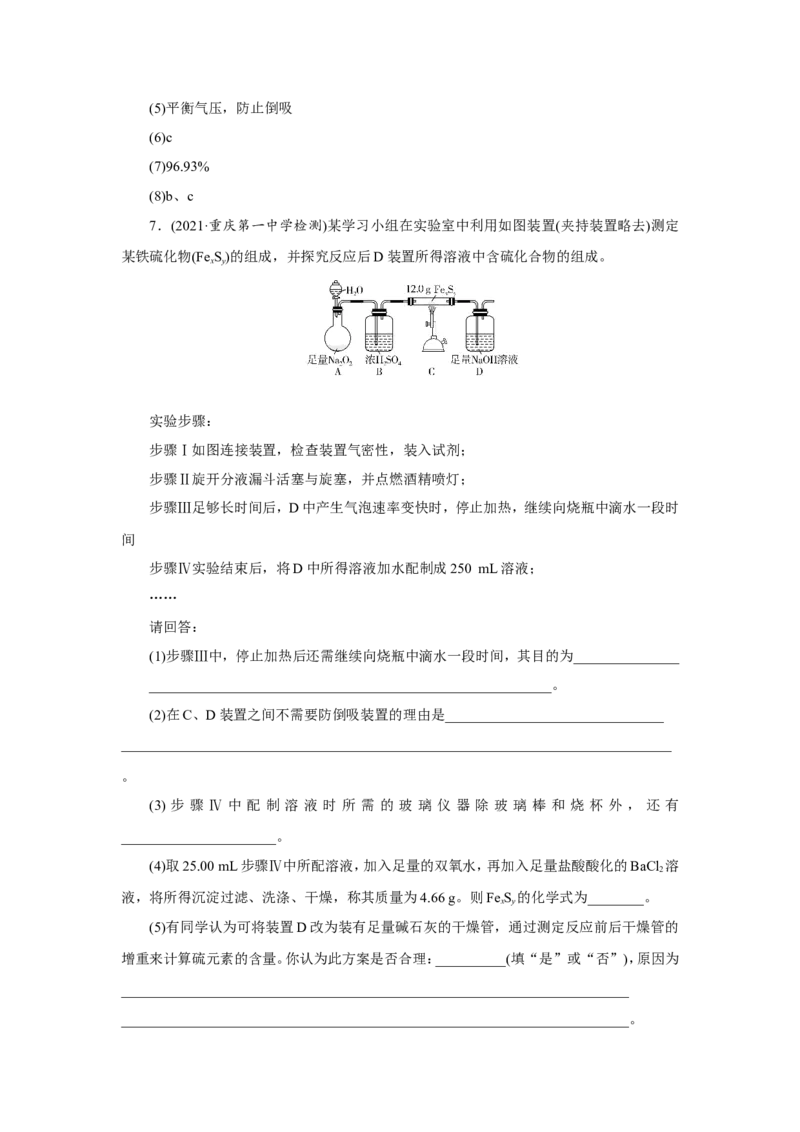
7.(2021·重庆第一中学检测)某学习小组在实验室中利用如图装置(夹持装置略去)测定
某铁硫化物(FeS)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
x y
实验步骤:
步骤Ⅰ如图连接装置,检查装置气密性,装入试剂;
步骤Ⅱ旋开分液漏斗活塞与旋塞,并点燃酒精喷灯;
步骤Ⅲ足够长时间后,D中产生气泡速率变快时,停止加热,继续向烧瓶中滴水一段时
间
步骤Ⅳ实验结束后,将D中所得溶液加水配制成250 mL溶液;
……
请回答:
(1)步骤Ⅲ中,停止加热后还需继续向烧瓶中滴水一段时间,其目的为_______________
_________________________________________________________。
(2)在C、D装置之间不需要防倒吸装置的理由是_______________________________
______________________________________________________________________________
。
(3) 步 骤 Ⅳ 中 配 制 溶 液 时 所 需 的 玻 璃 仪 器 除 玻 璃 棒 和 烧 杯 外 , 还 有
______________________。
(4)取25.00 mL步骤Ⅳ中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl 溶
2
液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66 g。则FeS 的化学式为________。
x y
(5)有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的
增重来计算硫元素的含量。你认为此方案是否合理:__________(填“是”或“否”),原因为
________________________________________________________________________
________________________________________________________________________。解析 本实验的目的是测定某铁硫化物(FeS)的组成,并探究反应后D装置所得溶液中
x y
含硫化合物的组成。观察装置,A装置中产生足量的氧气经干燥后,进入C装置与FeS 在加
x y
热条件下反应,生成硫的氧化物,进入D被NaOH溶液吸收。
(1)步骤Ⅲ中,停止加热后还需继续向烧瓶中滴水一段时间,继续产生氧气,FeS 其实已
x y
经反应完了,那么其目的为使生成的SO 全部进入D中被NaOH溶液吸收。
2
(2)此装置中,不需要防倒吸装置,虽然SO 易溶于水,但是其中还有难溶于水的氧气,不
2
会因为SO 溶于水而使气压迅速降低发生倒吸。
2
(3)步骤Ⅳ中配制250 mL溶液时,因为是要配制一定体积的溶液,故需要250 mL容量瓶,
所以所需的玻璃仪器除玻璃棒和烧杯外,还有250 mL容量瓶和胶头滴管。
(4)C装置中产生的气体,主要应为SO ,所以D中生成NaSO ,取25.00 mL步骤Ⅳ中所
2 2 3
配溶液,加入足量的双氧水,将其全部氧化为NaSO ,再加入足量盐酸酸化的BaCl 溶液,所
2 4 2
得沉淀为BaSO,质量为4.66 g,其物质的量为0.02 mol,250 mL溶液中含S元素的阴离子
4
的物质的量为0.2 mol,根据S原子守恒,12.0 g FeS 中n(S)=0.2 mol,m(S)=6.4 g,m(Fe)=
x y
5.6 g,n(Fe)=0.1 mol,所以,x∶y=1∶2,故FeS 的化学式为FeS。
x y 2
(5)装置D的作用是吸收装置中产生的SO ,若改为装有足量碱石灰的干燥管,空气中的
2
CO 和水蒸气可能使干燥管增重,而且SO 可能被氧化,使增重偏大。
2 2
答案 (1)继续生成O,驱赶装置内残留的SO ,使生成的SO 全部被NaOH溶液吸收
2 2 2
(2)SO 中含不溶于NaOH溶液的O
2 2
(3)250 mL容量瓶、胶头滴管
(4)FeS (5)否 部分SO 被氧化;空气中的CO 和水蒸气可能使干燥管增重
2 2 2