文档内容
训练(二十) 硫及其重要化合物
1.(2021·天津第一中学检测)下列各组物质混合后,没有明显现象的是( )
① HS 和 SO ② SO 和 SO ③ SO 和氯水 ④ SO (g)和 Cl ⑤ HS 和 SO (g)
2 2 2 3 2 3 2 2 3
⑥HS和Cl
2 2
A.①③⑥ B.②④⑤
C.②⑤⑥ D.③④⑤
B [①HS和SO 混合发生反应,生成单质S和HO,产生淡黄色固体;②SO 和SO 混
2 2 2 2 3
合不发生反应,无明显现象;③SO 和氯水混合,发生反应SO +Cl +2HO=== HSO +
2 2 2 2 2 4
2HCl,氯水褪色;④SO (g)和Cl 混合不发生反应,无明显现象;⑤HS和SO (g)混合,不发生
3 2 2 3
反应,无明显现象;⑥HS和Cl 混合发生氧化还原反应,生成单质S和HCl,产生淡黄色固
2 2
体。]
2.(2021·四川成都七中检测)已知①2HS+SO ===3S+2HO
2 2 2
②S+2HSO (浓)=====3SO ↑+2HO
2 4 2 2
③3S+6KOH===2K S+KSO +3HO
2 2 3 2
则下列说法正确的是( )
A.①说明SO 能与酸反应,故SO 具有碱性氧化物的通性
2 2
B.②若改用稀硫酸,则放出H
2
C.②和③说明硫具有两性元素的性质
D.上述反应说明硫既有氧化性又有还原性
D [①是氧化还原反应,SO 表现氧化性,A项错误;②稀硫酸与S不发生反应,B项错
2
误;②和③均为氧化还原反应,②中S作还原剂,表现还原性,③中S既是氧化剂又是还原剂,
表现氧化性和还原性,C项错误,D项正确。]
3.(2021·辽宁大连八中检测)下列有关硫及其化合物的说法正确的是( )
A.SO 、HSO 均具有还原性,故浓HSO 均能氧化SO 和HSO
2 2 3 2 4 2 2 3
B.HS与浓HSO 在不同的条件下反应的氧化产物只能是SO
2 2 4 2
C.单质――→氧化物――→酸或碱――→盐,能按照上述转化关系直接转化的可以是
硫元素
D.硫黄制备硫酸经历两步:S――→SO ――→HSO
3 2 4
C [浓硫酸中S显+6价,SO 和HSO 中S显+4价,+4和+6价S处于相邻价态,不
2 2 3
发生氧化还原反应,A项错误;HS和浓硫酸发生氧化还原反应,氧化产物可能是S、SO 等,
2 2
B项错误;S与O 反应生成SO ,SO 与水反应生成HSO ,可实现上述转化,C项正确;S与
2 2 2 2 3
O 点燃生成SO ,不能直接生成SO ,D项错误。]
2 2 3
4.(2020·广东顺德四模)蔗糖与浓硫酸反应的探究实验改进装置如图所示,该实验设计
更加体现了“绿色”“微型”的特点。下列说法正确的是( )A.该实验体现了浓硫酸的脱水性、酸性和强氧化性
B.反应中,品红褪色,加热后又恢复红色
C.紫色石蕊先变红后褪色
D.该装置无法证明二氧化硫具有氧化性
B [浓硫酸使蔗糖脱水碳化,同时放出大量的热,生成的碳再与浓硫酸发生反应生成
SO 、CO 和HO,体现浓硫酸的脱水性和强氧化性,A项错误;左侧试管中反应产生SO ,并
2 2 2 2
与品红化合生成无色物质而褪色,加热后无色物质分解,释放出SO ,溶液重新变红,B项正
2
确;SO 只能使紫色石蕊试液变红,但不能使其褪色,C项错误;NaS溶液中若出现淡黄色浑
2 2
浊,说明有单质硫生成,体现SO 的氧化性,D项错误。]
2
5.(2021·江西奉新检测)根据SO 通入不同溶液中的实验现象,所得结论不正确的是(
2
)
溶液 现象 结论
含HCl、BaCl 的
2
A 产生白色沉淀 SO 有还原性
2
FeCl 溶液
3
B HS溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
酸性:HSO >
2 3
D NaSiO 溶液 产生胶状沉淀
2 3
HSiO
2 3
C [A对:SO 通入含HCl、BaCl 的FeCl 溶液中,发生反应:SO +2Fe3++Ba2++
2 2 3 2
2HO===BaSO ↓+2Fe2++4H+,产生白色沉淀,该反应中SO 作还原剂,表现出还原性。B
2 4 2
对:SO 通入HS溶液中,发生反应:SO +2HS===3S↓+2HO,产生黄色沉淀,该反应中
2 2 2 2 2
SO 作氧化剂,表现出氧化性。C错:SO 通入酸性KMnO 溶液中,发生反应:5SO +2MnO+
2 2 4 2
2HO===5SO+2Mn2++4H+,该反应中,SO 作还原剂,表现出还原性而不是漂白性。D对:
2 2
SO 通入NaSiO 溶液中,发生反应:NaSiO+SO +HO===H SiO↓+NaSO ,该反应符合
2 2 3 2 3 2 2 2 3 2 3
“强酸制弱酸”的反应规律,则酸性:HSO >HSiO。]
2 3 2 3
6.(2021·安徽江淮联考)木炭在加热时可与浓硫酸发生反应:2HSO (浓)+C=====CO↑
2 4 2
+2SO ↑+2HO,为了验证该反应的所有产物,设计装置如图所示(夹持装置和加热装置略)。
2 2
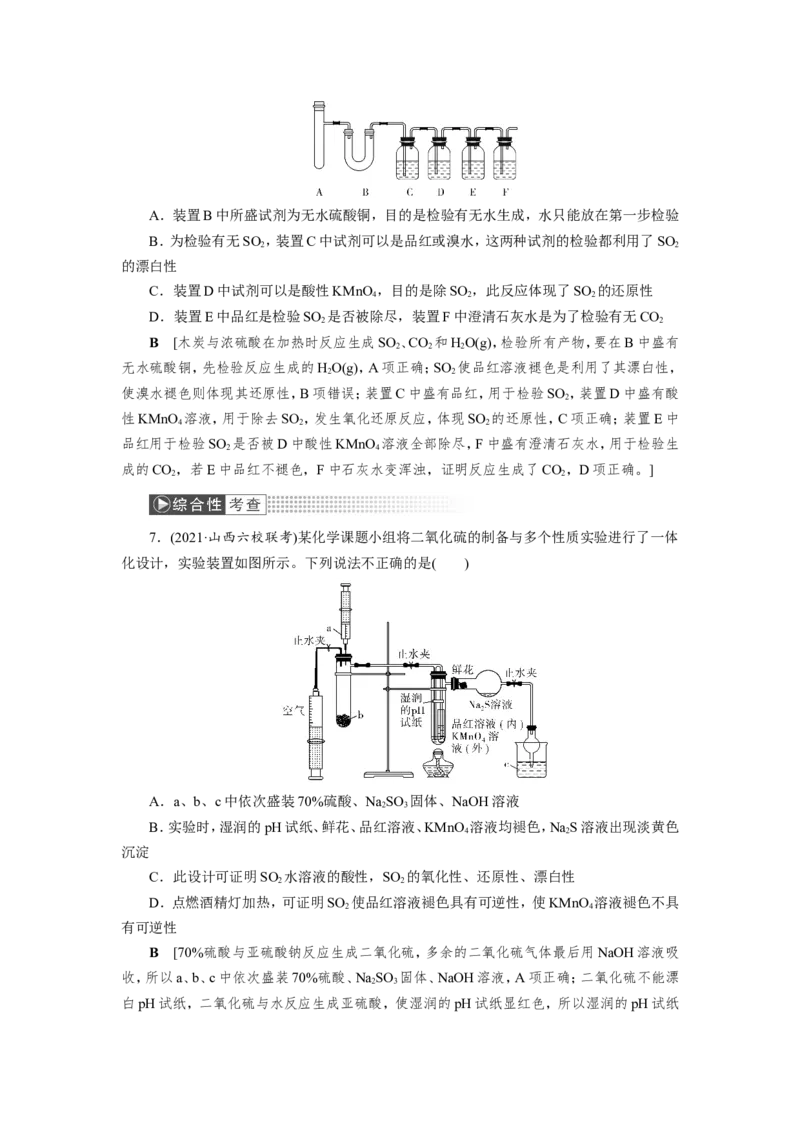
下列有关说法错误的是( )A.装置B中所盛试剂为无水硫酸铜,目的是检验有无水生成,水只能放在第一步检验
B.为检验有无SO ,装置C中试剂可以是品红或溴水,这两种试剂的检验都利用了SO
2 2
的漂白性
C.装置D中试剂可以是酸性KMnO ,目的是除SO ,此反应体现了SO 的还原性
4 2 2
D.装置E中品红是检验SO 是否被除尽,装置F中澄清石灰水是为了检验有无CO
2 2
B [木炭与浓硫酸在加热时反应生成SO 、CO 和HO(g),检验所有产物,要在B中盛有
2 2 2
无水硫酸铜,先检验反应生成的HO(g),A项正确;SO 使品红溶液褪色是利用了其漂白性,
2 2
使溴水褪色则体现其还原性,B项错误;装置C中盛有品红,用于检验SO ,装置D中盛有酸
2
性KMnO 溶液,用于除去SO ,发生氧化还原反应,体现SO 的还原性,C项正确;装置E中
4 2 2
品红用于检验SO 是否被D中酸性KMnO 溶液全部除尽,F中盛有澄清石灰水,用于检验生
2 4
成的CO,若E中品红不褪色,F中石灰水变浑浊,证明反应生成了CO,D项正确。]
2 2
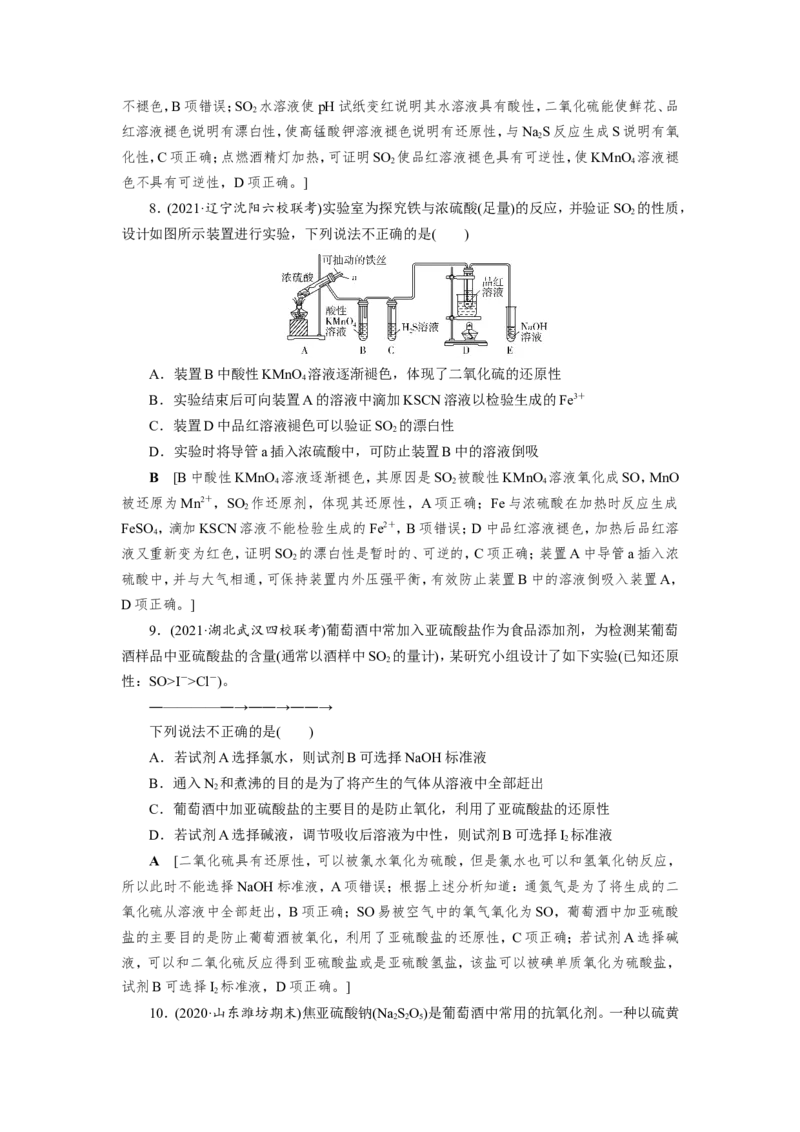
7.(2021·山西六校联考)某化学课题小组将二氧化硫的制备与多个性质实验进行了一体
化设计,实验装置如图所示。下列说法不正确的是( )
A.a、b、c中依次盛装70%硫酸、NaSO 固体、NaOH溶液
2 3
B.实验时,湿润的pH试纸、鲜花、品红溶液、KMnO 溶液均褪色,NaS溶液出现淡黄色
4 2
沉淀
C.此设计可证明SO 水溶液的酸性,SO 的氧化性、还原性、漂白性
2 2
D.点燃酒精灯加热,可证明SO 使品红溶液褪色具有可逆性,使KMnO 溶液褪色不具
2 4
有可逆性
B [70%硫酸与亚硫酸钠反应生成二氧化硫,多余的二氧化硫气体最后用NaOH溶液吸
收,所以a、b、c中依次盛装70%硫酸、NaSO 固体、NaOH溶液,A项正确;二氧化硫不能漂
2 3
白pH试纸,二氧化硫与水反应生成亚硫酸,使湿润的pH试纸显红色,所以湿润的pH试纸不褪色,B项错误;SO 水溶液使pH试纸变红说明其水溶液具有酸性,二氧化硫能使鲜花、品
2
红溶液褪色说明有漂白性,使高锰酸钾溶液褪色说明有还原性,与NaS反应生成S说明有氧
2
化性,C项正确;点燃酒精灯加热,可证明SO 使品红溶液褪色具有可逆性,使KMnO 溶液褪
2 4
色不具有可逆性,D项正确。]
8.(2021·辽宁沈阳六校联考)实验室为探究铁与浓硫酸(足量)的反应,并验证SO 的性质,
2
设计如图所示装置进行实验,下列说法不正确的是( )
A.装置B中酸性KMnO 溶液逐渐褪色,体现了二氧化硫的还原性
4
B.实验结束后可向装置A的溶液中滴加KSCN溶液以检验生成的Fe3+
C.装置D中品红溶液褪色可以验证SO 的漂白性
2
D.实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸
B [B中酸性KMnO 溶液逐渐褪色,其原因是SO 被酸性KMnO 溶液氧化成SO,MnO
4 2 4
被还原为Mn2+,SO 作还原剂,体现其还原性,A项正确;Fe与浓硫酸在加热时反应生成
2
FeSO ,滴加KSCN溶液不能检验生成的Fe2+,B项错误;D中品红溶液褪色,加热后品红溶
4
液又重新变为红色,证明SO 的漂白性是暂时的、可逆的,C项正确;装置A中导管a插入浓
2
硫酸中,并与大气相通,可保持装置内外压强平衡,有效防止装置B中的溶液倒吸入装置A,
D项正确。]
9.(2021·湖北武汉四校联考)葡萄酒中常加入亚硫酸盐作为食品添加剂,为检测某葡萄
酒样品中亚硫酸盐的含量(通常以酒样中SO 的量计),某研究小组设计了如下实验(已知还原
2
性:SO>I->Cl-)。
―————―→――→――→
下列说法不正确的是( )
A.若试剂A选择氯水,则试剂B可选择NaOH标准液
B.通入N 和煮沸的目的是为了将产生的气体从溶液中全部赶出
2
C.葡萄酒中加亚硫酸盐的主要目的是防止氧化,利用了亚硫酸盐的还原性
D.若试剂A选择碱液,调节吸收后溶液为中性,则试剂B可选择I 标准液
2
A [二氧化硫具有还原性,可以被氯水氧化为硫酸,但是氯水也可以和氢氧化钠反应,
所以此时不能选择NaOH标准液,A项错误;根据上述分析知道:通氮气是为了将生成的二
氧化硫从溶液中全部赶出,B项正确;SO易被空气中的氧气氧化为SO,葡萄酒中加亚硫酸
盐的主要目的是防止葡萄酒被氧化,利用了亚硫酸盐的还原性,C项正确;若试剂A选择碱
液,可以和二氧化硫反应得到亚硫酸盐或是亚硫酸氢盐,该盐可以被碘单质氧化为硫酸盐,
试剂B可选择I 标准液,D项正确。]
2
10.(2020·山东潍坊期末)焦亚硫酸钠(Na SO)是葡萄酒中常用的抗氧化剂。一种以硫黄
2 2 5为原料制取NaSO 的生产工艺如下:
2 2 5
已知:结晶脱水发生的反应:2NaHSO===Na SO+HO。回答下列问题:
3 2 2 5 2
(1)Na SO 中硫元素的化合价为________。
2 2 5
(2)焚烧炉中反应的化学方程式为__________________________________。
(3)反应器中发生反应的离子方程式为________________________________________。
(4)葡萄酒酿造过程中添加NaSO 会放出一种有刺激性气味的气体,该气体是一种食品
2 2 5
添加剂。实验室中检验该气体的常用试剂是______________________________。
(5)废水中的硫单质(S )能与碱反应,化学反应:3S +48KOH=====16KS+8KSO +
8 8 2 2 3
24HO,反应中氧化剂与还原剂的物质的量之比为________。
2
解析 (1)Na SO 中Na元素显+1价,O元素显-2价,根据化合物中各元素化合价代
2 2 5
数和为0推知,S元素显+4价。
(3)结合结晶脱水发生的反应推知,反应器中NaCO 溶液吸收SO ,生成NaHSO 和
2 3 2 3
CO,离子方程式为2SO +CO+HO===2HSO+CO。
2 2 2 2
(5)硫单质(S )与碱反应中,S 既是氧化剂又是还原剂,KS是还原产物,KSO 是氧化产
8 8 2 2 3
物,根据反应产物的量及S元素守恒推知,氧化剂与还原剂的物质的量之比为16∶8=2∶1。
答案 (1)+4 (2)S+O=====SO
2 2
(3)2SO +CO+HO===2HSO+CO
2 2 2
(4)品红溶液 (5)2∶1
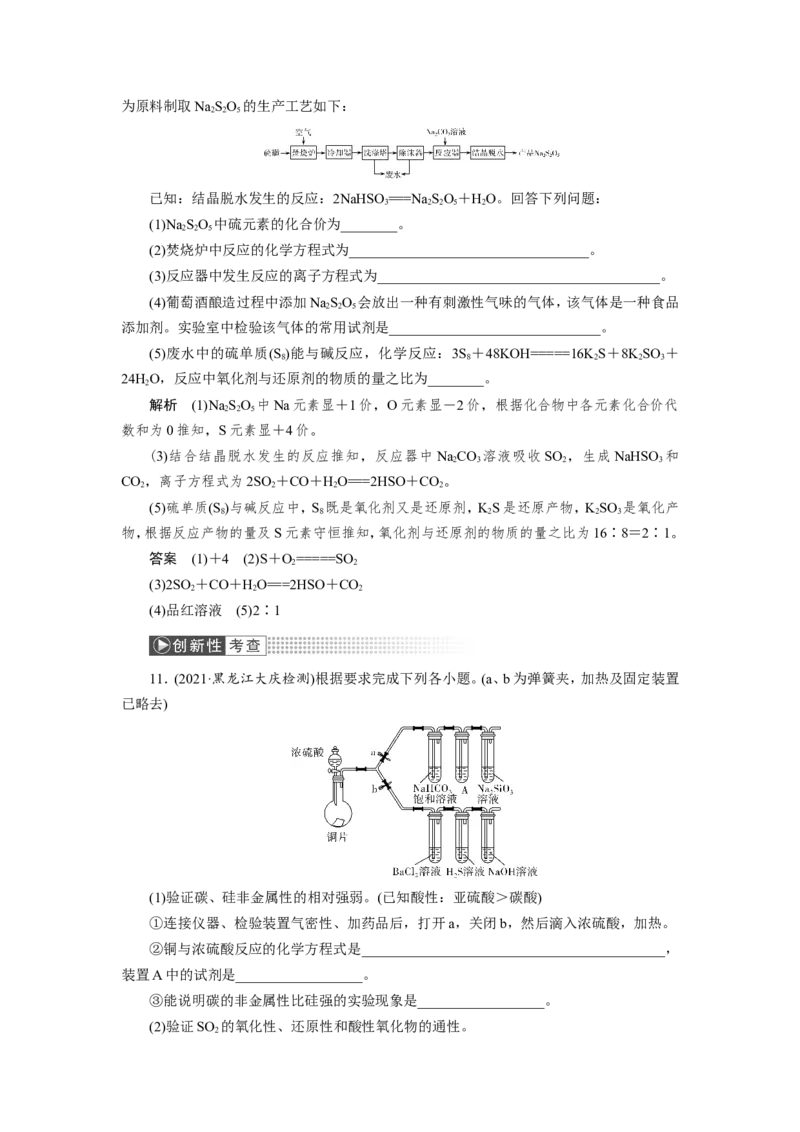
11.(2021·黑龙江大庆检测)根据要求完成下列各小题。(a、b为弹簧夹,加热及固定装置
已略去)
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①连接仪器、检验装置气密性、加药品后,打开a,关闭b,然后滴入浓硫酸,加热。
②铜与浓硫酸反应的化学方程式是___________________________________________,
装置A中的试剂是__________________。
③能说明碳的非金属性比硅强的实验现象是__________________。
(2)验证SO 的氧化性、还原性和酸性氧化物的通性。
2①打开b,关闭a,HS溶液中有浅黄色沉淀出现。
2
②BaCl 溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式
2
填入下表相应位置。
滴加的溶液 氯水 氨水
沉淀的化学式 ______ ______
写出其中SO 表现还原性并生成沉淀的离子方程式__________________。
2
答案 (1)②Cu+2HSO (浓)=====CuSO +SO ↑+2HO 酸性KMnO 溶液(答案合理
2 4 4 2 2 4
即可)
③A中酸性KMnO 溶液没有完全褪色,盛有NaSiO 溶液的试管中出现白色沉淀
4 2 3
(2)②BaSO BaSO Ba2++SO +Cl+2HO===BaSO ↓+4H++2Cl-
4 3 2 2 2 4
12.(2021·河南开封模拟)某校合作学习小组的同学设计实验验证NaSO 与焦炭高温加
2 4
热后的产物。回答下列问题。
(1)Na SO 与焦炭反应的实验装置如图所示:
2 4
①先通入N,然后加热,直至反应结束,整个过程中N 的作用是_____________。
2 2
②装置B的作用是____________________。
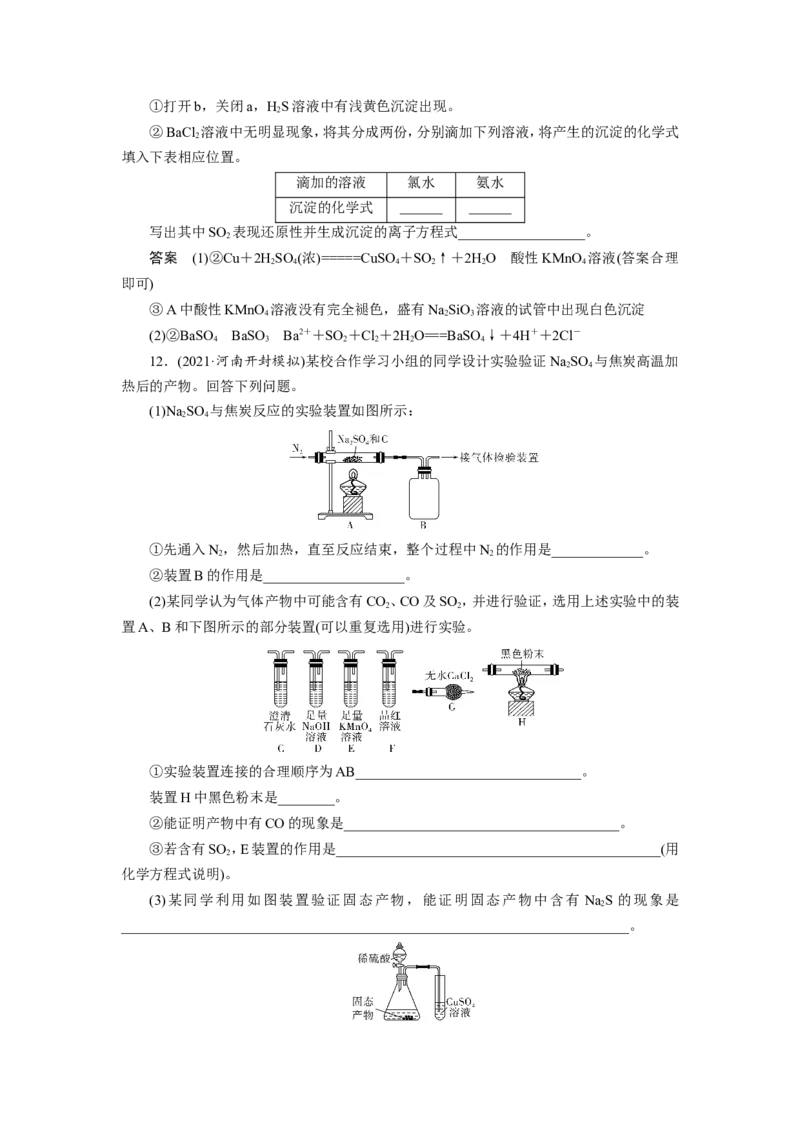
(2)某同学认为气体产物中可能含有CO、CO及SO ,并进行验证,选用上述实验中的装
2 2
置A、B和下图所示的部分装置(可以重复选用)进行实验。
①实验装置连接的合理顺序为AB________________________________。
装置H中黑色粉末是________。
②能证明产物中有CO的现象是_______________________________________。
③若含有SO ,E装置的作用是______________________________________________(用
2
化学方程式说明)。
(3)某同学利用如图装置验证固态产物,能证明固态产物中含有 NaS 的现象是
2
________________________________________________________________________。若实验中发现固态产物完全反应后,锥形瓶底部还产生少量黄色沉淀,说明固体产物中
除含有NaS外,还含有少量的____________(填一种可能的物质)。
2
解析 (1)①碳能够与空气中的氧气反应生成碳的氧化物,为了防止氧气对实验的干扰,
先通入N ,然后加热,直至反应结束,可以排出装置中的空气并将生成的气体吹出。
2
②NaSO 与焦炭高温加热后的产物中可能含有二氧化硫等易溶于水的气体,装置B可以防
2 4
止倒吸,为安全瓶。
(2)①气体中可能含有CO、CO及SO ,由于SO 也能使澄清石灰水变浑浊,需要先检验
2 2 2
SO ,然后除去SO 后再检验CO,最后除去CO 后再检验CO,故实验装置的合理连接顺序
2 2 2 2
为A、B、F、E、C、D、G、H、C;一氧化碳具有还原性,可以还原金属氧化物,故装置H中黑色
粉末可以是氧化铜。②H中黑色粉末变为红色,其后的C中的澄清石灰水变浑浊,即可证明
产物中有CO。③二氧化硫能够与高锰酸钾溶液发生氧化还原反应,反应的化学方程式为
5SO +2KMnO +2HO===K SO +2MnSO +2HSO 。
2 4 2 2 4 4 2 4
(3)若存在NaS,则NaS能够与硫酸反应生成硫化氢气体,硫化氢与硫酸铜溶液反应生
2 2
成黑色的硫化铜沉淀;锥形瓶底部还产生少量黄色沉淀,该黄色沉淀是硫单质,可能是硫化
氢与+4价的硫的化合物反应生成的,说明固体产物中除含有NaS外,还可能含有少量的
2
NaSO 。
2 3
答案 (1)①排出装置中的空气并将生成的气体吹出 ②防止倒吸
(2)①FECDGHC CuO ②H中黑色粉末变为红色,其后的C中的澄清石灰水变浑浊
③5SO +2KMnO +2HO===K SO +2MnSO +2HSO
2 4 2 2 4 4 2 4
(3)试管中出现黑色沉淀 NaSO
2 3