文档内容
第4课时 必备知识——盐类的水解
[基本规律]①盐类水解的规律;②外界条件对盐类水解的影响
知识
清单
[重要应用]①盐类水解的应用;②水解常数(K )与电离常数的关系及应用
h
知识点1 盐类水解及其规律
1.盐类的水解
2.盐类水解的规律
有弱才水解,越弱越水解;谁强显谁性,同强显中性。
盐的类型 示例 是否水解 水解的离子 溶液的酸碱性 溶液的pH
强酸强碱盐 NaCl、KNO 否 中性 pH = 7
3
NH Cl、
强酸弱碱盐 4 是 NH 、 Cu 2 + 酸性 pH < 7
Cu(NO )
3 2
CHCOONa、 CH 3 COO - 、
弱酸强碱盐 3 是 碱性 pH>7
NaCO
2 3
3.盐类水解离子方程式的书写要求
(1)一般来说,盐类水解的程度不大,一般应用“”连接。盐类水解一般不会产生沉
淀和气体,一般不用符号“↓”和“↑”表示水解产物。
(2)多元弱酸根离子水解的离子方程式应分步书写,水解以第一步水解为主。例如,SO水
解的离子方程式为 SO + H O HSO + OH - 。
2
(3)多元弱碱阳离子的水解比较复杂,一般一步写出。值得注意的是,其最终生成的弱碱
即使是难溶物也不标“↓”等状态符号,因其水解生成的量极少,不会生成沉淀。例如,Fe3+
水解的离子方程式常写成: Fe 3 + + 3H O Fe (OH) + 3H + 。
2 3
(4)水解分别显酸性和碱性的离子由于相互促进水解程度较大,书写时一般要用“===”“↑”“↓”等。
(5)书写盐类水解的离子方程式时,要遵循质量守恒定律和电荷守恒规律。
[通关1] (易错排查)判断正误
(1)(2020·天津卷)相同浓度的 HCOONa 和 NaF 两溶液,前者的 pH 较大,则
K(HCOOH)>K(HF)(×)
a a
(2)(2020·天津卷)相同浓度的CHCOOH和CHCOONa两溶液等体积混合后pH约为
3 3
4.7,则溶液中c(CHCOO-)>c(Na+)>c(H+)>c(OH-)(√)
3
(3)(2020·天津卷)在1 mol·L-1 NaS溶液中,c(S2-)+c(HS-)+c(H S)=1 mol·L-1(√)
2 2
(4)常温下,pH=11的CHCOONa溶液与pH=3的CHCOOH溶液,水的电离程度相同
3 3
(×)
[通关2] (2020.7·浙江选考)水溶液呈酸性的是( )
A.NaCl B.NaHSO
4
C.HCOONa D.NaHCO
3
B [NaCl水溶液显中性,A项错误;NaHSO 在水中电离产生Na+、H+、SO,其水溶液显
4
酸性,B项正确;HCOONa和NaHCO 均为强碱弱酸盐,其水溶液均显碱性,C、D项错误。]
3
[通关3] (人教选修4·P53,1题改编)下列水解离子方程式及有关说法正确的是( )
A.NaHC O 溶于水显碱性是因为HC O+HOHC O +OH-,HC OH++C O,
2 4 2 2 2 2 4 2 2
HC O的水解程度大于其电离程度
2
B.常温下,0.1 mol·L-1的一元酸HX溶液的pH=3,可推知NaX溶液中存在X-+
HO===HX+OH-
2
C.向KCO 溶液中滴入酚酞溶液,溶液变红色的原因是CO+HO===HCO+OH-,滴加
2 3 2
BaCl 溶液,颜色无变化
2
D.NaHSO 溶于水显酸性是因为HSOSO+H+,HSO+HOHSO +OH-,HSO的
3 2 2 3
电离程度小于其水解程度
A [显碱性说明HC O的水解程度大于其电离程度,离子方程式均正确,A项正确;应用
2
“”,正确的离子方程式为X-+HOHX+OH-,B项错误;应用“”,正确的离子
2
方程式为CO+HOHCO+OH-,滴加BaCl 溶液,平衡逆向移动,C项错误;显酸性说明
2 2
HSO的电离程度大于其水解程度,D项错误。][通关4] (人教选修4·P53,2题改编)物质的量浓度相同的下列溶液中,按pH由小到大的
顺序排列的是( )
A.Na CO NaHCO NaCl NH Cl
2 3 3 4
B.Na CO NaHCO NH Cl NaCl
2 3 3 4
C.(NH )SO NH Cl NaNO NaS
4 2 4 4 3 2
D.NH Cl (NH )SO NaS NaNO
4 4 2 4 2 3
C [A、B两项中四种盐相同,在同浓度时,其pH由小到大的排列顺序为NH Cl、NaCl、
4
NaHCO 、NaCO ;C、D两项中四种盐相同,因(NH )SO 溶液中c(NH)大于NH Cl溶液中
3 2 3 4 2 4 4
c(NH),其前者酸性更强,pH更小,则这四种盐溶液pH由小到大的排列顺序为(NH )SO 、
4 2 4
NH Cl、NaNO 、NaS。]
4 3 2
知识点2 盐类水解的影响因素及应用
1.影响盐类水解平衡的因素
(1)内因
其他条件相同时,形成盐的酸或碱越弱,其盐就越易水解。已知酸性:HSO >HCO>
2 3 2 3
HSO>HCO,则水解程度:NaCO>NaSO (填“>”或“<”,下同),NaCO>NaHCO 。
2 3 2 3 2 3 3
(2)外因
以FeCl 的水解为例(Fe3++3HOFe(OH) +3H+)分析如下表
3 2 3
条件 平衡移动方向 n(H+) 溶液的pH 现象
升温 向右 增多 减小 颜色变深通HCl 向左 增多 减小 颜色变浅
加HO 向右 增多 增大 颜色变浅
2
生成红褐色沉
加NaHCO 向右 减小 增大
3
淀,放出气体
水解平衡向右移动,水解程度不一定增大。水解程度增大,水解产生的离子浓度
不一定增大。
2.盐类水解的应用
应用 举例
热的纯碱溶液去污力强(纯碱水解显碱性,在碱性条件下
(1)加热促进水解方便生活
油脂水解,并不是纯碱和油脂直接反应)
(2)分析盐溶液的酸碱性、比较 等物质的量浓度的NaCO、NaHCO 溶液均显碱性,且碱
2 3 3
对应酸碱性强弱 性:NaCO>NaHCO
2 3 3
(3)判断离子能否大量共存 Al3+和HCO因发生水解相互促进反应不能大量共存
配制FeCl 溶液,要向FeCl 溶液中加入适量盐酸(不能将
(4)配制或贮存盐溶液方法 3 3
其直接溶于水中)
(5)胶体制备与作净水剂原理 铝盐、铁盐净水; 制备Fe(OH) 胶体
3
(6)化肥的使用禁忌 铵态氮肥不宜与草木灰混合使用
Al3++3HCO===Al(OH) ↓+3CO↑,水解相互促进的
(7)泡沫灭火器的反应原理 3 2
结果
(8)无水盐制备的条件控制 由MgCl ·6H O制MgCl ,在干燥的HCl 气流中加热
2 2 2
为除去MgCl 酸性溶液中的Fe3+,可在加热搅拌的条件
2
(9)某些盐的分离除杂措施 下加入MgO、MgCO 或Mg(OH) ,过滤后再加入适量的
3 2
盐酸
(10)盐溶液除锈原理解释 NH Cl溶液除去金属表面的氧化物(NH水解显酸性)
4
[通关1] (易错排查)判断正误
(1)(2018·天津卷)某温度下,一元弱酸HA的K 越小,则NaA的K (水解常数)越小(×)
a h
(2)(2017·海南卷)向硫酸铝溶液中滴加碳酸钠溶液的离子方程式为 2Al3++
3CO===Al(CO)↓(×)
2 3 3
(3)水解平衡向右移动,盐的离子的水解程度一定增大(×)
(4)NaHCO 和NaHSO 都能促进水的电离(×)
3 4
(5)Na CO 溶液加水稀释,促进水的电离,溶液的碱性增强(×)
2 3
(6)稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强(×)
[通关2] (2021·河北张家口检测)浓度均为0.1 mol/L的下列八种溶液:①HCl;②HSO ;
2 4③CHCOOH;④Ba(OH) ;⑤KOH;⑥NaF;⑦KCl;⑧NH Cl 的pH由小到大的顺序是(
3 2 4
)
A.②①③⑧⑦⑥⑤④ B.②①③⑥⑦⑧⑤④
C.①②③⑧⑦⑥④⑤ D.②①⑧③⑦⑥④⑤
A [NH Cl溶液因NH水解而呈酸性,NaF溶液因F-水解而呈碱性,考虑盐类水解程
4
度较小,NH Cl溶液的酸性比①②③三种酸的弱,NaF溶液的碱性比④⑤两种碱的碱性弱;
4
HCl是一元强酸,HSO 是二元强酸,CHCOOH是一元弱酸,KOH是一元强碱,Ba(OH) 是
2 4 3 2
二元强碱,KCl 是强酸强碱盐,由于八种溶液的浓度均为 0.1 mol/L,故溶液的 pH:
②<①<③<⑧<⑦<⑥<⑤<④。]
[通关3] (2020·江苏启东检测)下列有关问题,与盐的水解有关的是( )
①NH Cl与ZnCl 溶液可作焊接金属中的除锈剂 ②用NaHCO 与Al (SO ) 两种溶液
4 2 3 2 4 3
可作泡沫灭火剂 ③草木灰与铵态氮肥不能混合施用 ④实验室盛放碳酸钠溶液的试剂瓶
不能用磨口玻璃塞 ⑤加热蒸干AlCl 溶液得到Al(OH) 固体
3 3
A.①②③ B.②③④
C.①④⑤ D.①②③④⑤
D [①中NH Cl与ZnCl 溶液水解均显酸性,可以除去金属表面的锈;②HCO与Al3+
4 2
两种离子水解能相互促进,产生二氧化碳气体和氢氧化铝沉淀,可作灭火剂;③草木灰的主
要成分为碳酸钾,水解显碱性,而铵态氮肥水解显酸性,因而不能混合施用;④碳酸钠溶液水
解显碱性,而磨口玻璃塞中的二氧化硅会与碱反应生成硅酸钠将瓶塞与瓶口黏合在一块儿
而打不开,因此实验室盛放碳酸钠溶液的试剂瓶应用橡胶塞;⑤AlCl 溶液中存在水解平衡:
3
AlCl +3HOAl(OH) +3HCl,加热时,HCl挥发使平衡不断右移,最终得到Al(OH) 固体
3 2 3 3
(如果灼烧,会得到Al O 固体)。]
2 3[通关4] (2021·河南部分校联考)已知:[FeCl (H O) ]-为黄色,溶液中可以存在可逆反应:
4 2 2
Fe3++4Cl-+2HO[FeCl (H O) ]-,下列实验所得结论不正确的是( )
2 4 2 2
① ② ③ ④
加热前溶液接近无 加入NaCl后,溶液立
加热前溶液为浅黄 加热前溶液为黄色,
色,加热后溶液颜色 即变为黄色,加热后
色,加热后颜色变深 加热后溶液颜色变深
无明显变化 溶液颜色变深
注:加热为微热,忽略体积变化。
A.实验①中,Fe (SO ) 溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)
2 4 3 3
B.实验②中,酸化对Fe3+水解的影响程度大于温度的影响
C.实验③中,加热,可逆反应:Fe3++4Cl-+2HO[FeCl (H O)]-正向移动
2 4 2 2
D.实验④,可证明升高温度,颜色变深一定是因为Fe3+水解平衡正向移动
D [加热促进水解,铁离子水解生成氢氧化铁,则实验①中,Fe (SO ) 溶液显浅黄色原
2 4 3
因是Fe3+水解产生了少量Fe(OH) ,A项正确;由Fe3++3HOFe(OH) +3H+可知,酸化后
3 2 3
加热溶液颜色无明显变化,氢离子抑制水解,则实验②中酸化对Fe3+水解的影响程度大于温
度的影响,B 项正确;加入 NaCl 后,溶液立即变为黄色,发生 Fe3++4Cl-+
2HO[FeCl (H O)]-,[FeCl (H O)]-为黄色,加热时平衡正向移动,溶液颜色变深,C项正
2 4 2 2 4 2 2
确;实验④中存在Fe3++4Cl-+2HO[FeCl (H O)]-,升高温度平衡正向移动,溶液颜色
2 4 2 2变深,不能证明对Fe3+水解平衡的影响,D项错误。]
知识点3 水解常数(K )与电离常数的关系及应用
h
1.水解常数
在一定温度下,能水解的盐(强碱弱酸盐、强酸弱碱盐或弱酸弱碱盐)在水溶液中达到水
解平衡时,生成的弱酸(或弱碱)浓度和氢氧根离子(或氢离子)浓度之积与溶液中未水解的弱
酸根阴离子(或弱碱的阳离子)浓度之比是一个常数,该常数就叫水解常数。
2.水解常数(K )与电离常数的定量关系
h
(1)盐的水解常数与对应的一元弱酸(或弱碱)的电离平衡常数的乘积等于 K ,以
w
CHCOONa为例:
3
CHCOONa溶液中存在水解平衡:CH COO - + H O CH COOH + OH - ,则CHCOO-
3 3 2 3 3
的水解常数为K ===
h
=,因此K(或K )与K 的定量关系为K · K =K 或K ·K =K
a h w a h w b h w
(2)多元弱酸强碱盐,如NaCO 的水解常数K =、K =。
2 3 h1 h2
(3)一元弱酸一元弱碱盐,如醋酸铵:K =
h
3.水解常数的影响因素
水解常数是描述能水解的盐水解平衡的主要参数,只受温度的影响,因水解过程是吸热
过程,故它随温度的升高而增大。
[通关1] (2021·江西九江六校联考)在NaCN溶液中存在水解平衡:CN-+HOHCN+
2
OH-,水解常数K (CN-)=≈[c(NaCN)是NaCN溶液的起始浓度]。25 ℃时,向1 mol·L-1的
h 0
NaCN溶液中不断加水稀释,NaCN溶液浓度的对数值lg c 与2pOH[pOH=-lg c(OH-)]的
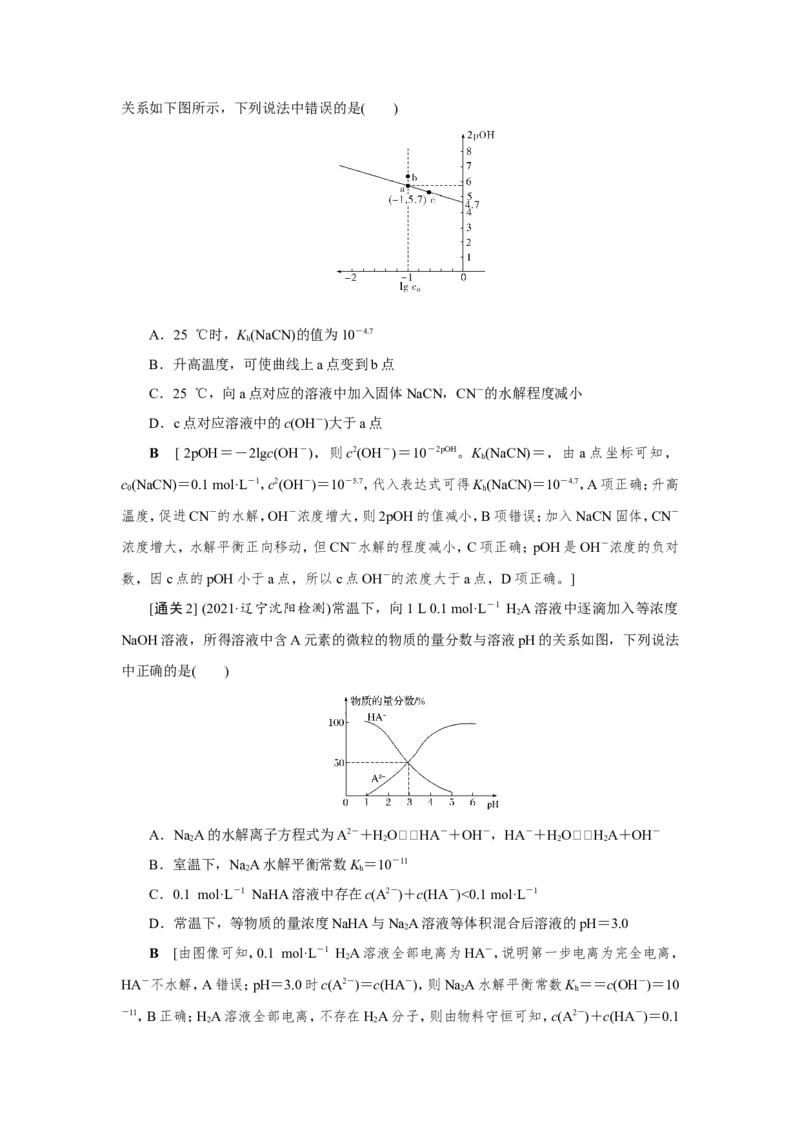
0关系如下图所示,下列说法中错误的是( )
A.25 ℃时,K (NaCN)的值为10-4.7
h
B.升高温度,可使曲线上a点变到b点
C.25 ℃,向a点对应的溶液中加入固体NaCN,CN-的水解程度减小
D.c点对应溶液中的c(OH-)大于a点
B [ 2pOH=-2lgc(OH-),则c2(OH-)=10-2pOH。K (NaCN)=,由a点坐标可知,
h
c(NaCN)=0.1 mol·L-1,c2(OH-)=10-5.7,代入表达式可得K (NaCN)=10-4.7,A项正确;升高
0 h
温度,促进CN-的水解,OH-浓度增大,则2pOH的值减小,B项错误;加入NaCN固体,CN-
浓度增大,水解平衡正向移动,但CN-水解的程度减小,C项正确;pOH是OH-浓度的负对
数,因c点的pOH小于a点,所以c点OH-的浓度大于a点,D项正确。]
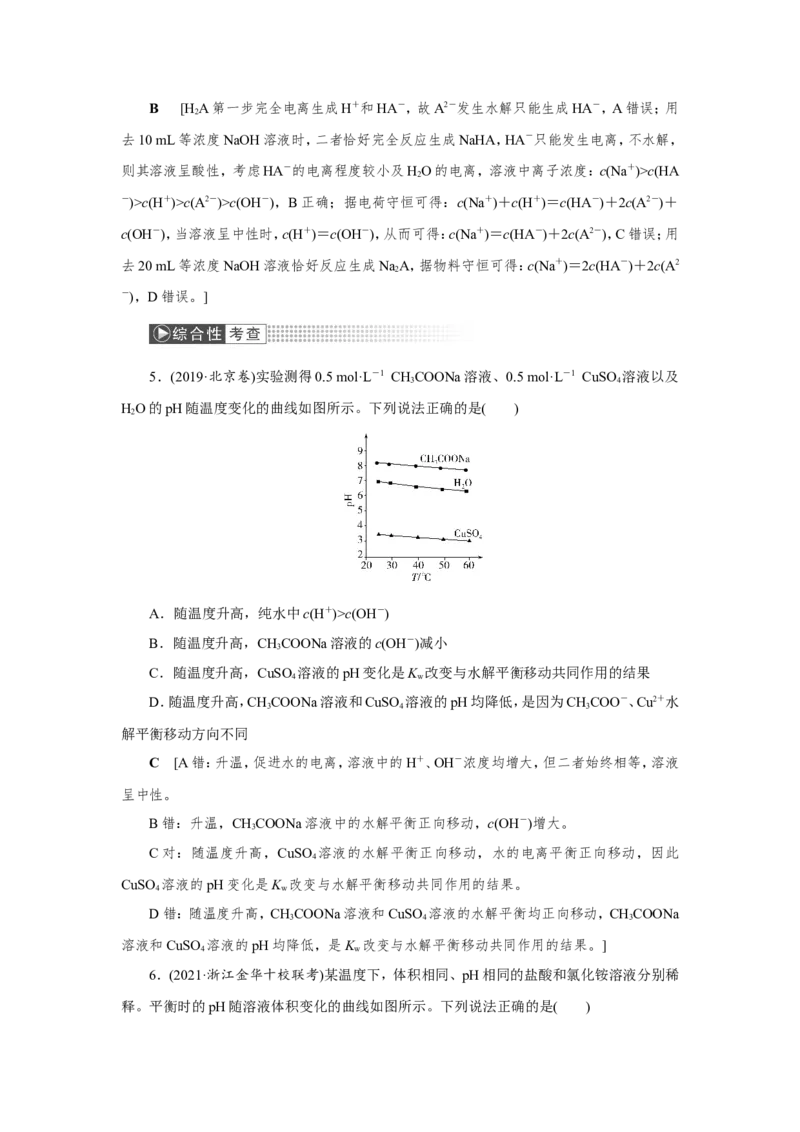
[通关2] (2021·辽宁沈阳检测)常温下,向1 L 0.1 mol·L-1 HA溶液中逐滴加入等浓度
2
NaOH溶液,所得溶液中含A元素的微粒的物质的量分数与溶液pH的关系如图,下列说法
中正确的是( )
A.NaA的水解离子方程式为A2-+HOHA-+OH-,HA-+HOHA+OH-
2 2 2 2
B.室温下,NaA水解平衡常数K =10-11
2 h
C.0.1 mol·L-1 NaHA溶液中存在c(A2-)+c(HA-)<0.1 mol·L-1
D.常温下,等物质的量浓度NaHA与NaA溶液等体积混合后溶液的pH=3.0
2
B [由图像可知,0.1 mol·L-1 HA溶液全部电离为HA-,说明第一步电离为完全电离,
2
HA-不水解,A错误;pH=3.0时c(A2-)=c(HA-),则NaA水解平衡常数K ==c(OH-)=10
2 h
-11,B正确;HA溶液全部电离,不存在HA分子,则由物料守恒可知,c(A2-)+c(HA-)=0.1
2 2mol·L-1,C错误;HA-H++A2-,电离常数K =,当c(A2-)=c(HA-),K =c(H+)=10-3,
a2 a2
K >K ,等物质的量浓度NaHA、NaA等体积混合,HA-的电离程度大于A2-的水解程度,所
a2 h 2
得c(HA-)3.0,D错误。]
[通关3] (深度思考)(1)已知25 ℃时,NH ·H O的电离平衡常数K =1.8×10-5,该温度下
3 2 b
1 mol·L-1的NH Cl溶液中c(H+)=________ mol·L-1。(已知≈2.36)
4
(2)已知某温度时,NaCO 溶液的水解常数K =2×10-4,则当溶液中c(HCO)∶c(CO)=
2 3 h
2∶1时,试求该溶液的pH=________。
解析 (1)K ==
h
c(H+)≈c(NH ·HO),而c(NH)≈1 mol·L-1。
3 2
所以c(H+)≈= mol·L-1≈2.36×10-5 mol·L-1。
(2)K ==2×10-4,
h
又c(HCO)∶c(CO)=2∶1,则c(OH-)=10-4 mol·L-1,结合K =10-14,可得c(H+)=10-
w
10 mol·L-1。
答案 (1)2.36×10-5 (2)10
训练(四十一) 盐类的水解
1.(2021·甘肃会宁检测)在一定条件下,NaCO 溶液中存在水解平衡:CO+HOHCO
2 3 2
+OH-。下列说法正确的是( )
A.稀释溶液,水解平衡常数增大
B.加入少量NH Cl固体,平衡向正反应方向移动
4
C.升高温度,减小
D.加入NaOH固体,溶液pH减小
B [水解平衡常数只与温度有关,温度不变,平衡常数不变,A错误;加入少量NH Cl固
4
体,NH和CO均发生水解,且相互促进,故CO的水解平衡向正反应方向移动,B正确;升高
温度,平衡正向移动,c(HCO)增大,c(CO)减小,故增大,C错误;加入NaOH固体,平衡逆向
移动,但溶液中c(OH-)增大,溶液pH增大,D错误。]
2.(2021·河北辛集中学检测)下列关于电解质溶液的叙述正确的是( )
A.常温下,同浓度的NaS与NaHS溶液相比,NaS溶液的pH大
2 2
B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同D.常温下,pH=7的NH Cl与氨水的混合溶液中离子浓度大小顺序为c(Cl-)>c(NH)>
4
c(H+)>c(OH-)
A [Na S的水解程度比NaHS大,水解程度越大,则碱性越强,所以NaS溶液的pH大,
2 2
A项正确;将pH=4的醋酸溶液稀释后,稀释时氢离子浓度减小,由于氢离子与氢氧根离子
的乘积不变,则氢氧根离子浓度增大,B项错误;pH相同时,盐酸与醋酸的浓度不同,由于醋
酸部分电离,盐酸完全电离,所以醋酸的浓度大于盐酸的浓度,则等体积时消耗的氢氧化钠
的量多,C项错误;常温下,pH=7的NH Cl与氨水的混合溶液存在电荷守恒:c(Cl-)+c(OH
4
-)=c(NH)+c(H+),pH=7溶液中c(H+)=c(OH-),则c(Cl-)=c(NH),所以离子浓度大小顺
序为c(Cl-)=c(NH)>c(H+)=c(OH-),D项错误。]
3.(2021·山东烟台一中检测)有①NaCO 溶液,
2 3
②CHCOONa溶液,③NaOH溶液各25 mL,物质的量浓度均为0.1 mol/L,下列说法正
3
确的是( )
A.三种溶液pH的大小顺序是③>②>①
B.若将三种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25 mL 0.1 mol/L 的盐酸后,pH最大的是①
D.若三种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
C [等浓度时,NaOH是强碱,其碱性最强;CHCOOH的酸性强于HCO,则NaCO 的
3 2 3 2 3
水解程度大于CHCOONa,故溶液pH:③>①>②,A错误;三种溶液分别加水稀释,CO、
3
CHCOO-的水解平衡正向移动,溶液的pH变化小,故pH变化最大的是NaOH,B错误;分
3
别加入25 mL等浓度盐酸,所得溶液中,①为等浓度NaHCO 、NaCl混合液,②为等浓度
3
CHCOOH、NaCl混合液,③为NaCl溶液,HCO的水解显碱性,故pH最大的是①,C正确;
3
NaCO 的水解程度大于CHCOONa,三种溶液的pH均为9时,其物质的量浓度:②>①>③,
2 3 3
D错误。]
4.(2021·福建莆田三校联考)室温下,取10 mL 0.1 mol·L-1某二元酸HA,滴加0.1 mol·L
2
-1 NaOH溶液。已知:HA===H++HA-,HA-H++A2-。下列说法正确的是( )
2
A.A2-可经过两步水解得到HA
2
B.当用去NaOH溶液体积10 mL时,溶液中离子浓度大小顺序为c(Na+)>c(HA-)>c(H
+)>c(A2-)>c(OH-)
C.当滴加至中性时,溶液中有c(Na+)=c(HA-)+c(A2-)
D.当用去NaOH溶液体积20 mL时,此时溶液中有c(Na+)=c(HA-)+c(A2-)B [H A第一步完全电离生成H+和HA-,故A2-发生水解只能生成HA-,A错误;用
2
去10 mL等浓度NaOH溶液时,二者恰好完全反应生成NaHA,HA-只能发生电离,不水解,
则其溶液呈酸性,考虑HA-的电离程度较小及HO的电离,溶液中离子浓度:c(Na+)>c(HA
2
-)>c(H+)>c(A2-)>c(OH-),B正确;据电荷守恒可得:c(Na+)+c(H+)=c(HA-)+2c(A2-)+
c(OH-),当溶液呈中性时,c(H+)=c(OH-),从而可得:c(Na+)=c(HA-)+2c(A2-),C错误;用
去20 mL等浓度NaOH溶液恰好反应生成NaA,据物料守恒可得:c(Na+)=2c(HA-)+2c(A2
2
-),D错误。]
5.(2019·北京卷)实验测得0.5 mol·L-1 CHCOONa溶液、0.5 mol·L-1 CuSO 溶液以及
3 4
HO的pH随温度变化的曲线如图所示。下列说法正确的是( )
2
A.随温度升高,纯水中c(H+)>c(OH-)
B.随温度升高,CHCOONa溶液的c(OH-)减小
3
C.随温度升高,CuSO 溶液的pH变化是K 改变与水解平衡移动共同作用的结果
4 w
D.随温度升高,CHCOONa溶液和CuSO 溶液的pH均降低,是因为CHCOO-、Cu2+水
3 4 3
解平衡移动方向不同
C [A错:升温,促进水的电离,溶液中的H+、OH-浓度均增大,但二者始终相等,溶液
呈中性。
B错:升温,CHCOONa溶液中的水解平衡正向移动,c(OH-)增大。
3
C对:随温度升高,CuSO 溶液的水解平衡正向移动,水的电离平衡正向移动,因此
4
CuSO 溶液的pH变化是K 改变与水解平衡移动共同作用的结果。
4 w
D错:随温度升高,CHCOONa溶液和CuSO 溶液的水解平衡均正向移动,CHCOONa
3 4 3
溶液和CuSO 溶液的pH均降低,是K 改变与水解平衡移动共同作用的结果。]
4 w
6.(2021·浙江金华十校联考)某温度下,体积相同、pH相同的盐酸和氯化铵溶液分别稀
释。平衡时的pH随溶液体积变化的曲线如图所示。下列说法正确的是( )A.曲线Ⅱ对应氯化铵溶液
B.与等浓度的NaOH溶液恰好反应时曲线Ⅰ对应的溶液消耗NaOH溶液体积大
C.b、c、d三点水的电离程度:c>b>d
D.a、c、d三点的水的离子积常数不等
A [盐酸是强酸,完全电离;氯化铵溶于水,NH水解,溶液显酸性,水解方程式是NH+
HONH ·HO+H+,稀释促进水解,n(H+)增加,c(H+)还是减小的,但c(H+)的变化量要
2 3 2
小于盐酸中c(H+)的变化量,所以曲线Ⅱ为氯化铵稀释时pH变化曲线,A项正确;与等浓度
的NaOH溶液恰好反应时,氯化铵消耗的NaOH溶液较多,曲线Ⅱ对应的溶液消耗NaOH溶
液体积大,B项错误;曲线Ⅰ表示盐酸稀释时pH变化曲线,盐酸是强酸,抑制水的电离,氯化
铵水解促进水的电离,则c点溶液中水的电离程度最大,溶液越稀越电离,故d点大于b点,
C项错误;离子积常数只与温度有关,D项错误。]
7.(2021·山西太原检测)实验室现有以下4种溶液,下列有关说法不正确的是(均在室温
下)
溶液 ① ② ③ ④
溶质 (NH )SO NH Cl AlCl CHCOONH
4 2 4 4 3 3 4
浓度 0.1 mol·L-1 0.01 mol·L-1 0.1 mol·L-1 0.1 mol·L-1
已知:室温下,0.1 mol·L-1 NH Cl溶液的pH=5。
4
A.溶液①中c(OH-)<1×10-9 mol·L-1
B.溶液②的pH<5,因为加水稀释后,促进水解平衡正向移动,c(H+)变大
C.溶液③的pH<5,且c(Cl-)>3c(Al3+)
D.若溶液④的pH=7,则电离常数:K(CHCOOH)=K(NH ·H O)
3 3 2
B [0.1 mol·L-1(NH )SO 、NH Cl溶液中c(NH)分别约为0.2 mol·L-1、0.1 mol·L-1,
4 2 4 4
c(NH)越大,其水解产生c(H+)越大,则0.1 mol·L-1(NH )SO 溶液的pH<5,c(OH-)<1×10-9
4 2 4
mol·L-1,A正确;加水稀释,促进NH的水解平衡正向移动,但c(H+)减小,溶液的pH>5,B
错误;NH ·H O的碱性强于Al(OH) ,等浓度时Al3+的水解程度大于NH,则溶液③的pH<5,
3 2 3
溶液中c(H+)>c(OH-),结合电荷守恒可得c(Cl-)>3c(Al3+),C正确;CHCOONH 溶液的pH
3 4=7,说明CHCOO-和NH的水解程度相同,则电离常数:
3
K(CHCOOH)=K(NH ·HO),D正确。]
3 3 2
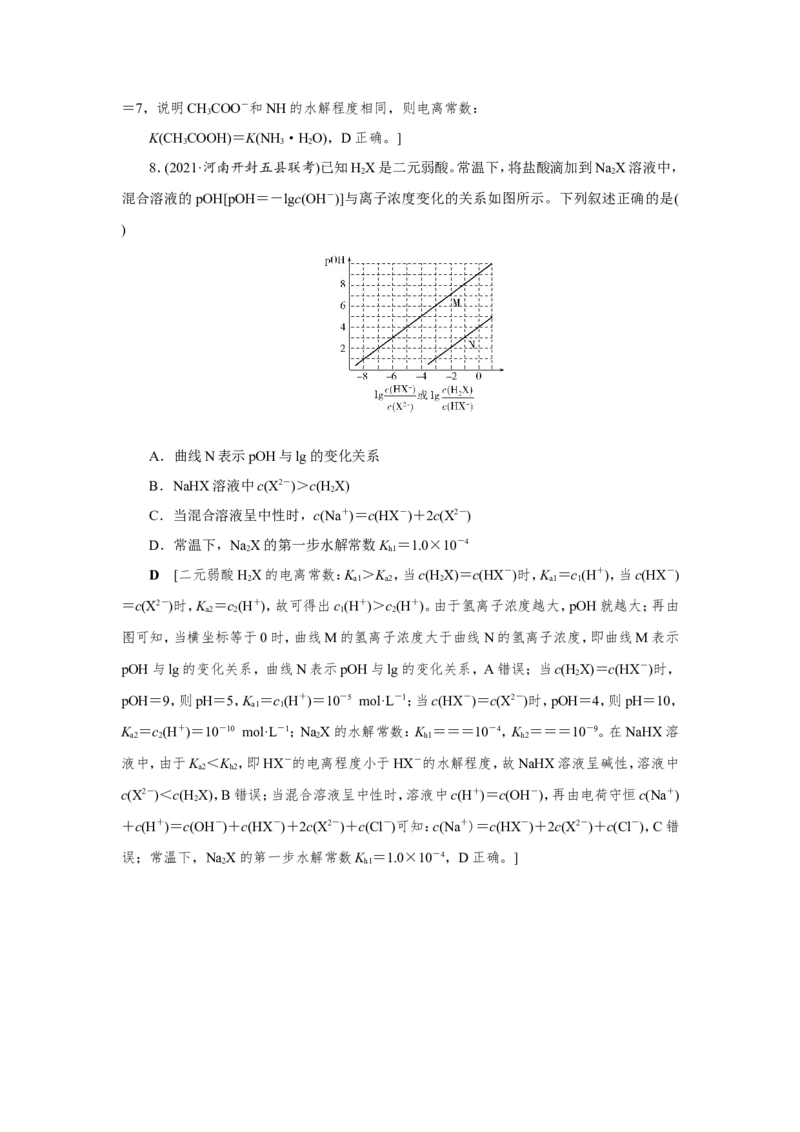
8.(2021·河南开封五县联考)已知HX是二元弱酸。常温下,将盐酸滴加到NaX溶液中,
2 2
混合溶液的pOH[pOH=-lgc(OH-)]与离子浓度变化的关系如图所示。下列叙述正确的是(
)
A.曲线N表示pOH与lg的变化关系
B.NaHX溶液中c(X2-)>c(H X)
2
C.当混合溶液呈中性时,c(Na+)=c(HX-)+2c(X2-)
D.常温下,NaX的第一步水解常数K =1.0×10-4
2 h1
D [二元弱酸HX的电离常数:K >K ,当c(H X)=c(HX-)时,K =c(H+),当c(HX-)
2 a1 a2 2 a1 1
=c(X2-)时,K =c(H+),故可得出c(H+)>c(H+)。由于氢离子浓度越大,pOH就越大;再由
a2 2 1 2
图可知,当横坐标等于0时,曲线M的氢离子浓度大于曲线N的氢离子浓度,即曲线M表示
pOH与lg的变化关系,曲线N表示pOH与lg的变化关系,A错误;当c(H X)=c(HX-)时,
2
pOH=9,则pH=5,K =c(H+)=10-5 mol·L-1;当c(HX-)=c(X2-)时,pOH=4,则pH=10,
a1 1
K =c(H+)=10-10 mol·L-1;NaX的水解常数:K ===10-4,K ===10-9。在NaHX溶
a2 2 2 h1 h2
液中,由于K <K ,即HX-的电离程度小于HX-的水解程度,故NaHX溶液呈碱性,溶液中
a2 h2
c(X2-)<c(H X),B错误;当混合溶液呈中性时,溶液中c(H+)=c(OH-),再由电荷守恒c(Na+)
2
+c(H+)=c(OH-)+c(HX-)+2c(X2-)+c(Cl-)可知:c(Na+)=c(HX-)+2c(X2-)+c(Cl-),C错
误;常温下,NaX的第一步水解常数K =1.0×10-4,D正确。]
2 h1