文档内容
1.元素周期表完美地将元素的结构、位置与性质结合在一起,根据元素的原子序数就能推
断出该元素在周期表中的位置,进而推断出该元素原子的结构和性质。下列关于 33号元素
的说法正确的是( )
A.该元素位于d区
B.该元素为金属元素
C.该元素位于第四周期第ⅢA族
D.该元素基态原子的电子排布式为1s22s22p63s23p63d104s24p3
2.下列说法正确的是( )
A.HF、HCl、HS、PH 的稳定性依次增强
2 3
B.在①P、S,②Mg、Ca,③Al、Si三组元素中,每组中第一电离能较大的元素的原子序
数之和为41
C.某主族元素的电离能I ~I 数据如表所示(单位:kJ·mol-1),可推测该元素位于元素周期
1 7
表第ⅤA族
I I I I I I I
1 2 3 4 5 6 7
578 1 817 2 745 11 575 14 830 18 376 23 293
D.原子半径由小到大的顺序:Mg、Si、N、F
3.(2022·安徽淮北模拟)铍元素与铝元素的单质及其化合物的性质相似。下列说法错误的是(
)
A.Be溶于NaOH溶液生成H
2
B.BeO、Be(OH) 均难溶于水
2
C.BeCl 与过量的NaOH溶液反应生成Be(OH)
2 2
D.BeSO 溶液呈酸性
4
4.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的
是( )
A.W、Y对应的简单氢化物的稳定性前者高
B.阴离子的还原性:W2->Q-C.离子半径:Y2->Z3+
D.元素的非金属性:Y>W
5.四种基态原子的价层电子排布式如下:
基态原子 X Y Z R
价层电子排布式 2s22p1 3s23p1 2s22p4 2s22p3
下列有关推断正确的是( )
A.原子半径:Y>R>Z>X
B.第一电离能:YR>X>Y
D.X的最高价氧化物对应水化物的酸性比R的强
6.(2022·烟台模拟)某种具有高效率电子传输性能的有机发光材料的结构简式如图所示。下
列关于该材料组成元素的说法错误的是( )
A.五种组成元素中有四种元素位于p区且均位于同一周期
B.原子半径:Al>C>N>O>H
C.气态氢化物的稳定性:HO>NH >CH
2 3 4
D.基态N原子核外有7种运动状态不同的电子
7.类推是一种重要的学习方法,但如果不具体问题具体分析就会得出错误结论。下列类推
结论正确的是( )
A.SiH 的熔、沸点比CH 高,则PH 的熔、沸点比NH 高
4 4 3 3
B.HO比NH 稳定,则HS也比NH 稳定
2 3 2 3
C.F 在暗处遇H 即爆炸,I 在暗处遇H 也爆炸
2 2 2 2
D.同族元素有Ca(OH) 的碱性强于Mg(OH) ,Pb(OH) 的碱性也应强于Sn(OH)
2 2 4 4
8.已知X、Y是短周期的两种主族元素,下列有关比较或说法中一定正确的是( )
选项 条件 结论
A 若原子半径:X>Y 原子序数:XY
n m
C 若价层电子数:X>Y 最高正价:X>Y
D 若X、Y最外层电子数分别为1、7 X、Y之间一定能形成离子键
9.我国科研人员发现了一种安全、高效的点击化学试剂FSO N ,下列有关元素F、O、N的
2 3
说法正确的是( )
A.电负性:F>N>O>S
B.第一电离能:F>S>O>NC.最高正价:F>S=O>N
D.以上物质涉及元素的原子中,N原子的基态原子核外未成对电子数最多
10.根据下表中五种元素的电离能数据(单位:kJ·mol-1),下列说法不正确的是( )
电离能
I I I I
1 2 3 4
元素代号
Q 2 080 4 000 6 100 9 400
R 500 4 600 6 900 9 500
S 740 1 500 7 700 10 500
T 580 1 800 2 700 11 600
U 420 3 100 4 400 5 900
A.T的氯化物最可能的化学式为TCl
3
B.氦元素最有可能与Q元素位于同一族
C.在周期表中,最可能处于同一族的是R和U
D.U元素最有可能为K,R元素最有可能为Li
11.下列有关元素性质的说法不正确的是( )
A.具有下列价层电子排布式的原子中,①3s23p1
②3s23p2 ③3s23p3 ④3s23p4,电负性最大的是③
B.某主族元素气态基态原子的逐级电离能(kJ·mol-1)分别为738、1 451、7 733、10 540、13
630、17 995、21 703,当它与氯气反应时可能生成的阳离子是X2+
C.①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的第一电离能随原子
序数增大而递增的是④
D.具有下列电子排布式的原子中, ① 1s22s22p63s23p2 ② 1s22s22p3 ③ 1s22s22p2
④1s22s22p63s23p4,原子半径最大的是①
12.一种新型漂白剂(结构如下图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族
的短周期元素,Z原子的核外电子排布式为1s1,W、Y、Z的最外层电子数之和等于X的最
外层电子数,X基态原子核外有两个单电子,W、X对应的简单离子核外电子排布相同。
回答下列问题:
(1)写出元素X在周期表中的位置:__________________________。
(2)写出W简单离子的核外电子排布式:______________________________________。
(3)Y元素基态原子核外电子的运动状态有______种,占据的原子轨道有________个。
(4)W、X、Y电负性由大到小的顺序是________________(用元素符号表示)。
(5)试解释W的第一电离能大于Al的第一电离能的原因:_____________________
________________________________________________________________________。
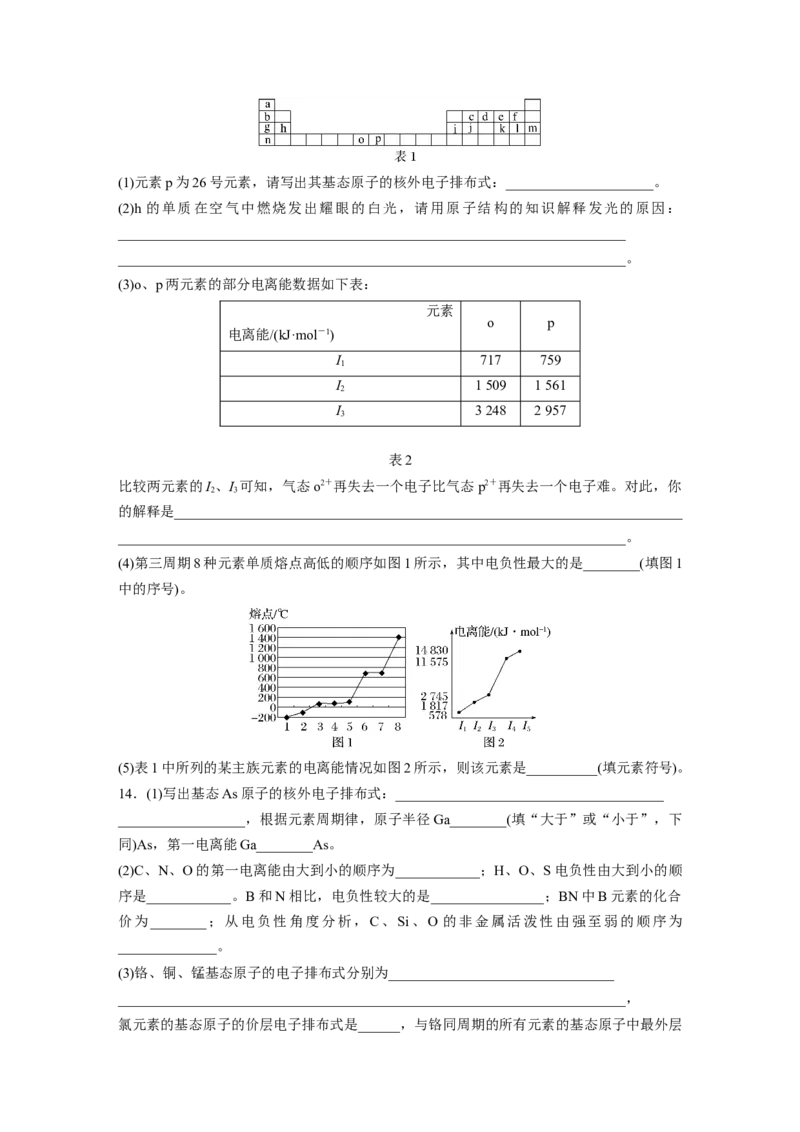
13.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:(1)元素p为26号元素,请写出其基态原子的核外电子排布式:_____________________。
(2)h 的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
________________________________________________________________________
________________________________________________________________________。
(3)o、p两元素的部分电离能数据如下表:
元素
o p
电离能/(kJ·mol-1)
I 717 759
1
I 1 509 1 561
2
I 3 248 2 957
3
表2
比较两元素的I 、I 可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你
2 3
的解释是________________________________________________________________________
________________________________________________________________________。
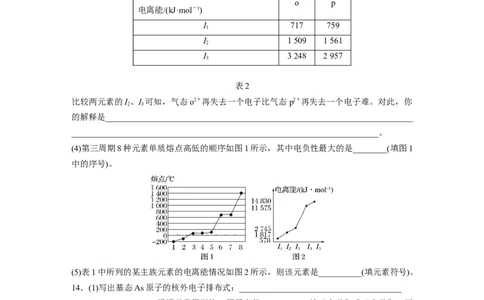
(4)第三周期8种元素单质熔点高低的顺序如图1所示,其中电负性最大的是________(填图1
中的序号)。
(5)表1中所列的某主族元素的电离能情况如图2所示,则该元素是__________(填元素符号)。
14.(1)写出基态As原子的核外电子排布式:______________________________________
__________________,根据元素周期律,原子半径Ga________(填“大于”或“小于”,下
同)As,第一电离能Ga________As。
(2)C、N、O的第一电离能由大到小的顺序为____________;H、O、S电负性由大到小的顺
序是____________。B和N相比,电负性较大的是________________;BN中B元素的化合
价为________;从电负性角度分析,C、Si、O 的非金属活泼性由强至弱的顺序为
______________。
(3)铬、铜、锰基态原子的电子排布式分别为________________________________
________________________________________________________________________,
氯元素的基态原子的价层电子排布式是______,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有__________(填元素符号)。
(4)基态 Fe3+的 M 层电子排布式为________,基态铝原子核外自旋平行的电子最多有
________个,与铝同族的第四周期元素原子的价层电子排布式为____________,基态磷原子
的核外电子运动状态共有__________种,其价层电子排布式为__________。在硼、氧、氟、
氮中第一电离能由大到小的顺序是______________________(用元素符号表示)。
(5)C、N、O、Al、Si、Cu是常见的六种元素。
①Si位于元素周期表第______周期______族。
②N的基态原子核外电子排布式为__________________________________________,
Cu的基态原子最外层有________个电子。
③用“>”或“<”填空:
原子半径 熔点 沸点
Al____Si 金刚石____晶体硅 CH____SiH
4 4
(6)O、Na、P、Cl四种元素中电负性最大的是______(填元素符号),其中P原子的核外电子
排布式为________________。
(7)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期
数相同,b的价层电子中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d
与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的
是______________(填元素符号),e的价层电子的轨道表示式为_________________________
________________________________________________________________________。