文档内容
第 31 讲 元素周期表、元素的性质
[复习目标] 1.掌握元素周期表的编排原则和整体结构。2.掌握元素周期律的内容和本质。3.
掌握元素的原子半径、金属性、非金属性、第一电离能、电负性等的变化规律。
考点一 元素周期表的结构与价层电子排布
1.元素周期表的编排原则
(1)周期:把____________相同的元素,按________________的顺序从左到右排成的横行。
(2)族:把不同横行中__________相同的元素,按__________的顺序从上而下排成的纵列。
2.原子结构与元素周期表的关系
(1)原子结构与周期的关系
原子的最大能层数=周期序数。
(2)原子结构与族的关系
①主族元素的价层电子排布特点
主族 ⅠA ⅡA ⅢA ⅣA
排布特点
主族 ⅤA ⅥA ⅦA
排布特点
②0族元素的价层电子排布:He为1s2;其他为ns2np6。
③过渡元素(镧系、锕系元素除外)的价层电子排布:(n-1)d1~10ns1~2。
(3)原子结构与元素周期表分区的关系
①元素周期表分区②各区价层电子排布特点
分区 价层电子排布
s区 ns1~2
p区 ns2np1~6(除He外)
d区 (n-1)d1~9ns1~2(除钯外)
ds区 (n-1)d10ns1~2
f区 (n-2)f0~14(n-1)d0~2ns2
(4)金属与非金属的分界线
①分界线:沿着元素周期表中______________与________________的交界处画一条虚线,即
为金属元素区和非金属元素区的分界线。
②各区位置:分界线左下方为____________,分界线右上方为____________。
③分界线附近元素的性质:既能表现出一定的________,又能表现出一定的________。
3.元素周期表应用
(1)科学预测:为新元素的发现及预测它们的原子结构和性质提供了线索。
(2)寻找新材料
1.所有非金属元素都分布在p区( )
2.价层电子排布式为4s24p3的元素位于第四周期第ⅤA族,是p区元素( )
3.价层电子排布式为5s25p1的元素位于第五周期第ⅠA族,是s区元素( )
4.最外层有2个未成对电子的可能是ns2np2或ns2np4,短周期元素中分别为C、Si和O、S(
)
一、元素周期表的结构
1.请在下表中画出元素周期表的轮廓,并在表中按要求完成下列问题:(1)标出族序数、周期序数。
(2)将主族元素前六周期的元素符号补充完整。
(3)画出金属与非金属的分界线,并用阴影表示出过渡元素的位置。
(4)标出镧系、锕系的位置。
(5)写出各周期元素的种类。
(6)写出稀有气体元素的原子序数,标出113号~117号元素的位置。
二、元素周期表的应用
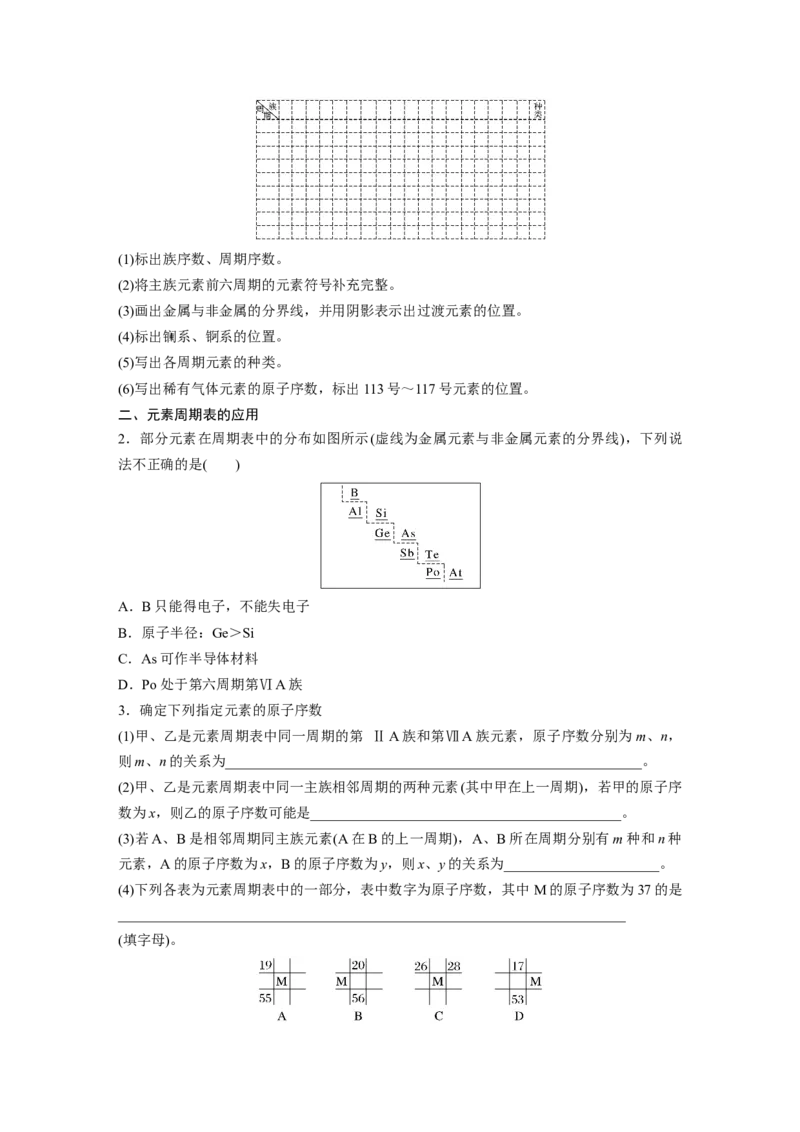
2.部分元素在周期表中的分布如图所示(虚线为金属元素与非金属元素的分界线),下列说
法不正确的是( )
A.B只能得电子,不能失电子
B.原子半径:Ge>Si
C.As可作半导体材料
D.Po处于第六周期第ⅥA族
3.确定下列指定元素的原子序数
(1)甲、乙是元素周期表中同一周期的第 ⅡA族和第ⅦA族元素,原子序数分别为m、n,
则m、n的关系为___________________________________________________________。
(2)甲、乙是元素周期表中同一主族相邻周期的两种元素(其中甲在上一周期),若甲的原子序
数为x,则乙的原子序数可能是____________________________________________。
(3)若A、B是相邻周期同主族元素(A在B的上一周期),A、B所在周期分别有m种和n种
元素,A的原子序数为x,B的原子序数为y,则x、y的关系为______________________。
(4)下列各表为元素周期表中的一部分,表中数字为原子序数,其中 M的原子序数为37的是
________________________________________________________________________
(填字母)。元素周期表中原子序数差的关系
(1)同周期主族元素原子序数差的关系
①短周期元素原子序数差=族序数差。
②长周期元素,两元素分布在过渡元素同侧时,原子序数差=族序数差;两元素分布在过渡
元素两侧时,第四或五周期元素:原子序数差=族序数差+10,第六或七周期元素:原子序
数差=族序数差+24。
(2)同主族、邻周期元素原子序数差的关系
①第ⅠA族元素,随电子层数的增加,原子序数依次相差2、8、8、18、18、32。
②第 ⅡA族元素,随电子层数的增加,原子序数依次相差8、8、18、18、32。
③第 ⅢA~ⅦA族元素,随电子层数的增加,原子序数依次相差8、18、18、32、32。
④0族元素,随电子层数的增加,原子序数依次相差8、8、18、18、32、32。
考点二 元素周期律 电离能、电负性
1.元素周期律
2.主族元素周期性变化规律
项目 同周期(从左到右) 同主族(从上到下)
电子层数
原子结构 最外层电
依次增加
子数
原子半径
金属性
非金属性
元素性质
最高正化合价:+1→+ 相同,最高正化合价=
化合价
7(O、F除外),负化合价=
____________(O、F除外)______(H为-1价)
最高价氧
化物对应 酸性____________, 酸性__________,
水化物的 碱性____________ 碱性__________
化合物性质 酸碱性
简单气态
氢化物的
稳定性
3.电离能
(1)含义
第一电离能:气态基态原子失去一个电子转化为气态基态正离子所需要的____________,符
号:____,单位:______。
(2)规律
①同周期元素:从左往右,元素第一电离能呈______的趋势,其中第ⅡA族、第ⅤA族元
素的第一电离能出现反常。
②同族元素:从上到下第一电离能逐渐______。
③同种原子:逐级电离能越来越大。
(3)应用
①判断元素金属性的强弱
电离能越小,金属越容易失去电子,金属性越强;反之金属性越弱。
②判断元素的化合价
如果某元素的I
n+1
≫I
n
,则该元素的常见化合价为+n,如钠元素的I
2
≫I
1
,所以钠元素的化
合价为+1。
③判断核外电子的分层排布情况
多电子原子中,元素的各级电离能逐渐增大,有一定的规律性。当电离能的变化出现突变时,
电子层数就可能发生变化。
4.电负性
(1)含义
不同元素的原子____________________的标度。元素的电负性越大,表示其原子对键合电子
的吸引力________。
(2)标准
以氟的电负性为____和锂的电负性为1.0作为相对标准,计算得出其他元素的电负性(稀有气
体元素未计)。
(3)变化规律
①在元素周期表中,同周期元素从左至右,元素的电负性逐渐________,同主族元素从上至
下,元素的电负性逐渐________。②金属元素的电负性一般________,非金属元素的电负性一般________,而位于非金属三角
区边界的“类金属”(如锗、锑等)的电负性则在1.8左右,它们既有金属性又有非金属性。
(4)应用
5.定性判断金属性、非金属性的一般方法
①单质与水或非氧化性酸反应制取氢气越容易,金属性越强
金属性 ②单质还原性越强或阳离子氧化性越弱,金属性越强
③最高价氧化物对应水化物的碱性越强,金属性越强
①与H 化合越容易,气态氢化物越稳定,非金属性越强
2
非金属性 ②单质氧化性越强或阴离子还原性越弱,非金属性越强
③最高价氧化物对应水化物的酸性越强,非金属性越强
1.元素的电负性越大,非金属性越强,第一电离能也越大( )
2.元素的氧化物对应的水化物酸性越强,非金属性越强,碱性越强,金属性越强( )
3.元素的气态氢化物越稳定,非金属性越强,其水溶液的酸性越强,还原性越弱( )
4.元素的原子得电子越多,非金属性越强,失电子越多,金属性越强( )
5.同周期元素,从左到右,原子半径逐渐减小,离子半径也逐渐减小( )
一、微粒半径、元素金属性和非金属性比较
1.比较下列微粒半径的大小(用“>”或“<”填空):
(1)Si________N________F。
(2)Li________Na________K。
(3)Na+________Mg2+________Al3+。
(4)F-________Cl-________Br-。(5)Cl-________O2-________Na+。
(6)H-________Li+________H+。
2.根据元素周期律比较下列各组性质(用“>”或“<”填空):
(1)金属性:K________Na________Mg;
非金属性:F________O________S。
(2)碱性:Mg(OH) ________Ca(OH) __________________________________KOH。
2 2
(3)酸性:HClO________HSO ________HClO。
4 2 4
(4)热稳定性:CH________NH ________HO。
4 3 2
(5)还原性:HBr________HCl,I-________S2-。
(6)氧化性:Fe3+________Cu2+________Fe2+。
3.A、B、C为三种短周期元素,A、B同周期,A、C的最低价离子分别为A2-、C-,B2+
与C-具有相同的电子层结构,下列叙述不正确的是( )
A.原子序数:A>B>C
B.原子半径:C>B>A
C.离子半径:A2->C->B2+
D.原子最外层电子数:C>A>B
电子层结构相同的微粒半径大小规律
电子层结构相同(核外电子排布相同)的离子半径(包括阴、阳离子)随核电荷数的增加而减小,
如O2->F->Na+>Mg2+>Al3+。可归纳为电子层排布相同的离子,(表中位置)阴离子在阳离子
前一周期,原子序数大的半径小,概括为“阴前阳下,序大径小”。
二、“10e-”“18e-”微粒的应用
4.A+、B+、C-、D、E五种粒子(分子或离子)中,每个粒子均有10个电子,已知:
①A++C-===D+E↑;②B++C-===2D。
回答下列问题:
(1)C-的电子式是____________。
(2)分别写出A+和D反应、B+和E反应的离子方程式: _______________________、
________________________________________________________________________。
(3)除D、E外,请再写出两种含10个电子的分子的分子式:______________________。
(4)除A+、B+外,请再写出两种含10个电子的阳离子:________________________。
等电子微粒的判断方法
(1)“10电子”微粒:(2)“18电子”微粒:
三、电离能、电负性的变化规律及应用
5.下表列出了某短周期元素R的各级电离能数据(用I、I……表示,单位为kJ·mol-1)。
1 2
I I I I ……
1 2 3 4
R 740 1 500 7 700 10 500
下列关于元素R的判断中一定正确的是( )
A.R的最高正价为+3价
B.R元素位于元素周期表中第ⅡB族
C.R元素第一电离能大于同周期相邻元素
D.R元素基态原子的电子排布式为1s22s2
6.(1)C、N、O、S四种元素中,第一电离能最大的是__________________。
(2)观察下面四种镧系元素的电离能数据,判断最有可能显示+3价的元素是________(填元
素名称)。
几种镧系元素的电离能(单位:kJ·mol-1)
元素 I I I I
1 2 3 4
Yb(镱) 604 1 217 4 494 5 014
Lu(镥) 532 1 390 4 111 4 987
La(镧) 538 1 067 1 850 5 419
Ce(铈) 527 1 047 1 949 3 547
7.根据信息回答下列问题:
不同元素的原子在分子内吸引电子的能力大小可用数值表示,该数值称为电负性。一般认为:
如果两个成键原子间的电负性差值大于1.7,原子之间通常形成离子键;如果两个成键原子
间的电负性差值小于1.7,通常形成共价键。下表是某些元素的电负性值:元素
Li Be B C O F Na Al Si P S Cl
符号
电负
1.0 1.5 2.0 2.5 3.5 4.0 0.9 1.5 1.8 2.1 2.5 3.0
性值
(1)通过分析电负性值的变化规律,确定Mg元素的电负性值的最小范围:________________。
(2)请归纳元素的电负性和金属性、非金属性的关系: __________________________。
(3)推测AlF、AlCl 、AlBr 是离子化合物还是共价化合物:
3 3 3
AlF__________________,AlCl _________________________________________,
3 3
AlBr ________________。
3
答题规范(3) 电离能规范答题的两个类型
1.电离能与原子结构
答题策略:从原子核对最外层电子的吸引力来判断。
答题模板:A原子比B原子的半径大,且A原子的核电荷数比B原子的小,所以A原子对
最外层电子的吸引力小于B, 故第一电离能A小于B。
2.电离能与半充满、全充满
答题策略:能量相同的原子轨道在全充满(p6、d10、f14)、半充满(p3、d5、f7)时,比较稳定,
难失电子。
答题模板:A原子的价层电子排布式为×××,处于半充满(全充满),比较稳定,难失电子,
×××电离能大。
1.请结合核外电子排布相关知识解释,第一电离能: C 小于 O,原因是:
_________________
________________________________________________________________________
________________________________________________________________________。
2.(1)第一电离能N大于O,原因是: _____________________________________
________________________________________________________________________。
(2)已知电离能:I(Ti)=1 310 kJ·mol-1,I(K)=3 051 kJ·mol-1。I(Ti)
1 1
I(Na),原因是_________________________________________________________。
1
I(Be)> I(B)> I(Li),原因是_______________________________________________
1 1 1
________________________________________________________________________。
I/(kJ·mol-1)
1
Li Be B
520 900 801
Na Mg Al
496 738 578
(2)[2018·全国卷Ⅲ,35(2)]黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电
离能I(Zn)________(填“大于”或“小于”)I(Cu)。原因是____________________
1 1
________________________________________________________________________。
(3)[2016·全国卷Ⅱ,37(3)节选]元素铜与镍的第二电离能分别为I =1 958 kJ·mol-1,I =1 753
Cu Ni
kJ·
mol-1,I >I 的原因是________________________________________________
Cu Ni
________________________________________________________________________。
(4)[2016·全国卷Ⅲ,37(2)]根据元素周期律,原子半径 Ga________As,第一电离能Ga__________(填“大于”或“小于”)As。
5.(1)[2022·山东,16(1)]基态Ni原子的价层电子排布式为________,在元素周期表中位置
为________。
(2)[2022·河北,17(1)(2)]①基态S原子的价电子中,两种自旋状态的电子数之比为________。
②Cu 与 Zn 相比,第二电离能与第一电离能差值更大的是 ________,原因是
________________________________________________________________________
________________________________________________________________________。
(3)[2022·全国甲卷,35(1)(2)]① 基态 F 原子的价层电子排布图(轨道表示式)为
________________________________________________________________________。
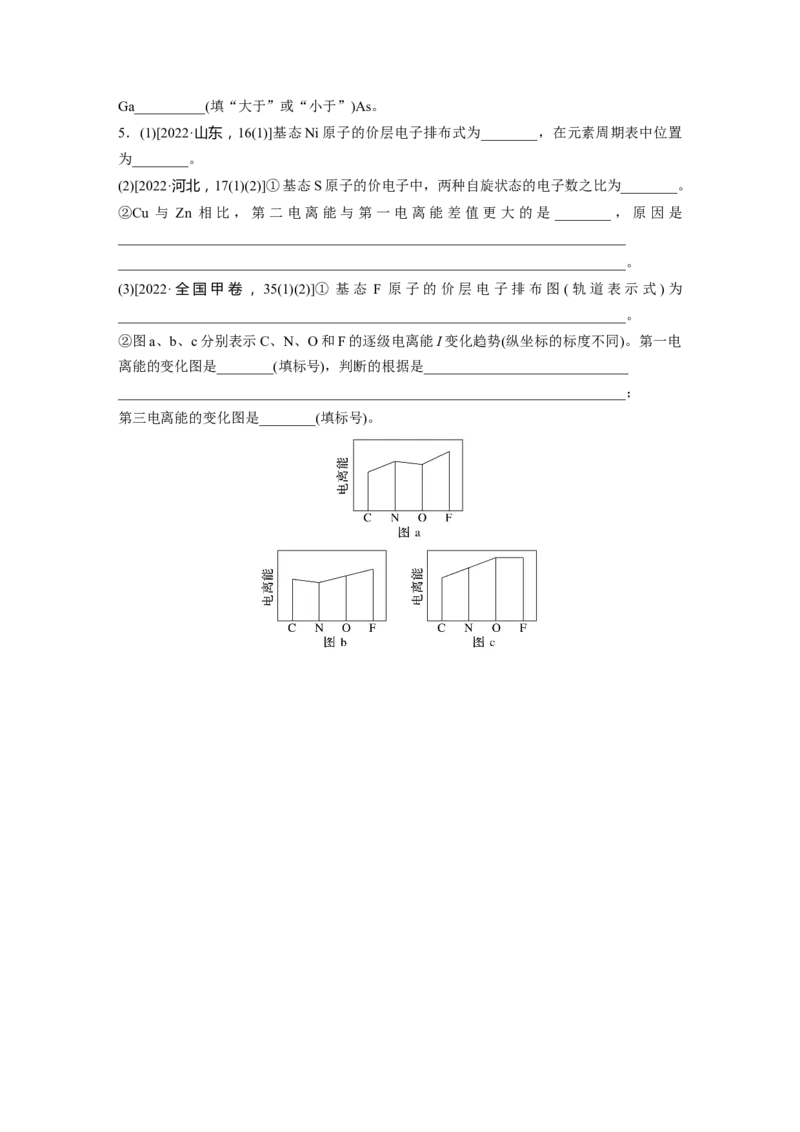
②图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电
离能的变化图是________(填标号),判断的根据是_____________________________
________________________________________________________________________;
第三电离能的变化图是________(填标号)。