文档内容
训练(四十三) 难溶电解质的溶解平衡
1.(2021·湖南长沙一中检测)下列有关沉淀溶解平衡的说法正确的是( )
A.K (AB )小于K (CD),说明AB 的溶解度小于CD的溶解度
sp 2 sp 2
B.在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的K 增大
sp
C.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡不移动
D.已知25 ℃时,K (AgCl)大于K (AgI),若向氯化银沉淀溶解平衡体系中,加入足量碘
sp sp
化钾固体,则有黄色沉淀生成
D [K (AB )小于K (CD),二者的表达形式不同,不能据此比较二者的溶解度,则AB
sp 2 sp 2
的溶解度不一定小于CD,A错误;AgCl的沉淀溶解平衡中,加入蒸馏水,K (AgCl)不变,B
sp
错误;CaCO 的沉淀溶解平衡中,加入稀盐酸,CO与H+反应生成CO,平衡正向移动,C错
3 2
误;25 ℃时,K (AgCl)大于 K (AgI),AgCl平衡体系中,加入足量KI固体,Ag+与I-结合生
sp sp
成溶解度更小的AgI,故有黄色沉淀生成,D正确。]
2.(2021·华中师大附中检测)下列有关溶度积常数K 的说法正确的是( )
sp
A.常温下,向Mg(OH) 饱和溶液中加入NaOH固体,Mg(OH) 的溶解度变小
2 2
B.溶度积常数越大,溶解度也越大
C.溶度积K 只受温度影响,温度升高,K 增大
sp sp
D.常温下,向Cl-和Br-共存的溶液中,滴加AgNO 溶液,最先生成的沉淀是AgBr
3
A [加入NaOH固体,Mg(OH) 的溶解平衡逆向移动,其溶解度变小,A正确;若溶度积
2
表达形式不同,K 数值大,其溶解度不一定大,B错误;影响K 大小的主要因素是难溶电解
sp sp
质的性质,对于同一物质,其K 只受温度影响,温度升高,K 增大,C错误;Cl-和Br-共存的
sp sp
溶液中滴加AgNO 溶液,先沉淀Cl-还是Br-与其浓度有关,只有满足Q>K 才产生沉淀,D
3 sp
错误。]
3.(2021·辽宁抚顺六校联考)化工生产中常用MnS作为沉淀剂除去工业废除水中Cu2+:
Cu2+(aq)+MnS(s) CuS(s)+Mn2+(aq),下列说法错误的是( )
A.MnS的K 比CuS的K 大
sp sp
B.该反应达平衡时c(Mn2+)=c(Cu2+)
C.往平衡体系中加入少量CuSO 固体后,c(Mn2+)变大
4
D.该反应的平衡常数K=
B [含Cu2+废水中加入MnS固体,MnS转化为更难溶的CuS,则有MnS的K 比CuS
sp的K 大,A正确;该反应达到平衡时,c(Mn2+)、c(Cu2+)均不变,但不一定相等,当二者相等时,
sp
不一定处于平衡状态,B错误;往平衡体系中加入少量CuSO 固体,c(Cu2+)增大,平衡正向移
4
动,则c(Mn2+)增大,C正确;该反应的平衡常数为K= =,D正确。]
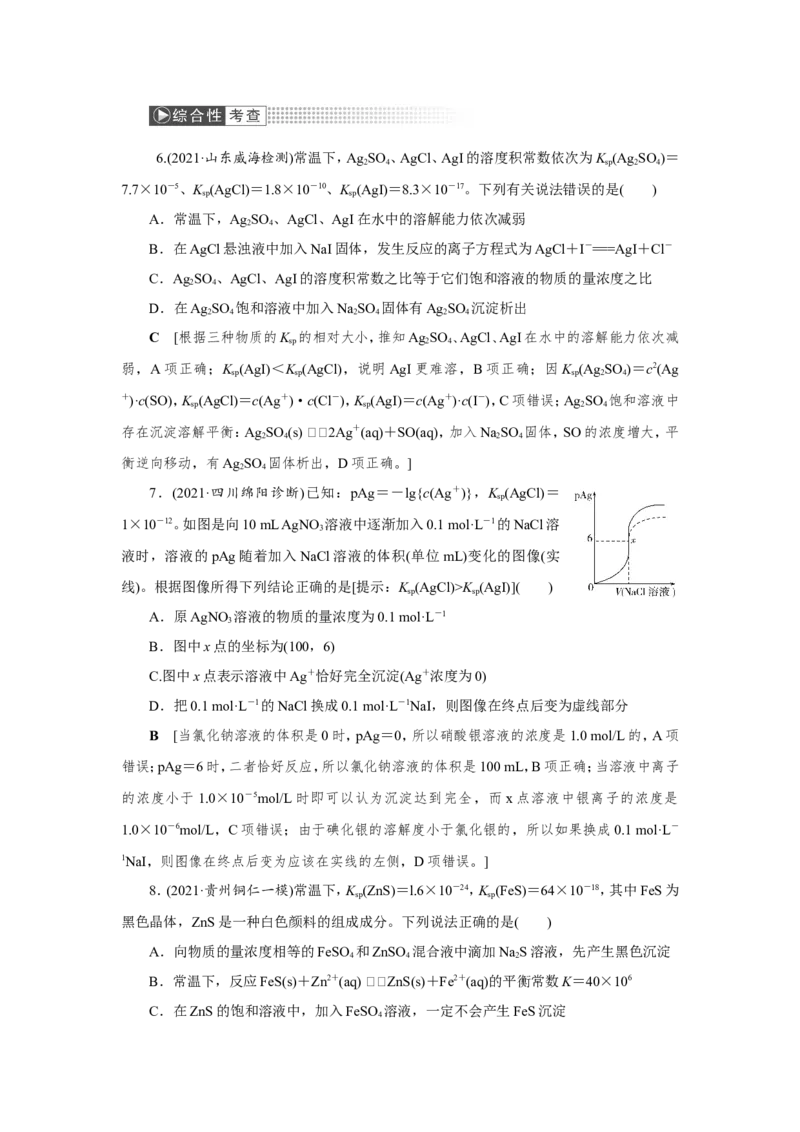
4.(2021·辽宁锦州检测)探究Mg(OH) 的溶解平衡时,利用下表三种试剂进行实验,下列
2
说法中不正确的是( )
编号 ① ② ③
分散质 Mg(OH) HCl NH Cl
2 4
备注 悬浊液 1 mol·L-1 1 mol·L-1
A.向①中滴加几滴酚酞试液后,溶液显红色,说明Mg(OH) 是一种弱电解质
2
B.为了使Mg(OH) 悬浊液溶解得更快,加入过量NH Cl浓溶液并充分振荡,效果更好
2 4
C.①、③混合后发生反应:Mg(OH) (s)+2NH(aq) Mg2+(aq)+2NH ·H O(aq)
2 3 2
D.向①中加入②,H+与OH-反应生成HO,使c(OH-)减小,Mg(OH) (s)的溶解平衡向
2 2
溶解方向移动
A [A.向①中滴入几滴酚酞试液后,溶液显红色,说明Mg(OH) 发生电离,但无法确定
2
电离程度,无法判断其是否为弱电解质,故A项错误;B.NHCl溶液中的NH与Mg(OH) 电
4 2
离的OH-结合生成NH ·HO,使Mg(OH) 悬浊液溶解得更快,B正确;①、③混合后,OH-
3 2 2
与NH生成NH ·HO,发生反应:Mg(OH) (s)+2NH(aq) Mg2+(aq)+2NH ·HO(aq),C
3 2 2 3 2
正确;Mg(OH) 悬浊液中加入 HCl 溶液,H+与 OH-反应生成 HO,使 c(OH-)减小,
2 2
Mg(OH) (s)的溶解平衡向溶解方向移动,D正确。]
2
5.(2021·吉林白城检测)已知:25 ℃时,K (Ag S)=6.3×10-50,K (CuS)=6.3×10-36。下
sp 2 sp
列说法正确的是( )
A.若向饱和Ag S溶液中加入NaS固体,则有Ag S固体析出
2 2 2
B.反应Ag S(s)+Cu2+(aq) CuS(s)+2Ag+(aq)的平衡常数K=1×10-24
2
C.相同条件下,CuS在水中的溶解度大于Ag S在水中的溶解度
2
D.0.1 L溶液中含0.1 mol Ag S固体,则溶液中Ag S的物质的量浓度为1 mol·L-1
2 2
A [饱和Ag S溶液中加入NaS固体,c(S2-)增大,Q大于K (Ag S),析出Ag S固体,A
2 2 sp 2 2
正确;该反应的平衡常数为K====1×10-14,B错误;25 ℃时,Ag S、CuS饱和溶液中c(S2
2
-)分别约为2.5×10-17mol/L、2.5×10-18mol/L,故相同条件下,Ag S的溶解度大,C错误;0.1
2
L溶液中0.1 mol Ag S不能完全溶解,D错误。]
26.(2021·山东威海检测)常温下,Ag SO 、AgCl、AgI的溶度积常数依次为K (Ag SO )=
2 4 sp 2 4
7.7×10-5、K (AgCl)=1.8×10-10、K (AgI)=8.3×10-17。下列有关说法错误的是( )
sp sp
A.常温下,Ag SO 、AgCl、AgI在水中的溶解能力依次减弱
2 4
B.在AgCl悬浊液中加入NaI固体,发生反应的离子方程式为AgCl+I-===AgI+Cl-
C.Ag SO 、AgCl、AgI的溶度积常数之比等于它们饱和溶液的物质的量浓度之比
2 4
D.在Ag SO 饱和溶液中加入NaSO 固体有Ag SO 沉淀析出
2 4 2 4 2 4
C [根据三种物质的K 的相对大小,推知Ag SO 、AgCl、AgI在水中的溶解能力依次减
sp 2 4
弱,A项正确;K (AgI)<K (AgCl),说明AgI更难溶,B项正确;因K (Ag SO )=c2(Ag
sp sp sp 2 4
+)·c(SO),K (AgCl)=c(Ag+)·c(Cl-),K (AgI)=c(Ag+)·c(I-),C项错误;Ag SO 饱和溶液中
sp sp 2 4
存在沉淀溶解平衡:Ag SO (s) 2Ag+(aq)+SO(aq),加入NaSO 固体,SO的浓度增大,平
2 4 2 4
衡逆向移动,有Ag SO 固体析出,D项正确。]
2 4
7.(2021·四川绵阳诊断)已知:pAg=-lg{c(Ag+)},K (AgCl)=
sp
1×10-12。如图是向10 mL AgNO 溶液中逐渐加入0.1 mol·L-1的NaCl溶
3
液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图像(实
线)。根据图像所得下列结论正确的是[提示:K (AgCl)>K (AgI)]( )
sp sp
A.原AgNO 溶液的物质的量浓度为0.1 mol·L-1
3
B.图中x点的坐标为(100,6)
C.图中x点表示溶液中Ag+恰好完全沉淀(Ag+浓度为0)
D.把0.1 mol·L-1的NaCl换成0.1 mol·L-1NaI,则图像在终点后变为虚线部分
B [当氯化钠溶液的体积是0时,pAg=0,所以硝酸银溶液的浓度是1.0 mol/L的,A项
错误;pAg=6时,二者恰好反应,所以氯化钠溶液的体积是100 mL,B项正确;当溶液中离子
的浓度小于1.0×10-5mol/L时即可以认为沉淀达到完全,而x点溶液中银离子的浓度是
1.0×10-6mol/L,C项错误;由于碘化银的溶解度小于氯化银的,所以如果换成0.1 mol·L-
1NaI,则图像在终点后变为应该在实线的左侧,D项错误。]
8.(2021·贵州铜仁一模)常温下,K (ZnS)=l.6×10-24,K (FeS)=64×10-18,其中FeS为
sp sp
黑色晶体,ZnS是一种白色颜料的组成成分。下列说法正确的是( )
A.向物质的量浓度相等的FeSO 和ZnSO 混合液中滴加NaS溶液,先产生黑色沉淀
4 4 2
B.常温下,反应FeS(s)+Zn2+(aq) ZnS(s)+Fe2+(aq)的平衡常数K=40×106
C.在ZnS的饱和溶液中,加入FeSO 溶液,一定不会产生FeS沉淀
4D.向FeS悬浊液中通入少许HCl,c(Fe2+)与K (FeS)均增大
sp
B [由于K (ZnS)<K (FeS),则ZnS的溶解度小于FeS,等浓度的FeSO 和ZnSO 混合
sp sp 4 4
液中滴加NaS溶液,先产生ZnS白色沉淀,A项错误;反应FeS(s)+Zn2+(aq) ZnS(s)+Fe2
2
+(aq)的平衡常数K=c(Fe2+)/c(Zn2+)===4.0×l06,B项正确;在ZnS的饱和溶液中,加入
FeSO 溶液,若c(Fe2+)·c(S2-)>K (FeS),可以产生FeS沉淀,C项错误;FeS悬浊液中存在沉
4 sp
淀溶解平衡:FeS(s) Fe2+(aq)+S2-(aq),通入少许HCl,S2-结合H+生成HS气体,平衡正
2
向移动,c(Fe2+)增大,由于温度不变,K (FeS)不变,D项错误。]
sp
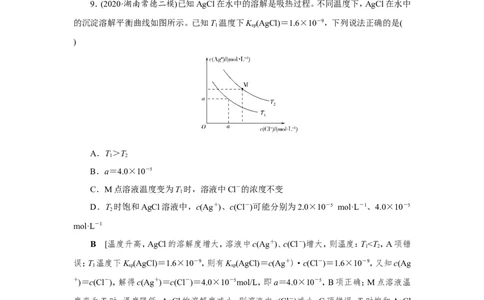
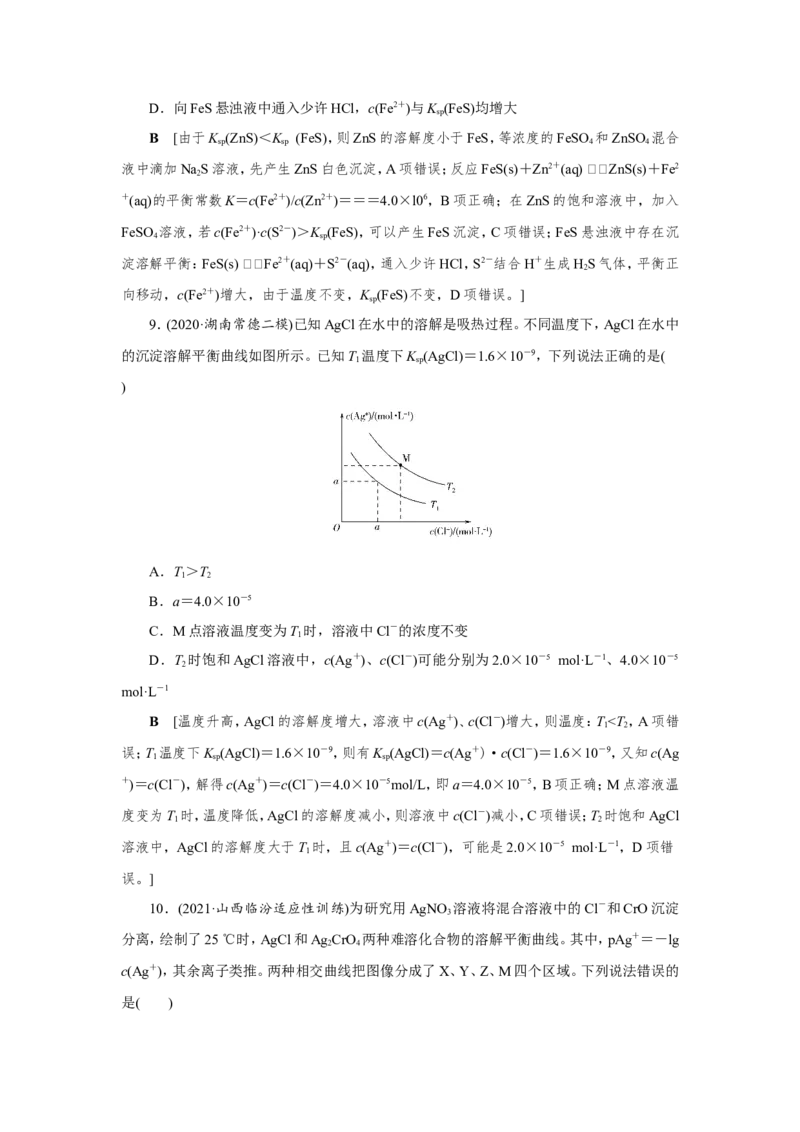
9.(2020·湖南常德二模)已知AgCl在水中的溶解是吸热过程。不同温度下,AgCl在水中
的沉淀溶解平衡曲线如图所示。已知T 温度下K (AgCl)=1.6×10-9,下列说法正确的是(
1 sp
)
A.T>T
1 2
B.a=4.0×10-5
C.M点溶液温度变为T 时,溶液中Cl-的浓度不变
1
D.T 时饱和AgCl溶液中,c(Ag+)、c(Cl-)可能分别为2.0×10-5 mol·L-1、4.0×10-5
2
mol·L-1
B [温度升高,AgCl的溶解度增大,溶液中c(Ag+)、c(Cl-)增大,则温度:T10.5,故d点
2
向f点迁移,C正确。在NiS和ZnS的浊液中,===104,D错误。]
12.(2021·山东聊城检测)钡餐造影是指用硫酸钡作为造影剂,在X线照射下显示消化道
有无病变的一种检查方法。用于消化道检查的钡餐是药用硫酸钡,即硫酸钡的悬浊液,存在
平衡BaSO(s) Ba2+(aq)+SO(aq),下列有关叙述正确的是( )
4
A.BaSO 难溶于水,外界条件改变不会影响BaSO 的溶解性
4 4
B.BaSO 达到沉淀溶解平衡时,再加入BaSO 固体,将促进溶解
4 4
C.若向BaSO 悬浊液中加入适量蒸馏水,平衡不发生移动
4
D.若加入适量饱和NaSO 溶液,K 保持不变,c(SO)增大
2 4 sp
D [升高温度,BaSO 的溶解度增大,A项错误;沉淀溶解达到平衡时,如果再加入难溶
4
性的该沉淀物,由于固体的浓度为常数,故平衡不发生移动,B项错误;加入少量水,c(Ba2+)、
c(SO)减小,沉淀溶解平衡正向移动,C项错误;加入适量NaSO 溶液,平衡逆向移动,但
2 4
c(SO)增大,K 保持不变,只受温度影响,D项正确。]
sp
13.(2021·湖南怀化检测)往锅炉注入 NaCO 溶液浸泡,将水垢中的 CaSO 转化为
2 3 4
CaCO ,再用盐酸去除,下列叙述中正确的是( )
3
A.温度升高,NaCO 溶液的K 和c(H+)均会增大
2 3 W
B.CaSO 能转化为CaCO ,说明K (CaCO)>K (CaSO)
4 3 sp 3 sp 4
C.CaCO 溶解于盐酸而CaSO 不溶,是因为硫酸酸性强于盐酸
3 4
D.沉淀转化的离子方程式为CO(aq)+CaSO(s) CaCO (s)+SO(aq)
4 3
D [温度升高,水的电离平衡正向移动,K 增大;温度升高,NaCO 的水解平衡正向移
W 2 3
动,c(OH-)增大,c(H+)减小,A项错误;K (CaCO)<K (CaSO),B项错误;CaCO 与盐酸反
sp 3 sp 4 3
应生成可溶性的氯化钙、水和二氧化碳,CaSO 与盐酸不满足复分解反应发生的条件,与酸性
4
强、弱无关,C项错误;硫酸钙较为致密,可转化为较为疏松且溶解度更小的碳酸钙,反应的
离子方程式为CaSO(s)+CO(aq) CaCO (s)+SO(aq),D项正确。]
4 3
14.(2021·湖南雅礼中学检测)草酸钴用途广泛,可用于指示剂和催化剂的制备。一种利
用水钴矿(主要成分为Co O,含少量Fe O、Al O、MnO、MgO、CaO等)制取CoC O·2H O的
2 3 2 3 2 3 2 4 2
工艺流程如下:已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Fe(OH) Fe(OH) Co(OH) Al(OH) Mn(OH)
3 2 2 3 2
完全沉淀的pH 3.7 9.6 9.2 5.2 9.8
(1)浸出过程中加入NaSO 的目的是__________________________________________。
2 3
(2)将氯气通入到热的浓氢氧化钠溶液可以来制取NaClO,请写出该反应的离子方程式:
3
______________________________________;实验需要制取10.65 g NaClO,需要的氯气由
3
电解食盐水生成,若不考虑反应过程中的损失,则同时生成的氢气的体积为
________________________________________________________________________
(标准状况下)。
(3)萃取剂对金属离子的萃取率与pH的关系如图所示。滤液Ⅱ中加入萃取剂的作用是
____________;使用萃取剂最适宜的pH是____________(填选项字母)。
A.接近2.0 B.接近3.0 C.接近5.0
(4)除“钙、镁”是将溶液中Ca2+与Mg2+转化为MgF 、CaF 沉淀。已知K (MgF )=
2 2 sp 2
7.35×10-11,K (CaF )=1.05×10-10。当加入过量NaF后,所得滤液中=________。
sp 2
(5)为测定制得的无水草酸钴样品的纯度,现称取样品m g,先用适当试剂将其转化,得
到纯净的草酸铵溶液,再用过量的稀硫酸酸化,用c mol·L-1高锰酸钾溶液去滴定,当溶液由
________________________________________________________________________
时(填颜色变化),共用去高锰酸钾溶液V mL,计算草酸钴样品的纯度为______________。
解析 (1)对比水钴矿的成分和浸出液中含有的阳离子,NaSO 具有还原性,能够将溶液
2 3
中的Co3+、Fe3+还原。(2)氯气在加热条件下和浓NaOH反应生成NaClO,发生反应的离子方
3
程式为 3Cl +6OH-=====ClO+5Cl-+3HO。电解食盐水的化学方程式为 2NaCl+
2 2
2HO=====2NaOH+H↑+Cl↑,可建立关系式:3H~3Cl~NaClO,可知标准状况下生成
2 2 2 2 2 3的H 的体积为×3×22.4 L·mol-1=6.72 L。(3)根据流程图,加入萃取剂的目的是除去Mn2+,
2
根据萃取率和pH的关系,当pH=3时,Mn2+萃取率高,Co2+萃取率低。(4)====0.7。(5)根
据得失电子数目守恒可得 n(C O)×2×1=V×10-3×c×5,解得 n(C O)=2.5×10-3×cV
2 2
mol,n(CoC O)=n(C O)=2.5×10-3×cV mol,纯度为×100%=×100%或%。
2 4 2
答案 (1)将Co3+、Fe3+还原 (2)3Cl +6OH-=====ClO+5Cl-+3HO 6.72 L
2 2
(3)除去Mn2+ B (4)0.7 (5)无色变为浅紫色(或紫红色),且半分钟内不变色 ×100%