文档内容
1.(2023·烟台模拟)中华传统文化中富含化学知识,下列叙述与氧化还原反应无关的是(
)
A.熬胆矾铁釡,久之亦化为铜
B.千锤万凿出深山,烈火焚烧若等闲
C.落红不是无情物,化作春泥更护花
D.有舶上铁丝日久起销
2.(2022·山东,1)古医典富载化学知识,下述之物见其氧化性者为( )
A.金(Au):“虽被火亦未熟”
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳(CaCO):“色黄,以苦酒(醋)洗刷则白”
3
3.(2023·广州调研)陈述Ⅰ和陈述Ⅱ均正确且具有因果关系的是( )
选项 陈述 Ⅰ 陈述 Ⅱ
A 用FeCl 溶液刻蚀铜质电路板 氧化性:Fe3+>Cu2+
3
B 用NaO 作呼吸面具的氧气来源 NaO 能氧化CO
2 2 2 2 2
C 用NaS除去废水中的Cu2+和Hg2+ NaS具有还原性
2 2
D 用石灰乳脱除烟气中的SO SO 具有氧化性
2 2
4.(2022·辽宁,6)镀锌铁钉放入棕色的碘水中,溶液褪色;取出铁钉后加入少量漂白粉,溶
液恢复棕色;加入CCl ,振荡,静置,液体分层。下列说法正确的是( )
4
A.褪色原因为I 被Fe还原
2
B.液体分层后,上层呈紫红色
C.镀锌铁钉比镀锡铁钉更易生锈
D.溶液恢复棕色的原因为I-被氧化
5.关于反应KHIO +9HI===2KI+4I+6HO,下列说法正确的是( )
2 3 6 2 2
A. K HIO 发生氧化反应
2 3 6
B.KI是还原产物
C.生成12.7 g I 时,转移0.1 mol电子
2
D.还原剂与氧化剂的物质的量之比为7∶1
6.(2023·德州模拟)工业上以铜阳极泥(主要成分是Cu Te)为原料提取碲,涉及反应:
2
①Cu Te+2O +2HSO ===2CuSO +TeO +2HO,②TeO +2SO +2HO===2HSO +Te。
2 2 2 4 4 2 2 2 2 2 2 4
以下说法正确的是( )
A.Cu Te中Cu元素的化合价是+2价
2B.反应①中氧化剂是O,氧化产物是TeO
2 2
C.每制备1 mol Te理论上共转移12 mol e-
D.氧化性强弱顺序为O>SO>TeO
2 2 2
7.(2021·湖南,8)KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第
3
一步反应为6I+11KClO+3HO=====6KH(IO)+5KCl+3Cl↑。下列说法错误的是( )
2 3 2 3 2 2
A.产生22.4 L(标准状况)Cl 时,反应中转移10 mol e-
2
B.反应中氧化剂和还原剂的物质的量之比为11∶6
C.可用石灰乳吸收反应产生的Cl 制备漂白粉
2
D.可用酸化的淀粉碘化钾溶液检验食盐中IO的存在
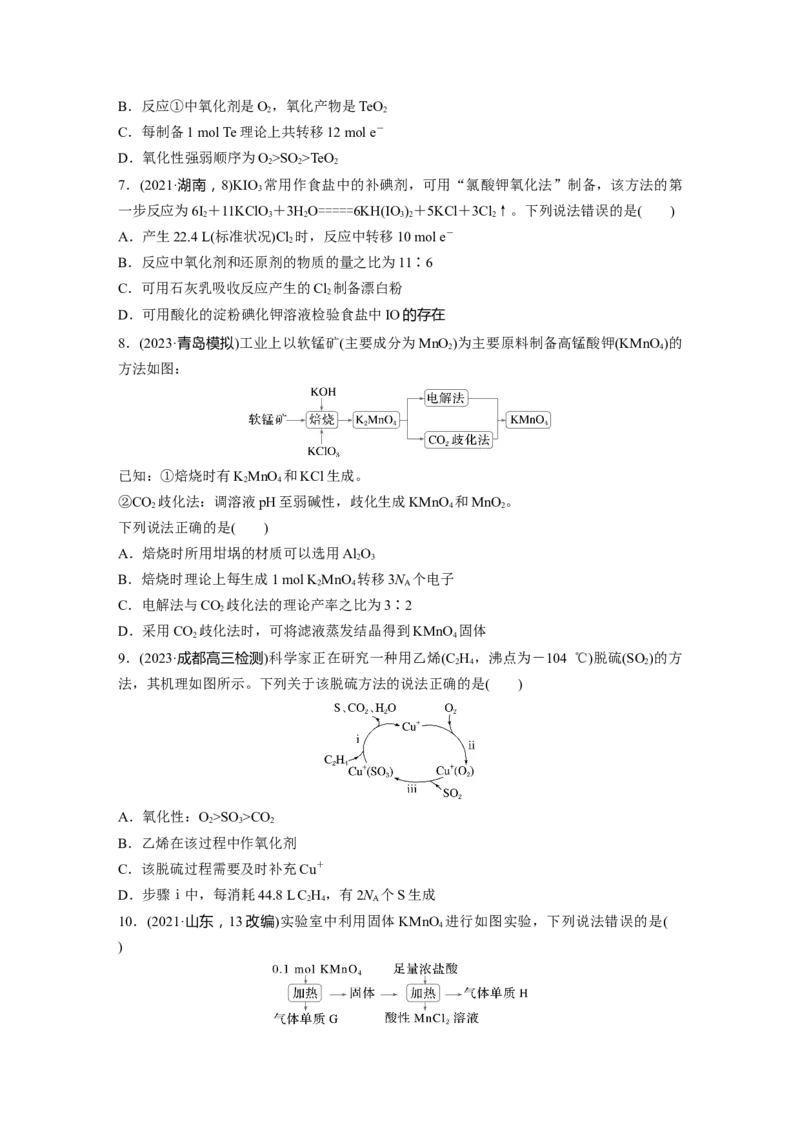
8.(2023·青岛模拟)工业上以软锰矿(主要成分为MnO )为主要原料制备高锰酸钾(KMnO)的
2 4
方法如图:
已知:①焙烧时有KMnO 和KCl生成。
2 4
②CO 歧化法:调溶液pH至弱碱性,歧化生成KMnO 和MnO 。
2 4 2
下列说法正确的是( )
A.焙烧时所用坩埚的材质可以选用Al O
2 3
B.焙烧时理论上每生成1 mol K MnO 转移3N 个电子
2 4 A
C.电解法与CO 歧化法的理论产率之比为3∶2
2
D.采用CO 歧化法时,可将滤液蒸发结晶得到KMnO 固体
2 4
9.(2023·成都高三检测)科学家正在研究一种用乙烯(C H ,沸点为-104 ℃)脱硫(SO )的方
2 4 2
法,其机理如图所示。下列关于该脱硫方法的说法正确的是( )
A.氧化性:O>SO>CO
2 3 2
B.乙烯在该过程中作氧化剂
C.该脱硫过程需要及时补充Cu+
D.步骤ⅰ中,每消耗44.8 L C H,有2N 个S生成
2 4 A
10.(2021·山东,13改编)实验室中利用固体KMnO 进行如图实验,下列说法错误的是(
4
)A.G与H均为氧化产物
B.实验中KMnO 既是氧化剂又是还原剂
4
C.Mn元素至少参与了3个氧化还原反应
D.G与H的物质的量之和可能为0.25 mol
11.氧化还原反应是一类重要的化学反应。
(1)已知反应:Cu+2Fe3+===Cu2++2Fe2+,反应中还原剂是__________,氧化性:Fe3+
________(填“<”或“>”)Cu2+。
(2)在2NaO +2CO===2NaCO +O 反应中,若转移3 mol电子,则所产生的氧气在标准状
2 2 2 2 3 2
况下的体积为________ L。
(3)在xR2++yH++O===mR3++nHO的离子方程式中,对系数m和R2+、R3+判断正确的是
2 2
________(填字母)。
A.m=y,R3+是还原剂
B.m=2y,R2+被氧化
C.m=2,R3+是氧化剂
D.m=4,R2+是还原剂
(4)用双线桥标出反应2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO中电子转移的
4 2 2 2
方向和数目。
12.(2023·济南高三模拟)CuI是难溶于水的白色固体。已知:氧化性:Cu2+>I >Cu+,还
2
原性:Cu>I->Cu+。
(1)根据物质氧化性和还原性的强弱推测,在溶液中Cu2+和I-反应的产物是______、______。
(2)久置于空气中的HI溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,反应的化学
方程式为_____________________________________________________________________。
(3)欲消除(2)中HI溶液的黄色,也可向其中通入少量HS,这是因为当浓度接近时,还原性:
2
HS__________(填“>”“<”或“=”)I-;与加入铜粉的方法相比,用此方法得到的 HI
2
溶液浓度________(填“高”“低”或“相等”)。
(4)CuI可用于监测空气中是否含有汞蒸气:4CuI(白色)+Hg===Cu HgI (亮黄色)+2Cu。下列
2 4
关于该化学方程式的说法错误的是______(填字母)。
A.该反应中被氧化的元素是铜元素和汞元素
B.该反应的氧化剂为CuI
C.Cu HgI 既是氧化产物又是还原产物
2 4
D.反应中每生成1 mol Cu HgI 转移2 mol电子
2 4
13.某化学探究学习小组用如图所示装置进行SO 、Fe2+和Cl-还原性强弱比较实验,实验
2
过程如下:Ⅰ.先向B中的FeCl 溶液(约10 mL)中通入Cl,当B中溶液变黄时,停止通气。
2 2
Ⅱ.打开活塞k,使约2 mL的溶液流入试管A中,检验取出溶液中的离子。
Ⅲ.接着再向B中通入一定量的SO 气体。
2
Ⅳ.更新试管A,重复过程Ⅱ,检验取出溶液中的离子。
(1)棉花中浸润的溶液为________________,目的是___________________________________。
(2)实验室制备氯气的化学方程式为_________________________________________________
_______________________________________________________________________________
。
(3)过程Ⅲ中一定发生反应的离子方程式为___________________________________________
_______________________________________________________________________________
;
过程Ⅳ中检验取出溶液中是否含有硫酸根离子的操作是_______________________________
_______________________________________________________________________________
。
(4)该小组对SO 、Fe2+和Cl-还原性强弱比较得到的结论是____________________________。
2
(5)甲、乙、丙三位同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一
定能够证明SO 、Fe2+和Cl-还原性强弱关系的是____________________。
2
过程Ⅱ中检出离子 过程Ⅳ中检出离子
甲 有Fe3+无Fe2+ 有SO
乙 既有Fe3+又有Fe2+ 有SO
丙 有Fe3+无Fe2+ 有Fe2+