文档内容
1.(2022·浙江6月选考,2)下列物质属于强电解质的是( )
A.HCOOH B.Fe
C.NaCO D.C H
2 3 2 2
2.下列说法正确的是( )
A.CO 的水溶液能导电,所以CO 是电解质
2 2
B.BaSO 难溶于水,其水溶液的导电能力极弱,所以BaSO 的电离方程式为BaSOBa2+
4 4 4
+SO
C.液溴不导电,所以溴是非电解质
D.强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强
3.(2023·重庆,2)下列离子方程式中,错误的是( )
A.NO 通入水中:3NO +HO===2H++2NO+NO
2 2 2
B.Cl 通入石灰乳中:Cl+2OH-===ClO-+Cl-+HO
2 2 2
C.Al放入NaOH溶液中:2Al+2OH-+2HO===2AlO+3H↑
2 2
D.Pb放入Fe (SO ) 溶液中:Pb+SO+2Fe3+===2Fe2++PbSO
2 4 3 4
4.(2022·湖北,4)下列各组离子在给定溶液中能大量共存的是( )
A.在0.1 mol·L-1氨水中:Ag+、Cu2+、NO、SO
B.在0.1 mol·L-1氯化钠溶液中:Fe3+、I-、Ba2+、HCO
C.在0.1 mol·L-1醋酸溶液中:SO、NH、Br-、H+
D.在0.1 mol·L-1硝酸银溶液中:K+、Cl-、Na+、CO
5.(2022·重庆,4)下列操作中,不会影响溶液中K+、Al3+、Fe3+、Ba2+、Cl-、NO等离子
大量共存的是( )
A.加入ZnSO B.加入Fe粉
4
C.通入NH D.通入CO
3 2
6.(2023·郑州高三联考)下列过程中的化学反应,相应的离子方程式正确的是( )
A.向石灰石中加入盐酸:CaCO +2H+===Ca2++CO↑+HO
3 2 2
B.利用氢氧化钠溶液吸收废气NO :2NO +2OH-===2NO+HO
2 2 2
C.向硫酸镁溶液中滴加氢氧化钡溶液:Mg2++2OH-===Mg(OH) ↓
2
D.将ICl滴入NaOH溶液中:ICl+2OH-===I-+ClO-+HO
2
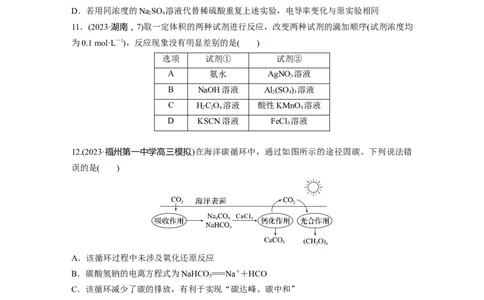
7.滴有酚酞的Ba(OH) 溶液显红色,在上述溶液中分别滴加X溶液后有下列现象。下列说
2
法不正确的是( )
序号 装置 X溶液 现象溶液红色褪去,无沉淀,灯泡亮
Ⅰ 盐酸
度没有明显变化
溶液红色不变,有白色沉淀生
Ⅱ NaSO 溶液
2 4
成,灯泡亮度没有明显变化
溶液红色褪去,有白色沉淀生
Ⅲ HSO 溶液
2 4
成,灯泡逐渐变暗
A.实验Ⅰ中溶液红色褪去,说明发生了反应:H++OH-===HO
2
B.实验Ⅱ中溶液红色不变,且灯泡亮度没有明显变化,说明溶液中依然存在大量的Na+与
OH-
C.实验Ⅲ中溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗,说明发生了反应:Ba2++
2OH-+2H++SO===BaSO↓+2HO
4 2
D.将实验Ⅱ中NaSO 溶液换成CuSO 溶液,现象与原实验Ⅱ中的现象相同
2 4 4
8.(2022·全国甲卷,9)能正确表示下列反应的离子方程式为( )
A.硫化钠溶液和硝酸混合:S2-+2H+===HS↑
2
B.明矾溶液与过量氨水混合:Al3++4NH +2HO===AlO+4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO+CO+HO===HSiO+HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H+
2 4 4
+SO===BaSO↓+2HO
4 2
9.(2023·浙江6月选考,9)下列反应的离子方程式正确的是( )
A.碘化亚铁溶液与等物质的量的氯气:2Fe2++2I-+2Cl===2Fe3++I+4Cl-
2 2
B.向次氯酸钙溶液通入足量二氧化碳:ClO-+CO+HO===HClO+HCO
2 2
C.铜与稀硝酸:Cu+4H++2NO===Cu2++2NO ↑+2HO
2 2
D.向硫化钠溶液通入足量二氧化硫:S2-+2SO +2HO===HS+2HSO
2 2 2
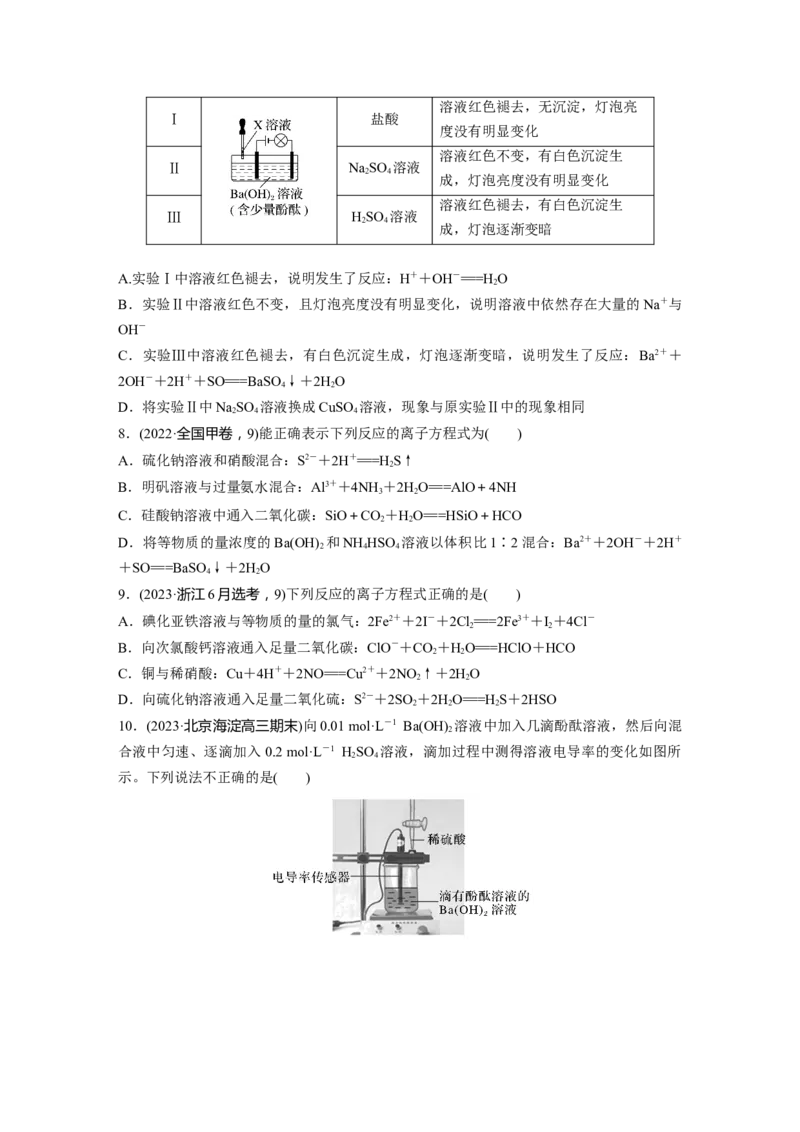
10.(2023·北京海淀高三期末)向0.01 mol·L-1 Ba(OH) 溶液中加入几滴酚酞溶液,然后向混
2
合液中匀速、逐滴加入0.2 mol·L-1 HSO 溶液,滴加过程中测得溶液电导率的变化如图所
2 4
示。下列说法不正确的是( )A.烧杯中红色逐渐变浅直至完全褪去
B.由于水存在微弱电离、BaSO 存在微弱溶解,理论上电导率不会为0
4
C.电导率减小的过程中,发生反应:2H++SO+Ba2++2OH-===BaSO↓+2HO
4 2
D.若用同浓度的NaSO 溶液代替稀硫酸重复上述实验,电导率变化与原实验相同
2 4
11.(2023·湖南,7)取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均
为0.1 mol·L-1),反应现象没有明显差别的是( )
选项 试剂① 试剂②
A 氨水 AgNO 溶液
3
B NaOH溶液 Al (SO ) 溶液
2 4 3
C HC O 溶液 酸性KMnO 溶液
2 2 4 4
D KSCN溶液 FeCl 溶液
3
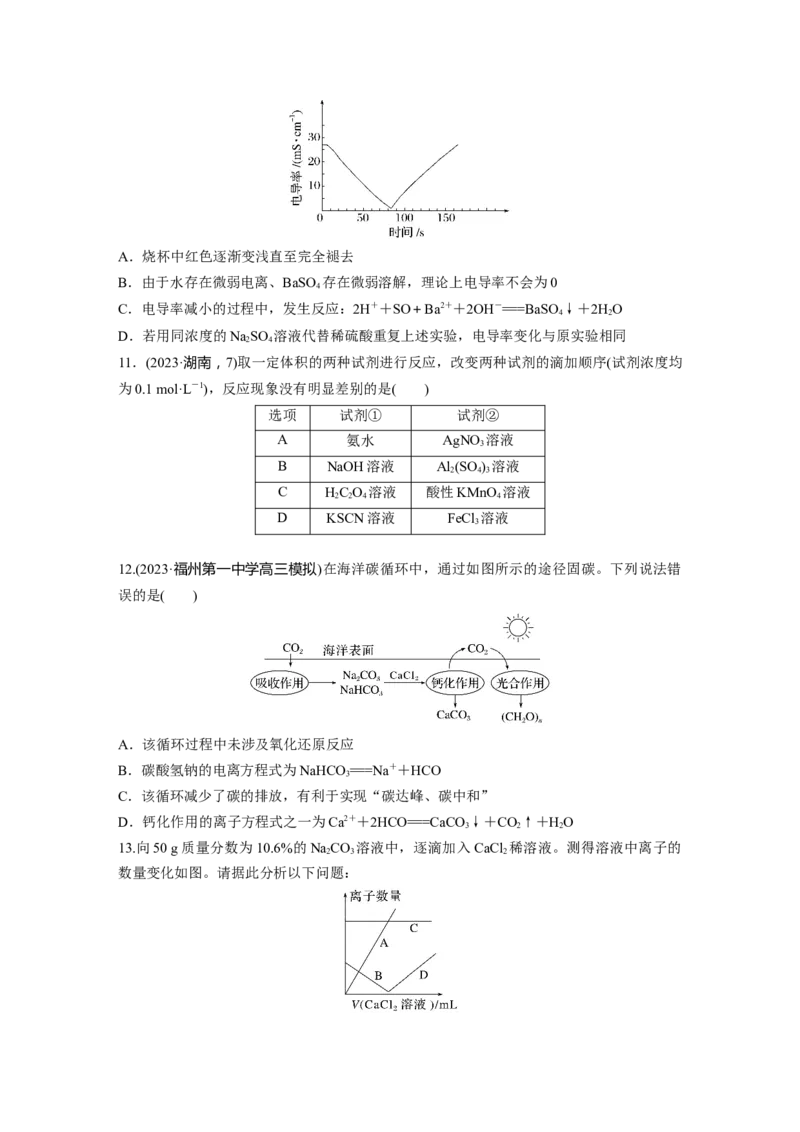
12.(2023·福州第一中学高三模拟)在海洋碳循环中,通过如图所示的途径固碳。下列说法错
误的是( )
A.该循环过程中未涉及氧化还原反应
B.碳酸氢钠的电离方程式为NaHCO ===Na++HCO
3
C.该循环减少了碳的排放,有利于实现“碳达峰、碳中和”
D.钙化作用的离子方程式之一为Ca2++2HCO===CaCO ↓+CO↑+HO
3 2 2
13.向50 g质量分数为10.6%的NaCO 溶液中,逐滴加入CaCl 稀溶液。测得溶液中离子的
2 3 2
数量变化如图。请据此分析以下问题:(1)请指出图中曲线表示的离子符号:
A________;C________;D________。
(2)反应的离子方程式为_________________________________________________________
_____________________________________________________________________________。
(3)当A、C曲线相交时,生成的沉淀质量为____g。
14.请按要求书写下列离子方程式:
(1)向 Ba(HCO ) 溶液中滴入 NaHSO 溶液,至沉淀完全,写出反应的离子方程式:
3 2 4
_____________________________________________________________________________
_____________________________________________________________________________。
在上述溶液中继续滴入NaHSO 溶液,此时离子方程式为___________________________。
4
(2)0.2 mol·L-1的NH Al(SO ) 溶液与0.3 mol·L-1的Ba(OH) 溶液等体积混合:
4 4 2 2
________________________________________________________________________。
(3)CuCl 溶液与NaHS溶液反应,当n(CuCl )∶n(NaHS)=1∶2时:__________+________
2 2
_____________________________________________________________________________。
(4)标准状况下,2.24 L CO 通入250 mL 0.5 mol·L-1的 NaOH溶液中:________________
2
_____________________________________________________________________________。
(5)100 mL 0.1 mol·L-1的NaCO 溶液中加入0.01 mol CH COOH:____________________
2 3 3
_____________________________________________________________________________。