文档内容
1.一定条件下,硝酸铵受热分解的化学方程式(未配平)为NH NO ―→HNO+N↑+HO,
4 3 3 2 2
下列说法错误的是( )
A.配平后HO的化学计量数为6
2
B.NH NO 既是氧化剂又是还原剂
4 3
C.该反应既是分解反应也是氧化还原反应
D.氧化产物和还原产物的物质的量之比为5∶3
2.把图2中的物质补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平)。
对该氧化还原反应的离子方程式,下列说法不正确的是( )
A.IO是氧化剂,具有氧化性
B.氧化性:MnO>IO
C.氧化剂和还原剂的物质的量之比为5∶2
D.若有2个Mn2+参加反应,则转移10个电子
3.已知反应:①SO +2Fe3++2HO===SO+2Fe2++W;②Cr O+aFe2++bH+―→Cr3++
2 2 2
Fe3++HO (未配平)
2
下列有关说法正确的是( )
A.方程式①中W为4OH-
B.还原性强弱:SO >Fe2+
2
C.a=6,b=7
D.反应Cr O+3SO +2H+===2Cr3++3SO+HO不能发生
2 2 2
4.(2024·大连模拟)NaSO 去除酸性废水中HAsO 的反应机理如图所示(图中“HS·”为自
2 2 3 3 3
由基)。下列说法错误的是( )
A.X的化学式为HS
2 2
B.HS·反应活性较强,不能稳定存在
C.步骤Ⅲ反应中氧化剂与还原剂的物质的量之比为8∶1
D.步骤Ⅳ除砷的化学方程式为3HS+2HAsO ===As S↓+6HO
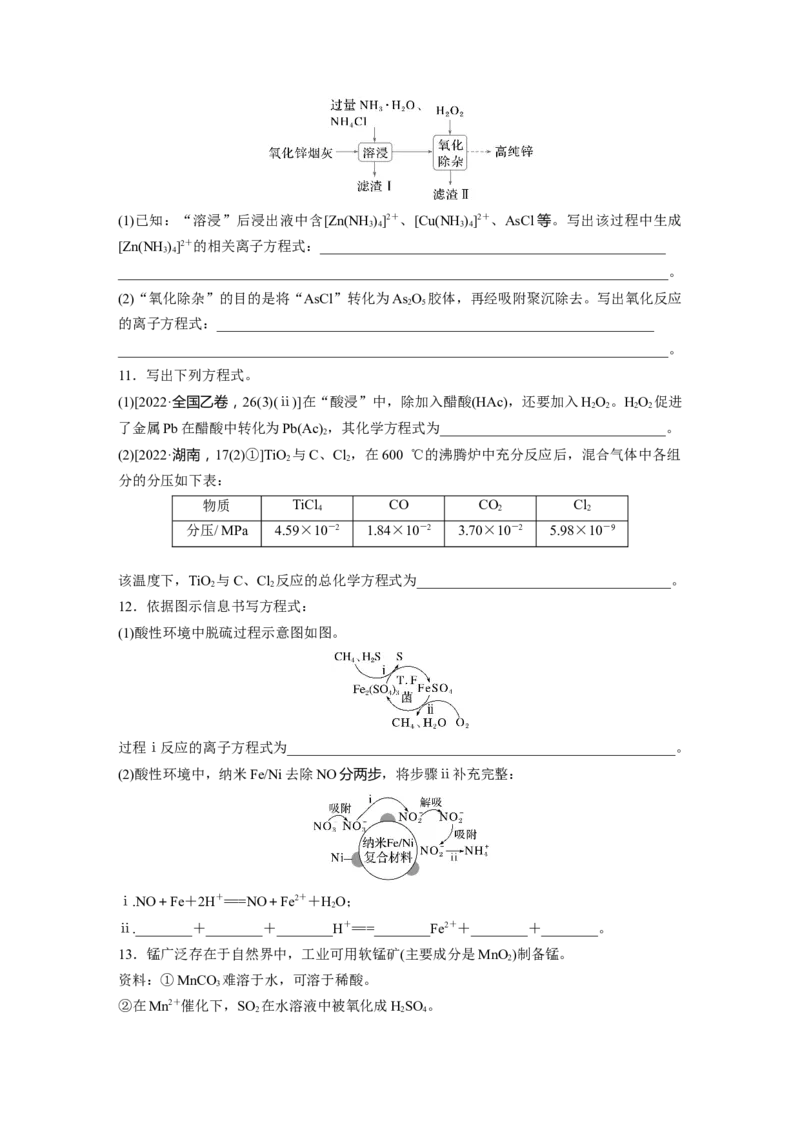
2 3 3 2 3 25.(2023·深圳一中高三模拟)一种在恒温、恒定气流流速下,催化氧化HCl生产Cl 工艺的
2
主要反应机理如图。下列说法不正确的是( )
A.该过程中Cu元素的化合价发生变化
B.Cu(OH)Cl、Cu OCl 均为中间产物
2 2
C.Cu(OH)Cl分解生成两种产物,物质X为HO
2
D.该过程涉及反应:2Cu OCl +O2Cl+4CuO
2 2 2 2
6.配平下列离子方程式:
(1)____NO+____Fe2++____H+===____NO↑+____Fe3++____HO
2
(2)____Mn2++____HO+____OH-===____MnO ↓+____HO
2 2 2 2
(3)____MnO +____SO+____H+===____Mn2++____SO+____HO
2 2
7.配平下列反应。
(1)____Li CO + ____C H O + ____FePO ===____LiFePO + ____CO↑ + ____HO +
2 3 6 12 6 4 4 2
____CO↑
2
(2)____(NH )MoO +____H=====____Mo+____NH +____HO
4 2 4 13 2 3 2
(3)____H S+____NO===____S+____HO+____N
2 x 2 2
(4)____FeCl ·6H O+____SOCl =====____FeCl +____SO ↑+____HCl↑
3 2 2 3 2
8.(1)[2022·全国甲卷,27(1)]工业上常用芒硝(Na SO ·10H O)和煤粉在高温下生产硫化钠,
2 4 2
同时生成CO,该反应的化学方程式为_____________________________________________
______________________________________________________________________________。
(2)[2022·江苏,14(1)①]在弱碱性溶液中,FeS与CrO反应生成Fe(OH) 、Cr(OH) 和单质
3 3
S , 其 离 子 方 程 式 为
________________________________________________________________
______________________________________________________________________________。
9.[2021·全国甲卷,26(2)]以NaIO 为原料制备I 的方法是先向NaIO 溶液中加入计量的
3 2 3
NaHSO ,生成碘化物;再向混合溶液中加入NaIO 溶液,反应得到I 。上述制备I 的总反
3 3 2 2
应的离子方程式为________________________________________________________________
______________________________________________________________________________。
10.现代工业上用氧化锌烟灰(主要成分为ZnO,含少量Pb、CuO和As O)制取高纯锌的部
2 3
分工艺流程如图所示。(1)已知:“溶浸”后浸出液中含[Zn(NH )]2+、[Cu(NH )]2+、AsCl等。写出该过程中生成
3 4 3 4
[Zn(NH )]2+的相关离子方程式:_________________________________________________
3 4
______________________________________________________________________________。
(2)“氧化除杂”的目的是将“AsCl”转化为As O 胶体,再经吸附聚沉除去。写出氧化反应
2 5
的离子方程式:______________________________________________________________
______________________________________________________________________________。
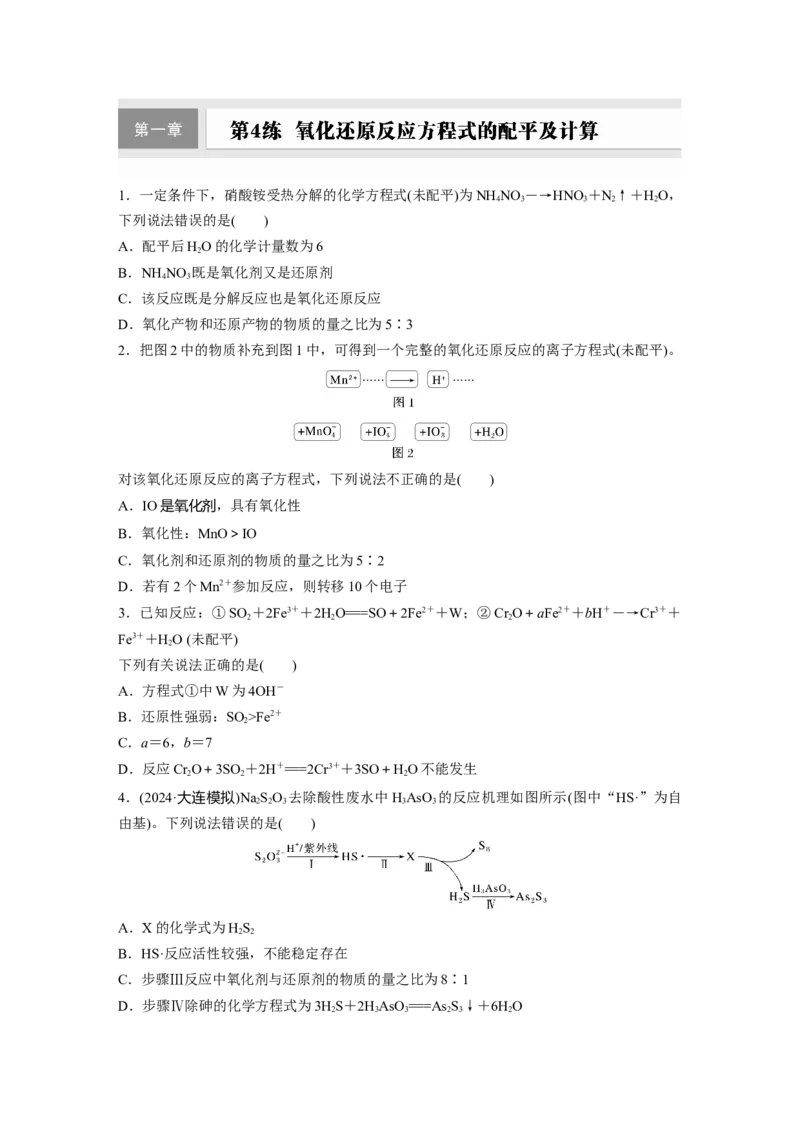
11.写出下列方程式。
(1)[2022·全国乙卷,26(3)(ⅱ)]在“酸浸”中,除加入醋酸(HAc),还要加入HO 。HO 促进
2 2 2 2
了金属Pb在醋酸中转化为Pb(Ac) ,其化学方程式为________________________________。
2
(2)[2022·湖南,17(2)①]TiO 与C、Cl ,在600 ℃的沸腾炉中充分反应后,混合气体中各组
2 2
分的分压如下表:
物质 TiCl CO CO Cl
4 2 2
分压/ MPa 4.59×10-2 1.84×10-2 3.70×10-2 5.98×10-9
该温度下,TiO 与C、Cl 反应的总化学方程式为____________________________________。
2 2
12.依据图示信息书写方程式:
(1)酸性环境中脱硫过程示意图如图。
过程ⅰ反应的离子方程式为_______________________________________________________。
(2)酸性环境中,纳米Fe/Ni去除NO分两步,将步骤ⅱ补充完整:
ⅰ.NO+Fe+2H+===NO+Fe2++HO;
2
ⅱ.________+________+________H+===________Fe2++________+________。
13.锰广泛存在于自然界中,工业可用软锰矿(主要成分是MnO )制备锰。
2
资料:①MnCO 难溶于水,可溶于稀酸。
3
②在Mn2+催化下,SO 在水溶液中被氧化成HSO 。
2 2 4Ⅰ.制备
(1)写出铝热法还原MnO 制备锰的化学方程式:_____________________________________。
2
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度 SO 的烟气,可用
2
以下方法处理。
方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用MnO
2
进行脱硫的化学方程式:_________________________________________________________。
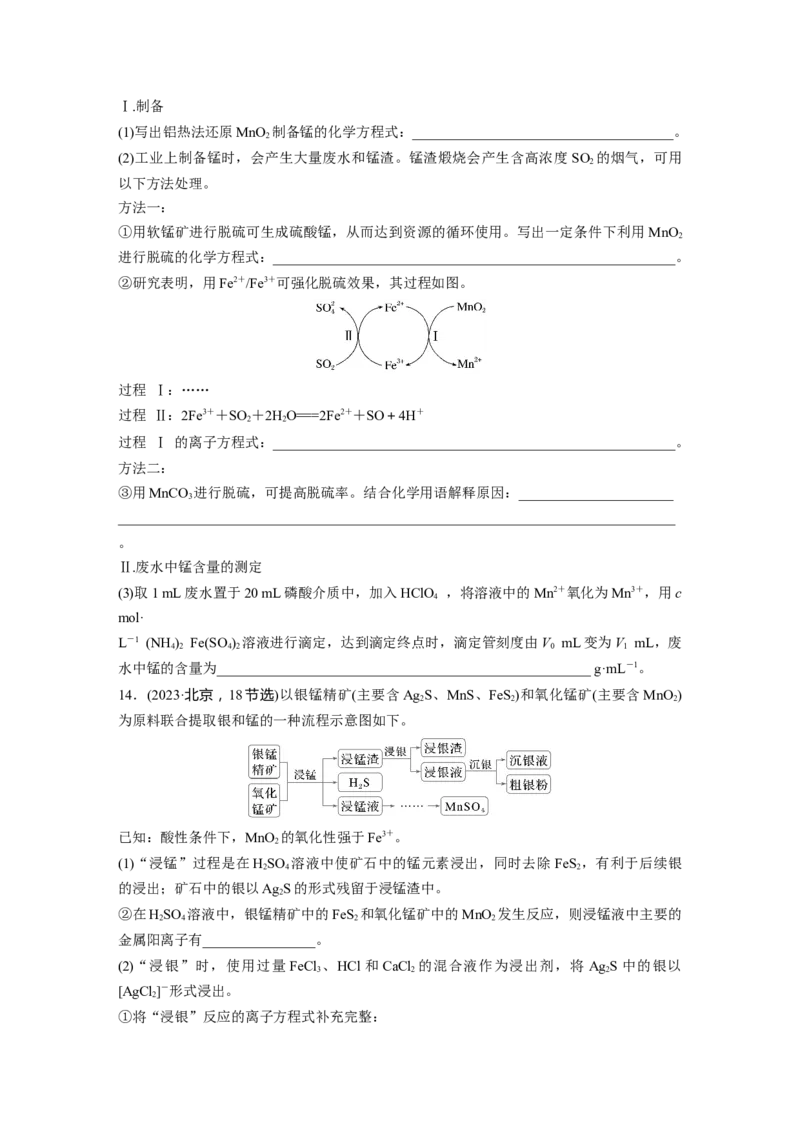
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如图。
过程 Ⅰ:……
过程 Ⅱ:2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
过程 Ⅰ 的离子方程式:_________________________________________________________。
方法二:
③用MnCO 进行脱硫,可提高脱硫率。结合化学用语解释原因:______________________
3
_______________________________________________________________________________
。
Ⅱ.废水中锰含量的测定
(3)取1 mL废水置于20 mL磷酸介质中,加入HClO ,将溶液中的Mn2+氧化为Mn3+,用c
4
mol·
L-1 (NH ) Fe(SO ) 溶液进行滴定,达到滴定终点时,滴定管刻度由V mL变为V mL,废
4 2 4 2 0 1
水中锰的含量为_____________________________________________________ g·mL-1。
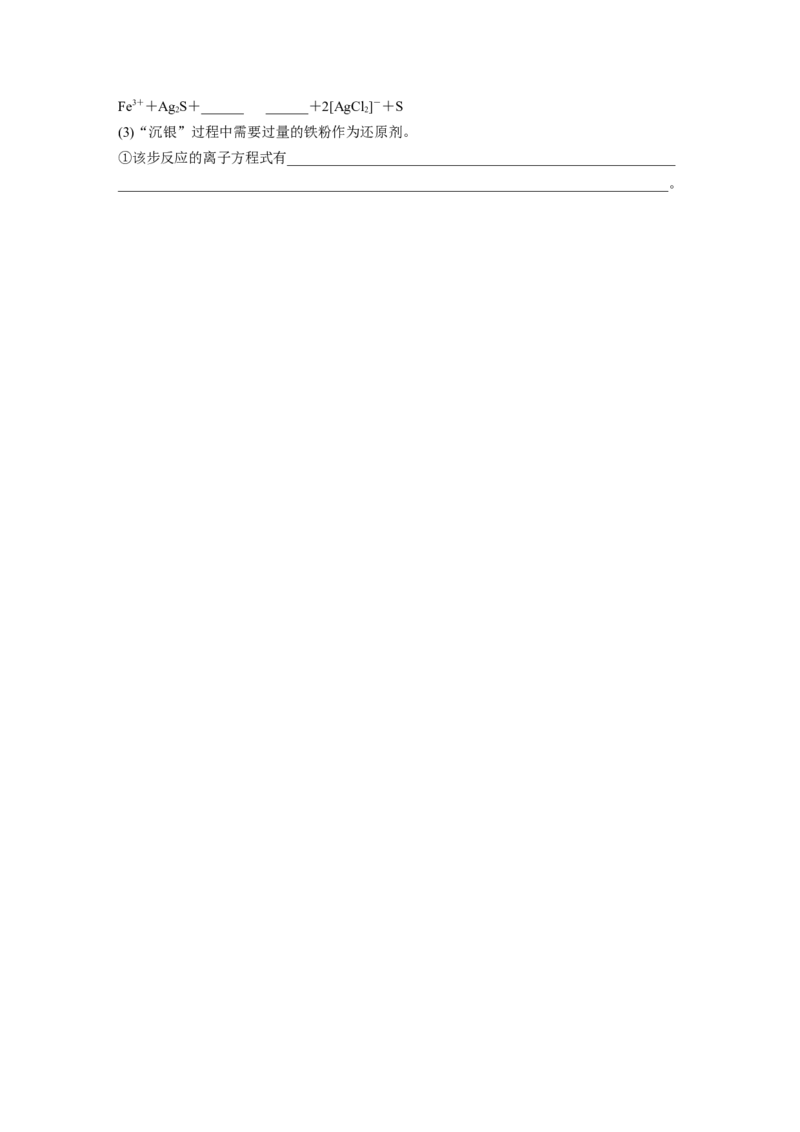
14.(2023·北京,18节选)以银锰精矿(主要含Ag S、MnS、FeS)和氧化锰矿(主要含MnO )
2 2 2
为原料联合提取银和锰的一种流程示意图如下。
已知:酸性条件下,MnO 的氧化性强于Fe3+。
2
(1)“浸锰”过程是在HSO 溶液中使矿石中的锰元素浸出,同时去除 FeS ,有利于后续银
2 4 2
的浸出;矿石中的银以Ag S的形式残留于浸锰渣中。
2
②在HSO 溶液中,银锰精矿中的FeS 和氧化锰矿中的MnO 发生反应,则浸锰液中主要的
2 4 2 2
金属阳离子有________________。
(2)“浸银”时,使用过量 FeCl 、HCl 和 CaCl 的混合液作为浸出剂,将 AgS 中的银以
3 2 2
[AgCl ]-形式浸出。
2
①将“浸银”反应的离子方程式补充完整:Fe3++Ag S+____________+2[AgCl ]-+S
2 2
(3)“沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有_______________________________________________________
______________________________________________________________________________。