文档内容
第一章 化学计量
测试卷
时间:90分钟 分值:100分
可能用到的相对原子质量:H 1 Li 7 C 12 O16 Na 23 P 31 S 32 Cl 35.5 K 39 Ca 40 Fe 56
Cu 64
一、选择题(每小题只有一个正确选项,共15×3分)
1.(2023·上海金山·统考二模)将一定量锌与100 mL 18 mol∙L−1的浓硫酸充分反应,锌完全溶解时产生
0.8 mol气体(不考虑气体在溶液中的溶解),将反应后的溶液稀释至400 mL,测得溶液中c(H+)=x mol∙L−1,
则下列叙述错误的是
A.共消耗锌48.0 g B.共转移电子1.6 mol
C.气体中 D.生成气体体积约为17.92 L(STP)
2.(2023·上海杨浦·统考二模)室温下,甲同学配制5%的 溶液100g,乙同学配制 的
溶液100mL( 的溶解度为 水),下列说法正确的是
A.所需溶质的质量相同 B.所需仪器均包括100mL容量瓶
C.所配溶液均为不饱和溶液 D.所配溶液质量相同
3.(2023·上海·模拟预测)下列叙述中,正确的是
A.同温同压下,等体积的 和 具有相同的分子数
B.等物质的量浓度的盐酸和硫酸中, 的物质的量浓度也相等
C.同温同压下,等质量的 和 物质的量之比为
D.标准状况下, 气体溶于 水形成的溶液物质的量浓度为
4.(2022·福建省龙岩第一中学模拟预测)过硫酸钾 常用作强氧化剂,可发生反应:
。过硫酸根 的离子结构如图所示。下列说法正确的是
A. 中氧元素的化合价有: 、
B. 中含 极性共价键
C. 固体中阴阳离子总数为
D. 和水反应产生
5.(2022·天津市新华中学一模)设 为阿伏加德罗常数的值,下列有关叙述正确的是A. 白磷 中白磷分子总数为
B. 含 为 的矿泉水含 数目为
C.由乙烯制备一氯乙烷若获得 产品需 个 分子
D.标准状况下, 与足量水反应可获得 个 分子
6.(2022·北京育才学校三模)下列各项比较中,正确的是
A.7.8g Na O 中含有的离子数为0.4N
2 2 A
B.标准状况下,等体积乙烷和苯,所含分子数相等
C.等物质的量的Fe和Cu分别与足量的Cl 反应,转移的电子数相等
2
D.质量相同的 HO 和 DO(重水)所含的原子数不相同
2 2
7.(2023·浙江金华·浙江省东阳中学校考模拟预测)下列说法不正确的是
A.把7.2 g纯铁粉加入40 mL浓度未知的HNO 溶液中,充分反应后剩余固体1.6 g,产生NO 和NO的混
3 2
合气体0.08 mol,若不考虑NO 的存在,则原HNO 溶液的物质的量浓度为7.0 mol·L-1
2 4 3
B.将质量分数为a%,物质的量浓度为c mol·L-1的稀HSO 溶液蒸发掉一定量的水,使之质量分数为
1 2 4
2a%,此时物质的量浓度为c mol·L-1,则c 和c 的数值关系是c>2c
2 1 2 2 1
C.将标准状况下的a L HCl气体溶于1 000 mL水中,得到的盐酸溶液密度为b g·mL-1,则该盐酸溶液的
物质的量浓度为 mol·L-1
D.V L Fe (SO ) 溶液中含Fe3+m g,则溶液中 的物质的量浓度为 mol·L-1
2 4 3
8.(2022·北京海淀·二模)下列说法正确的是
A.室温下,1L0.1mol·L-1盐酸中H+的数目约为6.02×1022
B.标准状况下,5.6LCCl 中所含C—Cl键的数目约为6.02×1023
4
C.5.6gFe和足量Cl 反应转移电子的物质的量为0.2mol
2
D.室温下,pH相同的盐酸和硫酸中,溶质的物质的量浓度相同
9.(2023·广西南宁·统考二模)N 是阿伏加德罗常数的数值。下列说法正确的是
A
A.标准状况下,2.24LHF中含有的分子数为0.1N
A
B.2gDO和H18O的混合物含有质子数为N
2 2 A
C.pH=3的HPO 溶液中氢离子数目为10-3N
3 4 A
D.1molCl 与足量的水充分反应转移的电子数为N
2 A
10.(2023·上海杨浦·统考二模)关于 硫酸 的说法错误的是
A.质量分数为98% B. 为
C.可干燥 等气体 D.稀释时有共价键断裂
11.(2022·重庆市天星桥中学一模)溶质均为 的 两种酸, 与足量铝反应生成 体
积为 (标准状况,下同): 与足量锌反应生成 体积为 。下列说法错误的是A. 和 生成氢气的物质的量之比一定为
B. 和 消耗铝和锌的物质的量之比一定为
C.
D.由题给条件无法确定m和n的具体数值
12.(2023·上海虹口·统考二模)在两个容积相同的容器中,一个盛有NH 气体,另一个盛有H 和O 的混
3 2 2
合气体。在同温同压下,两容器内的气体不可能具有相同的
A.原子数 B.分子数 C.质量 D.电子数
13.(2023·辽宁·模拟预测)绿矾( )分解可制备铁红,同时产生 、 和 。设N 为阿
A
伏加德罗常数的值,下列说法错误的是
A. 溶液含有的阳离子数大于N
A
B.0.5mol三聚 分子( )中含有σ键数目为6 N
A
C.绿矾分解生成16g 时,转移电子数为0.2 N
A
D.22.4L 溶于水,溶液中 、 、 的数目总和为N
A
14.(2022·辽宁·沈阳二中模拟预测)纯碱在生产、生活中有广泛应用。例如可用足量的纯碱溶液吸收含
氯气的尾气,生成三种盐(反应1);工业上也可用纯碱溶液从海水中提取溴,其主要原理如下:
反应2: ;反应3:
。
下列说法正确的是
A.反应2中氧化剂与还原剂的质量之比为1∶5
B.标准状况下,22.4L溴单质中含有2mol溴原子
C.反应1中生成的三种盐是NaClO, 和
D.反应2中的 与反应1中的 表现出了相似的化学性质
15.(2023·山西·统考二模)设 为阿伏加德罗常数的值,下列说法正确的是
A. 中 键的数目为
B. 中 杂化的碳原子数目为
C.标准状况下, 中含有的电子数目为
D.常温下,将 投入足量浓硝酸中,反应转移电子数目为二、主观题(共5小题,共55分)
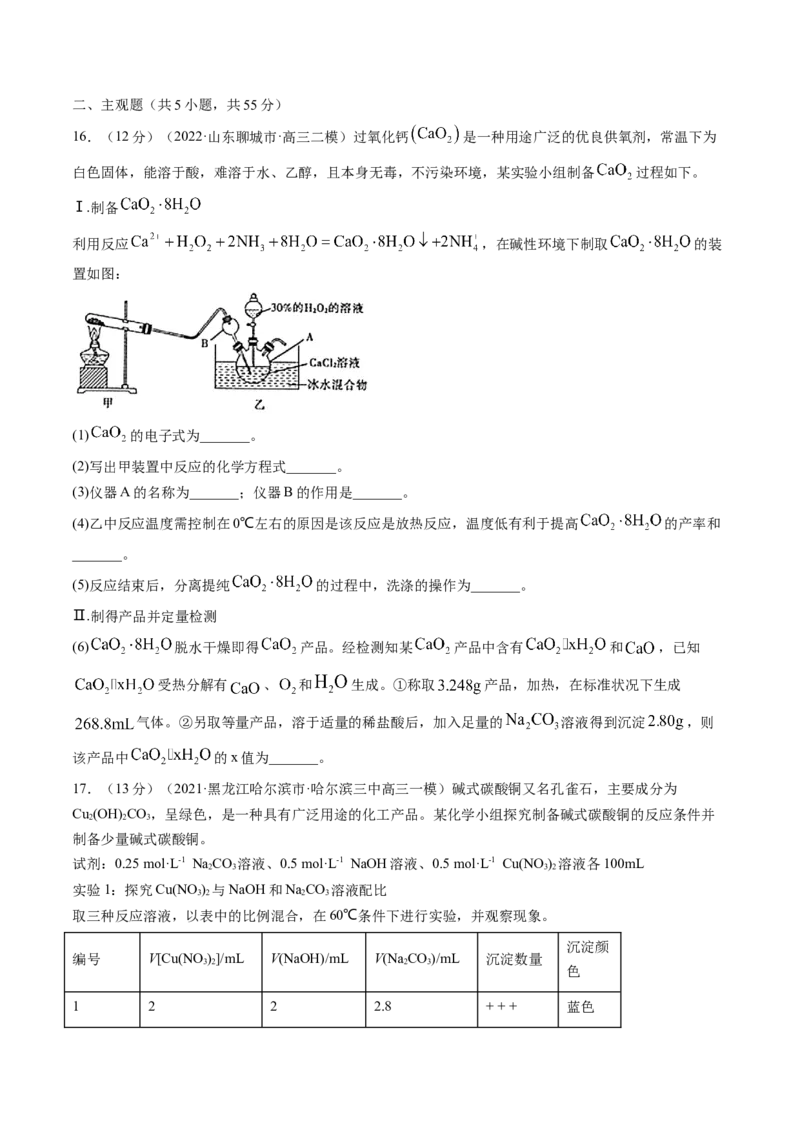
16.(12分)(2022·山东聊城市·高三二模)过氧化钙 是一种用途广泛的优良供氧剂,常温下为
白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备 过程如下。
Ⅰ.制备
利用反应 ,在碱性环境下制取 的装
置如图:
(1) 的电子式为_______。
(2)写出甲装置中反应的化学方程式_______。
(3)仪器A的名称为_______;仪器B的作用是_______。
(4)乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低有利于提高 的产率和
_______。
(5)反应结束后,分离提纯 的过程中,洗涤的操作为_______。
Ⅱ.制得产品并定量检测
(6) 脱水干燥即得 产品。经检测知某 产品中含有 和 ,已知
受热分解有 、 和 生成。①称取 产品,加热,在标准状况下生成
气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的 溶液得到沉淀 ,则
该产品中 的x值为_______。
17.(13分)(2021·黑龙江哈尔滨市·哈尔滨三中高三一模)碱式碳酸铜又名孔雀石,主要成分为
Cu (OH) CO,呈绿色,是一种具有广泛用途的化工产品。某化学小组探究制备碱式碳酸铜的反应条件并
2 2 3
制备少量碱式碳酸铜。
试剂:0.25 mol·L-1 Na CO 溶液、0.5 mol·L-1 NaOH溶液、0.5 mol·L-1 Cu(NO ) 溶液各100mL
2 3 3 2
实验1:探究Cu(NO ) 与NaOH和NaCO 溶液配比
3 2 2 3
取三种反应溶液,以表中的比例混合,在60℃条件下进行实验,并观察现象。
沉淀颜
编号 V[Cu(NO )]/mL V(NaOH)/mL V(Na CO)/mL 沉淀数量
3 2 2 3
色
1 2 2 2.8 + + + 蓝色2 2 2 2.4 + + + 蓝色
3 2 2 2 + + 浅绿色
4 2 2 1.6 + 浅绿色
注:“+”越多表示沉淀的相对量越多
实验2:探究反应温度
按上述实验得到的合适反应液用量,在不同温度下进行实验,并观察现象。
反应温度/℃ 沉淀数量 沉淀颜色
室温 + + + + 蓝色
40 + + + + 蓝色
60 + 浅绿色
75 + + 绿色
80 + + + 绿色(少量黑色)
实验3:制备碱式碳酸铜
按最佳物料比取50mL 0.5 mol·L-1 Cu(NO ) 溶液、50mL 0.5 mol·L-1 NaOH溶液和相应体积的0.25
3 2
mol·L-1NaCO 溶液,在最佳反应温度下进行实验,待反应完全后,静置,过滤、洗涤、干燥后,得到2.5 g
2 3
产品。
请回答下列问题:
(1)本实验配制溶液时用到的玻璃仪器除烧杯、玻璃棒以外还有_______。
(2)制备碱式碳酸铜时,Cu(NO )、NaOH和NaCO 溶液的最佳物质的量之比为_______,最佳反应温度为
3 2 2 3
_______,本实验的加热方式为_______。
(3)请写出本实验制备碱式碳酸铜的化学方程式_______。
(4)实验2中在80℃反应生成的沉淀中有少量黑色的物质,产生该物质的原因可能是_______。
(5)计算本实验的产率_______%(保留三位有效数字)。
18.(10分)(2022·浙江·模拟预测) 在不同温度下失水和分解,随着温度升高分别生成
,现称取 在敞口容器加热一定时间后,得到 固体,
测得生成的 的体积为 (已折算为标准标况),求:
(1)固体的成分和物质的量比_______。
(2)标准状态下生成 的体积_______。
19.(10分)(2022·浙江嘉兴·统考二模)天然水常含有较多钙、镁离子而称之为硬水,硬水软化是指除
去钙、镁离子。若某天然水中离子含量如下表:
离子 Ca2+ Mg2+ HCO 其他含量(mol/L) 1.2×10-3 6.0×10-4 8.0×10-4 /
现要用化学方法软化10m3这种天然水,则需要先加入Ca(OH) _______g以除去Mg2+和HCO ,后加入
2
NaCO_______g以除去Ca2+(要求写出计算过程)。
2 3
20.(10分)(2022·浙江宁波·统考二模)单质硫在热的NaOH溶液中发生如下反应:3S+6NaOH
2NaS+Na SO +3H O。若硫过量,会进一步生成NaS 和NaSO:(x-1)S+Na S NaS,S+Na SO
2 2 3 2 2 x 2 2 3 2 2 x 2 3
NaSO。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na S 和b mol Na SO,
2 2 3 2 x 2 2 3
在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO 。
请计算:
(1)a mol Na S 和b mol Na SO 中a∶b=____。
2 x 2 2 3
(2)NaClO溶液的物质的量浓度为____mol·L-1 (写出计算过程)。