文档内容
第六章 化学反应与能量
测试卷
时间:75分钟 分值:100分
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O16 Na 23 Al 27 P 31 S 32 Cl 35.5 K 39 Ca
40 Fe 56 Cu 64 Br 80 Ag 108 Ba 137
一、选择题(每小题只有一个正确选项,共15×3分)
1.(2024·浙江省丽水湖州衢州三地市高三下学期教学质量检测)我国科学工作者进行了如下模拟实验:
将甲、乙两片相同的铁片用导线连接插入海水中,铁片甲附近通入氧气,铁片乙附近通入氮气,下列说法
正确的是( )
A.铁片乙作正极 B.氮气在铁片乙上失电子
C.在海水中阳离子向铁片乙移动 D.铁片乙的腐蚀速率明显高于铁片甲
2.下列两组热化学方程式中,有关ΔH的比较正确的是( )
①CH(g)+2O(g)===CO (g)+2HO(g) ΔH
4 2 2 2 1
CH(g)+2O(g)===CO (g)+2HO(l) ΔH
4 2 2 2 2
②NaOH(aq)+HSO (浓)===NaSO (aq)+HO(l) ΔH
2 4 2 4 2 3
NaOH(aq)+CHCOOH(aq)===CH COONa(aq)+HO(l) ΔH
3 3 2 4
A.ΔH>ΔH;ΔH>ΔH B.ΔH>ΔH;ΔH<ΔH
1 2 3 4 1 2 3 4
C.ΔH=ΔH;ΔH<ΔH D.ΔH<ΔH;ΔH>ΔH
1 2 3 4 1 2 3 4
3.(2024·浙江省绍兴市高三选考科目诊断性考试)已知反应NO (g)+CO(g) NO(g)+CO(g)的能
2 2
量变化如图所示,下列说法正确的是( )
A.该反应的ΔH=(E - E )kJ·mol−1
2 1
B.正反应活化能E 等于反应物的键能之和
1
C.由图可知升温对NO (g)+CO(g) NO(g)+CO(g)的逆反应速率影响更大
2 2
D.恒温条件下,缩小容器体积,平衡不移动,所以正逆反应速率均不变
4.(2024·浙江省金华市曙光中学调研)“北溪”天然气管道至少泄漏8万吨天然气,近20年间甲烷的温
室效应率是 的84倍。已知管道接口处有钢铁材料等,海水的pH约为8.0。设 为阿伏伽德罗常数的
值。下列有关叙述不正确的是( )A.损坏的钢铁材料在海水中主要发生吸氧腐蚀
B.制造管道时表面涂层能起到抗腐蚀作用
C.w g铁在海水中完全发生电化学腐蚀时转移电子数一定为
D.修复管道时在钢管表面镶嵌锌块,这种方法叫牺牲阳极法
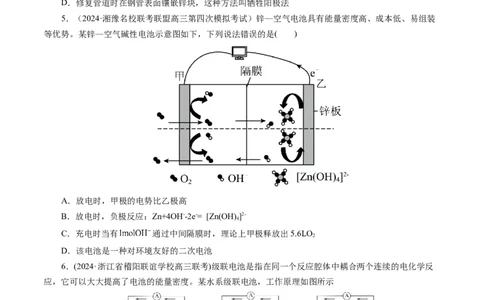
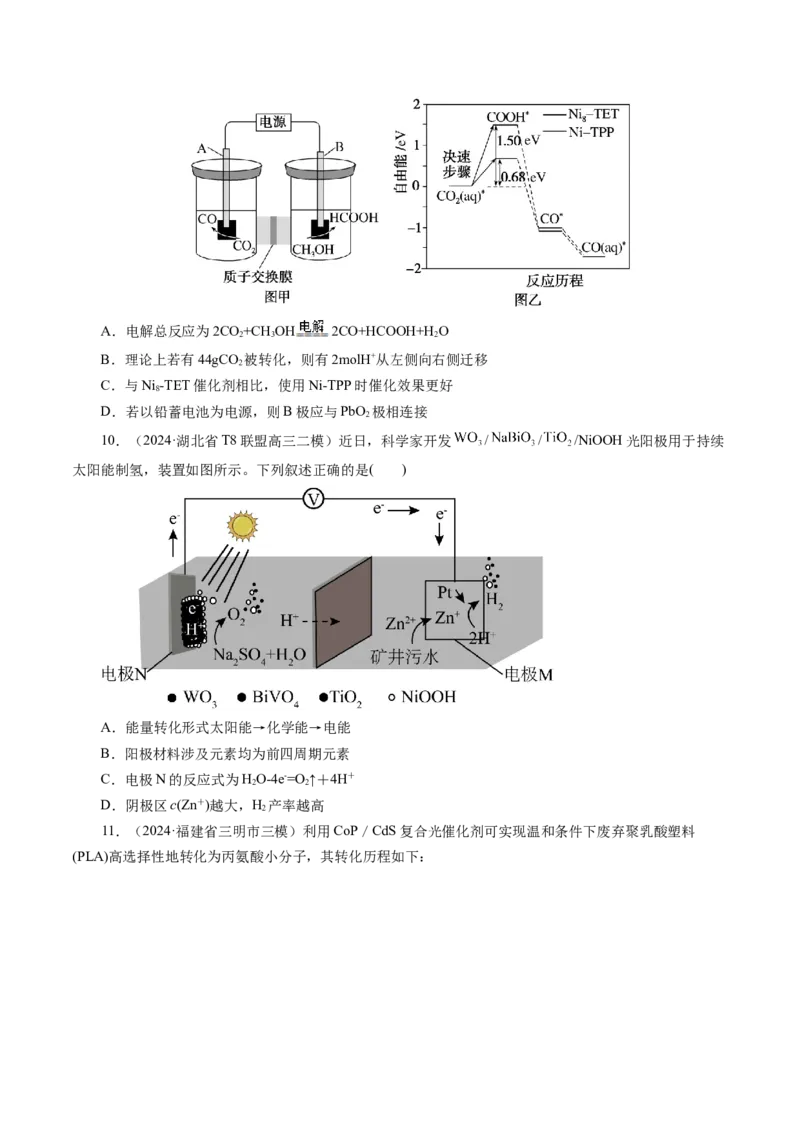
5.(2024·湘豫名校联考联盟高三第四次模拟考试)锌—空气电池具有能量密度高、成本低、易组装
等优势。某锌—空气碱性电池示意图如下,下列说法错误的是( )
A.放电时,甲极的电势比乙极高
B.放电时,负极反应:Zn+4OH--2e-= [Zn(OH) ]2-
4
C.充电时当有 通过中间隔膜时,理论上甲极释放出5.6LO
2
D.该电池是一种对环境友好的二次电池
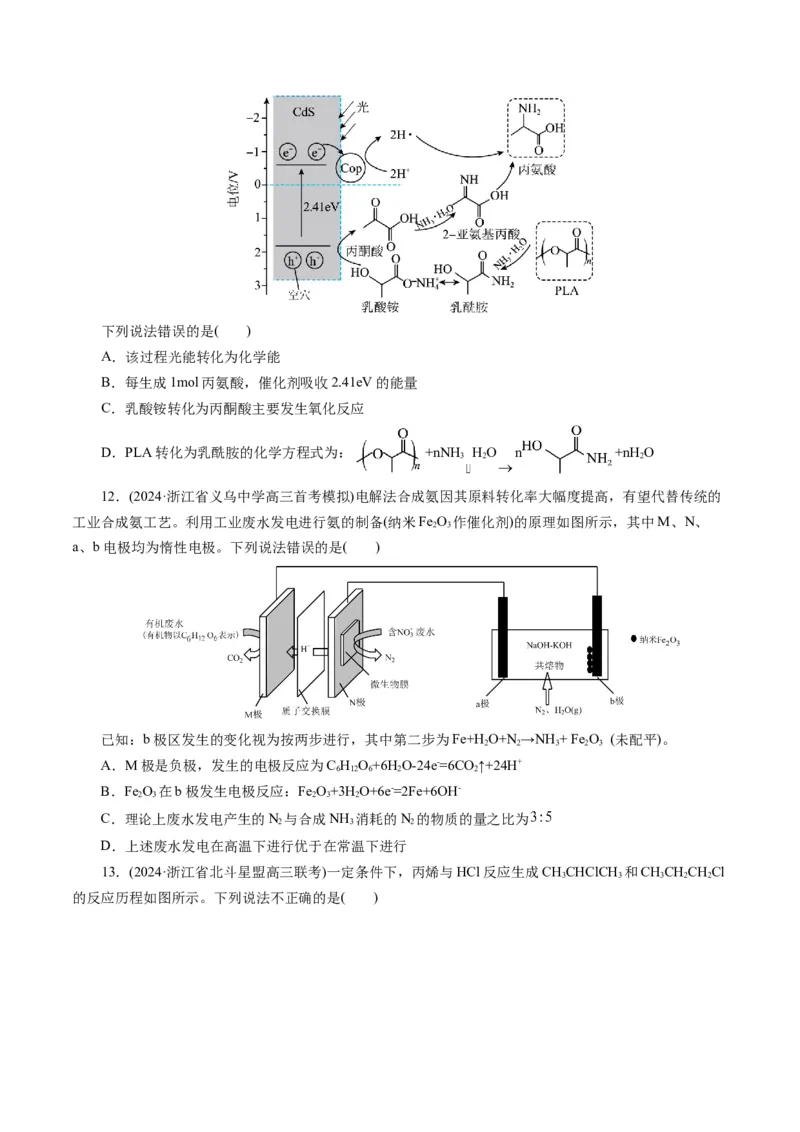
6.(2024·浙江省稽阳联谊学校高三联考)级联电池是指在同一个反应腔体中耦合两个连续的电化学反
应,它可以大大提高了电池的能量密度。某水系级联电池,工作原理如图所示
已知电解质为CuSO 溶液,步骤2中的电池反应为: (单独
4
构建该步电池时效率较低)。下列说法不正确的是( )
A.放电时,步骤1的正极反应式为2Cu2++S+4e-=Cu S
2
B.Cu S对步骤2的正极反应可能起催化作用,提高了电池工作效率
2C.若用该电池进行铜的电解精炼,则消耗6.5g锌时,得到的精铜质量大于6.4g
D.步骤2工作过程中,电池工作环境氧气浓度越大,正极板质量增加也越多
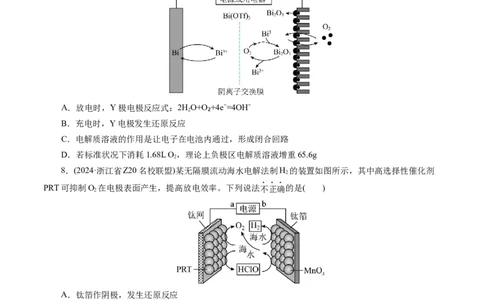
7.(2024·山东省泰安市高三四模)我国科学家首次设计了一种可充电的铋-空气电池,具有较强稳定
性 , 该 电 池 使 用 了 非 碱 性 的 三 氟 甲 磺 酸 铋 水 系 电 解 质 溶 液 , 简 写 为
Bi(OTf)₃(Mr=656g·mol⁻¹),该电池工作原理如图所示。下列说法正确的是( )
A.放电时,Y极电极反应式:2HO+O₂+4e⁻=4OH⁻
2
B.充电时,Y电极发生还原反应
C.电解质溶液的作用是让电子在电池内通过,形成闭合回路
D.若标准状况下消耗1.68L O ,理论上负极区电解质溶液增重65.6g
2
8.(2024·浙江省Z20名校联盟)某无隔膜流动海水电解法制H 的装置如图所示,其中高选择性催化剂
2
PRT可抑制O 在电极表面产生,提高放电效率。下列说法不正确的是( )
2
A.钛箔作阴极,发生还原反应
B.阳极反应主要为:Cl--2e-+H O=HClO+H+
2
C.电解后海水pH明显下降
D.理论上生成1molH 转移电子数为2N
2 A
9.(2024·浙江省义乌五校高三联考)华南师范大学兰亚乾教授课题组从催化剂结构与性能间关系的角
度,设计了一种催化剂同时作用在阳极和阴极,用于CHOH氧化和CO 还原反应耦合的混合电解,工作
3 2
原理如图甲所示。不同催化剂条件下CO→CO电极反应历程如图乙所示。下列说法不正确的是( )
2A.电解总反应为2CO+CH OH 2CO+HCOOH+H O
2 3 2
B.理论上若有44gCO 被转化,则有2molH+从左侧向右侧迁移
2
C.与Ni -TET催化剂相比,使用Ni-TPP时催化效果更好
8
D.若以铅蓄电池为电源,则B极应与PbO 极相连接
2
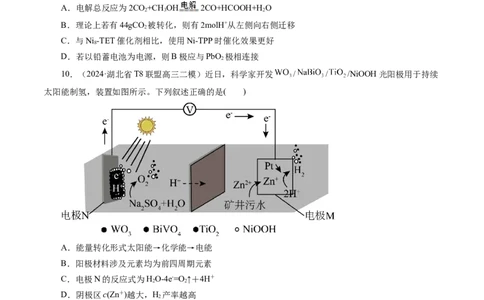
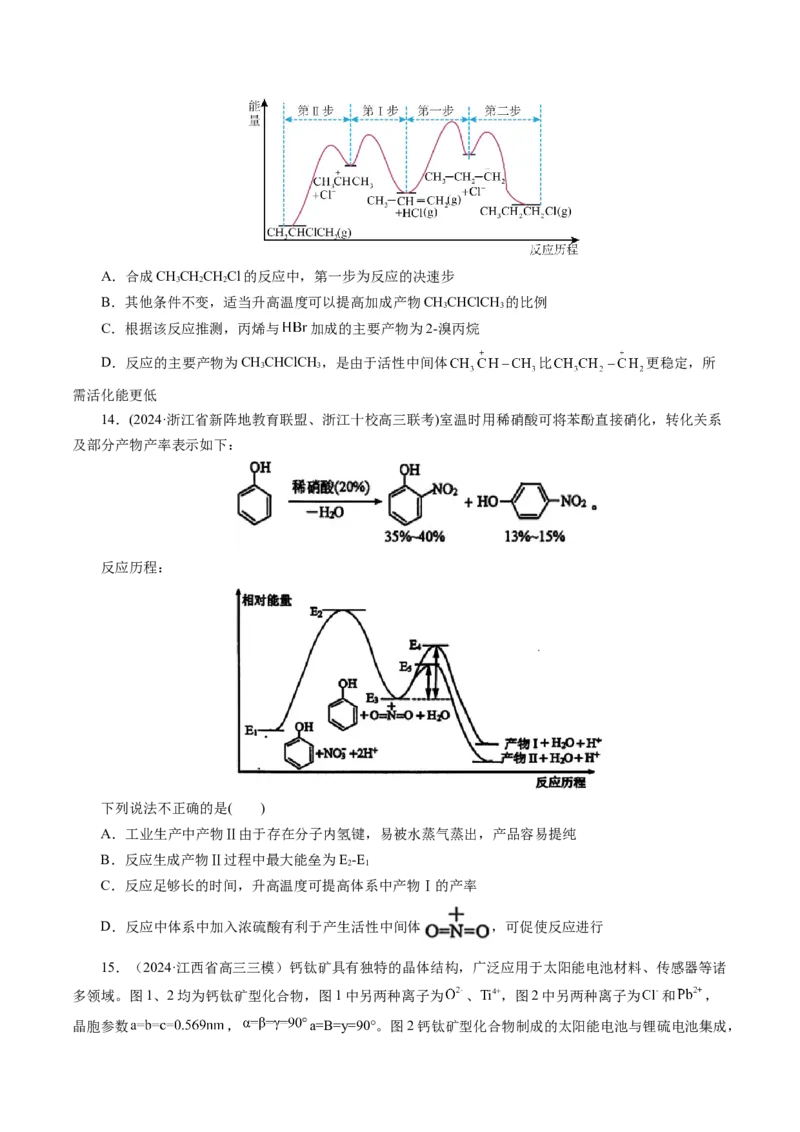
10.(2024·湖北省T8联盟高三二模)近日,科学家开发 / / /NiOOH光阳极用于持续
太阳能制氢,装置如图所示。下列叙述正确的是( )
A.能量转化形式太阳能→化学能→电能
B.阳极材料涉及元素均为前四周期元素
C.电极N的反应式为HO-4e-=O ↑+4H+
2 2
D.阴极区c(Zn+)越大,H 产率越高
2
11.(2024·福建省三明市三模)利用CoP/CdS复合光催化剂可实现温和条件下废弃聚乳酸塑料
(PLA)高选择性地转化为丙氨酸小分子,其转化历程如下:下列说法错误的是( )
A.该过程光能转化为化学能
B.每生成1mol丙氨酸,催化剂吸收2.41eV的能量
C.乳酸铵转化为丙酮酸主要发生氧化反应
D.PLA转化为乳酰胺的化学方程式为: +nNH HO n +nH O
3 2 2
12.(2024·浙江省义乌中学高三首考模拟)电解法合成氨因其原料转化率大幅度提高,有望代替传统的
工业合成氨工艺。利用工业废水发电进行氨的制备(纳米Fe O 作催化剂)的原理如图所示,其中M、N、
2 3
a、b电极均为惰性电极。下列说法错误的是( )
已知:b极区发生的变化视为按两步进行,其中第二步为Fe+H O+N→NH + Fe O (未配平)。
2 2 3 2 3
A.M极是负极,发生的电极反应为C H O+6H O-24e-=6CO ↑+24H+
6 12 6 2 2
B.Fe O 在b极发生电极反应:Fe O+3H O+6e-=2Fe+6OH-
2 3 2 3 2
C.理论上废水发电产生的N 与合成NH 消耗的N 的物质的量之比为
2 3 2
D.上述废水发电在高温下进行优于在常温下进行
13.(2024·浙江省北斗星盟高三联考)一定条件下,丙烯与HCl反应生成CHCHClCH 和CHCHCHCl
3 3 3 2 2
的反应历程如图所示。下列说法不正确的是( )A.合成CHCHCHCl的反应中,第一步为反应的决速步
3 2 2
B.其他条件不变,适当升高温度可以提高加成产物CHCHClCH 的比例
3 3
C.根据该反应推测,丙烯与 加成的主要产物为2-溴丙烷
D.反应的主要产物为CHCHClCH,是由于活性中间体 比 更稳定,所
3 3
需活化能更低
14.(2024·浙江省新阵地教育联盟、浙江十校高三联考)室温时用稀硝酸可将苯酚直接硝化,转化关系
及部分产物产率表示如下:
反应历程:
下列说法不正确的是( )
A.工业生产中产物Ⅱ由于存在分子内氢键,易被水蒸气蒸出,产品容易提纯
B.反应生成产物Ⅱ过程中最大能垒为E-E
2 1
C.反应足够长的时间,升高温度可提高体系中产物Ⅰ的产率
D.反应中体系中加入浓硫酸有利于产生活性中间体 ,可促使反应进行
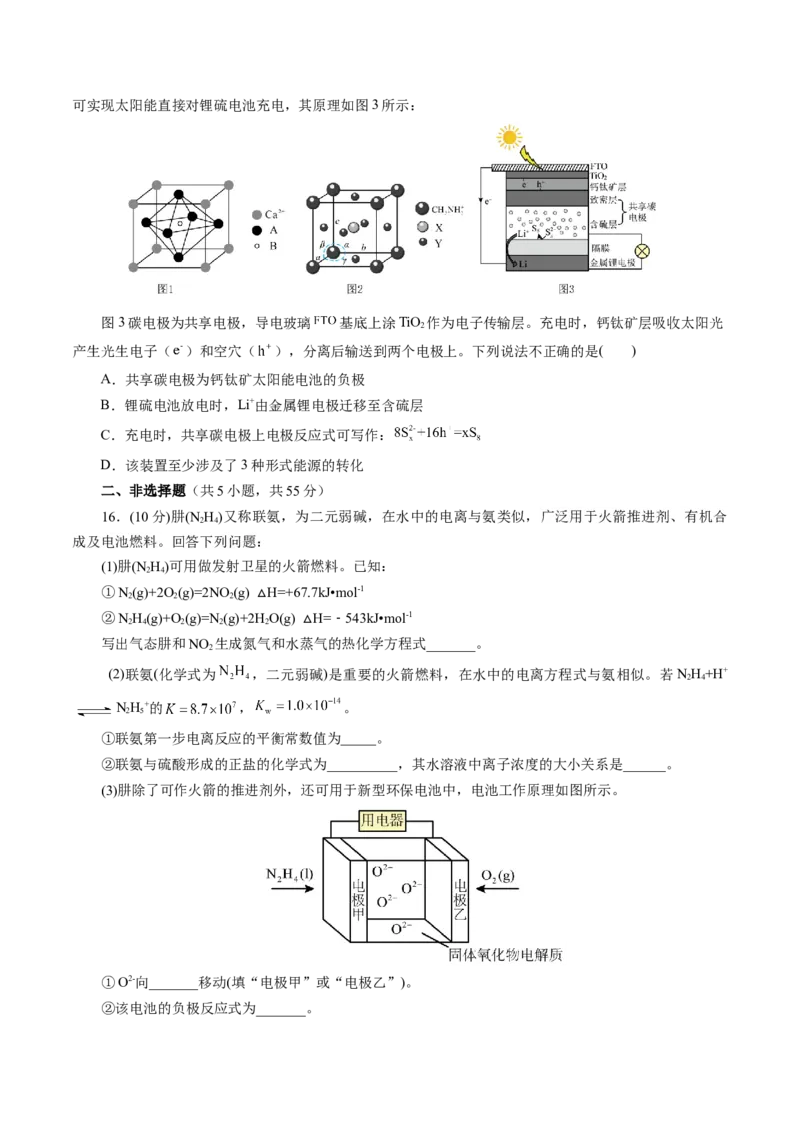
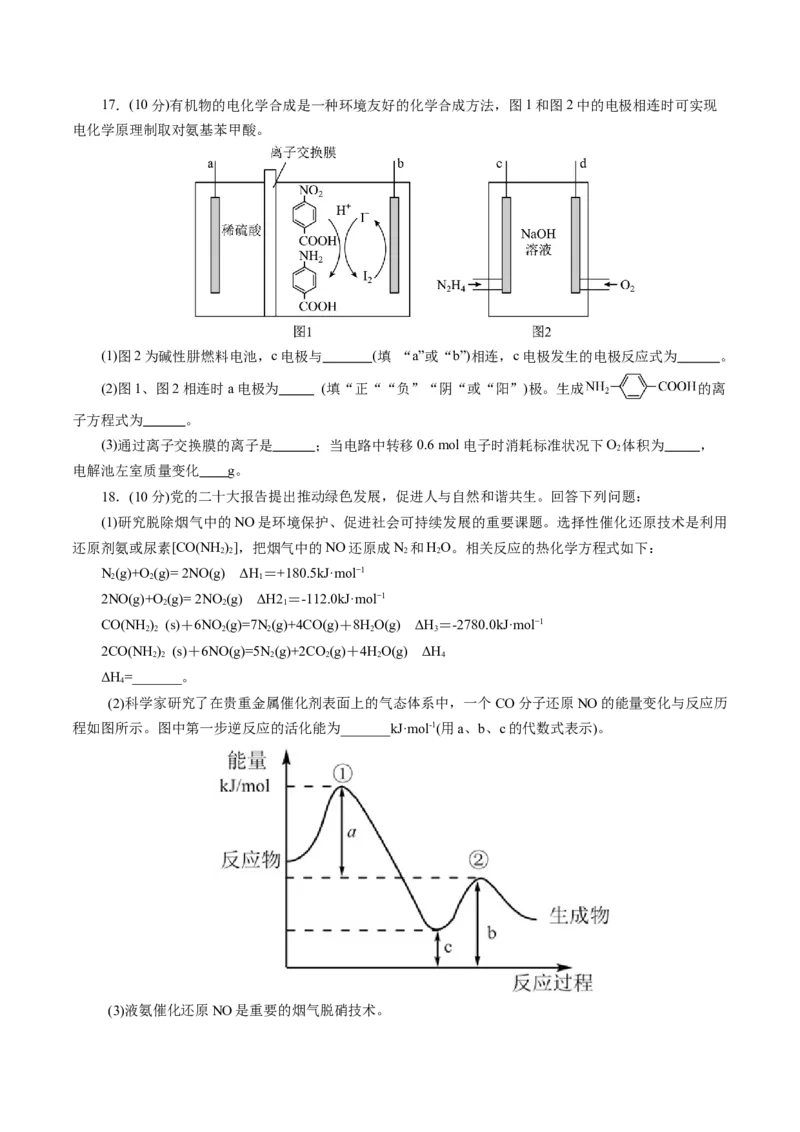
15.(2024·江西省高三三模)钙钛矿具有独特的晶体结构,广泛应用于太阳能电池材料、传感器等诸
多领域。图1、2均为钙钛矿型化合物,图1中另两种离子为 、Ti4+,图2中另两种离子为 和 ,
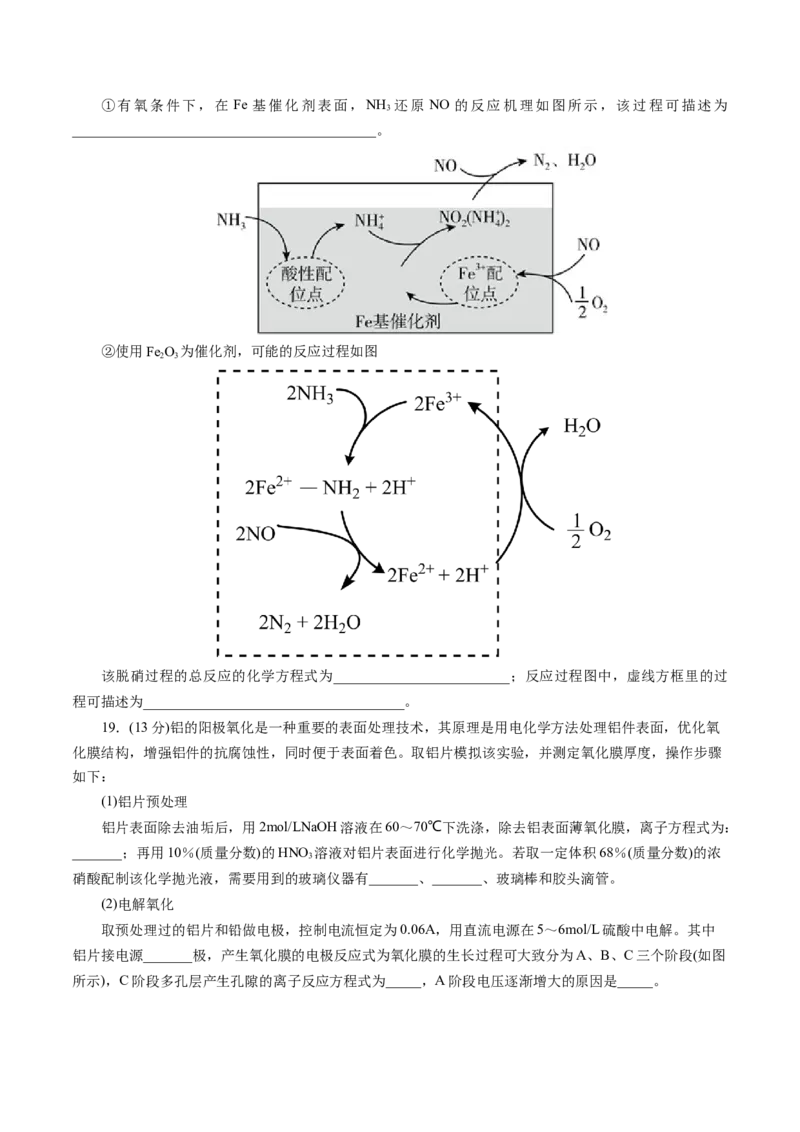
晶胞参数 , a=B=y=90°。图2钙钛矿型化合物制成的太阳能电池与锂硫电池集成,可实现太阳能直接对锂硫电池充电,其原理如图3所示:
图3碳电极为共享电极,导电玻璃 基底上涂TiO 作为电子传输层。充电时,钙钛矿层吸收太阳光
2
产生光生电子( )和空穴( ),分离后输送到两个电极上。下列说法不正确的是( )
A.共享碳电极为钙钛矿太阳能电池的负极
B.锂硫电池放电时,Li+由金属锂电极迁移至含硫层
C.充电时,共享碳电极上电极反应式可写作:
D.该装置至少涉及了3种形式能源的转化
二、非选择题(共5小题,共55分)
16.(10分)肼(N H)又称联氨,为二元弱碱,在水中的电离与氨类似,广泛用于火箭推进剂、有机合
2 4
成及电池燃料。回答下列问题:
(1)肼(N H)可用做发射卫星的火箭燃料。已知:
2 4
①N(g)+2O(g)=2NO (g) H=+67.7kJ•mol-1
2 2 2
②NH(g)+O(g)=N(g)+2HO(g) H=﹣543kJ•mol-1
2 4 2 2 △2
写出气态肼和NO 生成氮气和水蒸气的热化学方程式_______。
2 △
(2)联氨(化学式为 ,二元弱碱)是重要的火箭燃料,在水中的电离方程式与氨相似。若NH+H+
2 4
NH+的 , 。
2 5
①联氨第一步电离反应的平衡常数值为_____。
②联氨与硫酸形成的正盐的化学式为__________,其水溶液中离子浓度的大小关系是______。
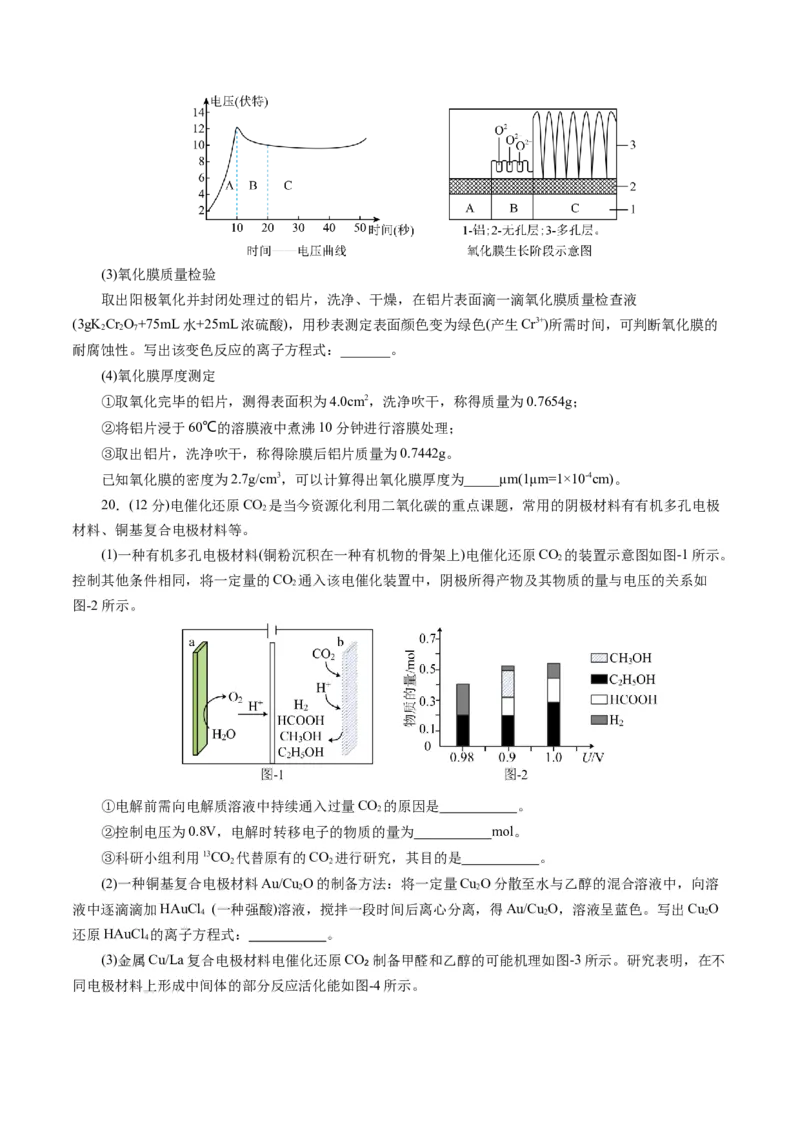
(3)肼除了可作火箭的推进剂外,还可用于新型环保电池中,电池工作原理如图所示。
①O2-向_______移动(填“电极甲”或“电极乙”)。
②该电池的负极反应式为_______。17.(10分)有机物的电化学合成是一种环境友好的化学合成方法,图1和图2中的电极相连时可实现
电化学原理制取对氨基苯甲酸。
(1)图2为碱性肼燃料电池,c电极与 (填 “a”或“b”)相连,c电极发生的电极反应式为 。
(2)图1、图2相连时a电极为 (填“正““负”“阴“或“阳”)极。生成 的离
子方程式为 。
(3)通过离子交换膜的离子是 ;当电路中转移0.6 mol电子时消耗标准状况下O 体积为 ,
2
电解池左室质量变化 g。
18.(10分)党的二十大报告提出推动绿色发展,促进人与自然和谐共生。回答下列问题:
(1)研究脱除烟气中的NO是环境保护、促进社会可持续发展的重要课题。选择性催化还原技术是利用
还原剂氨或尿素[CO(NH)],把烟气中的NO还原成N 和HO。相关反应的热化学方程式如下:
2 2 2 2
N(g)+O(g)= 2NO(g) ΔH =+180.5kJ·mol−1
2 2 1
2NO(g)+O (g)= 2NO (g) ΔH2 =-112.0kJ·mol−1
2 2 1
CO(NH) (s)+6NO (g)=7N(g)+4CO(g)+8HO(g) ΔH =-2780.0kJ·mol−1
2 2 2 2 2 3
2CO(NH) (s)+6NO(g)=5N (g)+2CO (g)+4HO(g) ΔH
2 2 2 2 2 4
ΔH=_______。
4
(2)科学家研究了在贵重金属催化剂表面上的气态体系中,一个CO分子还原NO的能量变化与反应历
程如图所示。图中第一步逆反应的活化能为_______kJ·mol-1(用a、b、c的代数式表示)。
(3)液氨催化还原NO是重要的烟气脱硝技术。①有氧条件下,在 Fe 基催化剂表面,NH 还原 NO 的反应机理如图所示,该过程可描述为
3
___________________________________________。
②使用Fe O 为催化剂,可能的反应过程如图
2 3
该脱硝过程的总反应的化学方程式为_________________________;反应过程图中,虚线方框里的过
程可描述为_____________________________________。
19.(13分)铝的阳极氧化是一种重要的表面处理技术,其原理是用电化学方法处理铝件表面,优化氧
化膜结构,增强铝件的抗腐蚀性,同时便于表面着色。取铝片模拟该实验,并测定氧化膜厚度,操作步骤
如下:
(1)铝片预处理
铝片表面除去油垢后,用2mol/LNaOH溶液在60~70℃下洗涤,除去铝表面薄氧化膜,离子方程式为:
_______;再用10%(质量分数)的HNO 溶液对铝片表面进行化学抛光。若取一定体积68%(质量分数)的浓
3
硝酸配制该化学抛光液,需要用到的玻璃仪器有_______、_______、玻璃棒和胶头滴管。
(2)电解氧化
取预处理过的铝片和铅做电极,控制电流恒定为0.06A,用直流电源在5~6mol/L硫酸中电解。其中
铝片接电源_______极,产生氧化膜的电极反应式为氧化膜的生长过程可大致分为A、B、C三个阶段(如图
所示),C阶段多孔层产生孔隙的离子反应方程式为_____,A阶段电压逐渐增大的原因是_____。(3)氧化膜质量检验
取出阳极氧化并封闭处理过的铝片,洗净、干燥,在铝片表面滴一滴氧化膜质量检查液
(3gK Cr O+75mL水+25mL浓硫酸),用秒表测定表面颜色变为绿色(产生Cr3+)所需时间,可判断氧化膜的
2 2 7
耐腐蚀性。写出该变色反应的离子方程式:_______。
(4)氧化膜厚度测定
①取氧化完毕的铝片,测得表面积为4.0cm2,洗净吹干,称得质量为0.7654g;
②将铝片浸于60℃的溶膜液中煮沸10分钟进行溶膜处理;
③取出铝片,洗净吹干,称得除膜后铝片质量为0.7442g。
已知氧化膜的密度为2.7g/cm3,可以计算得出氧化膜厚度为_____μm(1μm=1×10-4cm)。
20.(12分)电催化还原CO 是当今资源化利用二氧化碳的重点课题,常用的阴极材料有有机多孔电极
2
材料、铜基复合电极材料等。
(1)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO 的装置示意图如图-1所示。
2
控制其他条件相同,将一定量的CO 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如
2
图-2所示。
①电解前需向电解质溶液中持续通入过量CO 的原因是 。
2
②控制电压为0.8V,电解时转移电子的物质的量为 mol。
③科研小组利用13CO 代替原有的CO 进行研究,其目的是 。
2 2
(2)一种铜基复合电极材料Au/Cu O的制备方法:将一定量Cu O分散至水与乙醇的混合溶液中,向溶
2 2
液中逐滴滴加HAuCl (一种强酸)溶液,搅拌一段时间后离心分离,得Au/Cu O,溶液呈蓝色。写出Cu O
4 2 2
还原HAuCl 的离子方程式: 。
4
(3)金属Cu/La复合电极材料电催化还原CO₂制备甲醛和乙醇的可能机理如图-3所示。研究表明,在不
同电极材料上形成中间体的部分反应活化能如图-4所示。X为 ,补充完整虚线框内Y的结构