文档内容
1.以含镍废料(主要成分为NiO,含少量FeO、Fe O 、CoO、BaO和SiO)为原料制备NiO
2 3 2 x y
和碳酸亚钴(CoCO)的工艺流程如图:
3
下列说法不正确的是( )
A.“滤渣Ⅰ”的主要成分是SiO、BaSO
2 4
B.“氧化”时的离子反应为6Fe2++6H++ClO===6Fe3++Cl-+3HO
2
C.“调pH”过程中形成黄钠铁矾渣,NaCO 必须过量
2 3
D.“沉钴”过程发生的反应为Co2++2HCO===CoCO↓+CO↑+HO
3 2 2
2.某铬贫矿主要成分为Fe(CrO ) ,还含有Fe O 、MgO、Al O ,采用次氯酸钠法处理矿石
2 2 2 3 2 3
并制备CrO 的工艺流程如图,已知“氧化浸出”时铁以最高价氧化物存在。下列说法错误
3
的是( )
A.“氧化浸出”时煮沸的目的是加快氧化浸出速率
B.滤渣的主要成分是MgO、Fe O
2 3
C.化合物Ⅰ为NaOH,化合物Ⅱ为NaHCO
3
D.实验室进行“混合”时,将NaCr O 溶液缓慢倒入浓硫酸中,边倒边搅拌
2 2 7
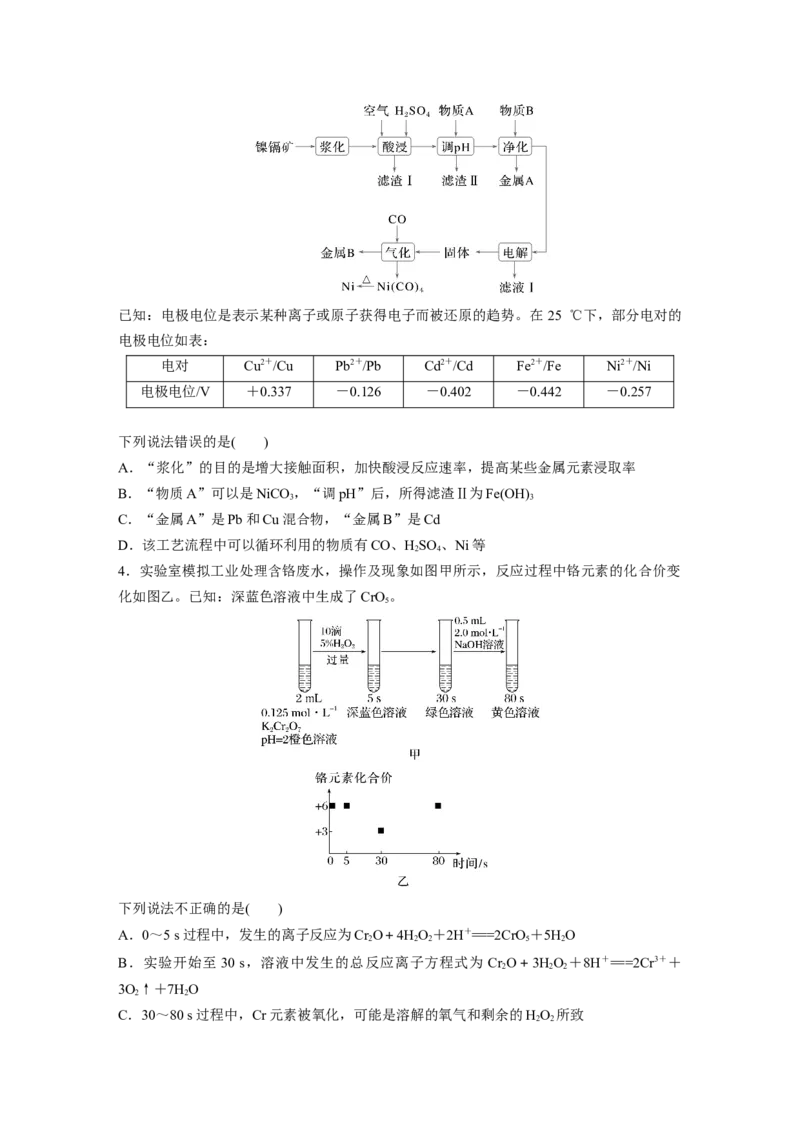
3.(2023·山东省实验中学一模)以红土镍镉矿(NiS、CdO,含SiO 、CuO、PbO、Fe O 等杂
2 2 3
质)为原料回收部分金属单质,其工艺流程如图所示:已知:电极电位是表示某种离子或原子获得电子而被还原的趋势。在 25 ℃下,部分电对的
电极电位如表:
电对 Cu2+/Cu Pb2+/Pb Cd2+/Cd Fe2+/Fe Ni2+/Ni
电极电位/V +0.337 -0.126 -0.402 -0.442 -0.257
下列说法错误的是( )
A.“浆化”的目的是增大接触面积,加快酸浸反应速率,提高某些金属元素浸取率
B.“物质A”可以是NiCO,“调pH”后,所得滤渣Ⅱ为Fe(OH)
3 3
C.“金属A”是Pb和Cu混合物,“金属B”是Cd
D.该工艺流程中可以循环利用的物质有CO、HSO 、Ni等
2 4
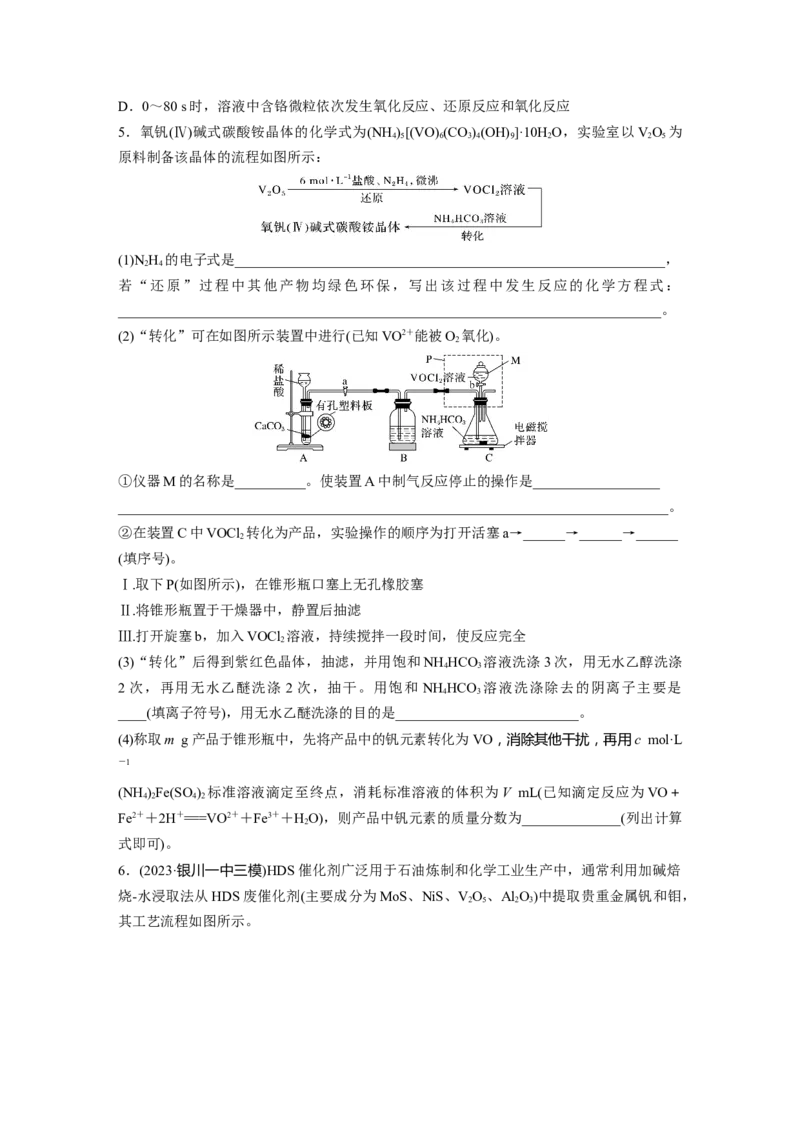
4.实验室模拟工业处理含铬废水,操作及现象如图甲所示,反应过程中铬元素的化合价变
化如图乙。已知:深蓝色溶液中生成了CrO。
5
下列说法不正确的是( )
A.0~5 s过程中,发生的离子反应为Cr O+4HO+2H+===2CrO+5HO
2 2 2 5 2
B.实验开始至 30 s,溶液中发生的总反应离子方程式为 Cr O+3HO +8H+===2Cr3++
2 2 2
3O↑+7HO
2 2
C.30~80 s过程中,Cr元素被氧化,可能是溶解的氧气和剩余的HO 所致
2 2D.0~80 s时,溶液中含铬微粒依次发生氧化反应、还原反应和氧化反应
5.氧钒(Ⅳ)碱式碳酸铵晶体的化学式为(NH )[(VO) (CO)(OH) ]·10H O,实验室以VO 为
4 5 6 3 4 9 2 2 5
原料制备该晶体的流程如图所示:
(1)N H 的电子式是_____________________________________________________________,
2 4
若“还原”过程中其他产物均绿色环保,写出该过程中发生反应的化学方程式:
_____________________________________________________________________________。
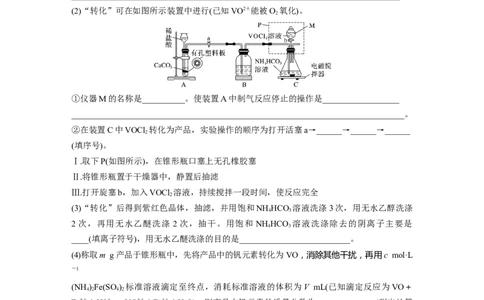
(2)“转化”可在如图所示装置中进行(已知VO2+能被O 氧化)。
2
①仪器M的名称是__________。使装置A中制气反应停止的操作是__________________
______________________________________________________________________________。
②在装置C中VOCl 转化为产品,实验操作的顺序为打开活塞a→______→______→______
2
(填序号)。
Ⅰ.取下P(如图所示),在锥形瓶口塞上无孔橡胶塞
Ⅱ.将锥形瓶置于干燥器中,静置后抽滤
Ⅲ.打开旋塞b,加入VOCl 溶液,持续搅拌一段时间,使反应完全
2
(3)“转化”后得到紫红色晶体,抽滤,并用饱和NH HCO 溶液洗涤3次,用无水乙醇洗涤
4 3
2次,再用无水乙醚洗涤 2次,抽干。用饱和 NH HCO 溶液洗涤除去的阴离子主要是
4 3
____(填离子符号),用无水乙醚洗涤的目的是__________________________。
(4)称取m g产品于锥形瓶中,先将产品中的钒元素转化为VO,消除其他干扰,再用c mol·L
-1
(NH )Fe(SO ) 标准溶液滴定至终点,消耗标准溶液的体积为V mL(已知滴定反应为VO+
4 2 4 2
Fe2++2H+===VO2++Fe3++HO),则产品中钒元素的质量分数为______________(列出计算
2
式即可)。
6.(2023·银川一中三模)HDS催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙
烧-水浸取法从HDS废催化剂(主要成分为MoS、NiS、VO 、Al O)中提取贵重金属钒和钼,
2 5 2 3
其工艺流程如图所示。已知:Ⅰ.MoO、VO、Al O 均可与纯碱反应生成对应的钠盐,而NiO不行。
3 2 5 2 3
Ⅱ.高温下,NH VO 易分解产生N 和一种含氮元素的气体。
4 3 2
回答下列问题:
(1)“浸渣”的成分为______(填化学式);“滤液2”中的成分除了NaMoO 外,还含有
2 4
__________(填化学式)。
(2)请写出“焙烧”过程中MoS及Al O 分别与纯碱反应的化学方程式:_________________
2 3
______________________________________________________________________________,
____________________________________。
(3)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始钒
的 浓 度 和 NH Cl 的 加 入 量 分 别 为
4
____________________________________________________、
______________。
(4)“沉钒”时生成NH VO 沉淀,则“煅烧”后生成氧化产物和还原产物的物质的量之比为
4 3
______________________________________________________________________________。
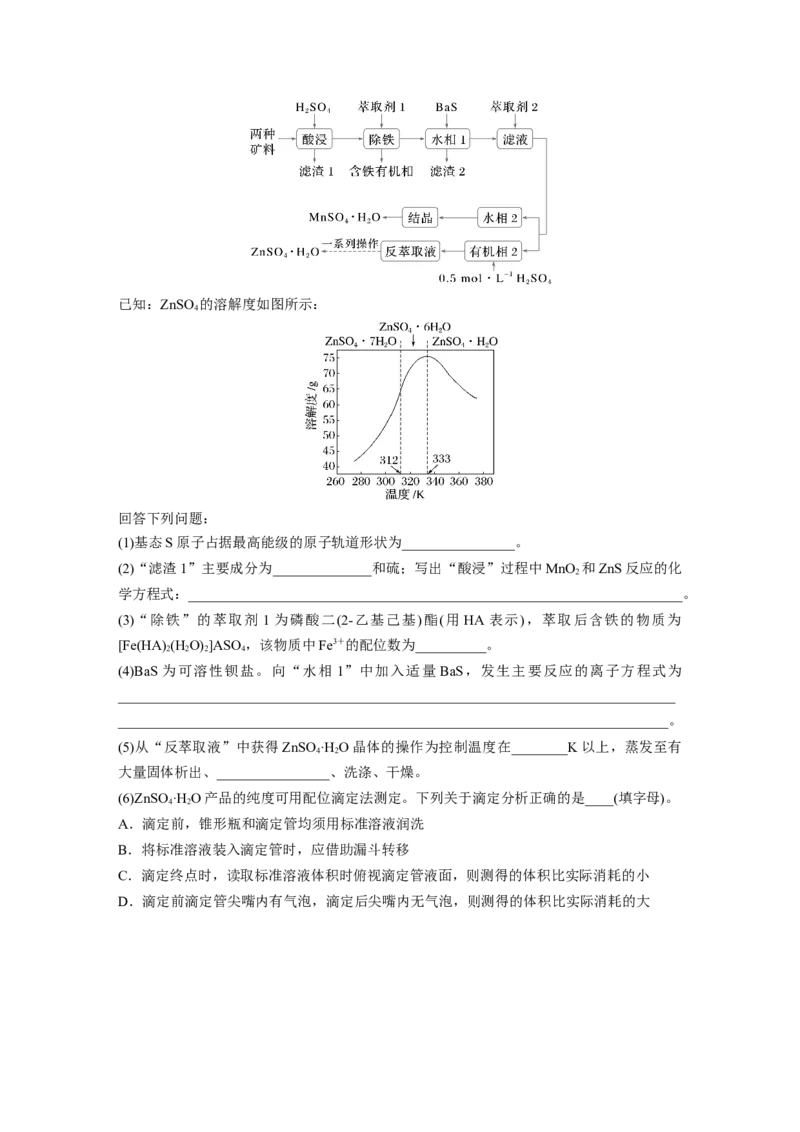
7.(2023·哈尔滨三中校考模拟)用锌精矿(ZnS)和软锰矿(MnO )两种矿料(含少量杂质Fe、
2
Cu、Pb等元素的化合物及SiO)生产硫酸锌和硫酸锰的流程如下:
2已知:ZnSO 的溶解度如图所示:
4
回答下列问题:
(1)基态S原子占据最高能级的原子轨道形状为________________。
(2)“滤渣1”主要成分为______________和硫;写出“酸浸”过程中MnO 和ZnS反应的化
2
学方程式:______________________________________________________________________。
(3)“除铁”的萃取剂 1 为磷酸二(2-乙基己基)酯(用 HA 表示),萃取后含铁的物质为
[Fe(HA) (H O) ]ASO ,该物质中Fe3+的配位数为__________。
2 2 2 4
(4)BaS 为可溶性钡盐。向“水相 1”中加入适量 BaS,发生主要反应的离子方程式为
_______________________________________________________________________________
______________________________________________________________________________。
(5)从“反萃取液”中获得ZnSO·H O晶体的操作为控制温度在________K以上,蒸发至有
4 2
大量固体析出、________________、洗涤、干燥。
(6)ZnSO ·H O产品的纯度可用配位滴定法测定。下列关于滴定分析正确的是____(填字母)。
4 2
A.滴定前,锥形瓶和滴定管均须用标准溶液润洗
B.将标准溶液装入滴定管时,应借助漏斗转移
C.滴定终点时,读取标准溶液体积时俯视滴定管液面,则测得的体积比实际消耗的小
D.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡,则测得的体积比实际消耗的大